中-低恶性程度的孤立性颈胸段脊柱转移瘤的手术疗效及生存分析
2020-08-17李冬月刘忠军刘晓光
李冬月,刘忠军,刘晓光*
随着脊柱外科技术的进步,许多脊柱转移瘤患者更加倾向于积极的手术治疗[1-5],以期缓解疼痛,改善神经功能,提高生活质量以及延长生存时间。由于颈胸段脊柱(CTJS)是脊柱形态变化和应力集中的部位,此处受到转移瘤侵犯时,多表现为病理性骨折或神经根受压所致的严重疼痛,脊髓压迫出现的不全截瘫或完全截瘫,有时甚至伴发脊柱后凸畸形[6-8],对患者生存质量有着明显的负面影响。对于原发肿瘤中-低恶性程度的孤立性CTJS转移瘤的外科治疗相关报道较少,广泛或边缘的手术治疗[2-3],如全脊椎整块切除、肿瘤分块切除等[2-5],是否可以降低患者的局部复发率,延长其生存时间,目前还没有定论。本研究通过回顾性分析北京大学第三医院收治的CTJS转移瘤患者资料,探讨原发肿瘤中-低恶性程度的孤立性CTJS转移瘤广泛或边缘的完全切除术后的临床疗效和生存情况。
1 对象与方法
1.1 研究对象 选择北京大学第三医院2011年1月—2015年5月收治的CTJS转移瘤患者10例为研究对象,纳入标准:(1)脊柱孤立性转移瘤患者;(2)C7~T4段脊柱受累且为责任节段;(3)初次脊柱手术;(4)原发肿瘤为中-低恶性程度;(5)Tomita转移瘤评分[9]≤3分;(6)预期生存时间>6个月。排除标准:(1)转移瘤为高度恶性;(2)多发脊柱转移瘤;(3)转移瘤复发者;(4)一般情况不能耐受手术者;(5)预期生存时间较短(<6个月)。患者均有不同程度的胸背部疼痛、根性疼痛、肢体麻木、不全截瘫或者完全截瘫等症状。
1.2 手术方式 采用两种手术方法行病椎切除,切除范围为广泛或者边缘切除:5例行肿瘤整块切除术,5例行肿瘤分块切除术。患者肿瘤切除后,均用蒸馏水、0.5 mg/ml的顺铂溶液(齐鲁制药有限公司,H20023460)浸泡伤口2.5 min,减少肿瘤细胞的污染。前方为钛网加/不加钛板重建,后方为胸椎椎弓根钉加/不加颈椎侧块螺钉固定。
1.2.1 肿瘤整块切除术 肿瘤整块切除术指整块切除转移瘤侵及的脊椎骨性结构及周围累及的组织。其中3例行后路全脊椎整块切除术(TES),2例行前路病椎椎体整块切除术(PVE-En)。(1)TES:肿瘤累及范围较大(W-B-B分期1~12区[10]的全部或大部分)。后正中单一切口,固定上下至少两个节段,用线锯锯断病椎的椎弓根,整块切除后方附件,游离前方椎体并整块切除,注意切除边界。(2)PVE-En:肿瘤累及范围局限(W-B-B分期4~9区[10])。显露病椎上下至少两个椎体,整块或分块切除病椎椎体。
1.2.2 肿瘤分块切除术 肿瘤分块切除术指分块切除转移瘤侵及的脊椎骨性结构及周围累及的组织。其中3例行后路全脊椎分块切除术(TS),2例行前路病椎椎体分块切除术(PVE)。此两种手术方式在行病椎切除时采用分块切除,其余同整块切除的手术操作。
1.3 术后处理 切除的病椎及组织均送病理检查。抗生素应用1周左右,伴术前脊髓压迫或术中牵拉时间较长者,予以神经营养药物〔(1)注射用单唾液酸四己糖神经节苷脂钠,黑龙江哈尔滨医大药业有限公司(H20060422);(2)甲钴胺片:华北制药康欣有限公司(H20031126)〕等对症治疗。指导患者肢体功能锻炼,术后卧床1周左右,佩戴支具下地活动。
1.4 临床效果评价、观察指标及随访 疼痛评估按视觉模拟评分法评分(VAS评分,0~10分)[11],神经功能评估按脊髓损伤功能评定(Frankel分级)[12]评分,从A至E换算成1~5分,功能状况评价采用美国东部肿瘤协作组评分(ECOG评分,0~5分)[13]。Tomita评分系统[9]是依据恶性肿瘤等级(缓慢生长1分、中速生长2分、快速生长4分)、内脏转移情况(无转移0分,可治疗转移2分,不可治疗转移4分)、骨转移情况(孤立转移1分,多发转移2分)综合评分,共计10分,其中2~3分为长期局部控制,广泛或边缘切除;4~5分为中期局部控制,边缘或经瘤切除;6~7分为短期缓解,姑息手术治疗;8~10分为非手术保守治疗。记录两组患者手术前后VAS评分、Frankel分级评分及ECOG评分。术后前两年内每3个月门诊随访一次,以后每6个月门诊随访一次。复查内容包括上述临床评分指标、X线片、CT或磁共振成像(MRI),观察局部复发、植骨融合、内固定稳定情况及生存情况。生存时间定义为手术至死亡或最近一次随访时间。若患者未来复查,则电话随访。
1.5 统计学方法 使用SPSS 17.0统计学软件进行分析。计量资料以(±s)表示,手术前后比较采用配对t检验,使用Kaplan-Meier法绘制生存曲线并计算中位生存时间,采用Log-rank检验进行组间比较。以P<0.05为差异有统计学意义。
2 结果
2.1 患者一般情况 10例患者,年龄29~70岁,平均年龄(51.8±13.3)岁;男5例,女5例;转移瘤侵及CTJS单节段者6例(2例C7,3例T2,1例T3),两节段者4例(2例C7~T1,2例T3~4)。原发肿瘤病理类型:乳腺癌3例,前列腺癌2例,甲状腺癌3例,肾透明细胞癌2例(见表1)。患者原发肿瘤均已切除,术前原发肿瘤相关敏感指标理想,均行辅助治疗。根据Tomita评分系统[9],2分8例,3分2例。无围术期死亡病例。手术时间为160~410 min,平均(262.2±85.7)min,术中出血量为 800~3 200 ml,平均(1 770.0±766.0)ml。1例术中胸膜破裂,予以修补,术后无胸腔积液或其他肺部并发症。1例术后脑脊液瘘,对症处理后症状好转。1例术后出现双下肢肌力下降,Frankel分级由D级下降到C级,予以甲泼尼龙琥珀酸钠〔Pfizer Manufacturing Belgium NV:40 mg(H20080284)、125 mg(H20080286)、500 mg(H20080285)〕冲击治疗,10 d后改善至术前水平。
2.2 手术前后患者VAS评分、Frankel分级评分、ECOG评分比较 术后患者VAS评分〔(2.10±0.99)分〕低于术前〔(6.20±1.48)分〕,差异有统计学意义(t配对=22.841,P<0.001)。10例患者中9例伴有不全截瘫或截瘫,术后7例神经功能Frankel分级至少改善一个等级(见表2),评分由术前(3.30±1.16)分提高到术后(4.20±0.63)分,差异有统计学意义(t配对=3.857,P=0.004)。患者术后功能状态均较术前好转(见表3),ECOG评分由术前(2.60±0.97)分下降到术后(1.80±0.63)分,差异有统计学意义(t配对=4.000,P=0.003)。
2.3 术后患者生存分析 10例患者随访时间26~72个月,平均随访时间(52.8±14.7)个月,至末次随访时1例死亡,2例失访。其中1例前列腺癌脊柱转移瘤因冠心病行冠状动脉支架术,术前心脏评估可耐受手术,术后26个月随访时死于冠心病急性发作。其余9例中位生存时间为54个月,1年生存率均为100%。整块切除与分块切除患者的中位生存时间分别为48、54个月,两种手术方式的生存时间比较,差异无统计学意义(χ2=0.471,P=0.493,见图1)。随访期内患者均未出现内固定失败。除1例患者死亡外,其他患者CT均显示植骨融合。

表1 患者的临床资料Table 1 Clinical data of patients
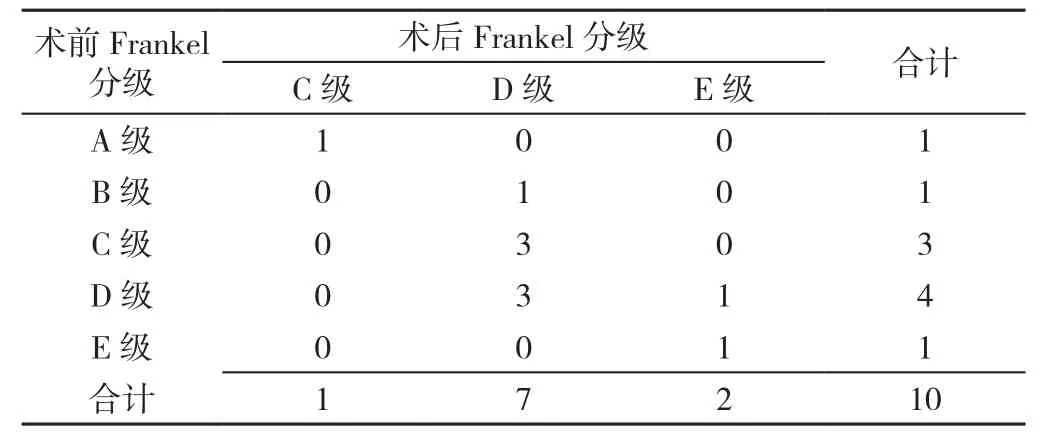
表2 手术前后Frankel分级情况(例)Table 2 Frankel classification before and after operation

表3 手术前后ECOG评分情况(例)Table 3 ECOG score before and after operation
3 讨论
随着外科手术技术及相关内固定器械的进步,脊柱转移瘤越来越倾向于手术治疗,对患者生存质量的改善和生存时间的延长均有较大的临床意义[1-3,6]。但是脊柱外科手术的风险和并发症相对较大,部分预期寿命短,一般状况较差的患者,不一定能从创伤较大的手术中获益[9,14],甚至可能死于较大的手术创伤或者围术期的严重并发症。
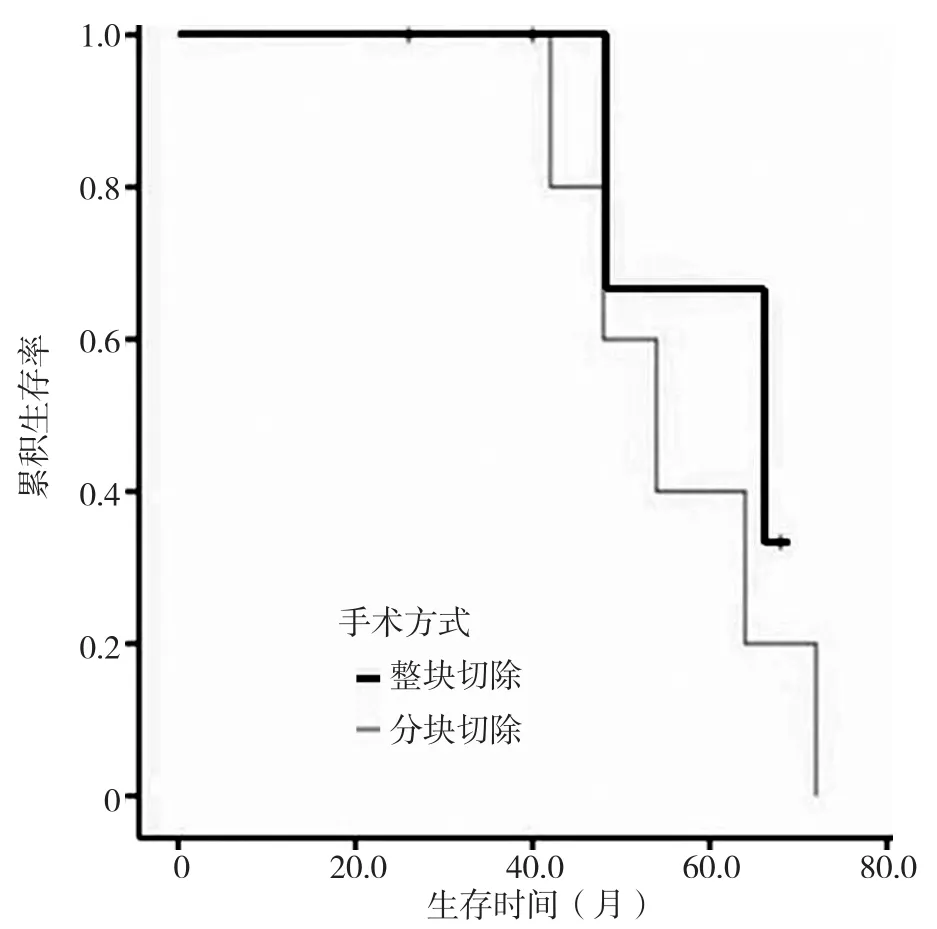
图1 两种手术方式患者的Kaplan-Meier生存曲线Figure 1 Kaplan-Meier survival curve of patients with two surgical methods
脊柱转移瘤患者的预期寿命和预后评估影响外科治疗的决策。FINKELSTEIN等[15]回顾性分析987例脊柱转移瘤患者的手术疗效,发现肿瘤原发于肺、上消化道等恶性等级较高者,1年生存率分别为16%、7%,中位生存时间分别为87 d、56 d;肿瘤原发于甲状腺、乳腺、前列腺等恶性等级较低者,1年生存率分别为73%、48%、40%,中位生存时间分别为587 d、346 d、223 d。PARK等[16]报道原发肿瘤恶性程度较高的非小细胞肺癌脊柱转移术后的中位生存时间仅5.2个月,而MENG等[17]和KATO等[18]分别报道了原发肿瘤恶性程度较低的前列腺癌和乳腺癌脊柱转移术后的中位生存时间分别为44个月、6.4年。可见对于脊柱转移瘤中原发肿瘤低度恶性的患者,其术后预期生存时间比较满意[17-18]。TOMITA等[9]建议依据原发恶性肿瘤等级、内脏转移情况、骨转移情况综合评价,指导外科治疗。对于原发肿瘤中-低恶性程度、孤立性脊柱转移并且原发灶控制良好的患者,其生存预期较长,建议广泛或者边缘切除[2,9]。本研究中10例患者均为上述情况,术后中位生存期为54个月,除1例死于心脏疾病外,其余患者末次随访均仍存活,可见对于此类患者的外科手术治疗具有很大的临床意义。
由于CTJS骨性形态和应力集中的特点,一旦发生肿瘤转移侵及骨性结构,容易早期出现椎体压缩后凸畸形,压迫脊髓造成患者的神经功能受损[8]。本研究中9/10的患者出现了不全截瘫或者完全截瘫(Frankel 分级:A级~D级),可见由于CTJS的解剖特点,此处转移瘤神经功能受损的比例较高。脊柱外科手术可以解除压迫,矫正畸形,改善患者的临床症状,提高患者的生存质量。根据W-B-B分期[10]中肿瘤所在的位置和范围,选择不同的手术方式,本研究中采用整块切除和分块切除两种手术方法。患者术后的疼痛、神经功能、生活功能状态较术前均有明显的改善。在治疗CTJS转移瘤时,如果患者的身体条件允许手术,应考虑手术治疗。
本研究中,对于原发肿瘤中-低恶性程度、孤立性脊柱转移并且原发灶控制良好的患者,其手术治疗的原则应同脊柱原发恶性肿瘤一样,广泛或者边缘切除病椎,其目的是达到肿瘤的根除而不仅是局部病灶的控制。KATO等[19]发现10例孤立性脊柱转移瘤在全脊椎TES之后存活超过10年,包括5例肾癌,2例甲状腺癌,2例乳腺癌,1例前列腺癌。从该文献报道中,发现这10例转移瘤患者的情况为原发肿瘤恶性等级中-低度、孤立性脊柱转移、广泛或边缘的全脊椎整块切除。考虑到CTJS解剖结构的特殊性,周围毗邻复杂的、重要的组织结构,如大动静脉(主动脉、腔静脉等)、重要器官(肺、气管、食管、胸导管等)、神经结构(脊髓、神经根、喉返神经等)、骨性结构(胸骨、锁骨等),有时难以完成病椎的整块切除。本研究中在广泛或边缘切除的前提下,比较整块和分块切除病椎患者的生存时间无统计学差异。
CTJS转移瘤的外科治疗需考虑到多种因素,如患者的临床症状、脊柱转移范围、全身情况、预期生存寿命、Tomita脊柱转移瘤评分[9]等。但对于身体条件允许的患者,考虑其出现不全截瘫或完全截瘫的风险较高,应给予积极的手术治疗,其临床效果满意。对于原发恶性肿瘤中-低度、孤立性脊柱转移,在原发灶控制理想的情况下,其治疗原则应同脊柱原发恶性肿瘤一样,给予患者病椎的广泛或边缘切除,以期获得更长的生存时间。本研究仍有不足之处,病例数相对较少,随访时间相对较短,仍需前瞻性的大规模、多中心的临床研究。
作者贡献:李冬月进行文章的构思与设计,数据收集、整理,统计学处理,结果的分析与解释,撰写论文,进行论文的修订,负责文章的质量控制及审校;李冬月、刘晓光进行研究的实施与可行性分析;刘忠军、刘晓光对文章整体负责,监督管理。
本文无利益冲突。
