CTO病变新技术研究进展
2020-07-12石宇杰韩运峰崔振双田新利李俊峡
石宇杰,韩运峰,崔振双,田新利,李俊峡
在冠状动脉(冠脉)造影确诊为冠状动脉粥样硬化性心脏病(冠心病)的患者中,约20%为慢性完全闭塞(CTO)病变,可以说CTO仍是目前经皮冠脉介入治疗(PCI)中的难点和前沿。研究证明,PCI可有效改善CTO患者的心绞痛症状,提高生活质量,降低远期死亡率和冠脉旁路移植术(CABG)需求[1,2],而随着以美国医生为主的CTO治疗流程图(hybrid algorithm)的问世[3],把千差万别的CTO PCI程序化、简单化,对其治疗起着有益的推动作用。在hybrid algorithm的基础上,亚太CTO俱乐部又出台了CTO PCI流程图[4],中国冠脉慢性完全闭塞病变介入治疗俱乐部(CTOCC)也出台了CTO PCI流程图[5],提高了CTO PCI的成功率。CTO病变治疗上,首先要考虑的是PCI治疗策略,同时操作技术及器械选择也很重要,术者应认真阅读冠脉造影、冠脉CTA等影像学资料,分析患者病变特征及临床情况,结合自身技术水平及对器械的理解,选择合适的手术策略及相关技术和器械。近年来CTO介入新技术日新月异,促进了CTO介入治疗的飞速发展。本文现对近年来CTO介入技术的进展进行综述。
1 正向技术钢丝通过困难时技术
1.1 move the cap技术当闭塞病变近端纤维帽斑块钙化严重,致使导丝不能穿透进入,或近端纤维帽模糊,无法准确确定近端位置时,可通过内膜下绕开斑块,达到“移除斑块”的目的。
1.2 Scratch and go技术用坚硬的导丝扎进血管结构内(多角度或以钙化作为参考、并与血管一起舞动等特点进行判断),形成夹层,轻送入微导管(不超过1~2 mm),再换亲水导丝进行knuckle向前推进。微导管不能跟太快,除非确定导丝在血管结构内。
move the cap技术常与Scratch and go技术同步实施,步骤为:①正向及逆向钢丝分别到达闭塞段的近、远端;②应用同近端血管等径球囊高压扩张病变近端以撕裂内膜;③调整正向导丝头端角度以利于在微导管支撑下将其送入内膜下;④正向导丝在内膜下knuckle向前推进;⑤于正向内膜下行Reverse CAR技术,而后插入Guidezilla,逆向导丝通过主动迎客技术(AGT)完成体外化[6]。
1.3 BASE power knuckle技术亦称为BAS技术,是在球囊辅助下强行knuckle技术,用于导丝扎不进纤维帽,而在其边上的血管结构内作一个假腔,通过假腔越过闭塞段斑块。目的是要前向进入夹层行ADR或逆向进入夹层行R-CART。步骤为:①用普通工作导丝送到近端纤维帽处(当然进不了斑块内);②沿钢丝送入与血管直径1:1的非顺应性球囊;③扩张数次造成临近闭塞处血管小的夹层;④送入微导管,用前球囊锚定微导管;⑤换用亲水导丝,微导管辅助进入内膜下,强行knuckle通过假腔越过闭塞段斑块[6]。
1.4 S-BASE技术(边支球囊辅助下内膜下进入技术)在CTO病变中,近端纤维帽模糊增加了手术难度,如果闭塞近端同时存在分支血管则困难程度明显增高。此时采用“Move the cap”技术,最终采用ADR策略可能完成整个手术,但极易丢失边支。如采用S-Base技术,既增加了整个系统的支撑力和稳定性、提高了导丝的穿刺能力,又能最大程度地避免了导丝在CTO入口进入内膜下时造成边支丢失的风险,在提高效率的同时兼顾了安全性。步骤为:①靠近入口的边支送进一根导丝;②沿钢丝送入一个与边支1:1大小的半顺应性球囊,该球囊一部分在边支、一部分在主支;③扩张球囊堵掉边支;④主支在微导管辅助下用亲水导丝knuckle到CTO病变(也可能在内膜下),进入后边支球囊立刻撤压(图1)[7]。
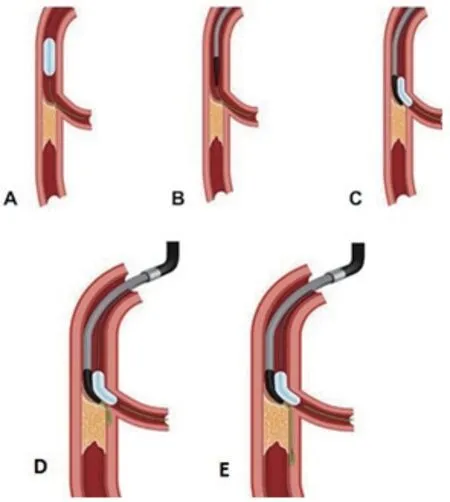
图1 side-base 技术
1.5 Carlino技术STAR技术之所以被淘汰,是因其造成的假腔过长、夹层过大,导致分支丢失较多,远期预后较差。Carlino等改良了STAR技术,也称为Carlino改良方法,通过对比剂的前向液压修饰闭塞段内相对疏松组织,因此亦称造影剂引导的STAR技术(Contrast-guided STAR技术),相比于传统STAR技术,其操作相对温和。其机制为使CTO病变近端产生夹层,同时通过对比剂在局部滞留辨析血管走形,指导导丝走行方向,是一种有用的能帮助导丝高效通过CTO病变的补充策略,正、逆向治疗时都可采用,且非常安全。但Carlino技术并不适用于开通血管本身,而是一种辅助开通复杂CTO病变的有效方法。特别是对于之前有开通失败史、扭曲、钙化或位于远端的CTO,较为适合且安全。步骤为:①微导管置于近端纤维帽;②2 ml锁扣注射器高压手推<1 ml的造影剂。该技术要在透视下控制性使用,以免穿孔出现造影剂外溢(纯粹靠手感);③用硬导丝尝试穿过纤维帽[8]。
1.6 改良LAST技术此技术主要预防LAST技术时knuckle导丝前行导致血肿存在。步骤为:①导丝进入内膜下后,在不越过远端纤维帽时停止;②交换为不塑形的pilot150导丝扎入远端纤维帽以远的内膜下,并推送corsair进行跟进;③换用穿刺型导丝如Conquest pro,在对侧造影指示下确定切线位及穿刺角度,之后完成reentry。
1.7 血管内超声指导前向主动真腔寻径(IVUS-ATS)IVUS引导下主动性真腔寻径,是一种开通复杂冠脉慢性完全闭塞病变的创新技术[9]。ATS技术的优势在于不仅有明确导丝是否位于真腔内的传统“诊断功能”,还具有明确真腔方向,以利“靶向”调整导丝刺入真腔从而开通CTO的“治疗功能”,从而提高复杂CTO PCI的成功率,同时有助于避免大的分支闭塞、冠脉穿孔等严重并发症。
IVUS-ATS是一种在前向平行导丝技术未成功到达远端真腔时启动的主动真腔寻径技术,步骤为:①送入第1根中等硬度CTO导丝(通常是Ultimate bros3,ASAHI,日本)用于IVUS检查即“诊断”,送入第2根高硬度导丝(通常Conquest pro,ASAHI,日本)用于穿刺真腔的“治疗”,必要时两根导丝的角色可互换;②沿第1根“诊断导丝”送入1.0~1.25 mm球囊预扩张闭塞近端穿入点,再送入IVUS导管(通常采为Eagle eye短头,Volcano,美国)至CTO起始段,明确2根平行导丝的实际位置和“解剖真腔”所在的方位;③真腔寻径(TS),包括IVUS引导钝头CTO近端纤维帽的穿刺,使导丝直接穿刺进入或接近“解剖真腔”,和将进入内膜下甚或已穿出血管中膜的导丝撤回重新调整穿刺“解剖真腔”的过程;④真腔追踪(TT),是指 TS成功后使导丝继续沿着闭塞段“斑块内”行走至远端血管真腔的过程。⑤微导管交换普通工作导丝,再次IVUS检查确认导丝位于真腔内。
IVUS-ATS是传统前向导丝升级技术失败的延伸,ADR和逆向技术均无机会时(如侧支循环差)的首选,或均未成功的复杂CTO PCI新技术的必要补充。但对于严重钙化性病变,IVUS导管到达CTO段困难,ATS难于成功。
1.8 Subintimal plaque modification(SPM)技术即内膜下斑块修饰技术,是在CTO-PCI失败时不得已而为之的一种方法[10]。其在CTO内膜下进行了球囊扩张,但并未成功植入支架。Hirai T在所有CTO-PCI失败的患者中,根据是否进行内膜下斑块修饰分为2组:SPM组(n=59)与未SPM组(n=79)。术后SPM组TIMI 0级血流的患者明显少很多(25.4%vs. 75.9%,P<0.001)。院内总MACCE事件、心肌梗死、卒中、冠脉穿孔的不良事件也无明显差异。但术后1个月随访时的SAQ总分的改善程度(28.36±21.7vs. 16.86±20.2,P=0.012)、SAQ心绞痛评分的改善程度(27.96±29.6vs. 16.36±25.5,P=0.050),SPM组显著优于未SPM组。意味着即使无法支架植入,仅单纯内膜下斑块修饰也可使患者生活质量获得改善,而且进行斑块修饰后还可为日后CTO-PCI做准备。因此,内膜下斑块修饰的做法也许可作为CTO-PCI失败后的备选方案。
2 常规ADR不成功时应用的技术
2.1 STRAW技术ADR失败的原因多是内膜下血肿形成后真腔被挤压。控制血肿最简单的方法是在stick-and-drive或stick-and-swap前抽吸stingray导管,血液重新进入前可有几分钟进行穿刺操作。步骤为:①送入1根导丝及OTW球囊(1:1大小);②在纤维帽近端打起球囊;③抽去导丝,用针筒抽吸掉血肿。这是一种堵住入口减少血肿再入真腔的技术[11]。
2.2 stick-and-drive或stick-and-swap技术stingray导丝穿刺失败后,还可用塑好型的专业级CTO穿刺导丝,如Asahi公司的 conquest Pro12等,这些导丝事先塑好不同的弯,称为stick-and-drive,如果专业级CTO导丝穿刺后换为亲水中等克数的导丝进入远段真腔,称为stick-and-swap[12,13]。
2.3 Bob-sled技术ADR有也有一定的失败率,当使用Stingray球囊导丝穿刺失败、stingray着陆点不合适时,可采用Bob-sled技术。步骤为:①抽瘪stingray球囊;②通过硬导丝或近或远移至更少钙化、更接近真腔、更不扭曲、更小血肿的位置重新穿刺[14]。
2.4 Antegrade fenestration and re-entry技术即前向开窗再入技术(AFR),是一种新型内膜下策略。步骤为:①微导管支持下使导丝进入内膜下并到达远端纤维帽;②撤掉微导管,在内膜下置入第2根导丝,保证2根导丝距离足够近;③沿着第1根导丝置入与动脉1:1的球囊到远端纤维帽。④缓慢扩张球囊;⑤在球囊收缩、开窗尚未闭合时,快速使用第2根导丝穿越开窗进入真腔[14]。这种AFR策略有点像CART策略,只不过球囊是正向通过的,且使用了导管室常用的器械,而不需要使用CrossBoss/Stingray设备,大大降低了开展成本,对于没有装备CrossBoss/Stingray设备的中心来说,可进行尝试,作为前向策略中的一种新的选择。
2.5 Double Stingray技术目前流行病学研究发现30%左右的CTO病变会累及分叉处。CTO病变合并分叉病变使得PCI难度增加,且如不慎导致分支闭塞的话有可能出现急性心肌梗死。而ADR策略本身就很有可能造成分支血管闭塞,因此在合并分支病变的情况下应慎用。Tajti P在处理伴有分叉病变的CTO时运用Double Stingray技术以保护CTO病变附近的分支[15]。但此方法需进入分叉处2支血管的内膜下,难度较大,需要更加丰富的Stingray系统使用经验。
3 钢丝通过而球囊不能通过的高阻力病变时的技术
3.1 BAM技术BAM技术即球囊辅助微夹层技术或球囊爆破技术,主要是在钢丝通过病变而球囊或微导管不能通过病变时应用。是将小球囊尽可能推送到近端纤维帽的远端进行扩张,直至球囊破裂导致近端纤维帽出现小的夹层以利其后球囊或微导管的通过。步骤为:①当导丝通过高阻力CTO病变后,沿导丝送入一短、直径小的顺应性球囊并紧紧抵住CTO近端纤维帽;②慢慢高压扩张直至球囊破裂,人为造成CTO近端纤维帽处的微夹层;③进一步推进第2个球囊重复,直到顺利通过病变。该技术有良好的安全性,冠脉穿孔等血管并发症非常低[16,17]。
3.2 铁撬棍效应(crowbar effect)技术铁撬棍效应技术主要应用于高阻力病变,步骤为:①导丝通过高阻力CTO病变后,沿该导丝送入第2根较硬和第3根更硬的导丝到达远端真腔;②沿第1根导丝送入1.25~1.5 mm小球囊,抵住病变高压扩张,重复该动作,直至球囊通过闭塞病变[18]。报道该技术虽有较高的成功率,但血管并发症也较高。
3.3 球囊-导丝跷跷板切割技术主要用于高阻力病变。步骤为:①导丝A通过高阻力病变;②小心操作更硬的导丝B沿导丝A通过病变到达远端血管真腔;③分别沿导丝A、B送入短小球囊A及球囊B;④首先将球囊A沿导丝A尽可能远地推送到高阻力病变处,高压扩张病变同时挤压导丝B,使得导丝B产生对病变的切割效应;⑤回撤球囊A,球囊B再重复上述操作,反复交替进行,最终使得球囊通过CTO病变[19,20]。
3.4 external cap crush技术即斑块挤压技术,用于高阻力病变。步骤为:①第1根导丝进入远段真腔;②送入第2套导丝及微导管,用scratch-and-go或BASE技术把亲水的软导丝knuckle到内膜下,从外挤压真腔的病变;③撤出第2套系统的微导管,沿第2根钢丝送入与血管直径1:1的球囊,送到受阻的部位对真腔进行挤压;④亦可2根导丝各套入1个球囊,交替挤压;⑤撤出球囊,尝试真腔微导管或球囊通过[14]。
4 逆向钢丝体外化技术
4.1 Pick up技术即当逆向导丝通过闭塞病变后,经反复尝试无法进入正向指引导管时,正向送入Gudiezilla或5in6导管至冠脉内便于逆向导丝进入。
4.2 主动迎客技术(AGT)是指将延长导管,如子母导管、Guidezilla、4或5 Fr导管等正向插入,主动迎接逆向导丝而有利于导丝体外化[21]。步骤为:①逆向导丝通过闭塞病变;②将子母导管的头端送入逆向CART技术所造成的腔内或接近近端入口;③将逆向导丝送入子母导管中。操纵逆向导丝之前若子母导管只到达口部或近端,AGT技术的有效性则会受限。
4.3 Back-end技术当逆向微导管进入正向指引导管后,更换为RG3 330 cm超长导丝,经逆向系统一直前送出正向系统,并正向经RG3导丝完成PCI过程。
4.4 Rendezvous技术当逆行导丝通过病变并进入正向指引导管后, 推送逆向微导管进入正向指引导管并回撤逆向导丝,将正向微导管与之在指引导管内对吻,操控正向导丝穿入逆向微导管并到达远端。亦可采用单微导管法,即正向不带微导管,将正向导丝直接穿入逆向微导管中[22]。
4.5 改良Rendezvous技术指逆向导丝、微导管不能够进入正向指引导管,在冠脉内或病变内正向导丝穿入逆向微导管,或逆向导丝穿刺正向微导管(Pick up技术均能解决这类问题,仅在条件不允许情况下使用)[23]。
4.6 Tip-in技术指在主动脉弓处进行的Rendezvous技术,这样前向与逆向微导管在同一根指引导管内会往同一弧度贴靠,利于导丝穿入。
4.7 trap and occlude技术是导丝体外化的一种技术,其优势为可以有效的节约时间、减少射线暴露(为了透视逆向导丝在正向guiding里的位置)、避免过多的失血(因其堵塞了导引导管阻断了回流的血液,尤其在应用更大指引导管的情况下)以及稳定整个介入系统,术者可以更加从容的断开Y型接头的连接进行操作。步骤为:①逆向导丝通过闭塞段进入正向指引导管;②逆向Corsair微导管跟进至正向指引导管内;③通过正向导管送入2.5×15 mm球囊至指引导管,扩张球囊以固定微导管,应用Introducer最终完成体外化[24]。
5 结语
CTO病变在血运重建策略的选择上,必须对患者进行综合评估,在器具上选用合适的以及自己熟悉的工具,在技术上采用多种技术的融合,才能真正提高手术成功率。
