UPLC同时测定铁棒锤中6种酯型生物碱类成分的含量
2020-07-02付雪艳
张 妍,付雪艳
(1.宁夏医科大学 宁夏回药现代化工程技术研究中心,宁夏 750001;2.宁夏医科大学 宁夏回医药现代化省部共建教育部重点实验室,宁夏 750001)
铁棒锤为毛茛科乌头属植物铁棒锤AconitumpendulumBusch和伏毛铁棒锤AconitumflavumHand-Mazz,药用部位为干燥的块根[1],主要分布在中国西藏、云南、四川、甘肃、宁夏、青海、陕西[2-3]。具有活血祛瘀、通络、消肿止痛之功效,常用于跌打损伤、风湿关节疼痛、外伤肿痛等症[4-5]。铁棒锤属于毒性药材,含有苯甲酰乌头碱、苯甲酰次乌头碱、苯甲酰新乌头碱、乌头碱、次乌头碱、新乌头碱6种乌头类生物碱,既是有效成分,也是其主要毒性成分。作为陕、甘、宁等省应用较广的一种大宗民间药材,并没有相应的技术标准对其进行检测。目前,对铁棒锤中总生物碱[6-7]以及三种双酯型生物碱[8][9]的含量测定方法已有研究,但采用超高效液相色谱法同时测定铁棒锤药材中单酯型生物碱和双酯型生物碱类成分的研究国内还未见报道。本试验以铁棒锤为研究对象,首次采用UPLC法建立铁棒锤药材中3种单酯型酯和3种双酯型生物碱的含量测定方法,该方法方便、快捷,更为高效,能为快速地评价铁棒锤药材质量提供方法。
1 仪器与材料
1.1 仪器
Waters Acquity超高效液相色谱仪,PDA检测器(美国Waters公司);Merrler AL-204天平(万分之一,瑞士梅特勒公司);CPA天平(十万分之一,德国赛多利斯);KQ3200超声波清洗仪(昆山市超声仪器有限公司)。
1.2 材料
苯甲酰乌头原碱对照品(批号17102610),苯甲酰新乌头原碱对照品(批号18032406),苯甲酰次乌头原碱对照品(批号18032807),乌头碱对照品(批号17110910),新乌头碱对照品(批号17111010),次乌头碱对照品(批号17111310)均购自成都曼斯特生物科技有限公司。铁棒锤药材采自以下产地(见表1),经宁夏医科大学药学院董琳博士鉴定为乌头属植物铁棒锤AconitumpendulumBusch和伏毛铁棒锤AconitumflavumHand-Mazz干燥的块根。乙腈、冰醋酸、三乙胺均为色谱纯,乙酸乙酯、异丙醇、甲醇、盐酸均为分析纯;氨试液为化学纯;水为纯化水。

表1 铁棒锤样品来源
2 方法与结果
2.1 色谱条件
ACQUITY UPLC BEH C18(2.1 mm×50 mm,1.7 μm);流速0.4 mL·min-1;柱温35 ℃;检测波长235 nm;流动相A相为乙腈,B相为0.2%冰醋酸水溶液(三乙胺调节pH至6.2)溶液梯度洗脱(0~5 min,21%A→29%A;5~9 min,29%A→35%A;9~10 min,35%A→21%A)。在上述色谱条件下,分别吸取混合对照品溶液、供试品溶液各2 μL,注入超高效液相色谱仪。

1.苯甲酰新乌头原碱;2.苯甲酰乌头原碱;3.苯甲酰次乌头原碱;4.新乌头碱;5.次乌头碱;6.乌头碱
图1 混合对照品(A)、铁棒锤药材(B)UPLC图谱
2.2 对照品溶液制备
分别精密称取对照品适量,加0.1%盐酸甲醇配制成每mL含苯甲酰新乌头原碱40.34 μg,苯甲酰乌头原碱194.00 μg,苯甲酰次乌头原碱15.34 μg,新乌头碱53.00 μg,次乌头碱27.00 μg,乌头碱366.67 μg的混合对照品溶液,摇匀备用。
2.3 供试品溶液的制备
取本品粉末(过四号筛)约5 g,精密称定,置具塞锥形瓶中,加氨试液6 mL浸润10 min,精密加入乙酸乙酯-异丙醇(1∶1)混合溶液50 mL,称定质量,25°C以下超声处理30 min(功率300 W,频率40 kHz),放冷,称定重量,用乙酸乙酯-异丙醇(1∶1)混合溶液补足减失重量,摇匀,滤过,滤液浓缩至干。用0.1%盐酸甲醇溶解并定容于10 mL容量瓶中,摇匀,用微孔滤膜(0.22 μm)滤过,即得。
2.4 方法学考察
2.4.1 线性关系考察 精密吸取“2.2”项下混合对照品溶液0.25、0.5、1.0、2.0、3.0、5.0 mL,置于5.0 mL量瓶中,用0.1%盐酸甲醇定容至刻度,摇匀,分别注入液相色谱仪,并以峰面积(Y)为纵坐标,进样浓度(X)为横坐标,见表2。

表2 线性关系
2.4.2 精密度试验 精密吸取混合对照品溶液2μL注入液相色谱仪,连续进样6次,测得苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱、新乌头碱、次乌头碱、乌头碱峰面积的RSD分别为0.89%、0.76%、1.29%、1.45%、0.98%、0.39%。
2.4.3 重复性试验 取同一批药材(产地:宁夏固原)6份,按“2.3”项下的方法制备供试品溶液,依上述色谱条件测定,测得苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱、新乌头碱、次乌头碱、乌头碱含量平均值分别为0.063 8、0.173 1、0.011 2、0.042 9、0.021 6、0.582 2 mg·g-1,RSD分别为0.28%、0.97%、1.23%、0.86%、0.68%、0.65%。
2.4.4 稳定性试验 精密吸取同一供试品溶液2 μL,分别于0,4,8,12,18,24 h在上述色谱条件下进样测定,测得24 h内苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱、新乌头碱、次乌头碱、乌头碱峰面积的RSD分别为1.05%、0.53%、0.68%、1.33%、2.13%、1.32%。供试品溶液24 h内稳定。
2.4.5 加样回收率试验 精密称取6份已知含量的药材(产地:宁夏固原),每份约2.5 g,分别精密加入6种被测成分混合对照品溶液(苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱、新乌头碱、次乌头碱、乌头碱分别为0.032、0.086、0.056、0.021、0.011、0.290 mg),按“2.3”项下的方法制备供试品溶液,并按上述色谱条件进行测定,计算回收率。见表3。
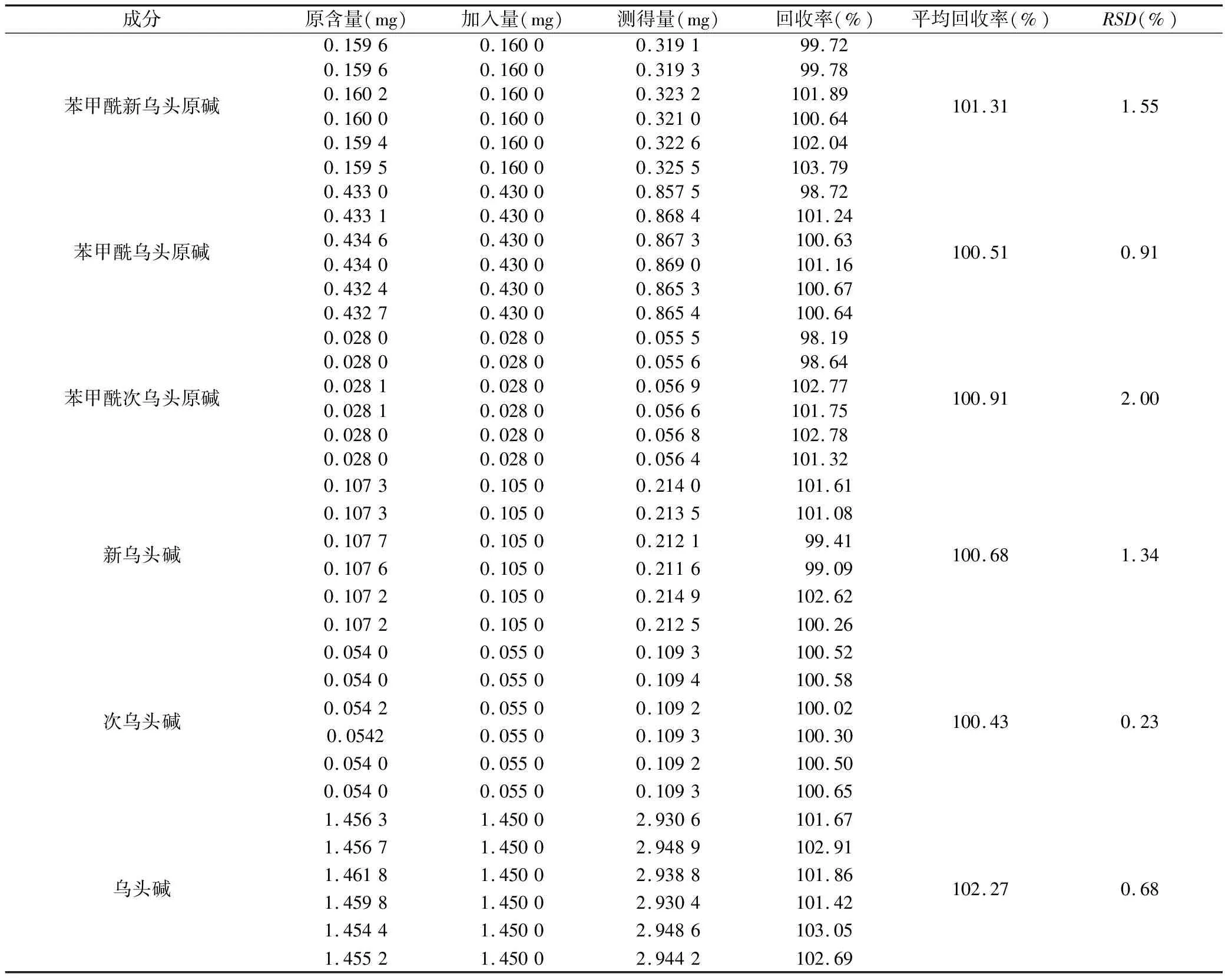
表3 回收率测定结果 (n=6)
2.5 含量测定
取11批铁棒锤药材,产地见表1,按“2.3”项下的方法制成供试品溶液。精密吸取混合对照品溶液和供试品溶液各2 μL注入液相色谱仪,按上述色谱条件进行测定,以外标法计算样品中生物碱类成分的含量。结果见表4。

表4 样品含量测定结果 (mg·g-1)
3 讨论
在流动相的选择中,考察了乙腈-磷酸水系统、乙腈-甲酸水体统、乙腈-冰醋酸水系统,发现使用冰醋酸作为抑制剂,生物碱类成分分离度良好;但乌头碱和次乌头碱很难达到基线分离,故在流动相中加入三乙胺做缓冲剂,增加两者的基线分离;后又考察了不同pH的流动相配比,最终发现用三乙胺调节pH=6.2时,色谱峰峰型对称,分离度高。故选择流动相A相为乙腈,B相为0.2%-冰醋酸水溶液(用三乙胺调节pH=6.2)。后又考察了不同梯度的洗脱过程,最终确立在此梯度洗脱(0~5 min,21%A→29%A;5~9 min,29%A→35%A;9~10 min,35%A→21%A)时6种生物碱类成分能全部分离,且与相邻色谱峰的分离度大于1.5,故选其为流动相梯度。
提取方法的选择中,曾考察采用超声、浸泡、回流等提取方式,发现回流后双酯型生物碱类成分含量大大下降,这可能与酯型生物碱受热降解有关,所以在提取过程中控制温度非常重要。在25 ℃以下超声提取30 min,和浸泡过夜样品含量差异不大,故采用快速的超声方法进行提取。在提取溶剂的选择过程中,尝试过乙醚、三氯甲烷、异丙醇-乙酸乙酯(1∶1)、无水乙醇、1%盐酸甲醇,最后发现异丙醇-乙酸乙酯(1∶1)提取的6种酯型生物碱含量最多。
在定容溶剂的选择中,发现采用三氯甲烷-异丙醇(1∶1)的溶剂时其色谱会在2~3 min左右出现一个很大的溶剂峰,色谱图基线不稳,妨碍被测成分的含量测定。用甲醇当定容溶剂时基线平稳,峰型较好,但酯型生物碱不稳定,含量会随着时间的放置而逐渐降低[10]。故采用0.1%盐酸甲醇作为定容溶剂,既没有溶剂峰的影响,又能保持有效成分的稳定性。
由于本实验配置的混合对照品溶液中乌头碱线性范围为18.334~366.67 μg·mL-1,部分被测样品不在此线性范围内。故另外配置乌头碱对照品溶液1.812 mg·mL-1,精密吸取对照品溶液0.1、0.25、0.5、1.0、2.0、5.0 mL置于5.0 mL量瓶中,用0.1%盐酸甲醇定容至刻度,摇匀,分别注入液相色谱仪,并以峰面积(Y)为纵坐标,进样量(X)为横坐标,进行线性回归,求得乌头碱线性回归方程为Y=2 223.98X-4274.71,R2=0.999 0;在36.24~1812 μg·mL-1范围内,进样质量浓度与峰面积呈良好线性关系,待测样品符合要求。
本实验样品来源范围较广,不同产地铁棒锤药材中生物碱类成分含量差异较大,与产地的环境因素、采收期等有着密切的关系。本实验采用UPLC法在10 min内对11批铁棒锤药材中6个主要酯型生物碱类成分进行定量分析,过程简单、快捷,能更加全面、客观,可科学评价铁棒锤药材的质量。
