2,5-二甲基苯甲酰甲基酯合成方法的优化
2020-08-26张俊杰
李 萱,张俊杰
(1.巴音郭楞职业技术学院,新疆 库尔勒 841000;2.华北理工大学,河北 唐山 063009)
苯甲酰甲基类物质作为羧基保护基,具有一定的光化学性能。1962年Sheehan[1]的报道中就提到,在具有氢给体能力的溶剂中,或在苯中加入具有氢给体能力的溶剂,对-甲氧基苯甲酰甲基表现出良好的光化学反应活性,可以作为保护基应用。Falvey等[2-3]认为,脱羧反应是一个快速过程,均裂发生后,如果脱羧后的产物是一个稳定的自由基(如苯甲基自由基),则脱羧反应为主要反应。Klan[4-5]在研究2,5-二甲基苯甲酰甲基作为羧酸的保护基时发现,2,5-二甲基苯甲酰甲基酯在光解时发生烯醇化反应而放出羧酸。羧基是一个较氯原子更好的离去基团[6-7]。
本文首先利用傅-克酰基化反应,制得2-5-二甲基苯甲酰甲基氯,再使其在以DBU为催化剂的情况下,成功合成了2,5-二甲基苯甲酰甲基酯。在合成保护基和优化酯化方法后发现,以DUB为催化剂,不仅可以大大提高酯化反应的速度,蒸发干燥后,产物的产率也更高(苯甲酸-2,5-二甲基苯甲酰甲基酯产率高达90%以上),产物底色不深,为下一步的光解反应释放羧酸提供了可能。酯化合成中所用的酸有乙酸、苯甲酸、苯乙酸和月桂酸,可以代表各种脂肪酸和芳香酸。
1 实验部分
1.1 仪器与试剂
Bruker-300 MHz核磁共振谱仪,HP 6890SERIAL气相色谱仪,Bruker EQUINOX 55 红外光谱分析仪。
二甲苯、三甲苯、氯乙酰氯、三氧化铝、乙酸、苯甲酸、苯乙酸、月桂酸、苯、石油醚(均为分析纯)。
1.2 取代苯甲酰甲基氯的合成
吸取石油醚15mL置于50mL四口烧瓶中,加入9.50mL对二甲苯和3.0mL氯乙酰氯(1.0eq),在氮气保护下,加入5.5g无水三氯化铝,在电磁搅拌和冰浴条件下,反应1h,然后在室温条件下搅拌2h。反应方程式见图1。
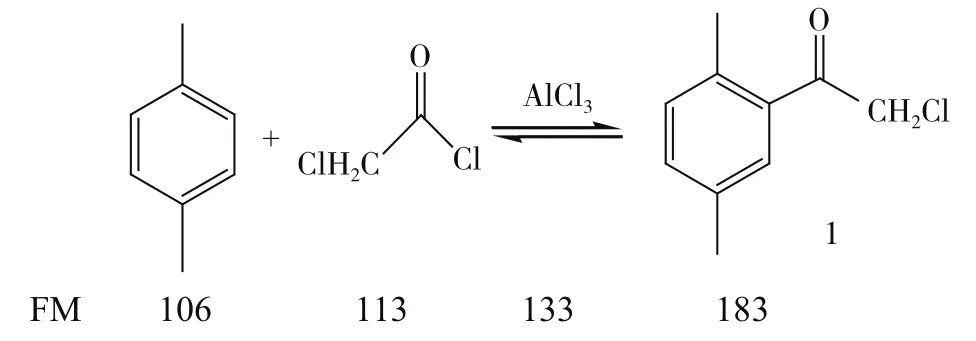
图1 2,5-二甲基苯甲酰甲基氯的合成
2,5-二甲基苯甲酰甲基氯,白色晶体,mp. 34~35℃。IR (KBr),υ/cm-1:3021(υCH,Ar-H),2983,2937(υCH,-CH3),1699(υC=O,C=O),1568,1494(υC=C,Ar),1440(δCH,-COCH2-),829,794(δCH, Ar-H)。1H-NMR(300MHz):δ 7.41 (1H,s,H-6),7.26~7.16(2H, m,H-3,4),4.64 (2H, s, CH2),2.47(3H,s,CH3-5),2.37(3H,s,CH3-2)。13C NMR(75.5 MHz,CDCl3):δ 194.23,136.10,135.34,134.46,132.99,132.13,129.06,47.89,20.81,20.73。MS (EI),m/z(rel. intensity):182(5)(M+),133(100),105(55),79(25),51(5)。tR=10.50 min;Anal. Calcd for C10H11ClO:C 65.76,H 6.07,Cl 19.41,O 8.76; Found: C 65.36,H 6.03,Cl 19.14。
1.3 2,5-二甲基-苯甲酰甲基酯的合成
2,5-二甲基苯甲酰甲基酯的合成可以有两种途径。第一种方法是在碘化钠和三乙胺的存在下,α-氯-2,5-二甲基苯乙酮和相应酸的钠盐在丙酮中回流,反应4h,产率在65%~80%之间,反应方程式见图2。这个用酸本身来代替相应钠盐的反应进行得并不完全。

图2 2,5-二甲基苯甲酰甲基氯的酯化反应
第二种方法是以DBU为催化剂,在苯或甲苯溶剂中回流。此时,无论用酸还是其钠盐,所得的产率均较高,一般可以达到定量反应(TLC板监测)。本实验以DUB为催化剂直接进行反应。
1.3.1 乙酸-(2,5-二甲基)-苯甲酰甲基酯的合成
分别称取(2,5-二甲基)-苯甲酰甲基氯300mg(1.0eq)和碘化钠325mg(1.2eq)于25mL圆底烧瓶中,加入15mL苯或甲苯为溶剂,依次再加入0.2mL(2.0eq)冰乙酸和 0.2mL DBU(15d,2.0eq),加热回流。反应时间3h,反应方程式见图3。

图3 乙酸-(2,5-二甲基)-苯甲酰甲基酯的合成
乙酸-(2,5-二甲基)-苯甲酰甲基酯:IR(KBr):2926,1750,1701,1372,1231,1080,966,819,788。1H NMR(300 MHz,CDCl3):δ 7.37(s,1H),7.17(d,J=7.535,1H),7.10(d,J=7.535,1H),5.10(s,2H),2.41(s,3H),2.31(s,3H),2.15(s,3H)。13C NMR(75.5 MHz,CDCl3):δ 195.57,170.13,135.57,135.11,134.11,132.65,131.89,128.37,67.08,20.60,20.36,20.26。MS (EI),m/z (rel. intensity): 206(M+),163(4),146(8),133(100),105(60),77(20) ,51(5)。tR=11.55 min。
1.3.2 苯甲酸-(2,5-二甲基)-苯甲酰甲基酯的合成
分别称取(2,5-二甲基)-苯甲酰甲基氯300mg(1.0eq)、碘化钠 325mg(1.2eq)于 25mL圆底烧瓶中,加入15 mL苯或甲苯为溶剂,再加入240mg(1.2eq)苯甲酸和 0.1mL 的 DBU(10d,1.2eq),加热回流反应3h。反应方程式见图4。
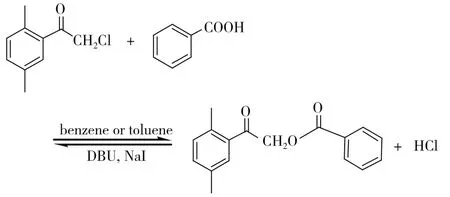
图4 苯甲酸-(2,5-二甲基)-苯甲酰甲基酯的合成
苯甲酸-(2,5-二甲基)-苯甲酰甲基酯:IR(KBr):3060,3031(υCH,Ar-H),2945,2921(υCH,-CH3),1731(υC=O,羧基 C=O),1698(υC=O,苯乙酮,C=O),1599,1560(υC=C,Ar),1448,1421(δCH,-COCH2-),1272(υC-O-C,羧基-CO-C-),883,817,782(δCH,Ar-H)。1H NMR(300 MHz,CDCl3):δ 8.14 (2H,d,H`-2,6,J=7.535),7.58(1H,t,H`-4,J=6.782),7.50~7.44(3H,m,H-5,H`-3,5),7.24(1H,d,H-4,J=7.535),7.15(1H,d,H-3,J=8.289),5.42(2H,s,CH2),2.50(3H,s,CH3-5),2.37(3H,s,CH3-2)。13C NMR(75.5 MHz,CDCl3):δ 195.67,166.00,135.84,135.31,134.36,133.24,132.85,132.09,129.88,129.44,128.64,128.37,67.65,20.83,20.61。MS (EI),m/z (rel. intensity):268(M+),209(2),163(5),146(25),133(100),105(50),77(25),51(8)。tR=15.70 min。Anal. Calcd for C17H16O3:C 76.10,H 6.01,O 17.89;Found:C 75.92,H 6.05。
1.3.3 苯乙酸-(2,5-二甲基)-苯甲酰甲基酯的合成
分别称取(2,5-二甲基)-苯甲酰甲基氯300mg(1.0eq)、碘化钠 325mg(1.2eq)于 25mL圆底烧瓶中,加入15mL苯或甲苯为溶剂,再加入266mg(1.2eq)苯乙酸和 0.1mL DBU(10d,1.2eq),加热回流反应3h,反应方程式见图5。

图5 苯乙酸-(2,5-二甲基)-苯甲酰甲基酯的合成
苯乙酸-(2,5-二甲基)-苯甲酰甲基酯:IR(KBr):2963,2928,1746,1695,1497,1240,1145,968,819,711。1H NMR(300 MHz,CDCl3):δ 7.38(s,1H),7.36~7.27(m,5H),7.24(d,J=8.289,1H),7.16(d,J=7.535,1H),5.18(s,2H),3.82(s,2H),2.48(s,3H),2.35(s,3H)。13C NMR(75.5 MHz,CDCl3):δ195.84,170.94,135.56,135.18,134.32,133.49,132.69,131.92,129.26,128.46,127.04,67.57,40.68,20.72,20.38。MS (EI),m/z (rel. intensity):282(M+),264(1),191(2),164(8),146(25),133(100),105(40),91(20),79(15),65(5)。tR=16.06 min。
1.3.4 月桂酸-(2,5-二甲基)-苯甲酰甲基酯的合成
分别称取(2,5-二甲基)-苯甲酰甲基氯300mg(1.0eq)、碘化钠 325mg(1.2eq)于 25mL圆底烧瓶中,加入15mL苯或甲苯为溶剂,再加入400mg(1.2eq)月桂酸和 0.1mL DBU(10d,1.2eq),加热回流反应3h。反应方程式见图6。
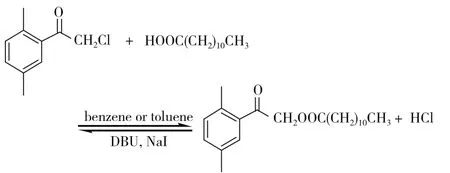
图6 月桂酸-(2,5-二甲基)-苯甲酰甲基酯的合成
月桂酸-(2,5-二甲基)-苯甲酰甲基酯:IR(KBr):2924,2852,1746,1702,1240,1158,968,817,721。1H NMR(300 MHz,CDCl3):δ 7.38(s,1H),7.19(d,J=8.289,1H),7.13(d,J=7.535,1H),5.14(s,2H),2.47~2.42(m,5H),2.34(s,3H),1.71~1.61(m,2H),1.26(broad s,16H),0.87(t,J=6.825,3H)。13C NMR(75.5 MHz,CDCl3):δ 196.09,173.10,135.57,135.14,134.46,132.62,131.92,128.46,67.06,33.79,31.82,29.52,29.36,29.25,29.18,28.99,24.77,22.59,20.72,20.38,14.00。MS(EI),m/z (rel. intensity):364(M+),315(1),281(1),164(3),147(8),133(100),105(20),79(6) 。tR=17.88min。
2 结果与讨论
试液加水少许,转移到分液漏斗中,用30mL甲苯萃取后,用水洗,再用饱和碳酸氢钠水溶液、饱和氯化钠水溶液各洗涤2次,无水硫酸钠干燥过夜后,再次过滤,旋转蒸发。用二氯甲烷溶解合成的酯样,以石油醚∶乙酸乙酯=10∶1为洗脱剂,过柱分离,旋转蒸发脱除溶剂,真空干燥后,制得4种类型的2,5-二甲基-苯甲酰甲基酯,最终的产率见表1。

表1 不同类型的酸合成苯甲酰甲基酯产率
从表1可以看出,用不同的酸与2,5-二甲酰甲基氯反应,都能得到较高产率的2,5-二甲基苯甲酰甲基酯,产率的高低顺序为:苯甲酸>乙酸>苯乙酸>肉桂酸。除苯甲酸-(2,5-二甲基)-苯甲酰甲基酯为固体外,其他3种产物均为液体。
3 结论
以DBU作为酯化反应的催化剂,不仅可以顺利合成目标产物,且反应步骤短,保护羧酸的速度加快,反应产物的颜色更浅。其中,苯甲酸-(2,5-二甲基)-苯甲酰甲基酯为固体,更有利于结晶分离,且更容易进行下一步的光解实验及产物结构的鉴定,可为光致脱保护实验提供优质原料。
