“杂交”策略开通冠状动脉慢性完全闭塞病变1 例
2020-06-18吴玺张琪周蔡杰谭国娇黄河
吴玺 张琪周 蔡杰 谭国娇 黄河
1 临床资料
患者 女,69岁。因“反复胸闷1年余”入院,患者诉1年多前,步行1000 m或爬3楼后出现胸闷不适,部位为心前区,呈憋闷感,持续10 min左右,含服硝酸甘油后症状逐渐好转,但症状于活动后反复出现。患者为求进一步治疗曾于2018年3月于外院住院治疗,行冠状动脉造影发现左前降支出现慢性完全闭塞(chronic total occlusion,CTO)病变,并行经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI),但失败。术后出院规律服用抗血小板聚集、调脂、抗心肌重构等药物,胸闷症状仍反复发作,现患者为求再次行PCI于2018年6月21日就诊于湖南省湘潭市中心医院。既往有高血压病和高脂血症病史。入院查体:体型匀称,血压130/82 mmHg(1 mmHg=0.133 kPa),颈动脉不充盈;心界向左下扩大,心率82次/min,律齐,心脏听诊区无杂音;腹部未见明显异常,四肢外周动脉搏动可,双下肢无水肿。实验室检查示:肝、肾功能均正常。心电图示:窦性心律,ST-T改变,V1~V4导联呈qrS、qRs型。超声心动图示:节段性室壁运动异常;左心房、左心室扩大;主动脉瓣退行性钙化并狭窄(轻度)、关闭不全(轻度);二尖瓣后叶瓣环退行性钙化并二尖瓣关闭不全(轻中度);三尖瓣反流(少量);左心室收缩功能减低,左心室舒张功能减低(Ⅰ级);左心房内径45 mm,左心室舒张末期内径62 mm,右心房内径34 mm,右心室舒张末期内径18 mm,左心室射血分数40%。
患者因仍有胸闷症状,故再次尝试使用介入手术开通左前降支CTO病变。80~100 U/kg的普通肝素经右侧桡动脉血管鞘内注入体内后,经右侧桡动脉鞘送6 F JR 4.0指引导管至右侧冠状动脉开口,经右侧股动脉鞘送7 F EBU 3.75指引导管至左侧冠状动脉开口,活化凝血时间(activated clotting time,ACT)维持在250~350 s。通过冠状动脉造影发现,左前降支近段为CTO病变(J-CTO评分2分)[1],并且第二对角支(the second diagnoal branch,D2)的开口位于CTO病变处,该对角支走行扭曲并存在狭窄(图1A)。图1B白色箭头所示有两处可疑的CTO病变残端入口,但通过造影图像还不能确定真正的CTO病变残端入口点。为了确认真正的残端入口点,并指导导丝穿刺进入到CTO病变内部,我们使用血管内超声(intravascular ultrasound,IVUS)指导手术进行。
手术过程如下:将一根Sion(朝日,日本)导丝送入D2内。沿Sion导丝送入IVUS探头(40 MHz OptiCrosstm,波士顿科学,美国),IVUS在D2内回撤过程中发现残端入口后,将IVUS探头固定于残端部位,再通过多体位造影确定病变残端部位(图2)。以造影图像为指导,在Crusade分叉微导管(Kaneka Corp)的支撑下,先后正向尝试Fielder XT-R(朝日,日本)、CS PJ08008(和心伊达,日本)和Pilot 150(雅培,美国)导丝穿通CTO病变,但导丝均进入了假腔(图3A)。故尝试使用逆向技术开通CTO病变。通过150 cm Corsair微导管(朝日,日本)对间隔支进行选择性造影后,发现有一条走行为“b”字型间隔支血管连通右侧冠状动脉与左前降支中段(图3B)。操作Sion导丝(朝日,日本)和Corasair微导管通过该间隔支到达左前降支CTO病变远端(图3C)。使CD 14045导丝(和心伊达,日本)在Corsair微导管的支撑下,通过CTO病变闭塞段(图3D)。从D2内开始回撤IVUS导管至左前降支开口(图4A),发现逆行导丝从CTO病变近端真腔内穿出(图4A~C)。使用RG3(朝日,日本)进行导丝体外化后,对CTO病变部位进行球囊预扩张,并置入3枚药物洗脱支架(图5)。最终造影及IVUS图像显示左前降支CTO病变闭塞解除。患者于术后第3天病情稳定出院。出院后3个月每个月门诊复查1次,一般情况良好。

图1 冠状动脉造影图像 A.基线造影发现左前降支近段为慢性完全闭塞病变;B.两个箭头所指为可能的病变残端入口

图2 用IVUS寻找CTO病变残端位置 A.造影发现IVUS探头所在位置即CTO病变残端部位(距分叉口隆起1.5 mm的地方);B.IVUS横轴影像发现合适的病变入口

图3 导丝逆向通过CTO病变 A.双侧造影提示正向导丝位于左前降支假腔中;B.通过Corsair微导管对间隔支进行选择性造影后,发现有一条“b”字型间隔支连通右侧冠状动脉与左前降支中段;C.Sion导丝和Corsair微导管通过间隔支到达CTO病变远端;D.在Corsair的支撑下CD 14045导丝逆向穿通CTO病变进入左前降支近段
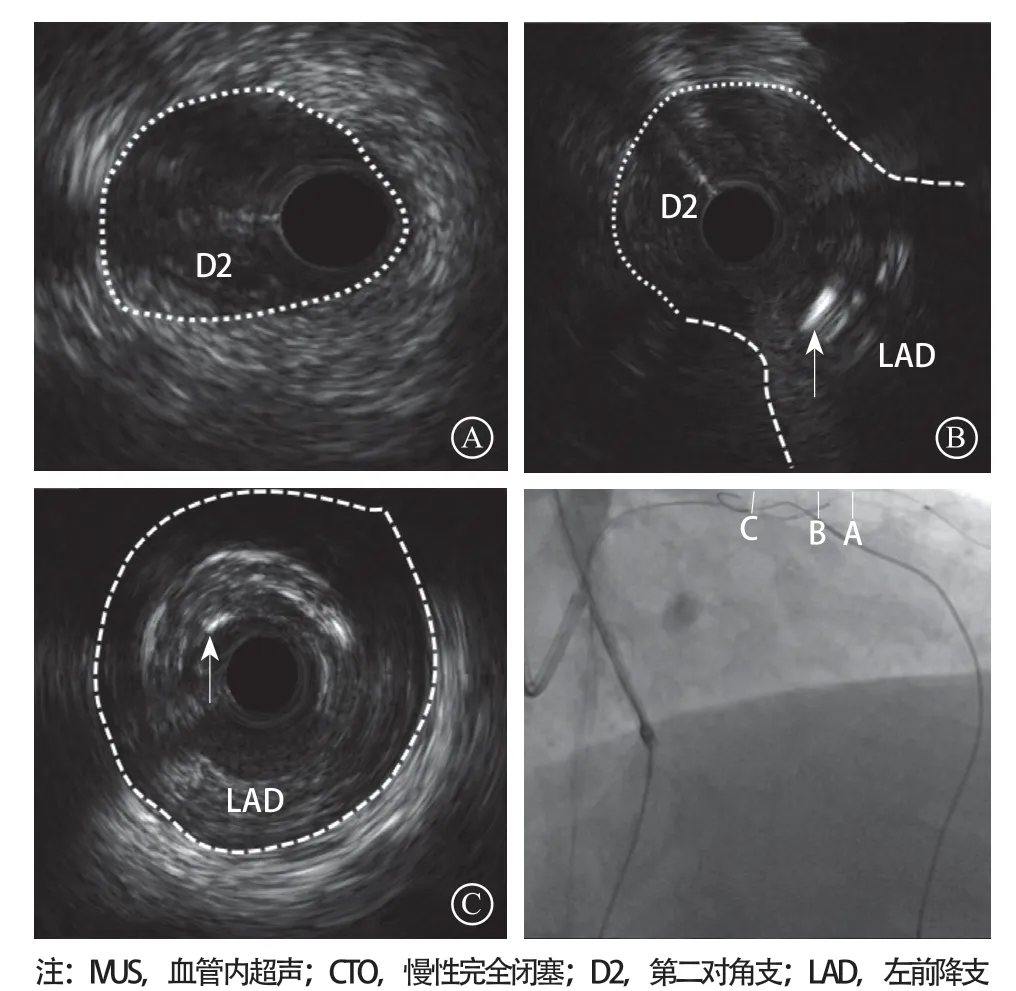
图4 IVUS证实逆向导丝通过CTO病变 A.从D2开始回撤IVUS导管至LAD开口;B~C.逆行导丝(白色箭头所指)从CTO病变近端真腔内穿出
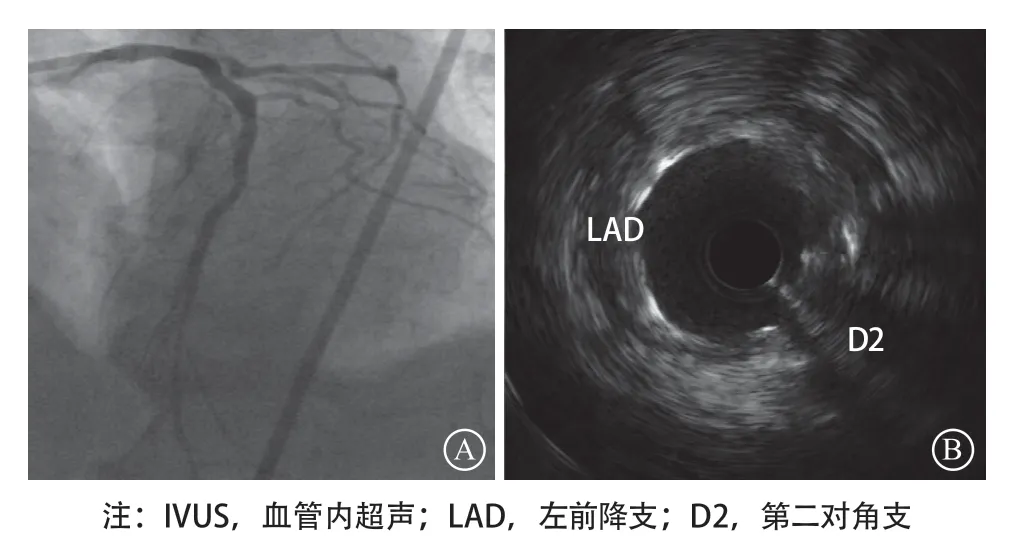
图5 左前降支开通后造影及IVUS图像 A.左前降支开通后造影图像;B.左前降支支架内IVUS图像
2 讨论
冠状动脉CTO病变是指远端血流心肌梗死溶栓治疗试验(thrombolysis in myocardial infarction,TIMI)血流分级0级且闭塞时间超过3个月的冠状动脉阻塞性病变,如果存在同侧桥侧支或同侧侧支血管,尽管闭塞远端血管TIMI血流分级>0级,仍视为完全闭塞病变[2-3]。由于导丝无法顺利穿通CTO病变[4],CTO病变行PCI术的成功率较低[5]。在过去的数十年中,很多介入治疗技术(例如逆向技术[6-8]和正向夹层再入真腔技术[9-10])被开发应用,使得手术成功率较前明显提高。“杂交”手术策略采用所有可用技术(正向、逆向、真腔-真腔和夹层再入真腔技术),可更加安全、有效及快速地开通CTO病变[11-13]。虽然冠状动脉造影已经是判断冠状动脉粥样硬化和指导PCI术的“金标准”,但是IVUS能准确发现CTO病变残端的具体位置[14-15],也能指导导丝从假腔重新进入真腔内[15]。本病例展示了通过IVUS寻找无残端CTO病变的残端部位,并指导导丝扎入近端纤维帽内;同时,采用“杂交”策略顺利完成手术。
导致CTO-PCI手术失败的最常见原因是导丝无法顺利通过CTO病变[5]。在开通CTO病变过程中,从合适的部位“扎入”近端帽也是非常重要的。但是,若出现无残端CTO病变时,术者仅通过造影图像难以准确地发现病变入口。在本病例中,我们将IVUS送入病变残端附近的分支血管中,在回撤过程中确定残端的位置,并指导导丝“扎入”CTO病变近端帽。
在本病例中,虽然IVUS能找到合适的残端入口,但是正向导丝在前进过程中,无可避免地进入了假腔。之后,我们立即尝试逆向开通CTO病变,并最终完成手术。在经验丰富的CTO-PCI术者中,运用“杂交”策略进行手术就是灵活地运用各种开通技术(正向、逆向、真腔-真腔和夹层再入真腔技术)以最安全、高效的方式开通CTO病变。“杂交”策略的基本原则是目前没有一种手术策略能解决所有的CTO病变,当某一种开通技术无法顺利完成手术时,此时应及时更改手术策略以完成手术[13]。因此,采用“杂交”策略开通CTO病变,不仅是为了提高手术成功率,更重要的是运用目前所拥有的介入治疗技术以更高效的方式完成手术[16]。手术过程中,适时更改合适手术策略能更高效地开通CTO病变。更早地变更手术策略也许能更快地完成手术。Kimura等[17]发现,在224例采用逆向技术开通CTO病变的患者中,其技术成功率和手术成功率分别为92.4%和90.6%。Tsuchikane等[18]报道,在2名介入医师中,93例患者使用逆向技术的成功率为98.9%。Rathore等[19]报道,在31例使用IVUS指导反向内膜下寻径技术的患者中,其手术成功率达100%。从多中心收集的病例中发现,1361例CTO病变患者,在使用“杂交”策略完成手术之前,其技术成功率仅为85.4%[20]。因此,虽然目前CTO-PCI的总体成功率较前有所提高,但是采用“杂交”策略完成手术能进一步提高手术成功率与效率。
处理无残端CTO病变时,IVUS能有效帮助术者找到残端入口。此外,适时运用“杂交”手术策略能有效提高手术成功率与效率。
