右美托咪定用于硬膜外镇痛联合无保护会阴接生对子痫前期孕妇围产结局的影响
2020-06-08杨丽丽贾燚鑫冯小明武启芸皇甫彪
么 爽,杨丽丽,贾燚鑫,冯小明,武启芸,皇甫彪,王 婧
0 引言
子痫前期为妊娠期常见并发症,常造成不良妊娠结局,以往多采取适时终止妊娠进行处理[1-3]。但近年来,随着分娩镇痛技术的不断进步,采取阴道分娩的子痫前期患者日益增多,对于宫颈条件成熟、胎儿较小、经药物治疗后症状好转、产程已发动的子痫前期孕妇,可在严密监护下行阴道分娩[4]。无保护会阴接生充分利用了产妇妊娠后期会阴体的良好弹性,通过胎头对会阴进行扩张,可减少人为干预,减轻分娩创伤,在子痫前期阴道分娩孕妇中广泛应用[5]。良好的分娩镇痛是确保产妇分娩舒适度、新生儿安全出生的前提,其中硬膜外分娩镇痛是最常用、最成熟的分娩镇痛方法。右美托咪定为高选择性α2受体激动剂,研究发现,其与局麻药共用可发挥协同镇痛作用,同时具有清醒镇静、抑制肌颤、胎盘转移率低等优点,具有较大的临床价值[6]。本研究以108例待产的子痫前期孕妇为例,探讨右美托咪定用于硬膜外镇痛联合无保护会阴接生对围产结局的影响,现报道如下。
1 资料与方法
1.1 基本资料 选取唐山市妇幼保健院产科2016年9月至2018年9月收治的108例待产的子痫前期孕妇,按随机数表法分为观察组与对照组,各54例。
纳入标准:①符合《妇产科学(第九版)》[7]中子痫前期诊断标准:妊娠20周后出现收缩压≥160 mmHg 和(或)舒张压≥110 mmHg,蛋白尿≥0.3 g/24 h;②于本院分娩,初产妇,单胎、头位;③具备经阴道分娩条件;④ASA分级Ⅰ、Ⅱ级;⑤孕35~39周;⑥对研究知情,签署知情同意书。
排除标准:①多胎产妇;②胎儿异常者;③对局部麻醉药物过敏者;④伴神经、肌肉或神经学病变的产妇;⑤有先兆子痫、瘢痕子宫的产妇;⑥伴心理障碍或精神障碍者;⑦伴其他妊娠合并症者;⑧早产产妇;⑨头盆不称、有椎管内麻醉禁忌证的产妇。
两组基线资料比较差异无统计学意义(P>0.05),具有可比性。见表1。
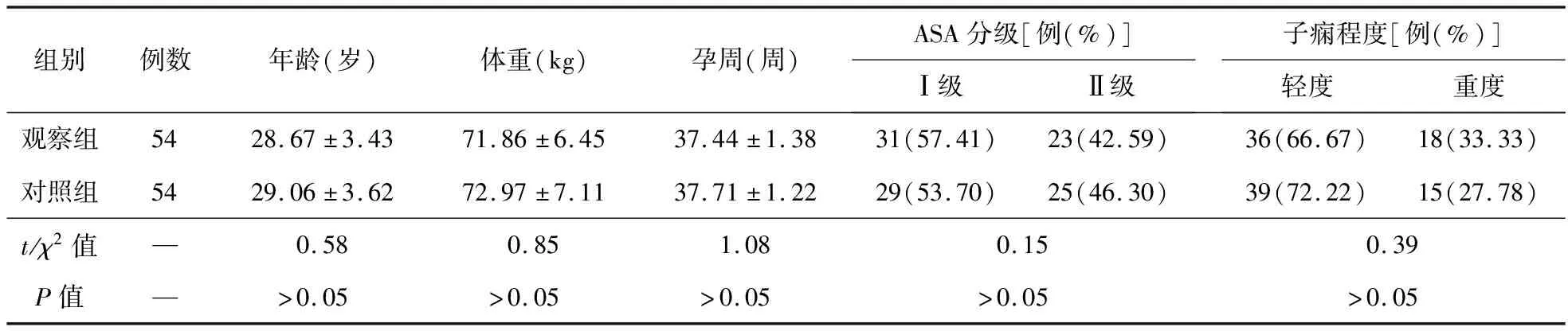
表1 两组孕妇一般资料的比较
1.2 方法 两组产妇均术前禁食8 h,禁饮2 h,入室后面罩吸氧4 L/min,开放外周静脉通路,静脉输注复方乳酸钠林格氏液(5 ml/kg)扩容,常规监测心电图、心率、血压和血氧饱和度。
1.2.1 无保护会阴接生 产妇宫口开全后指导其均匀用力,使每次用力时胎头娩出1 cm左右。当胎头拔露5 cm×4 cm左右时,指导产妇放松全身肌肉,使胎头在宫缩间歇期缓慢娩出,待娩出胎儿双顶径后,保持胎头自然仰伸,控制胎头娩出速度,分娩全程助产士无需协助胎头进行俯屈。娩出胎头后由助产士双手托住胎头,等待至少1次自然宫缩,嘱产妇配合宫缩用力,至胎肩自行内旋后,前肩娩出。宫缩时双手托举胎头并轻微上抬,使胎后肩缓慢娩出。
1.2.2 硬膜外麻醉 于两组产妇宫口开至2~3 cm时,经L3~L4间隙硬膜外间隙穿刺,达硬膜外腔后,若回抽无脑脊液与血液,则给药物。麻醉诱导:观察组用0.1%罗哌卡因10 ml+0.5 μg/kg右美托咪定5 ml,对照组用0.1%罗哌卡因10 ml+生理盐水5 ml。麻醉维持:罗哌卡因50 mg+生理盐水至50 ml配置成药液,输注速度5 ml/h。术中血压低于术前基础值30%时,静脉予去氧肾上腺素0.05~0.10 mg;心率低于60次/min时,静脉予阿托品0.2~0.5 mg;血氧饱和度低于90%时,面罩加压给氧。
1.3 观察指标
1.3.1 镇痛效果 记录硬膜外镇痛起效后15 min、30 min、45 min的疼痛程度,采用视觉模拟评分法(Visual analogue scale,VAS)评估疼痛,0分为无痛,10分为难忍的剧痛,VAS评分越高,疼痛越明显。
1.3.2 围产结局 比较两组第一产程,第二产程,新生儿出生后1 min、5 min的Apgar评分,产钳助产率。
1.3.3 血清学检测 分别于临产时、分娩后1 h采集5 ml外周静脉血,2 500 r/min离心15 min。采用硝酸还原酶法测定血清NO水平,ELISA法测定血清E与NE水平,试剂盒购自上海双赢生物科技。
1.3.4 不良反应 记录两组不良反应发生情况(瘙痒、恶心呕吐、低血压、呼吸抑制、心动过缓、尿潴留),①低血压:血压低于基础值20%以上;②心动过缓:心率<60次/min;③呼吸抑制:吸氧时血氧饱和度≤94%或呼吸频率≤10 次/min。
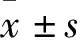
2 结果
2.1 镇痛效果 观察组镇痛后15 min、30 min、45 min的疼痛VAS评分显著低于对照组(P<0.05)。见表1。
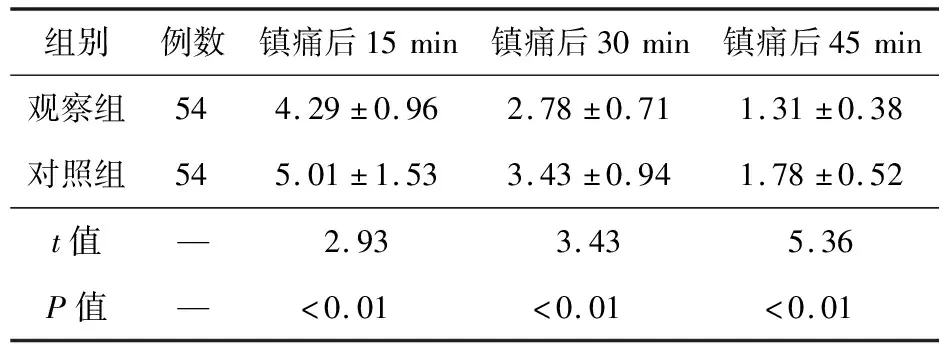
表1 两组孕妇疼痛VAS评分的比较(分)
2.2 产程与新生儿Apgar评分 两组产妇第一产程、第二产程、新生儿出生1 min与5 min的Apgar评分以及产钳助产率比较差异均无统计学意义(P>0.05)。见表2。
2.3 血清学指标 两组临产时的血清NO、E、NE比较差异无统计学意义(P>0.05)。分娩后1 h,两组血清NO、E、NE均大幅升高(P<0.05)。观察组分娩后1 h的血清NO、E、NE显著低于对照组(P<0.05)。见表3。
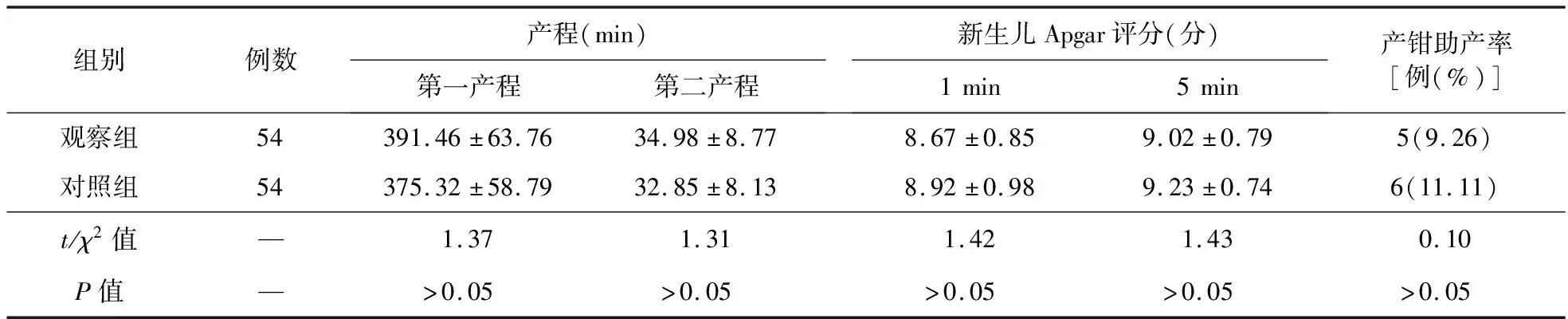
表2 两组孕妇产程与新生儿Apgar评分比较

表3 两组孕妇血清NO、E、NE比较
注:与临产时比较,*P<0.05
2.4 血清学指标 两组均未见严重低血压与呼吸抑制,不良反应总发生率比较差异无统计学意义(P>0.05)。见表4。
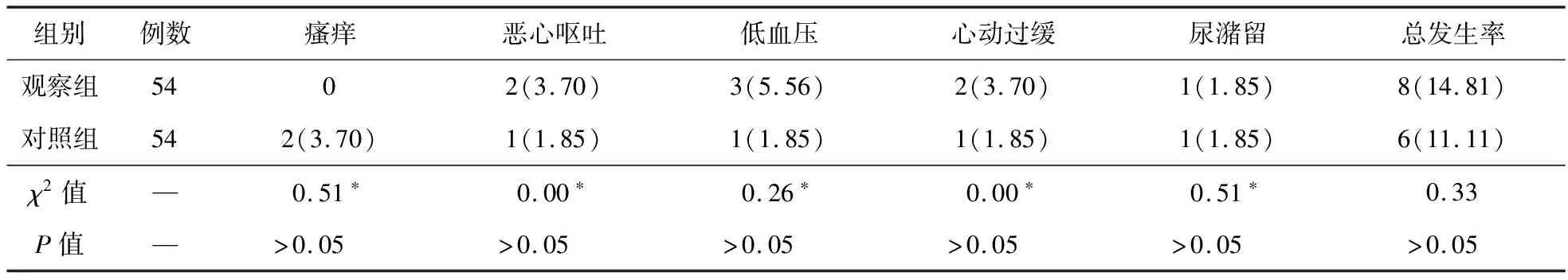
表4 两组孕妇不良反应的比较[例(%)]
注:*表示连续校正χ2检验
3 讨论
无保护会阴接生技术可有效减轻会阴裂伤、减少会阴侧切,得到临床认可。研究发现,硬膜外镇痛联合无保护会阴分娩可有效减轻分娩疼痛,缓解产妇生产时的不安和紧张,减轻心理应激,对促进子痫前期孕妇的顺利分娩有重要意义[8-9]。
本研究两组产妇均采取硬膜外镇痛联合无保护会阴接生,其中观察组在硬膜外镇痛基础上联合右美托咪定。结果显示,镇痛起效后的15 min、30 min、45 min,观察组的疼痛VAS评分均低于对照组,提示右美托咪定的应用有利于进一步减轻分娩疼痛。产妇分娩过程中,宫颈与子宫下段的收缩会对形成疼痛刺激,由交感神经内感觉神经传入,经下腹部与宫颈神经丛进入腰部交感丛,并传至胸-腰段[10]。此外,分娩过程会伴随会阴部位牵拉,经会阴神经将疼痛刺激传至脊髓骶水平。右美托咪定可对蓝斑核起到催眠与镇静作用,对脊髓后角也有抵抗有害性刺激的作用,并经中枢和外周途径降低交感神经活性,以减轻疼痛带来的刺激[11-12]。药物浓度监测结果显示,右美托咪定进入体内后,稳态分布容积约173 L,并可在10 min内起效,25 min左右达峰值,半衰期3 h左右,因此可在子痫前期孕妇的分娩全程发挥镇痛作用[13],这是观察组镇痛起效后15 min、30 min、45 min的疼痛VAS评分低于对照组的主要原因。也有研究表明,右美托咪定一方面可直接抑制外周神经上动作电位的发生,另一方面可与中枢神经元上的受体结合,抑制疼痛信号的传递,可有效增强镇痛效应[14],与本研究结论相符。
有研究认为,右美托咪定可加强子宫肌层收缩强度与频率,加速产妇的自然分娩进程,缩小产程[15]。但本研究中,两组的第一产程、第二产程均未见明显差异,考虑与无保护会阴接生侧重于利用会阴顺展性进行分娩,减少了人为干预,使右美托咪定对产程进展的影响并未得到凸显有关,详细原因有待进一步探讨。两组新生儿出生后1 min与5 min的Apgar评分以及产钳助产率均较为接近,提示右美托咪定的应用不会对新生儿造成明显影响,原因在于右美托咪定在新生儿体内消除快,因此,新生儿出生后Apgar评分未受明显影响。研究发现,疼痛刺激会导致子宫平滑肌缺血,引起血清NO、E、NE水平的异常上调,主要与疼痛引起的应激反应有关[16]。NO是一种信号分子,可传递神经介质与分子。目前认为,NO可作为疼痛介质提高疼痛阈值,故NO水平越高,疼痛感越强烈[17]。血清E、NE则与机体疼痛程度有关,疼痛刺激越明显,体内儿茶酚胺、E、NE分泌的越多,越易造成血液动力学、免疫等方面的不利改变。右美托咪定还可发挥中枢性抵抗交感的作用,对产妇的镇静效果与自然睡眠类似,不仅可强化镇痛作用,还可抵抗焦虑、减轻应激,因而观察组分娩后1 h的血清NO、E、NE水平均更低。
此外,右美托咪定主要经粪便、尿液消除,且不影响产妇肾功能,不良反应轻微。也有研究发现,右美托咪定不会产生呼吸抑制,对产妇脑、心和肾等器官还有一定保护作用[18]。本研究中,两组的不良反应总发生率比较差异无统计学意义,提示右美托咪定用于子痫前期孕妇的安全性较高。有报道,右美托咪定的主要不良反应包括低血压、心动过缓等[19]。本研究中,两组上述不良反应均较少且轻微,考虑与右美托咪定是硬膜外腔给药,药物不会直接进入循环有关。
综上所述,右美托咪定用于硬膜外镇痛联合无保护会阴接生可有效增强镇痛效果,减轻产妇应激,且对新生儿无不利影响,不良反应少。
