口服降糖药处方中代谢酶和转运体介导的药物相互作用的调查分析
2020-06-08邢亚群
张 莉,汪 龙,邢亚群,程 军
0 引言
当一种药物的药动学或药效学受到另一种同时使用的药物影响时即会发生药物相互作用(Drug-drug interactions,DDIs)[1]。DDIs可能导致药物不良反应的发生,甚至可成为患者住院治疗或住院时间延长的原因[2]。近年来,基于生理药代动力学(Physiologically based pharmacokinetic,PBPK)模型的研究越来越多地用于预测潜在DDIs的发生,其中以模拟细胞色素P450(CYP)酶和转运体介导的DDIs的研究最为多见[3]。糖尿病是一种复杂、慢性的代谢性疾病,在我国以2型糖尿病为主,且往往伴有高血压、心脏病和肾病等慢性疾病,故患者在应用口服降糖药的同时常合并使用其他药物,导致潜在DDIs的发生风险明显增加[4-5]。本研究以药代动力学为指导,从药物代谢酶及转运体方面调查蚌埠医学院第二附属医院门诊口服降糖药处方中的联合用药情况,并对其进行统计分析,发现潜在的DDIs,为口服降糖药的合理应用提供参考。
1 资料与方法
1.1 资料来源 利用医院信息管理系统(HIS)调取我院(三级甲等综合性医院,开放床位1 000张)2018年6月1-30日门诊含口服降糖药的所有处方,记录处方中的联合用药情况。
1.2 方法 依次详尽查阅处方内容,筛选出联合用药(2种及以上)处方,通过Excel软件进行分类汇总分析,查找出口服降糖药与其合并用药中存在CYP酶和转运体底物、诱导剂或抑制剂相关的相互作用情况,并对潜在的DDIs进行分析。药物相关的CYP酶和转运体底物、诱导剂或抑制剂以国内外药品说明书及文献报道为依据,所有药品按通用名进行处理。
2 结果
2.1 处方分布情况 本研究查阅我院2018年6月1-30日门诊含口服降糖药处方共计1 540张,其中单药处方208张,2、3、4、5种药物联合用药处方分别为487、248、226、371张。具体口服降糖药品种的处方分布见表1。
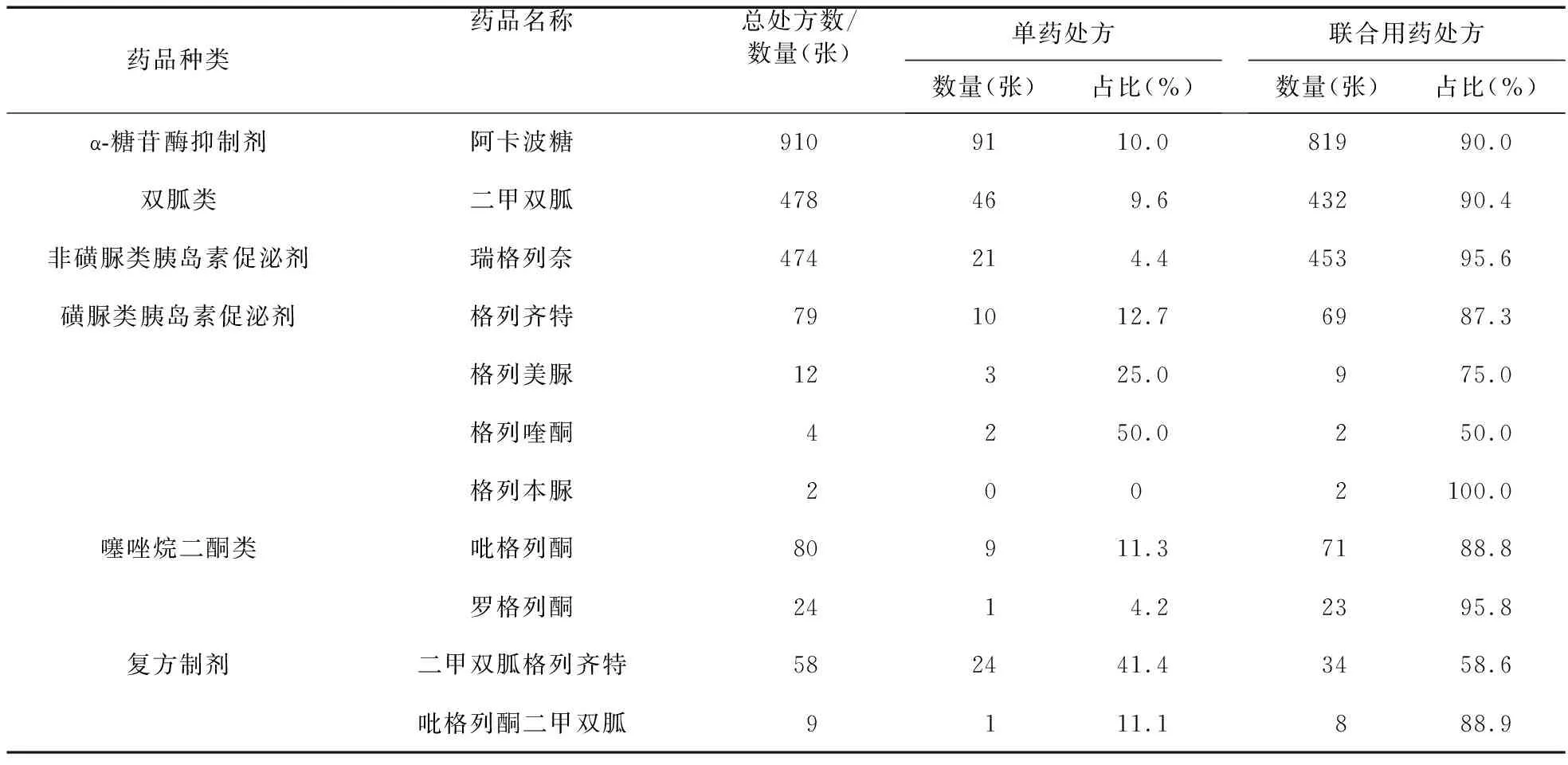
表1 口服降糖药处方分布
2.2 口服降糖药相关的CYP酶和转运体 口服降糖药药代动力学相关的CYP酶和转运体以国内外药品说明书及文献报道[5-15]为依据,主要涉及的代谢酶为CYP2C9、CYP2C8和CYP3A4等,相关转运体为P-糖蛋白(P-gp)、有机阴离子转运多肽(OATP)1B1和OATP1B3等,具体见表2。
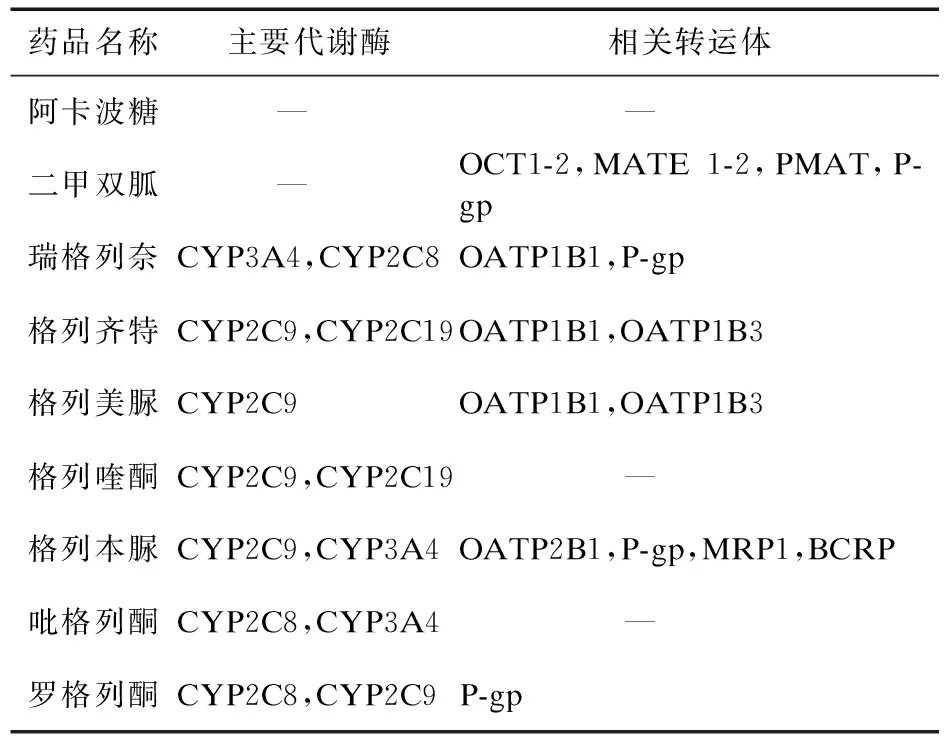
表2 口服降糖药药代动力学相关的CYP酶和转运体
注:OCT:有机阳离子转运蛋白;MATE:多药及毒性复合物外排转运体;PMAT:细胞膜单胺转运体;MRP:多药耐药相关蛋白;BCRP:乳腺癌耐药蛋白
2.3 CYP酶及转运体介导潜在的DDIs情况 我院门诊含口服降糖药处方中,存在潜在DDIs例次最多的3种药物分别为瑞格列奈(327例)、二甲双胍(264例)和格列齐特(90例)。其中,瑞格列奈常见的联用药物有二甲双胍(128例)、瑞舒伐他汀(108例)和阿托伐他汀(24例)等;二甲双胍常见的联用药物有瑞格列奈(128例)、美托洛尔(25例)和厄贝沙坦氢氯噻嗪(24例)等;格列齐特常见的联用药物有厄贝沙坦(37例)、瑞舒伐他汀(22例)和氯吡格雷(9例)等。见表3。
3 讨论
本次调查的口服降糖药处方中,存在代谢酶和(或)转运体介导潜在DDIs例次最多的为瑞格列奈(327例),瑞格列奈的主要代谢酶为CYP3A4和CYP2C8[6],涉及的转运体为OATP1B1[7]和P-gp[8]。在瑞格列奈与其他药物存在潜在DDIs的处方中,以二甲双胍最为多见(128例,39.1%),二甲双胍不仅为P-gp的底物,还能通过阻断细胞中多药耐药基因1(MDR1)的转录而降低P-gp的表达[9-10]。此外,Bachmakov等[16]关于口服降糖药对有机阳离子转运蛋白1(OCT1)转运1-甲基-4-苯基吡啶(MPP+,OCT1典型底物)影响的研究提示,瑞格列奈可显著抑制由OCT1介导的MPP+的转运,最大半抑制浓度(IC50)可达1.6~5.6 μmol/L,而OCT1是二甲双胍的主要转运体[9]。由此可见,二者存在的潜在DDIs可能由多种转运体参与所致。本研究显示,瑞格列奈与OATP1B1经典底物他汀类药物联合应用132例(40.4%)。Zhang等[17]在大鼠体内的药代动力学研究表明,瑞舒伐他汀与瑞格列奈的联合应用,可导致瑞舒伐他汀和瑞格列奈的药时曲线下面积(AUC)和药物峰浓度(Cmax)高于对照组(P<0.01,P<0.05)。Klatt等[18]研究表明,瑞格列奈能够抑制OATP1B1介导摄取阿托伐他汀。且同瑞格列奈一样,阿托伐他汀也是P-gp和CYP3A4的底物[19]。因此,瑞格列奈在临床与瑞舒伐他汀或阿托伐他汀联合应用时,医务人员应关注可能发生的DDIs,密切监测相关严重不良反应(如横纹肌溶解)的发生。

表3 口服降糖药处方中代谢酶和转运体介导潜在DDIs的情况
注:*括号内为存在潜在DDIs的例次
二甲双胍口服给药后,经小肠吸收入血,然后由OCT1摄取进入肝细胞,再经血窦侧反流入血,其不经过肝脏CYP酶代谢,全部以原型形式通过肾脏排泄,其中经肾小管分泌者超过80%,而OCT2则是介导其进入肾小管上皮细胞的主要转运体[10-11]。本研究显示,二甲双胍与OCT相关的联用药物有美托洛尔25例(9.5%)和罗格列酮14例(5.3%)。马彦荣等[20]关于美托洛尔对大鼠二甲双胍药动学影响的研究表明,与二甲双胍单药相比,二甲双胍联合美托洛尔应用中的二甲双胍Cmax显著降低(P<0.01),平均滞留时间(MRT)、半衰期(t1/2)和表观分布容积(V)显著增加(P<0.05)。由此可见,美托洛尔显著增加了二甲双胍的体内分布,降低了其血药浓度。另有文献提示,美托洛尔可能是OCT2的底物和抑制剂[21]。Bachmakov等[16]利用高表达OCT1细胞研究发现,罗格列酮能够通过OCT1降低细胞对MPP+和二甲双胍的摄取。因此,二甲双胍与美托洛尔或罗格列酮联用时,其药代动力学均可受到显著影响,处方医师应谨慎联用二者。
格列齐特、格列美脲和瑞舒伐他汀均为OATP1B1和OATP1B3底物,在与OATP1B1的结合方面,格列齐特和瑞舒伐他汀的能力基本相当,而格列美脲强于瑞舒伐他汀;与OATP1B3的结合方面,格列齐特和格列美脲均强于瑞舒伐他汀[12]。因此,当格列齐特和格列美脲分别与瑞舒伐他汀联合应用时,可能发生竞争性抑制,继而导致DDIs的发生。另外,格列本脲不仅是OATP2B1和P-gp的底物,还是OATP1B1和OATP1B3的抑制剂,并呈现浓度依赖性[13],故与瑞格列奈联用时,格列本脲可能会通过竞争性抑制OATP1B1及P-gp而发生DDIs。此外,在与磺脲类药物联用的其他药物中,与其底物重合或对其底物有抑制或诱导作用的药物有:厄贝沙坦、瑞舒伐他汀和来氟米特(均为CYP2C9底物),氯吡格雷(CYP2C19底物和CYP2C9抑制剂),奥美拉唑(CYP2C19强抑制剂)。Parekh等[22]研究提示,2型糖尿病患者在应用磺脲类药物时联合使用CYP2C9抑制剂,可增加患者低血糖的发生风险,且在老年患者中更为显著。李赟等[23]研究表明,CYP2C9和CYP2C19的基因多态性或酶活性改变对磺脲类药物的代谢及不良反应的发生均可产生显著影响。
然而,这种代谢酶和转运体介导的DDIs并非绝对,例如吡格列酮和瑞格列奈均为CYP3A4和CYP2C8的底物,且吡格列酮在体外还表现为CYP3A4抑制剂[24],理论上二者联用可能会发生DDIs。但是,Kajosaari等[25]的一项随机、交叉临床研究表明,在健康受试者体内,吡格列酮不会增加瑞格列奈的血药浓度,可能由于其较强的血浆蛋白结合能力,使得吡格列酮在体内对CYP3A4和CYP2C8抑制作用较弱。汤丽玲等[26]研究也发现,吡格列酮单药和吡格列酮与瑞格列奈联用在健康人体的药代动力学行为相近,提示瑞格列奈对吡格列酮及其主要活性代谢物的药代动力学无显著影响。
理论上可能存在的DDIs并非一定会给患者造成损伤,但联合用药影响不良反应发生的文献报道并不少见。修双玲等[27]报道,8例应用他汀类药物的糖尿病患者出现肌病,其中2例确诊为横纹肌溶解症,3例为肌炎,3例为较轻肌痛。卫晋菲等[28]对41例瑞格列奈致不良反应的文献报道进行了分析,其中6例患者联合应用了二甲双胍,不良反应表现为皮疹、视觉异常和无症状低血糖等。余小汉[29]通过对13例卡托普利致顽固性低血糖病例分析发现,低血糖反应在卡托普利联用口服降糖药时更常见。
综上,该院门诊患者服用降糖药物时常合并应用治疗其他疾病的多种药物,处方中代谢酶和转运体介导的潜在DDIs较为多见,成为不安全用药的危险因素,处方医师应学习药物的药代动力学特征,了解潜在DDIs发生的可能性,合理选择联合用药,尽量避免联合使用已有文献报道存在DDIs的药物,以降低患者的用药风险。处方审核药师也应加强学习,不断提高处方审核能力,及时发现不合理联合用药的现象,并给予建议及干预,提高药物治疗的安全性。
