双氯芬酸钠可溶微针在大鼠体内的药代动力学研究
2020-06-06李莹莹陈远政赵伟曼董智勇徐雨靓吴传斌王清清蚌埠医学院药学院药物分析教研室蚌埠33000中山大学药学院药剂学教研室通讯作者mailqingqingwangbbmceducn
李莹莹,陈远政,赵伟曼,董智勇,徐雨靓,魏 芳,吴传斌,王清清(蚌埠医学院药学院药物分析教研室,蚌埠 33000;中山大学药学院药剂学教研室;通讯作者,E-mail:qingqingwang@bbmc.edu.cn)
双氯芬酸钠(diclofenac sodium)是一种镇痛解热、非甾体类抗炎药[1]。双氯芬酸钠化学名为2-[(2,6-二氯苯基)氨基]苯乙酸钠,其作用机制为抑制环氧合酶的活性以减少前列腺素的合成,此外还能抑制脂氧合酶,减少白三烯的生成。因此本品广泛用于缓解轻至中度疼痛,治疗类风湿关节炎、骨关节炎和强直性脊柱炎、骨关节炎、肌肉骨骼损伤等[2]。
可溶微针贴片是一种具有广阔应用前景的新型经皮给药制剂,近年来受到了人们越来越多的关注[3]。可溶微针是由水溶性材料和药物混合制成的针长在25-2 000 μm的实心针,微针刺入皮肤后可自行降解,且能够在皮肤表面形成药物传递的通道,还可以通过调节针长,避开神经末梢和毛细血管丰富的真皮层,减少或消除疼痛与感染[4,5]。可溶微针贴片不仅避免了口服制剂的首过效应,还具有注射给药的高效性和准确性,同时还具有经皮给药的顺应性和方便性。
双氯芬酸钠大多为口服制剂,吸收迅速,解热镇痛作用较阿斯匹林强25-50倍,比布洛芬强8倍,经尿液和胆汁代谢排泄[6]。但其对胃肠道刺激性大[7],易导致上腹不适,胃肠出血甚至穿孔,且首过消除较为严重,生物利用度只有50%,血浆半衰期短,仅1.1-1.8 h,每日需给药3次,患者依从性差,并产生血药浓度的“峰谷现象”[8,9]。若将双氯芬酸钠包载于可溶微针中经皮给药,则可直接应用于靶部位,避免了药物的首过效应,消除了严重的胃肠道反应,同时可提高用药顺应性,也可自由调节药量,随时停药。
高效液相色谱法(HPLC)已被广泛用于各种定性定量的分析研究[10],但少有报道利用可溶微针给药并测定生物样品中药物的含量。本文旨在建立HPLC法测定可溶微针给药后生物样品中药物含量的方法,并为相关微针制剂和今后临床应用提供可靠、准确的检测依据。
1 材料与方法
1.1 仪器
高效液相色谱仪(LC-16,岛津仪器有限公司);超声波清洗器(KQ-500B,昆山市超声仪器有限公司);电子天平(FA224,上海舜宇恒平科学仪器有限公司);多管漩涡混合仪(HD-2500,杭州佑宁仪器有限公司);台式高速离心机(Allegra X-22,贝克曼公司);纯水仪(Advantage A10,Milli-Q公司)。
1.2 试药
双氯芬酸钠可溶微针贴片(250 μg/片,本实验室自制);双氯芬酸钠标准品(中国食品药品检定研究院,批号:100334-201803,纯度:100.0%);萘普生对照品(中国药品生物制品检定所,批号:100198-200403);肝素(辰欣药业股份有限公司,批号:1710216421);冰醋酸(天津大茂试剂厂,批号:20181201);甲醇(TEDIA,色谱纯);超纯水。
1.3 动物
SD雄性大鼠购自南京市江宁区青龙山动物繁殖场,质量合格证号为NO.201905766,生产许可证号为SCXK(苏)2017-0001,SPF级,体质量170-200 g。
1.4 方法
1.4.1 色谱条件 色谱柱:Phenomenex C18柱(4.6 mm×250 mm,5 μm);流动相:甲醇-1.5%冰醋酸水溶液(80∶20);流速:1.0 ml/min;紫外检测波长:276 nm;柱温:30 ℃;进样量:20 μl。
1.4.2 溶液配制 精密称取双氯芬酸钠标准品和萘普生标准品,分别置于100 ml容量瓶中,均使用甲醇溶解并定容至刻度线,配制得到浓度为192.00 μg/ml的双氯芬酸钠标准储备液和29.00 μg/ml的萘普生内标液。
1.4.3 血浆样品的前处理 精密吸取5 μl萘普生内标液(29 μg/ml)置于1.5 ml EP管中,加入50 μl血浆样品,再加入100 μl甲醇,涡旋混合5 min后至于离心机中以12 000 r/min的转速,4 ℃离心10 min,取上清液,进样检测。
2 结果
2.1 专属性
取空白血浆、空白血浆加双氯芬酸钠和内标物以及可溶微针给药后的血浆样品,按照1.4.3项下方法处理,得到相应的待测样品,按1.4.1项下色谱条件进样分析,记录相应的色谱图。结果表明,在本实验条件下双氯芬酸钠的保留时间约为8.10 min,内标物萘普生的保留时间约为5.50 min,样品测定不受血浆内源性物质干扰,专属性强(见图1)。
2.2 标准曲线和线性关系考察
取上述双氯芬酸钠标准储备液按0.20,0.40,1.00,2.00,3.00,4.00 μg/ml的浓度配制血浆样品,按上述1.4.3项下方法处理样品,并按1.4.1项下测定。以双氯芬酸钠的浓度为横坐标,以样品与内标物的峰面积比为纵坐标,绘制标准曲线,得回归方程Y=0.362 6X+0.047 4,R2=0.999 3。表明血浆药物浓度在0.20-4.00 μg/ml的范围内线性关系良好。定量下限为0.20 μg/ml。

图1 双氯芬酸钠和萘普生在大鼠血浆中的HPLC图Figure 1 The HPLC chromatograms of diclofenac sodium and naproxen in rat plasma
2.3 精密度和准确度
精密吸取空白血浆45 μl加入1.5 ml EP管中,加入双氯芬酸钠标准储备液配制浓度为0.20,0.40,2.00,4.00 μg/ml的含药血浆样品。按1.4.3项下方法处理血浆样品后按1.4.1项下条件注入高效液相色谱仪测定。每个浓度制备5个样品,连续3 d进行重复测定,结果见表1。结果表明,各浓度日内准确度在92.6%-98.9%之间,日内精密度在3.7%-8.8%之间,日间准确度在93.0%-103.4%之间,日间精密度在1.1%-5.0%之间。日内、日间精密度的RSD值均<10.0%,准确度均在85.0%-115.0%内,符合生物样品检测要求。

表1 血浆中双氯芬酸钠的精密度和准确度 (n=5)Table 1 Precision and accuracy of diclofenac sodium in plasma (n=5)
2.4 提取回收率
精密吸取空白血浆45 μl,分别加入5 μl浓度为2.00,4.00,20.00,40.00 μg/ml的双氯芬酸钠储备液,配制成双氯芬酸钠浓度为定量下限(0.20 μg/ml)、低(0.40 μg/ml)、中(2.00 μg/ml)、高(4.00 μg/ml)的含药血浆样品,再加入5 μl内标溶液(29.00 μg/ml),取处理后的各血浆供试品20 μl,按1.4.1项下方法注入高效液相色谱仪测定,记录各峰面积之比为A。另取同样的样本,先用甲醇沉淀空白血浆后收集上清,然后配制成相同浓度的含药血浆进行检测,记录峰面积之比为B。提取回收率=A/B×100.0%。结果显示,各浓度的提取回收率分别为(94.1±9.5)%,(101.2±8.2)%,(105.4±9.5)%,(102.5±8.0)%;RSD分别为10.1%,8.1%,9.0%,7.8%(见表2),均满足生物样品测定的要求,说明该方法的提取回收率较高。
2.5 样品稳定性考察
取空白血浆样品加入双氯芬酸钠标准储备液制备浓度为0.20,2.00,4.00 μg/ml的含药血浆样品,分别将样品放置在常温下储存4 h、4 ℃储存24 h、-20 ℃冻融循环3次和-20 ℃储存7 d后,按照1.4.3项下方法处理后按1.4.1项下条件注入高效液相色谱仪进行测定,每个浓度样品进行5次样本分析。结果显示,各浓度在以上储存条件下的检测值相对于理论值分别在96.0%-104.5%,91.2%-105.0%和91.5%-106.1%之间波动,RSD均<10.0%(见表3),说明样品在实验设计的条件下稳定性好。
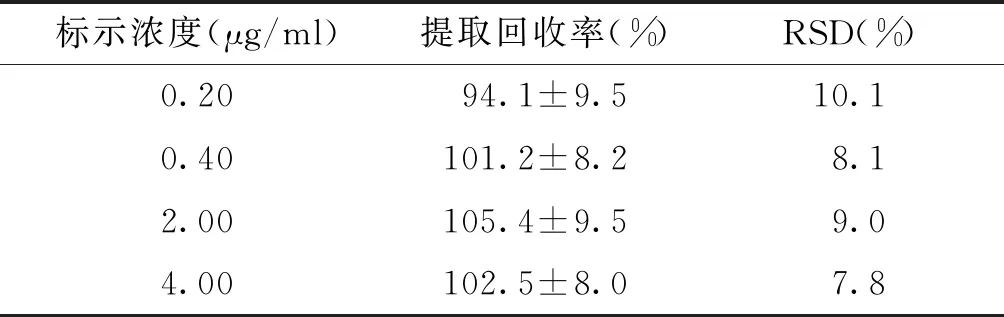
表2 血浆中双氯芬酸钠的提取回收率 (n=5)Table 2 Extraction recovery of diclofenac sodium in plasma (n=5)

表3 血浆中双氯芬酸钠的稳定性 (n=5)Table 3 Stability of diclofenac sodium in plasma (n=5)
2.6 药动学研究
2.6.1 血浆样品采集 取健康的雄性SD大鼠6只,耳部剃毛。每只大鼠耳部放置4片双氯芬酸钠可溶微针。分别于给药后2 min,5 min,10 min,20 min,40 min,1 h,2 h,4 h,6 h,8 h,10 h,12 h,24 h大鼠眼眶取血约0.3 ml,置于提前加入肝素的1.5 ml EP管中,4 ℃离心5 min(5 000 r/min)后取上层血浆,暂时保存在-20 ℃冰箱待测。
2.6.2 药动学参数计算 将可溶微针给药后的各血浆样品按1.4.3项下方法进行处理,按1.4.1项下色谱条件进行检测。根据随行标准曲线计算可溶微针给药后大鼠体内双氯芬酸钠的血药浓度,其血药浓度-时间曲线图见图2。经Phoenix WinNonlin 6.4软件分析得主要药动学参数,见表4。

图2 大鼠双氯芬酸钠可溶微针给药后的血药浓度-时间曲线 (n=6)Figure 2 Drug concentration-time curve of diclofenac sodium dissolving microneedles in rats after administration (n=6)

表4 大鼠双氯芬酸钠可溶微针给药后主要药动学参数 (n=6)Table 4 The main pharmacokinetic parameters of diclofenac sodium dissolving microneedles in rats after administration (n=6)
Cl:清除率;MRT:平均滞留时间;Vd:表观分布容积
3 讨论
本研究采用HPLC法对SD大鼠血浆中双氯芬酸钠的浓度进行了测定,以萘普生作为内标,利用甲醇去除蛋白沉淀的方法处理血浆样品,方法专属性高,不受内源性杂质影响。中国药典(2015版)收载的双氯芬酸钠高效液相色谱法以甲醇-4.0%冰醋酸溶液(70∶30)为流动相,而文献大多采用乙腈-乙酸盐或磷酸盐缓冲液等体系[11-13]。在建立方法学的过程中,本课题组对这些流动相都进行了考察,发现乙腈和磷酸盐缓冲液为主要流动相时分离效果并不理想,且乙腈的毒性较大。以甲醇-4.0%冰醋酸溶液为流动相时,目标峰的峰形不好。本方法以甲醇-1.5%冰醋酸(80∶20)作为流动相,峰形好、分离度高,而且甲醇毒性小、成本低,易冲洗。选取萘普生作为内标物,其色谱行为、色谱条件与待测物双氯芬酸钠较接近,且分离度较好,稳定性好,信号强。此外,采用等度洗脱法对样品进行分析,目标峰均出现在4.00 min之后,可以较好避免血浆中内源性物质的干扰,同时又能够显著缩短样品的分析周期,从而加快分析速度。有文献报道双氯芬酸钠血浆样品前处理方法为萃取法[14]和蛋白沉淀法[15,16]。萃取法首先酸化血浆样品,之后用有机溶剂进行萃取,其操作流程复杂,且萃取溶剂一般为乙醚、乙酸乙酯等毒性试剂。蛋白沉淀法与液液萃取法相比更为方便、安全,在满足定量要求的同时大大减少了预处理时间,一定程度可以加快分析速度,提升效率。对于蛋白沉淀剂的选择,考察了最常用的甲醇和乙腈,发现双氯芬酸钠的提取回收率均符合生物样品的测定要求,鉴于甲醇较乙腈毒性小、成本低。因此本实验选取甲醇去除蛋白沉淀以处理血浆样品。
本实验通过对双氯芬酸钠在大鼠体内药动学的研究,获得可溶微针给药的药动参数。实验结果显示,该药物的半衰期为(1.79±0.99)h,达峰时间为(0.21±0.10)h。本实验建立的测定大鼠血浆中双氯芬酸钠的HPLC法,能够满足双氯芬酸钠药动学的研究,得到的药动学数据为双氯芬酸钠可溶微针进一步的研究与开发提供科学依据。
