通过PI3K/AKT途径调节胶质母细胞瘤CD47表达对肿瘤侵袭性的影响
2020-06-02刘学键李玉花
刘学键, 武 霞, 李玉花
(1. 山东省立第三医院 两腺血管瘤科, 山东 济南, 250031; 2. 山东省临沂市第三人民医院 肿瘤科, 山东 临沂, 276023)
脑胶质瘤是中枢神经系统最常见的恶性肿瘤之一,约占大脑肿瘤的80%[1]。胶质母细胞瘤具有侵袭性,其治疗较为困难,易复发,中位生存时间为8~10个月[2-3]。CD47作为正常组织中广泛表达的跨膜糖蛋白,与巨噬细胞的信号调节蛋白α(SIRPα)相互作用,调节正常细胞的“自噬/凋亡”信号[4]。CD47的表达可促进多种肿瘤的侵袭性,如胃癌[5]、白血病[6]、乳腺癌[7]、宫颈癌[8]和黑色素瘤[9]等,表明CD47可作为治疗多种癌症的靶点[10-11], 但有关CD47在胶质母细胞瘤中的表达及侵袭的研究很少。研究[12-13]表明,磷脂酰肌醇3-激酶(PI3K)/蛋白质丝氨酸苏氨酸激酶(AKT)通路是抑制细胞凋亡和调节肿瘤细胞侵袭的重要通路。本研究探讨通过激活PI3K/AKT途径调节胶质母细胞瘤CD47表达对肿瘤侵袭性的影响,现报告如下。
1 资料与方法
1.1 一般资料
选取接受手术切除并经病理证实的脑胶质母细胞瘤患者30例,获取其胶质母细胞瘤脑组织标本,另收集10个正常脑组织标本为对照组。根据世界卫生组织(WHO)分类标准确定胶质母细胞瘤的组织学分型,并经2位具有副主任医师及以上职称的病理科医师确定每个样本,样本存放于-80 ℃冰箱中冷藏。纳入标准: ① 手术前未进行放疗、化疗及辅助治疗者; ② 未合并其他肿瘤者; ③ 血红蛋白≥110 g/L者; ④ 无严重的心肺功能不全、肝疾病、肾疾病或功能障碍者。
1.2 方法
1.2.1 主要试剂及耗材: 胶质母细胞瘤细胞U251、T98G和U87以及正常星形胶质细胞HEB购自中国科学院生物物理研究所(中国北京); DMEM培养基和胎牛血清(FBS)购自Gibco公司(美国); 添加FBS(10%)以及链霉素和青霉素(100 U/mL)(Gibco, 中国上海),在10%培养皿中于37 ℃、5% CO2的条件下应用于细胞培养。渥曼青霉素购自Invitrogen公司,抗PI3K和磷酸化PI3K(P-PI3K)、抗AKT和磷酸化AKT(P-AKT)抗体购自Abcam公司。
1.2.2 CD47表达载体构建及转染: 以pOTB7-CD47质粒为模板, PCR扩增CD47片段,用XhoI和HindIll分别将PCR产物CD47及目的载体pcDNA3.1-3xFlag进行双酶切。将酶切回收后的CD47基因片段和pcDNA3.1-3xFlag载体片段进行连接。将过夜连接的混合液直接转化DH5α感受态细胞,进行重组质粒的扩增与提取。将CD47过表达的质粒pcDNA3.1-3xFlag-CD47和空载Vector转染至细胞密度为60%~70%的脑胶质瘤细胞中,利用转染试剂,按照说明书进行转染,在转染前使用磷酸盐缓冲盐水洗涤细胞, 72 h后提取蛋白验证转染效率并进行后续实验。
1.2.3 实时荧光定量PCR(RT-PCR): 采用TRIzol试剂(Life Technologies, Carls bad, CA, USA)提取总核糖核酸。为了量化CD47转录,借助转基因生物技术(TransStart Top Green)进行基因组DNA(gDNA)去除和互补DNA(cDNA)合成超螺旋生成cDNA。应用于GAPDH以及CD47的寡核苷酸引物如下: GAPDH: 5′-GCA CCG TCA AGG CTG AGA AC-3′(有义)和5'-TGG TGA AGA CGC CAG TGGA-3′(反义); CD47: 5'-AGA TCC GGT GGT ATG GAT GAGA-3′(有义)和5'-GTC ACA ATT AAA CCA AGG CCA GTAG-3′(反义)。每个程序一式三份进行。通过2%琼脂糖凝胶电泳及熔解曲线鉴定qRT-PCR产物,并用公式(ΔCt)进行定量分析。ΔCt=目的基因Ct-内参基因Ct。CD47 cDNA循环阈值(Ct)根据ΔΔCt方法[12]对GAPDH进行归一化。
1.2.4 Western Blot分析: 将6孔板应用于细胞培养,直至在不含血清的100 U/mL双抗(青霉素/链霉素)的DMEM培养基中汇合达到80%。取出培养基,用PBS洗涤细胞2次。M-PER哺乳动物蛋白质提取试剂(Pierce Biotechnology, Rockford, IL, USA)加入细胞中,随后从平板上刮下细胞,并在4 ℃下以14 000 g离心10 min, 然后在添加有MTT(50 mmol/L)的Laemmli标本缓冲液的帮助下,将上清液加热5 min。经过裂解和加热的等量蛋白质(30 μg/孔)在聚丙烯酰胺凝胶的帮助下进行电泳(10%; BioRad, 中国上海)。将分离的蛋白质移至PVDF膜(GE Healthcare, Pittsburgh, PA, USA), 然后于室温环境下在脱脂乳(5%; BioRad)的帮助下封闭1 h。在4 ℃的情况下,在第一抗体的帮助下,膜进行过夜孵育。按照指示进行浓度的测定,然后用辣根过氧化物酶结合的膜孵育第二抗体在室温下持续1 h, 最后使用增强的化学发光试剂盒(GE Healthcare)检测蛋白质。
1.2.5 侵袭实验: 预先加入基底膜(200 μg/mL, BD Biosciences, Franklin Lakes, NJ, USA)的Transwell小室(24孔插入物, 8 μm孔径, Millipore, Billerica, MA, USA)用于侵袭实验,在转染后24 h, 用丝裂霉素C(10 μg/mL)处理细胞2 h。将细胞进行胰蛋白酶处理,并在不含血清的培养基中以每室1×105个细胞的密度种植于上面的室中。下面的室里装满了含有FBS(15%)的DMEM-F12培养基,可作为化学诱导剂。孵化持续了48 h, 随后位于室上部表面的细胞消除,位于下室的入侵细胞用甲醇和结晶紫染色并进行固定。应用光学显微镜评估5个随机视野中的细胞数量。
1.3 统计学分析
采用SPSS 17.0进行数据处理,计量资料以均数±标准差表示,比较采用t检验; 计数资料采用χ2检验,P<0.05为差异有统计学意义。
2 结 果
2.1 胶质母细胞瘤中CD47的表达
通过qRT-PCR技术评价CD47在30个胶质母细胞瘤标本以及10个正常对照标本中的表达,结果显示CD47存在于大多数胶质母细胞瘤组织中,见图1A。与正常星形胶质细胞HEB相比, U251、T98G以及U87细胞不仅促进转录,而且促进CD47的翻译,其中胶质母细胞瘤细胞U87中的CD47表达最显著(P<0.05), 见图1B。


A: CD47在胶质母细胞瘤标本及正常对照标本中的表达; B: CD47在U251、T98G、U87及正常星形胶质细胞HEB中的表达比较。
图1 胶质母细胞瘤中的CD47表达
2.2 低表达及过表达的CD47对胶质母细胞瘤细胞侵袭性的影响
2.2.1 低表达CD47对胶质母细胞瘤侵袭性的影响: 将CD47和对照siRNA分别转染入U87细胞,通过对CD47的siRNA(CD47-siRNA)进行干扰,阻止CD47细胞转录和翻译,敲除U87细胞的CD47。与对照siRNA相比,敲除CD47显著抑制U87的侵袭(P<0.05), 见图2。




A: 转染后24 h应用RT-PCR评估CD47转录; B: 转染后24 h的CD47翻译; C: 侵袭实验测定的特征图像; D: 对照siRNA与CD47 siRNA侵袭性。
图2 低表达CD47对胶质母细胞瘤细胞侵袭性的影响
2.2.2 过表达CD47对胶质母细胞瘤细胞侵袭的影响: 应用pcDNA3.1-3xFlag-CD47质粒转染T98G细胞,然后用Western Blott和qRT-PCR确认T98G细胞中过量的CD47表达。与对照组相比,过表达CD47显著增强了T98G细胞的侵袭性(P<0.05)。见图3。

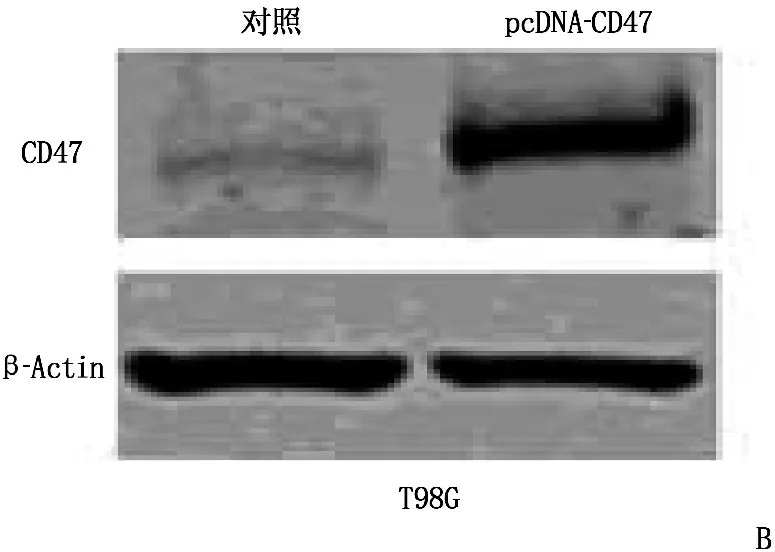


A: 转染后24 h应用RT-PCR评估CD47转录; B: 转染后24 h的CD47翻译; C: 侵袭实验测定的特征图像; D: 对照组与pcDNA-CD47的侵袭性。
图3 过表达CD47对胶质母细胞瘤细胞侵袭性的影响
2.3 PI3K/AKT信号通路调节胶质母细胞瘤CD47对肿瘤侵袭性的影响
将对照质粒(对照组)和pcDNA3.1-3xFlag-CD47质粒转染到T98G细胞中,随后进行渥曼青霉素(PI3K抑制剂)处理(即pcDNA-CD47+wortmannin组)和不进行渥曼青霉素处理(即pcDNA-CD47组)。结果显示,CD47过表达后AKT磷酸化有显著促进作用,应用渥曼青霉素抑制AKT磷酸化。通过侵袭测定证明,渥曼青霉素显著减轻了CD47在T98G细胞方面引发的侵袭性(P<0.05)。见图4。
3 讨 论
CD47是免疫球蛋白超家族的一员,广泛表达于多种正常组织细胞表面,发挥调节细胞运动、神经轴突发育和免疫调节等多种生理功能。CD47分子在大部分组织来源的肿瘤细胞中均表达上调,因此CD47可能与肿瘤逃脱免疫监视有关[8]。研究[14-17]表明, CD47可作为各种癌症的预测因子。Baccelli I等[4]研究证明,具有EPcam+CD47+MET+/-表型的乳腺导管癌患者具有更低的总体存活率,循环血液中具有CD47高表达的乳腺癌患者易复发和转移[18]。在结直肠癌病例中, CD47上调与远处转移有关。CD47单抗通过阻断肿瘤细胞表面的CD47与巨噬细胞表面的SIRPα结合,发挥抗肿瘤作用。研究[19]表明,阻断CD47-SIRPa信号通路能显著抑制黑色素瘤的生长以及肺转移。CD47信号通路的阻断抑制了癌症的发展和转移,证明了CD47对各种恶性肿瘤的治疗有效性[20-21]。
在中枢神经系统中,培养的神经细胞中CD47的过表达改善了突触的产生和分支,与CD47结合的SIRPa增强了培养的神经细胞中脊柱和丝状体的生成[22-23]。此外, CD47与血小板反应素-1(TSP-1)相结合,调节细胞内的信号通路活化,控制细胞存活、生长、运动和线粒体发生等生理活动,同时也调节血管中平滑肌细胞的迁移和生长[24]。多家研究机构迅速开发出多种以CD47为靶点的单克隆抗体药物,并在多种组织来源的肿瘤细胞移植动物模型实验中取得了良好的治疗效果,如在急性淋巴细胞白血病、非霍奇金淋巴瘤小鼠模型中, CD47单抗治疗后,可以明显缩小甚至清除荷瘤小鼠体内的肿瘤细胞,达到完全治愈的效果[25]。在实体肿瘤中, CD47单抗亦具有良好的治疗效果,如乳腺癌、卵巢癌、膀胱癌、肝癌等多种肿瘤的体外实验研究中, CD47单抗均可显著抑制肿瘤的生长和转移,并且延长生存期[26-27]。脑胶质瘤是最常见的颅内肿瘤,近年来发生率逐年递增,老年人群尤为明显。脑胶质瘤患者预后较差,易复发,病死率高,主要原因是胶质母细胞瘤的侵袭性使其具有易复发性和顽固性[2-3]。

A: 采用Western Blot评估转染后24 h的特定蛋白质的表达; B: 侵袭测定的特征图像; C: 3组侵袭性比较。图4 CD47通过PI3K/AKT信号通路引发胶质母细胞瘤的侵袭
本研究通过CD47在胶质母细胞瘤组织细胞中的表达与在正常脑标本和星形胶质细胞中的表达相比较,发现CD47在胶质母细胞瘤细胞中高表达并且在U87中CD47的表达最明显。通过对CD47的siRNA(CD47-siRNA)干扰,阻止CD47细胞转录和翻译,敲除U87细胞的CD47, 发现CD47的敲低显著抑制U87的侵袭。本研究用pcDNA3.1-3xFlag-CD47质粒转染T98G细胞,然后用Western Blott和qRT-PCR确认T98G细胞中过量的CD47表达,通过比较发现过量的CD47表达显著促进了T98G细胞的侵袭性。
本研究创新性地发现CD47通过激活PI3K/AKT途径增强胶质母细胞瘤的侵袭性。作者将对照质粒和pcDNA3.1-3xFlag-CD47质粒转染到T98G细胞中,随后进行渥曼青霉素差别处理(分为处理与不处理),结果显示CD47过表达后对AKT磷酸化有显著促进作用,渥曼青霉素显著减轻了CD47在T98G细胞方面引发的侵袭性。这些数据表明CD47的表达水平通过激活PI3K/AKT信号通路增强胶质母细胞瘤的侵袭性。PI3K/AKT是细胞内信号转导通路中最主要的信号通路之一,在调节细胞生长、运动、存活、增殖、蛋白质合成、自噬、转录及血管生成等方面有重要意义[28], 该途径包括3个主要的驱动分子: P13激酶(P13K)、丝氨酸/苏氨酸激酶(AKT)和哺乳动物雷帕霉素靶蛋白(mTOR)[29]。对于星形细胞瘤而言, PI3K/AKT途径通过调节葡萄糖转运蛋白Glut1定位于细胞表面,并通过激活己糖激酶引起糖酵解,己糖激酶作为糖酵解中的酶使AKT的IP3受体的磷酸化,抑制了U87细胞的凋亡[30]。AKT还针对胶质瘤中的mTOR调节各种细胞反应。mTOR是一种非典型的丝氨酸,主要参与调节细胞生长、生存及运动等过程[31]。
总之,本研究结果表明, CD47在胶质母细胞瘤细胞中高表达, CD47通过激活PI3K/AKT信号通路增强胶质母细胞瘤的侵袭性, CD47是胶质母细胞瘤的重要预测指标和治疗靶点。
