核磁共振氢谱定量法分析樟树籽油的甲酯化率
2020-05-24王云鹏杨德孟楼乔明张进杰杨文鸽
王云鹏 徐 华 杨德孟 楼乔明 张进杰 杨文鸽
(宁波大学食品与药学学院,宁波 315211)
樟树(Cinnamomumcamphora)属樟科属常绿乔木植物,主要分布于我国的热带和亚热带地区,是樟属植物中经济价值最大的树种之一[1]。樟树籽含油量高达40%以上,以甘油三酯为主,且脂肪酸主要为癸酸(C10∶0,51.49%)和月桂酸(C12∶0,40.08%),其甲酯衍生物比C16和C18等长链脂肪酸具有更高的十六烷值、更好的运动黏度和氧化稳定性,是制备脂肪酸甲酯的理想原料[2,3]。
目前,国内外用于测定脂肪酸甲酯纯度或产率的方法多以气相色谱(GC)为主[4],但GC定量过程烦琐,且对不易挥发的高沸点物质分析较难。同时,基于光谱技术建立的脂肪酸甲酯化率测量模型,前期均需测定大量样品,耗时耗力且适用范围较窄[5-7];而黏度法、酸值法、质量法、薄层层析法和分光光度法等方法,均因测定结果准确度较低等原因,未能广泛使用[8]。
核磁共振氢谱定量法(q1H-NMR)依据核磁共振峰的峰面积与产生该共振峰的质子数成正比的原理,通过内标法,可以直接测量标准物质的含量;其分辨率高、准确性强、操作简便、分析速度快,已成为众多学者关注的焦点。目前,q1H-NMR法在脂肪酸甲酯定量分析领域应用较少,国内外鲜有报道。因此本研究以月桂酸甲酯和甘油三月桂酸酯标准品为研究对象,对其核磁共振氢谱进行分析,确定定量峰的峰面积与混合标准品中月桂酸甲酯含量之间的定量关系,建立标准曲线,并用于樟树籽油衍生过程中甲酯化率的测定,以期为樟树籽油甲酯化率的定量分析提供参考。
1 材料与方法
1.1 材料与试剂
樟树籽、氘代三氯甲烷(CDCl3,氘代度99.8%+0.03%四甲基硅烷)、月桂酸甲酯、甘油三月桂酸酯和十三烷酸甲酯标准品;三氯甲烷、氢氧化钾、甲醇、正己烷、无水硫酸钠等分析纯。
1.2 仪器与设备
AVANCE III HD 500 MHz超导核磁共振谱仪;7890A型气相色谱仪;M7-80EI型质谱仪;RV-10型旋转蒸发仪;XO-5200DTD超声波清洗仪。
1.3 实验方法
1.3.1 樟树籽预处理
将樟树籽于50 ℃烘箱干燥至恒重,去壳粉碎,经40目过筛,置于4 ℃冰箱中冷藏备用。
1.3.2 油脂提取
采用Folch法[9]提取樟树籽油。称取 20 g樟树籽仁粉末,用400 mL三氯甲烷-甲醇(2∶1,V∶V)混合液超声 30 min(功率250 W,频率40 kHz,温度25 ℃),并浸提24 h;过滤后,滤液用 80 mL 0.9%氯化钠溶液洗涤,静置分层后,收集三氯甲烷层,用无水硫酸钠干燥,经减压浓缩,得樟树籽油。
1.3.3 标准品配制
分别取0、10、20、30、40、50 mg(精确至0.1 mg)月桂酸甲酯加入甘油三月桂酸酯中,使混合标准品总质量为50 mg,即月桂酸甲酯在混合标准品中所占质量百分含量分别为0%、20%、40%、60%、80%、100%。用0.6 mL氘代三氯甲烷溶解,并转移至核磁管中,用于核磁共振氢谱分析。
1.3.41H-NMR谱分析
氢谱参数:脉冲序列zg30,检测温度为298.0 K,90°脉冲宽度P1为11.11 μs,谱宽SWH为10 000 Hz,脉冲延迟时间D1为1 s,采样点数TD为65 536,采样时间at为3 s,扫描次数NS为16,空扫DS为2。使用MestReNova软件对图谱进行处理和分析。
1.3.5 q1H-NMR的定量关系
根据公式(1)确定本实验中q1H-NMR的定量关系[10,11],以混合标准品中月桂酸甲酯的含量(%)为X轴,1H-NMR定量峰的峰面积(以内标峰为参照)为Y轴,建立一元线性回归方程。
(1)
式中:S1和S2分别为待测样与内标峰的积分面积;N1和N2分别为待测样与内标物定量峰积分信号所包含的质子数;M1和M2分别为待测样与内标物的相对分子质量;m1和m2分别为待测样与内标物的质量;P1和P2分别为待测样和内标物的质量百分含量。
1.3.6 碱法甲酯化衍生[12]
取100 mg樟树籽油,加入3 mL 1 mol/L的氢氧化钾-甲醇溶液,振荡反应(0、0.1、0.5、1、3、5、10 min),依次加入1 mL 饱和氯化钠溶液和2 mL 正己烷,振荡后6 000 r/min离心3 min,取正己烷层,重复正己烷萃取3次,合并正己烷相,减压浓缩后,用于1H-NMR和GC-MS分析。
1.3.7 GC-MS分析[13-14]
以十三烷酸甲酯为内标,进行定量分析,以测定樟树籽油的甲酯化率。色谱条件:DB-WAX 毛细管柱(30 m × 0.25 mm × 0.25 μm),进样口温度250 ℃,检测器温度250 ℃;升温程序:初始温度150 ℃,保持2 min,以5 ℃/min升至200 ℃,保持5 min,再以5 ℃/min升至230 ℃,保持10 min;进样量1.0 μL,分流比50∶1;以氦气为载气,载气流量1 mL/min;溶剂延迟时间为3 min。质谱条件:GC-MS接口温度250 ℃,EI离子源,离子源温度230 ℃,电离能量70 eV,质量扫描范围:m/z50~650 u。
2 结果与分析
2.1 1H-NMR谱归属和定量峰确定
甘油三月桂酸酯和月桂酸甲酯的核磁共振氢谱见图1,参考Nieva等[15,16]对信号峰进行归属,结果列于表1。甘油三月桂酸酯与月桂酸甲酯结构上的差异,致使两者在核磁共振氢谱中具有各自的特征峰[17]。由表1可知,化学位移δ=4.13~4.18和δ=4.28~4.34谱峰归属为甘油骨架中亚甲基上的氢(—CH2—CH—CH2—),可作为甘油三月桂酸酯的特征峰;δ=3.67谱峰为脂肪酸甲酯中的甲氧基上的氢(—OCH3),可作为月桂酸甲酯的特征峰;此外,δ=5.25~5.30处的多重峰归属为甘油骨架中的次甲基上的氢(—CH2—CH—CH2—),也可作为甘油三月桂酸酯的特征峰。

图1 甘油三月桂酸酯a和月桂酸甲酯b的核磁共振氢谱图
用于定量分析的特征峰通常优先选择与相邻峰分离度好、无干扰信号的峰,且最好为含多个氢质子的单峰[18]。由图1可知,δ=5.25~5.30处的谱峰虽为特征峰,但含氢少,且为多重峰,分离度较差,因此不宜作为定量峰;而δ=4.13~4.18、δ=4.28~4.34和δ=3.67两组信号峰与其他峰完全分开,含氢较多,峰型对称,峰两侧基线平坦,无干扰,因此可作为定量分析的特征峰。
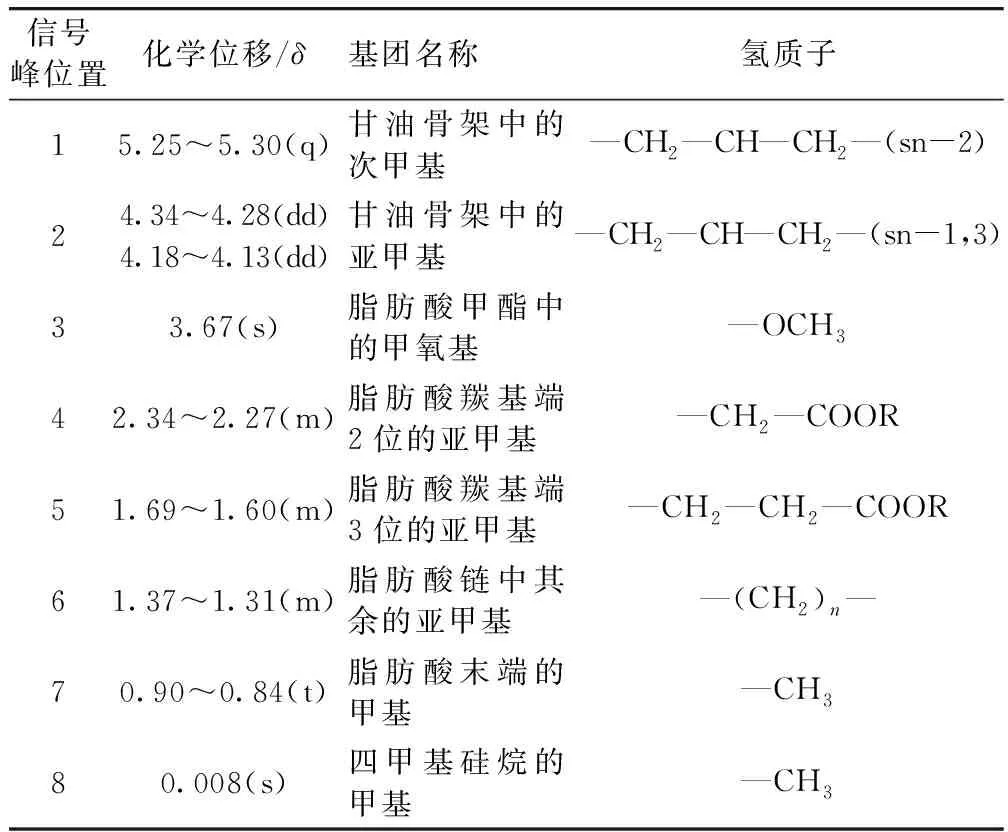
表1 信号峰的化学位移及官能团归属
注:s,单峰;t,三重峰;q,五重峰;m,多重峰;dd,双峰+双峰。
2.2 1H-NMR法线性关系的确定
分别以月桂酸甲酯中的甲氧基(—OCH3)和甘油三月桂酸酯中甘油骨架上的亚甲基(—CH2—CH—CH2—)作为定量峰进行线性关系的确定,定量峰和内标峰的核磁共振氢谱见图2。


图2 —OCH3(a)和—CH2—CH—CH2-(b)与Si(CH3)4的核磁共振氢谱局部放大图
由图3a可知,随着样品中月桂酸甲酯含量的增加,—OCH3信号峰(δ=3.67)强度也随之增大,二者成正比关系。将四甲基硅烷[Si(CH3)4]的甲基信号峰(δ=0.008)峰面积标定为1,获得—OCH3信号峰的峰面积,根据定量式(1),以混合标准品中月桂酸甲酯含量为横坐标,—OCH3信号峰的峰面积为纵坐标,经线性回归分析,得到线性回归方程y=-0.97+0.61x,R2=0.999 1(图3b)。结果表明,以—OCH3信号峰为定量峰时,定量峰的峰面积与月桂酸甲酯含量具有良好的线性关系,可用于月桂酸甲酯的定量分析。


图3 不同月桂酸甲酯含量样品中—OCH3信号峰a及建立的标准曲线b
由图4a可知,随着样品中月桂酸甲酯含量的增加,—CH2—CH—CH2—信号峰(δ=4.13~4.18和δ=4.28~4.34)强度在逐渐降低,二者成反比关系。将Si(CH3)4的甲基信号峰(δ=0.008)峰面积标定为1,获得—CH2—CH—CH2—信号峰的峰面积,根据定量式(1),以—CH2—CH—CH2—信号峰的峰面积与混合标准品中月桂酸甲酯含量建立校准曲线,得到线性回归方程y=34.6-0.35x,R2=0.999 8(图4b)。结果表明,以—CH2—CH—CH2—信号峰为定量峰时,定量峰的峰面积与月桂酸甲酯含量具有良好的线性关系,亦可用于月桂酸甲酯的定量分析。


图4 不同月桂酸甲酯含量样品中—CH2—CH—CH2—信号峰a及建立的标准曲线b
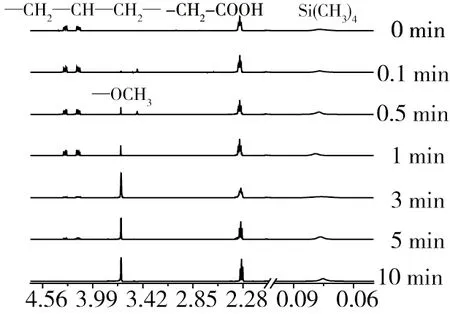
图5 樟树籽油不同衍生时间产物的核磁共振氢谱图
2.3 樟树籽油甲酯化率测定
樟树籽油经1 mol/L氢氧化钾-甲醇溶液不同时间的甲酯化衍生,其核磁共振氢谱见图5。从图5可知,随着衍生时间增加,甘油三酯中的—CH2—CH—CH2—信号峰(δ=4.13~4.18和δ=4.28~4.34)强度逐渐减弱,而脂肪酸甲酯中的—OCH3信号峰(δ=3.67)强度逐渐增强;当衍生时间为10 min时,—CH2—CH—CH2—信号峰完全消失,而—OCH3信号峰达到最大值,表明随着衍生时间的增加,樟树籽油中的甘油三酯逐渐转化为脂肪酸甲酯,这与Anderson等[19]报道的结果一致。
采用q1H-NMR法对樟树籽油不同衍生时间的甲酯化率进行定量分析,并与GC-MS法进行比较,结果列于表2。由表2可知,以—OCH3和—CH2—CH—CH2—为定量峰的两种q1H-NMR法所测结果基本一致。当衍生时间为0.1 min时,樟树籽油甲酯化率仅为6.0%;并随着衍生时间的增加,甲酯化率逐渐增加;当衍生时间为5 min时,甲酯化率达到87.6%;而当衍生时间为10 min时,樟树籽油甲酯化几乎完全,甲酯化率达到99.1%。将q1H-NMR法所测结果与GC-MS法进行t检验,结果显示无显著性差异(P>0.05),因此q1H-NMR法能有效用于樟树籽油甲酯化率的分析,且具有前处理简单、分析时间短、结果准确等优点。

表2 不同衍生时间樟树籽油的甲酯化率/%
3 结论
将月桂酸甲酯的特征峰(δ=3.67)和甘油三月桂酸酯的特征峰(δ=4.13~4.18和δ=4.28~4.34)作为定量峰,以混合标准品中月桂酸甲酯含量(%)为X轴,定量峰相对峰面积(内标峰为参照)为Y轴,得到甲氧基(—OCH3)峰面积与月桂酸甲酯含量的线性回归方程为y=-0.97+0.61x(R2=0.999 1);甘油骨架亚甲基(—CH2—CH—CH2—)峰面积与月桂酸甲酯含量的线性回归方程为y=34.6-0.35x(R2=0.999 8);两者均具有良好的线性相关系数,可用于脂肪酸甲酯的定量分析。
采用核磁共振氢谱定量法对樟树籽油衍生过程中甲酯化率进行测定,以—OCH3和—CH2—CH—CH2—为定量峰,两种定量法所测结果基本一致。樟树籽油的甲酯化率随着衍生时间的增加而逐渐增加,当衍生时间为10 min时,樟树籽油甲酯化率达到99.1%。q1H-NMR法所测结果与GC-MS法无显著性差异(P>0.05),表明q1H-NMR法能有效用于樟树籽油甲酯化率的分析测定,且具有前处理简单、分析时间短、结果准确等优点。
