不同钙化分型对TASCⅡA、B级股腘动脉硬化闭塞症腔内治疗的影响
2020-05-22陈吉冲王兵王越牛晓阳尚文煊郭鹏
陈吉冲 王兵 王越 牛晓阳 尚文煊 郭鹏
郑州大学第五附属医院血管外科(郑州450052)
目前股腘动脉硬化闭塞症(femoral popliteal atherosclerotic occlusive disease,FPAOD)的治疗进展主要集中在腔内治疗,但是较高的再狭窄率限制其进一步发展[1]。近年来“减容技术”(directional atherectomy,DA)以及药物涂层球囊(drug⁃coated balloon,DCB)等新技术相继应用于临床,为此类疾病的治疗提供了新思路。DCB 通过局部向动脉血管壁释放抗增殖药物,从而达到抑制血管内膜增生的效果,可明显降低术后血管再狭窄的发生率[2],但是对于伴有严重钙化的病变治疗效果差[3],内侧钙化通过干扰药物吸收和渗透到血管壁[4]而限制DCBs 的抗增殖作用。Turbohawk 可直接切除血管壁上的动脉硬化斑块,不仅使病变管腔血流显著增加,也可使支架补救的概率降低,能够有效治疗钙化及管腔再狭窄病变,但是同时也会对血管内膜造成损伤,增加再狭窄的发生率[5]。目前对伴有钙化病变的手术选择没有统一的标准,国内外仅少数中心在研究中强调了钙化对于FPAOD治疗影响[6-9],故本研究通过对不同方式治疗伴有钙化的TASCⅡA、B 级患者的有效性及安全性进行深一步的探究,为临床工作提供参考。
1 资料与方法
1.1 一般资料本文回顾性分析我中心自2016年10月至2018年10月股腘动脉硬化闭塞症TASCⅡA、B 级的82 例患者,将患者按手术方式分为两组。A 组:Turbohawk 联合DCB 治疗共42 例,其中男29 例(69.0%),平均(67.2 ± 8.1)岁;B 组:单纯DCB 治疗共40 例,其中男27 例(67.50%),平均(68.8±6.4)岁。两组患者的一般资料、高危因素、血管病变情况对比差异无统计学意义(均P>0.05,表1、2)。所有入选患者术前均接受完整的CTA 和DSA 评估,参照FANELLI 等[10]的研究,将CTA 图像轴向平面分为4 个90°扇区来量化钙的周向血管壁分布,由同一名经验丰富的血管外科医生进行评估,将钙化程度分为:轻度钙化(0 ~180°),中度钙化(180° ~270°),重度钙化(270° ~360°)。纳入标准:(1)TASC 股腘动脉分型A/B级,A 级患者伴有明显的间歇性跛行或静息痛;(2)主、髂动脉无明显狭窄;(3)心肺功能良好,可耐受介入手术;(4)此前未接受过血管介入治疗;(5)无活动性出血疾病及严重肝肾功能异常。排除标准:(1)术前有凝血功能障碍或出血倾向患者;(2)严重肝肾功能衰竭者;(3)对紫杉醇、阿司匹林、波立维、肝素等药物过敏者;(4)远端流出道小于1 条血管的患者;(5)预期生命小于2年的患者(6)病变长度>15 cm 或根据TASCⅡ推荐的C、D 型病变。
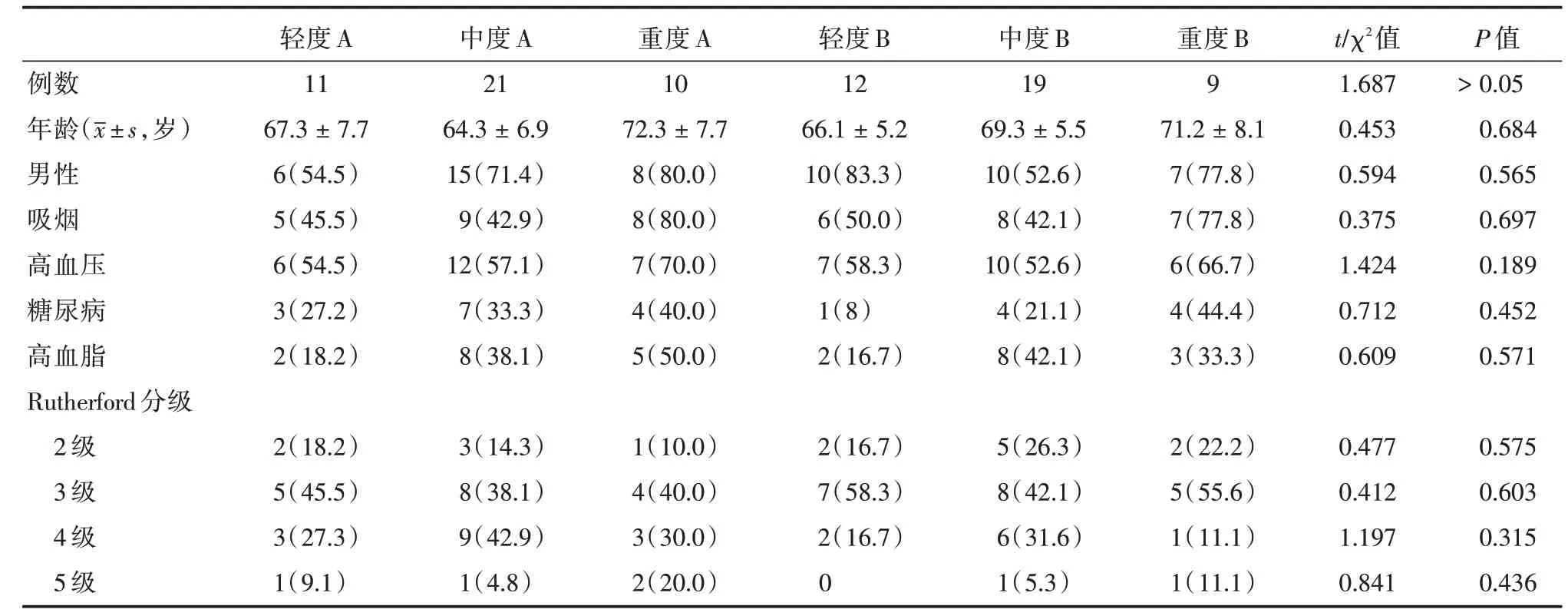
表1 两组患者一般情况及危险因素的比较Tab.1 Comparison of the general conditions and risk factors between the two groups of patients 例(%)
表2 两组患者的血管病变情况的比较Tab.2 Comparison of the vascular disease conditions between the two groups of patients ±s
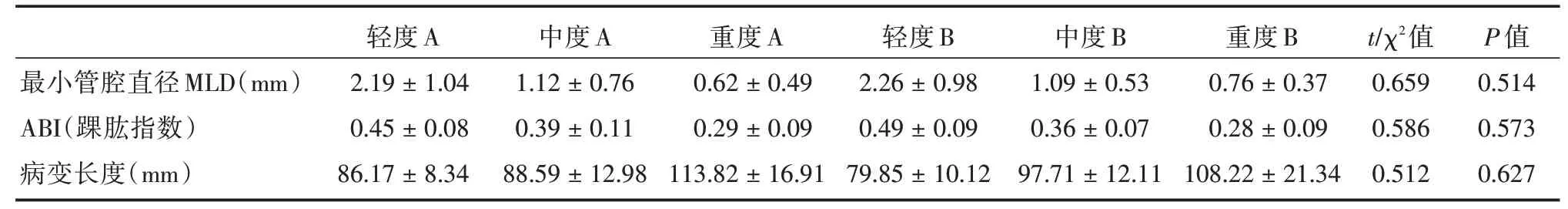
表2 两组患者的血管病变情况的比较Tab.2 Comparison of the vascular disease conditions between the two groups of patients ±s
最小管腔直径MLD(mm)ABI(踝肱指数)病变长度(mm)轻度A 2.19±1.04 0.45±0.08 86.17±8.34中度A 1.12±0.76 0.39±0.11 88.59±12.98重度A 0.62±0.49 0.29±0.09 113.82±16.91轻度B 2.26±0.98 0.49±0.09 79.85±10.12中度B 1.09±0.53 0.36±0.07 97.71±12.11重度B 0.76±0.37 0.28±0.09 108.22±21.34 t/χ2值0.659 0.586 0.512 P 值0.514 0.573 0.627
1.2 手术器械TurboHawk LS⁃C/LX⁃C 型斑块旋切导管(8 F,Medtronic),药物涂层球囊(Orchid),各型号外周动脉球囊、5F 和6F 动脉鞘(Medtronic),8F 翻山鞘、5F 单弯导管(Cook),0.035 英寸、260 cm超滑导丝(Terumo),0.018 英寸导丝(Boston),0.014英寸导丝、2.6F 支撑导管(Cook),21G 微穿针(Cook),Spider FX 远端保护伞装置(Medtronic);封堵器(Abbott)。
1.3 手术方法全部病例均由同一位资深血管外科介入医师主刀,局麻下采用改良Seldinger 技术穿刺入路,其中65 例逆行穿刺健侧股动脉翻山,13 例采用患侧股动脉顺行穿刺,4 例患者在超声引导下行同侧股动脉逆行穿刺。穿刺成功后置入5F 或6F 动脉鞘,静脉推注肝素(0.5 mg/kg),使全身肝素化后,行患肢动脉造影明确病变范围和程度。以0.035 导丝配合5F 单弯导管对闭塞段行进行顺行开通,对于重度狭窄或闭塞性病变难以开通时使用0.014 in 微导丝配合微导管开通。A 组到达病变远端后再次造影确保相关操作均在血管真腔内进行,随后引入Spider FX 远端保护伞装置,释放位置由手术者根据术中情况决定。路图下经导丝将TurboHawk 斑块旋切系统在关闭状态下缓慢前行至病变段,在透视状态下由病变近端向远端匀速(1 mm/s)切割病变,多角度操作3~5次,一旦推进系统开关时出现阻力,需考虑前方收集槽斑块容量接近承载负荷,此时退出斑块旋切装置,将粥样硬化斑块从贮藏鼻锥中移除,避免斑块满溢后脱落导致远端栓塞,将角度调整合适后继续重复上述操作,当造影显示残余狭窄≤30%结束操作。随后先选用小于正常管径0.5 ~1 mm的普通球囊进行预扩张,时间为1 ~2 min,然后再用直径与靶血管相同、长度在近端和远端边缘超出目标病变长度10 mm 的DCB 扩张,时间为2 ~3 min[11]。完成球囊扩张后,造影复查病变血管通畅情况(图1)。B 组患者穿刺成功后置入5F 或6F动脉鞘,全身肝素化后,路径图指导下导管、导丝配合通过病变段,造影确认位于血管真腔。同样按照先预扩后用DCB 扩张,具体操作过程同A组。手术完成后按需要选择合适规格的血管缝合器或封堵器进行止血,穿刺点采用局部压迫止血。术后常规给予低分子肝素皮下注射,4 000 IU/q12 h,疗程3 d,同时口服双联抗血小板(阿司匹林100 mg/d、氯吡格雷75 mg/d)药物,1年后改为单阿司匹林治疗,在无禁忌症前提下终生服用单抗药物治疗。
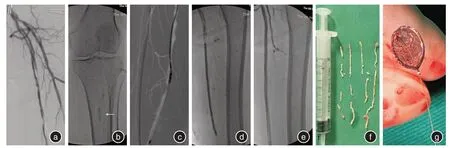
图1 患者手术过程Fig.1 Surgical procedure of patients
1.4 随访出院后嘱患者严格戒烟、低盐低脂饮食,严格控制血压及血糖,适当功能锻炼。术后第3、6、12 个月对全部82 例患者进行随访,包括一般体格检查,复查血管多普勒超声、ABI,对症状复现或超声多普勒检查怀疑有再狭窄时行CTA 检查,必要时行DSA 进一步评估靶血管通畅情况。
1.5 主要随访内容(1)术后Rutherford 分级、ABI以评估临床疗效;(2)晚期管腔丢失(LLL)、最小管腔直径(MLD)、管腔狭窄程度(>50%视为管腔再狭窄)评估管腔通畅情况;(3)术后并发症如造影剂肾病、动脉夹层等评估安全性。
1.6 统计学方法采用SPSS 26.0 统计软件数据进行分析,计量资料用者比较采用t检验;计数资料以百分率表示,采用χ2检验。以P< 0.05 为差异有统计学意义。
2 结果
2.1 手术结果A 组42 例靶病变均接受Turbo⁃Hawk 联合DCB 治疗方案再通成功,术中均使用保护伞,保护伞内有可视性栓子,无远端流出道栓塞(图1)。2 例出现非限流性小夹层,因未见明显血流受限及流速改变遂未给予特殊处理。1 例穿刺点血肿患者给予重新加压包扎并延长压迫时间后渗血停止,术后1 周行彩超检查提示基本吸收,并发症发生率7.1%(3/42)。住院期间无DA 相关并发症发生,1 例术前已有足趾坏死者接受截趾术,经治疗后创面愈合且不影响行走。B 组:40 例靶病变均再通成功,1 例出现非限流性夹层,给予置入补救性支架处理,1 例非限流性夹层未给予特殊处理,并发症发生率为5%(2/40)。两组中未出现围手术期死亡患者,术后即刻患肢缺血症状改善,3 d 后测量ABI 较术前明显改善,差异具有统计学意义(P<0.05)。
2.2 随访结果82 例患者均接受随访,随访时间随访11 ~16个月,平均随访(13.4±3.7)个月,82例患者全部保肢成功,随访期间下肢缺血症状无复发,保肢率为100%;彩超复查未见明显需手术干预的狭窄,一期管腔通畅率为100%。A 组和B 组两组患者的ABI 及Rutherford 分级对比:在伴有轻度钙化时,术前、术后3、6、12 个月两组患者ABI 比较差异均无统计学意义(均P> 0.05);在伴有中、重度钙化时,术前、术后3、6 个月两组患者ABI 比较差异均无统计学意义(均P> 0.05),术后12 个月A 组患者ABI 增长值高于B 组,差异有统计学意义(P<0.05,表3)。
2.2.1 MLD 及LLL 对比在伴有轻度钙化时,两组患者术前、术后即刻、术后12 个月MLD 差异均无统计学意义(均P> 0.05);在伴有中、重度钙化时,两组患者术前、术后即刻MLD 差异均无统计学意义(均P> 0.05,表2),术后12 个月A 组患者MLD 明显高于B 组,而A 组LLL 明显低于B 组(均P<0.05,表3)。
2.2.2 靶血管一期通畅率对比在伴有轻度钙化时,A 组和B 组术后12 个月通畅率比较,差异无统计学意义(P= 0.473);在伴有中、重度钙化时,12个月通畅率A 组高于B 组,差异具有统计学意义(均P<0.05)。
表3 术后两组患者情况对比Tab.3 Postoperative conditions of the two groups of patients were compared ±s
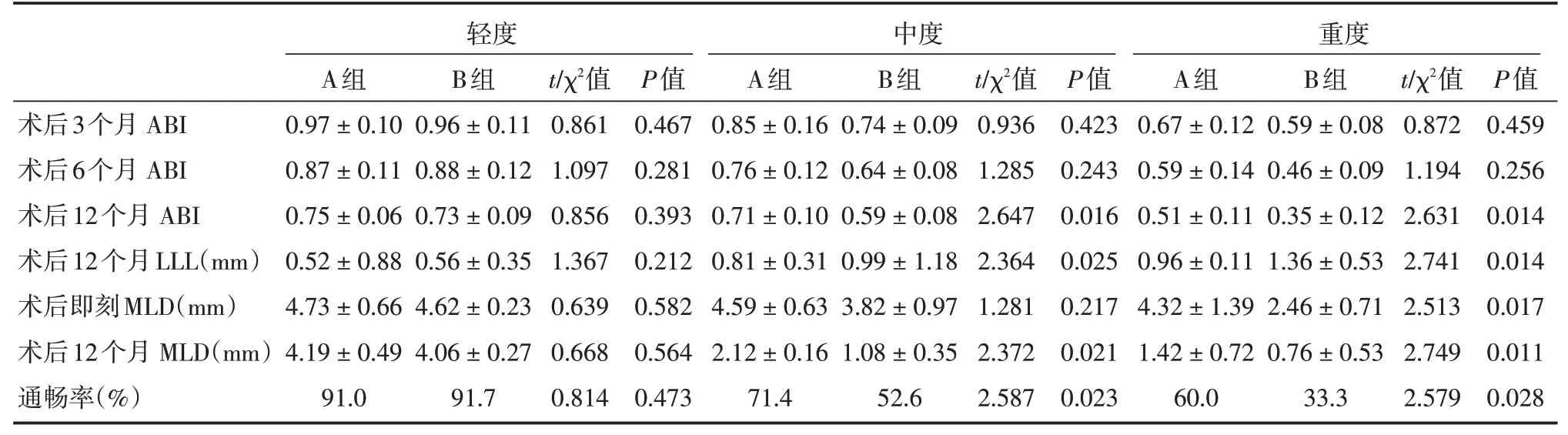
表3 术后两组患者情况对比Tab.3 Postoperative conditions of the two groups of patients were compared ±s
术后3个月ABI术后6个月ABI术后12个月ABI术后12个月LLL(mm)术后即刻MLD(mm)术后12个月MLD(mm)通畅率(%)轻度A组0.97±0.10 0.87±0.11 0.75±0.06 0.52±0.88 4.73±0.66 4.19±0.49 91.0 B组0.96±0.11 0.88±0.12 0.73±0.09 0.56±0.35 4.62±0.23 4.06±0.27 91.7 t/χ2值0.861 1.097 0.856 1.367 0.639 0.668 0.814 P值0.467 0.281 0.393 0.212 0.582 0.564 0.473中度A组0.85±0.16 0.76±0.12 0.71±0.10 0.81±0.31 4.59±0.63 2.12±0.16 71.4 B组0.74±0.09 0.64±0.08 0.59±0.08 0.99±1.18 3.82±0.97 1.08±0.35 52.6 t/χ2值0.936 1.285 2.647 2.364 1.281 2.372 2.587 P值0.423 0.243 0.016 0.025 0.217 0.021 0.023重度A组0.67±0.12 0.59±0.14 0.51±0.11 0.96±0.11 4.32±1.39 1.42±0.72 60.0 B组0.59±0.08 0.46±0.09 0.35±0.12 1.36±0.53 2.46±0.71 0.76±0.53 33.3 t/χ2值0.872 1.194 2.631 2.741 2.513 2.749 2.579 P值0.459 0.256 0.014 0.014 0.017 0.011 0.028
3 讨论
股腘动脉硬化闭塞症可引起供应肢体血液的血管内膜增厚、管腔狭窄或闭塞,从而导致肢体间歇性跛行、皮温降低、疼痛甚至溃疡或坏死等临床表现[12]。根据欧洲TASC⁃II 委员会建议,股腘动脉硬化闭塞症A 型和B 型病变更适合血管内介入治疗[13]。单纯球囊扩张术治疗会导致斑块破裂、管壁弹性回缩和限流性夹层形成,引起较高的再狭窄率[2]。多项研究表明支架的一期通畅率要高于单纯PTA,且两者在生存率和重大不良事件发生率方面无显著差异,但是在体内留置异物,容易出现支架变形、折断以及支架内再狭窄(in⁃stent restenosis,ISR)的风险[14-15]。国外的一项大型随机对照试验研究表明,DCB 所携带的紫杉醇虽然只是在血管壁短暂的转移,但是临床效果可持续5年之久[16]。DCB 已成为原发性TASC2A、B 级下肢动脉硬化闭塞症病变首选治疗方法,对于治疗TASCIIA、B 级股腘动脉硬化狭窄或闭塞的疗效得到了国内外专家的认可[4]。
有文献[17]指出,钙化病的存在阻碍了单纯DCB 治疗的效果,严重的钙化可能导致球囊被刺破。有研究发现钙化程度较轻的病变一期通畅率为100%,钙化程度较重的病变为69.37%,可以看出钙化对于DCB 有着出乎意料的影响。笔者分析主要是以下原因:(1)由于钙化的存在,DCB 在扩张过程中阻力更大,易扩张不完全,球囊不能与血管壁完全接触,导致所携带的抗增殖药物不能充分释放至内膜;(2)动脉血管钙化斑块是由于脂质沉积与血栓形成和机化所演变而成,DCB 所携带的抗内膜增生药物并不能穿透钙化斑块释放至血管内膜而发挥作用,所以术后再狭窄率随之升高。DA 利用斑块旋切导管对靶病变进行切割清除,是减少斑块体积和增加血流量的有效方式[18],能够给DCB 提供更好的血管条件,使其与靶血管贴合更充分以促进其表面药物的吸收[19],可单独应用DA 后将面临血管壁损伤、愈合和负性重塑的恶性循环,术后再狭窄率仍然很高[20]。DA 联合DCB 为伴有钙化的患者带来了益处,但TEPE 等[2]认为DA 联合DCB 手术会增加患者的经济负担,手术时间相对延长,从而导致术者及患者射线照射剂量增加,以及操作者本身对手术的熟练程度等均影响此类手术的广泛开展。
本中心通过对不同血管钙化程度下A 组和B组治疗效果的研究比较,对此类患者在手术方式的选择提供参考。在伴有轻度钙化的病变中,两组患者术后12 个月ABI、LLL 和通畅率无显著差异;在伴有中、重度钙化的病变中,12 个月通畅率A 组要高于B 组,在术后12 个月ABI 和LLL 差异均有统计学意义。FOLEY等[21]研究认为在伴有钙化的病变中,DA 联合DCB 比单纯DCB 治疗有更高的通畅率(88%vs. 68%),与本研究相仿;CIOPPA 等[6]报道采用DA联合DCB治疗严重钙化性股总动脉病变的30 例患者,12 个月一期通畅率仍为90.0%,高于单纯DCB 治疗50%;SIXT 等[22]则通过分析89 例股腘动脉再狭窄患者的1年通畅率及风险比证实了DA 联合DCB 效果明显。STAVROULAKIS 等[23]应用DA 联合DCB 对比单纯DCB 治疗ASO,认为两种方式治疗的血管区域都有良好的效果,二者差异无统计学意义。在本研究中,患者的并发症发生率要低于其他中心的数据,可能的原因是:(1)无论是DA 联合DCB 还是DCB 治疗,术前充分的血管准备是十分关键的,术中确保操作在真腔中进行,操作时应注意切割速度,明确待处理病变的血管内方向,避免非钙化区域反复切割[24];(2)为了使DCB 所携带的药物能够均匀的释放至血管内膜,在使用DCB 前给予预扩张是必要的;(3)保护伞的使用可明显降低下肢远端栓塞的风险,有研究[25-26]中使用SpiderFX 远端栓塞保护系统的患者,超过98%的患者获得了远端血管的保护,甚至在复杂病变的情况下,也获得了显著的临床改善。
综上所述,面对不同钙化程度的患者,应个体化选择治疗方案:在伴有轻度钙化病变的情况下,可以选择DCB 治疗,这样既可以减少并发症也可以减轻患者的经济负担;在中重度钙化病变中,选择DA 联合DCB 治疗要优于单纯DCB 治疗,可以给患者带来更好的治疗效果。本研究的不足之处在于病例数少、术后随访时间短,两者的远期通畅率有待多中心、大样本临床资料进一步研究、验证,笔者将会继续随访记录。
