药厂废液中的山梨醇纳滤分离实验研究
2020-04-30宗刚,张婷
宗 刚,张 婷
(西安工程大学 环境与化学工程学院,陕西 西安 710600)
山梨醇分子式C6H14O6,相对分子质量182.17。其重要存在形为液体或固体。工业上生产山梨醇通常由淀粉水解生成葡萄糖,在高压条件下加氢制得山梨醇。在实际的生产应用中,山梨醇最多用于生产VC。由于山梨醇有较好的保湿效果,在日化行业中,可以维持乳化剂的延伸作用与润湿性,增强乳化效果;在食品行业中可作为保湿剂,防止食品干燥;在造纸行业,添加山梨醇可以防止纸张表面粗糙干燥,使纸张光滑等等[1]。山梨醇的应用广泛,工业应用需求量也逐年增高,因此,山梨醇的资源化回收是必要可行且有经济价值的。
纳滤(NF)是一种介于反渗透(RO)和超滤(UF)之间的压力驱动膜分离过程,能截留的分子量在100~1000之间[2],纳滤膜的浓缩分离实质上是有机物或无机盐分子被选择性透过或截留的过程。分离机理类似于反渗透膜,主要分为S-K-K模型(非热力学模型)、空间-位阻模型、道南效应以及介电排斥效应等[3-6]。影响纳滤浓缩效果的因素主要有操作压力、溶液温度、回收率等。纳滤膜在工业上广泛应用于污废水中有机物的脱除与回收[7-10]。本研究采用分子量200~300聚酰胺纳滤膜回收药厂废液中的山梨醇,主要考察操作压力、温度、回收率及pH值对纳滤效果的影响,总结出纳滤技术回收山梨醇的最佳条件,为后期实现工业应用提供数据支撑。
1 实验部分
1.1 仪器与原料
AR224CN型分析天平(奥豪斯仪器有限公司);UV-1800型紫外可见分光光度计(上海美谱达仪器有限公司);JK205型COD恒温加热器(济南精密仪器仪表有限公司);FlowMem0021-HP型高压平板膜小试机(厦门福美科技有限公司)。
山梨醇水样(成分见表1陕西回天血液制品厂);CuSO4(AR);NaOH(AR);HgSO4(AR);K2Cr2O7(AR);(NH4)2Fe(SO4)2·6H2O(AR);Ag2SO4-H2SO4溶液;亚铁灵试剂。以上实验药品均来自天津市科密欧化学试剂有限公司,实验所用纳滤膜由厦门膜世达科技有限公司提供。膜参数见表2。

表1 原水水质特征Tab.1 Raw water quality characteristics

表2 纳滤膜参数Tab.2 Nanofiltration membrane parameters
纳滤反应装置采用三联高压纳滤小试机,见图1。

图1 纳滤实验装置Fig.1 Nanofiltration experiment device
1.2 实验内容与方法
从药厂取样山梨醇废水,检测其中山梨醇含量为33%,乙醇含量15%,此外还有少量无机盐Na+,分别在不同操作压力、温度、回收率、pH值条件下进行单因素纳滤膜浓缩分离实验,通过紫外可见分光光度法测定纳滤前后山梨醇含量变化,得到最优组合条件后进行正交实验进一步分析各因素之间的关系,研究不同影响因素下纳滤膜对山梨醇的分离特性。
1.3 紫外分光光度法
(1)原理 CuSO4与 NaOH 反应生成 Cu(OH)2,山梨醇与Cu(OH)2反应生成蓝色络合物,在一定波长下有最大吸收,可用紫外可见分光光度法测定。
(2)吸收曲线 烧杯中加入CuSO4溶液1.5mL、NaOH溶液1.4mL,混合均匀,再加入山梨醇溶液10mL,搅拌显色15min,离心分离,上层清液置于1cm厚的比色皿中,选择波长范围在620~700nm之间测定吸光度,每间隔10nm,测量一次,在最大吸收峰处每5nm测量一次。
(3)标准曲线 按(2)中实验方法,分别加入0.04、0.4、0.8、1.2、1.6、2.0g·L-1的山梨醇溶液,含量与吸光度呈良好线性关系,确定标准曲线。

图2 吸收曲线Fig.2 Absorption curve line

图3 标准曲线Fig.3 Stanadard curve line
由图3可以看出,山梨醇含量与吸光度线性关系R2=0.99992,呈显著相关性,可在后续实验中用于山梨醇含量的测定。
1.4 山梨醇纳滤浓缩效果参考指标
采用纳滤膜技术处理山梨醇废液,其浓缩效果好坏的评价指标主要有山梨醇截留率(γ)、膜通量(Jv)。

式中 Cp:透过液中山梨醇的质量浓度;Cb:原液中山梨醇的质量浓度。

式中 Vp:透过液的体积;A:膜的有效面积;t:操作时间。
2 结果与讨论
2.1 纯水渗透系数测定
在进行纳滤实验之前,在操作温度25℃,压力0.3~1.0MPa下进行纳滤膜的纯水透过实验,得到纳滤膜纯水通量随操作压力的线性关系见图4。其R2=0.99989,属于显著相关状态,说明纯水通量与压力的线性关系良好,即设备系统误差小,可以继续进行后续的纳滤实验。

图4 纳滤膜纯水通量与压力的线性关系Fig.4 Linear relationship between pure water flux and pressure of nanofiltration membrane
2.2 纳滤单因素实验
2.2.1 操作压力对纳滤膜浓缩分离的影响 进液为3L山梨醇水样,在pH值为7,温度25℃,设备连续运行90min,操作压力对纳滤实验结果的影响见图5。
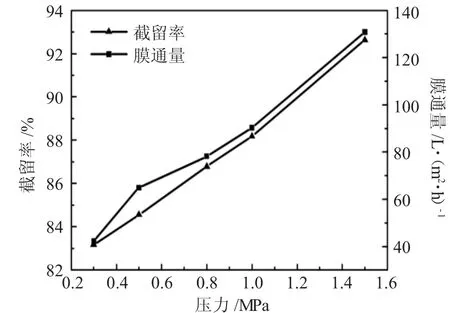
图5 操作压力对纳滤膜分离山梨醇原液的影响Fig.5 Effect of pressure on separation of sorbitol stock solution by nanofiltration membrane
由图5看出,随着压力的增加,山梨醇截留率与膜通量也随之增加,根据非热力学模型,可知溶剂渗透通量Jv与压力呈正相关,故压力增大,膜通量也随之增大;此外,由于纳滤过程为膜压力驱动过程,单位时间内透过膜的溶剂体积增大,但透过溶质的量没有增大,故山梨醇截留率也会随压力的增大而增大。在压力值最低点0.3MPa时,膜通量为最小值42.18L·(m2·h)-1,截留率为 83.17%;在压力值最大点 1.5MPa时,膜通量达到最大值 130.76L·(m2·h)-1,截留率增至92.63%。
2.2.2 温度对纳滤膜浓缩分离的影响 进液为3L山梨醇水样,在pH值为7,操作压力0.8MPa,设备连续运行90min,温度对纳滤实验结果的影响见图6。

图6 温度对纳滤膜分离山梨醇原液的影响Fig.6 Effect of temperature on separation of sorbitol stock solution by nanofiltratim membrane
由图6看出,糖醇类溶液的纳滤实验机制主要为扩散作用,随着温度的升高,膜通量上升,截留率减小。因为温度上升,则溶质扩散系数增大,单位时间内溶质通过膜的透过量增大,故膜通量增大;由截留率计算公式可知,透过液中的山梨醇含量升高,从而导致山梨醇截留率会下降。在温度最低点20℃时,膜通量为最小值 70.63L·(m2·h)-1,截留率为90.5%;在温度最高点35℃时,膜通量增加至93.28L·(m2·h)-1,截留率下降至 85.4%。
2.2.3 回收率对纳滤膜浓缩分离的影响 进液为3L山梨醇水样,在pH值为7,操作压力0.8MPa,温度25℃,设备连续运行90min,回收率(回收率为透过液体积与原液的体积比)对纳滤实验结果的影响见图7。
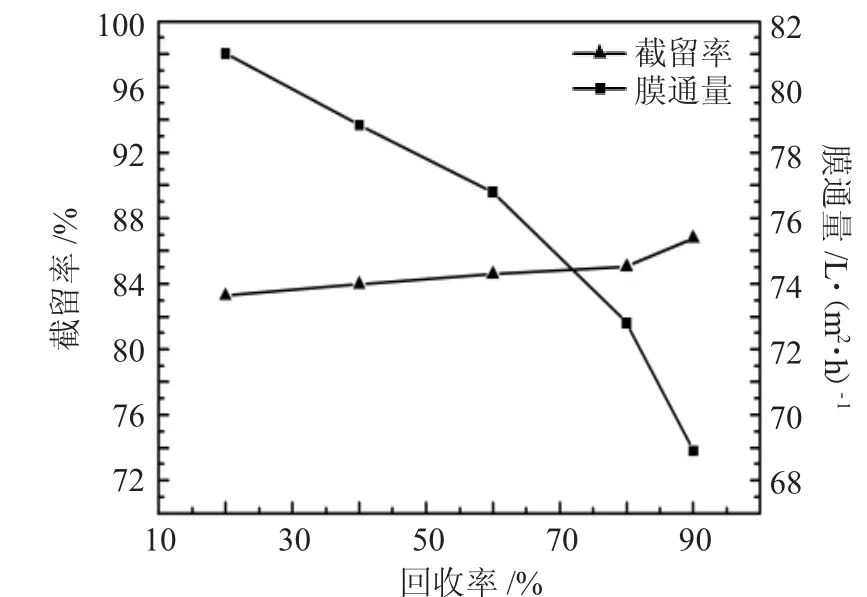
图7 回收率对纳滤膜分离山梨醇原液的影响Fig.7 Effect of recovery rate on separation of sorbitol stock solution by nanofiltration membrane
由图7可知,随着回收率的增高,膜通量下降,截留率增大。随着回收率的增加,吸附在纳滤膜的表面的山梨醇分子会增多,导致膜孔堵塞,单位时间内透过的溶质与溶剂通过量均会减小,相较溶剂的通过量而言,溶质的通过量下降的更多,因此,膜通量下降;同样由截留率计算公式可知,截留率会上升,但截留率上升缓慢。主要是由于溶液逐渐被浓缩,膜表面产生浓差极化现象,使得部分溶质透过膜又进入透过液中,透过液中的溶质含量随着回收率的上升而逐渐增大。在回收率最低点20%时,膜通量为最大值 80.95L·(m2·h)-1,截留率为 83.26%;当回收率提高至90%时,膜通量下降至最低点68.02L·(m2·h)-1截留率缓慢升高至86.76%。
2.2.4 pH值对纳滤膜浓缩分离的影响 进液为3L山梨醇水样,在操作压力为0.8MPa,温度25℃,设备连续运行90min,pH值对纳滤实验结果的影响见图8。
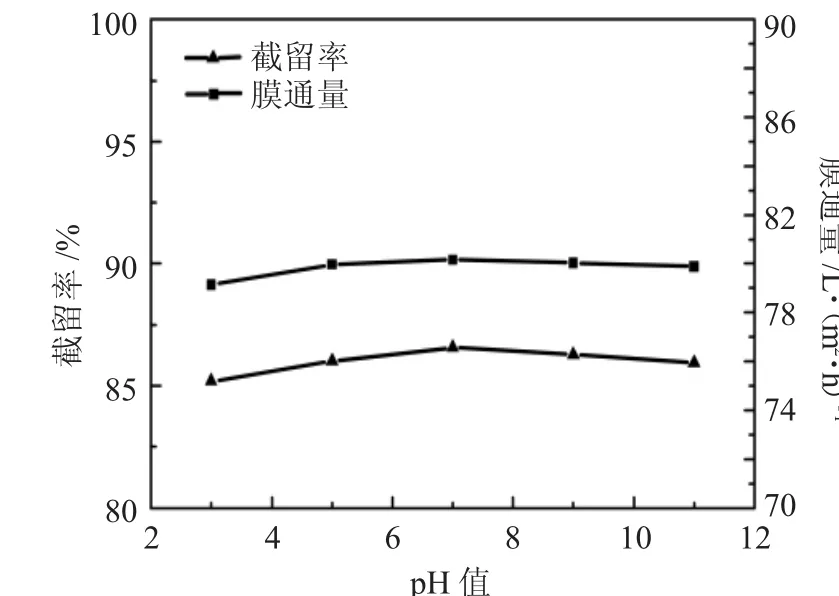
图8 pH值对纳滤膜分离山梨醇原液的影响Fig.8 Effect of pH on separation of sorbitol stock solution by nanofiltration membrane
由图8可知,pH值对山梨醇的截留率及膜通量影响并不明显,pH值为3时,膜通量为79.14L·(m2·h)-1,截留率85.18%;pH值为7时,膜通量为80.16L·(m2·h)-1,截留率86.56%;pH值为11时,膜通量79.89L·(m2·h)-1截留率85.93%。山梨醇为中性溶液,说明pH值对纳滤膜截留中性溶液的影响较弱,因此,后续实验中不将pH值做为变量因素,维持溶液中pH值为7即可。
2.3 纳滤正交实验
2.3.1 单因素最佳条件 根据2.2中实验结果,综合考虑设备的可持续性运行,选取NT103纳滤膜的浓缩山梨醇的最佳实验条件为操作压力1.0MPa,温度25℃,回收率60%,为了确定最佳的纳滤条件组合,探究各个影响因素之间的关系,运用Design Expert8.0.6软件进行正交实验分析。
2.3.2 正交实验结果
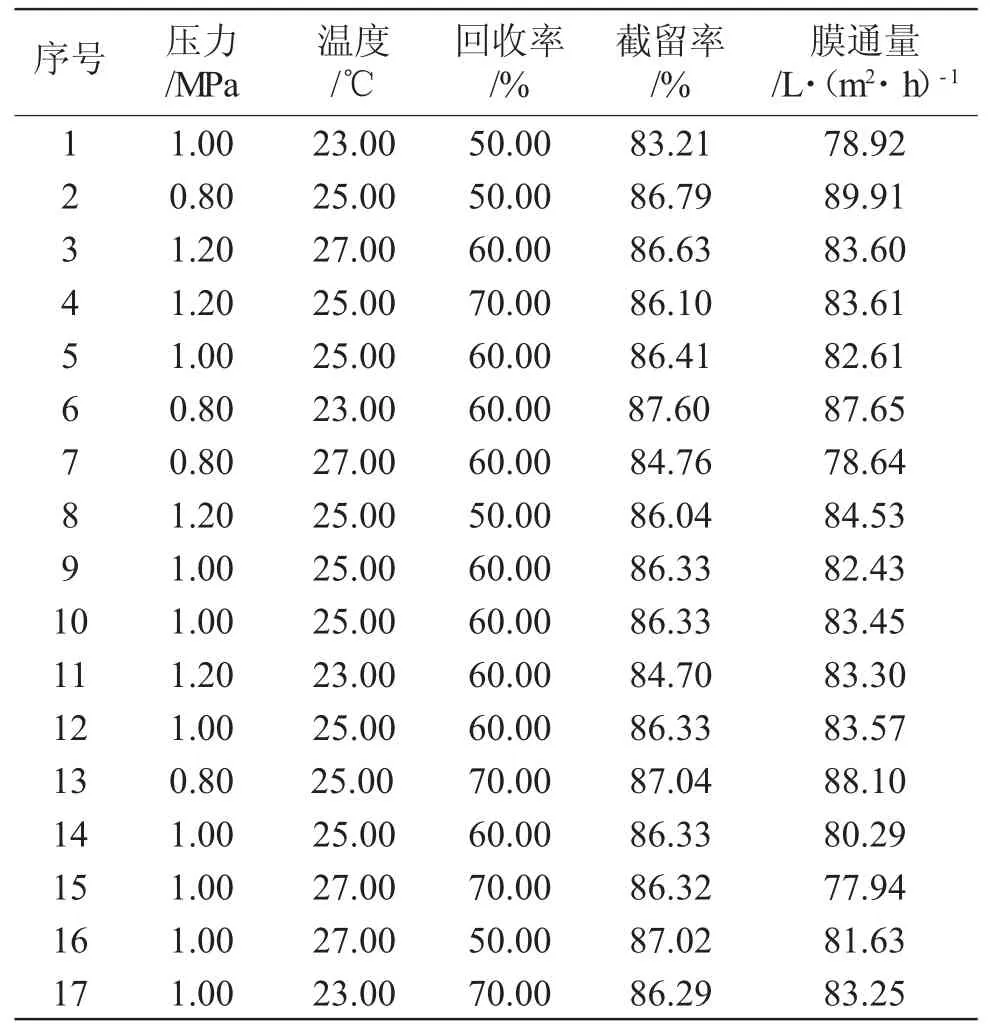
表3 正交实验表Tab.3 Orthogonal experiment table
Design Expert8.0.6软件安排出17组正交实验结果见表3,分别根据不同的实验条件进行实验,并得到相应的山梨醇截留率与膜通量。
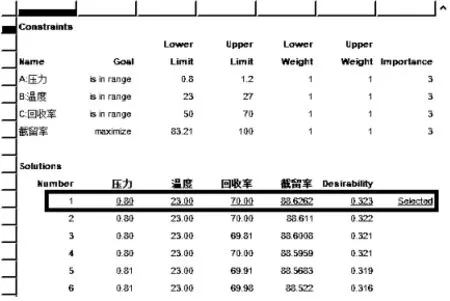
图9 软件预测结果Fig.9 Software prediction results
如图9所示,根据正交实验结果,系统预测出最佳的纳滤实验组合为:操作压力0.8MPa,温度23℃,回收率70%,此时截留率可达到88.62%。
为了进一步验证预测结果的准确性,设计进行一组验证试验,根据预测组合条件进行纳滤试验,试验结果见表4。

表4 验证实验结果Tab.4 Verification experiment results
由表4可知,软件预测值与实际验证值之间误差为0.75%,没有显著性差异。因此纳滤实验最佳组合条件即为:操作压力0.8MPa,温度23℃,回收率70%。
3 结论
聚酰胺纳滤膜NT103能够有效的浓缩分离出药厂废液中的山梨醇。对于成分比较稳定的山梨醇废液,操作压力,操作温度,回收率是影响纳滤膜浓缩分离效果的主要影响因素。
(1)在纳滤膜浓缩回收山梨醇实验中,在保持其他因素稳定的前提下:操作压力的提高有利于膜通量与山梨醇截留率的提高;温度增加有利于膜通量的提高,但却会使山梨醇的截留率下降;回收率的提高,会导致膜通量下降,并产生浓差极化现象,使得截留率缓慢提高;pH值对山梨醇溶液的纳滤效果影响较弱。
(2)分析各个因素的互相关系,由17组正交实验结果得到山梨醇的最佳操作条件为:操作压力0.8MPa,温度23℃,回收率70%,此最优条件下的山梨醇截留率可达到87.96%,膜通量为84.32L·(m2·h)-1。
