人工智能辅助诊断肺结节的临床价值研究
2020-04-21李甜李晓东刘敬禹
李甜,李晓东,刘敬禹*
近年来,肺癌已经成为威胁人类健康最常见的恶性肿瘤,其发病率、死亡率均居所有恶性肿瘤首位[1],早期诊断和精准治疗能从根本上减少我国肺癌患者的死亡人数。当前提高肺癌生存率的唯一方法就是端口前移,早期肺癌的影像学多表现为肺结节,在临床实践中,低剂量螺旋CT(LDCT)是用于检测肺结节病变的主要手段[2]。LDCT是一种易获取、辐射小、成本低、耐受良好的实验室检查。然而,其结果受到阅片者主观方面的影响大,这意味着缺乏经验的放射科医生更容易误诊或漏诊。人工智能(artificial intelligence,AI)在医学诊断领域的应用备受国内外学者关注,其中肺结节筛查系统凭借深度学习记忆及强大图片识别功能,能充分显示肺结节诊断的内在价值[3]。本研究参考病理和影像学结果,比较AI与医师阅片对磨玻璃结节(ground glass nodule,GGN)和恶性肺结节的诊断情况,以指导临床应用。
1 对象与方法
1.1 研究对象 选取2017年7月—2019年7月于锦州医科大学附属第三医院确诊的120例肺结节患者(共筛查出256个肺结节)为研究对象。研究对象纳入标准:(1)符合《肺结节诊治中国专家共识(2018年版)》相关诊断标准[4];(2)对本研究知情同意,自愿参加。排除标准:(1)直径≤5 mm的肺结节;(2)弥漫性分布的磨玻璃影;(3)既往被确诊为肺结核;(4)其他部位恶性肿瘤患者。本研究经锦州医科大学附属第三医院伦理委员会审核批准。120例研究对象中,男47例(39.2%),女73例(60.8%),平均年龄(59.7±9.3)岁;256个肺结节中实性结节147个(57.4%),平均直径(9.01±3.11)mm;GGN 109个(42.6%),平均直径(10.24±5.26)mm。
1.2 研究方法
1.2.1 影像学扫描 所有患者均由东芝128层CT扫描系统完成LDCT检查,低剂量扫描参数为[2]:管电压120 kVp,管电流≤ 40 mAs,扫描层厚 5 mm,重建图像层厚为1 mm,纵隔窗:窗宽350 HU,窗位50 HU;肺窗:窗宽 1 500 HU,窗位 -600 HU。
1.2.2 阅片方法 分别采用AI阅片和医师阅片方法判读120例肺结节患者胸部CT。(1)AI阅片法由1例呼吸科医师使用肺结节筛查系统进行辅助诊断。即将所有患者胸部LDCT影像资料导入推想科技提供的InferRead CT Lung肺癌智能筛查系统中,该系统以40万训练数据集为根基,数据库数据来源于全国多家大型三级甲等医院,软件能将疑似肺结节的部位进行准确标记,右侧栏目内可显示结节直径、CT值、性质(实性结节或GGN)、征象(分叶征、毛刺征、血管集束征等)及恶性概率(恶性概率>70%为高危结节,恶性概率50%~70%为中危结节,恶性概率<50%为低危结节;其中高危结节提示为恶性肺结节,其他提示为良性肺结节)等信息,此外医师可借助右侧工具栏内的工具更加清晰地呈现肺结节形态,如软件自动提供的三维重建栏目可清晰显示肺结节与周边血管、细支气管及胸膜之间的关系(见图1)。(2)医师阅片法由2例具有30年工作经验的呼吸科医师对120例肺结节患者胸部CT进行分析诊断(未使用肺结节筛查系统的情况下进行),按照《肺结节诊治中国专家共识(2018年版)》诊断标准进行分类[4],并根据肺结节大小、密度、与血管和支气管关系进行良恶性评估,人为将病变划分为可能良性及可疑恶性。3例审查员均未知患者的任何病情。
1.2.3 病理检查 54个GGN行手术切除后,标本均在锦州医科大学附属第三医院病理科完成病理检查。所有标本均经福尔马林固定,石蜡包埋切片,用特殊方法染色,最终病理诊断由2例主治医师以上职称的病理医师确定。不典型腺瘤样增生为单排的不典型上皮细胞衬覆在肺泡壁的非侵犯性病变;原位腺癌是指肿瘤细胞沿肺泡结构单纯附壁式生长;微浸润腺癌(minimally invasive adenocarcinoma,MIA)是以附壁式结构生长为主且浸润灶范围<5 mm的腺癌;浸润性腺癌(invasive adenocarcinoma,IAC)特指至少1个浸润范围 >5 mm的病灶,其生长方式包括附壁式、乳头状、微乳头样、腺泡样和实性生长等;结核球病理基础主要是纤维组织包裹的干酪坏死灶或增殖性结核灶。其中,除结核球外,其他均为恶性肺结节。
1.3 统计学方法 采用SPSS 16.0统计软件对数据进行统计学分析。计量资料以(x ±s)表示;计数资料以相对数表示,组间比较采用χ2检验;AI阅片与医师阅片的一致性评价采用Kappa检验,以Kappa值≥0.400为一致性较好[5]。应用受试者工作特征(ROC)曲线分析两种阅片方式对恶性肺结节的诊断价值,ROC曲线下面积(AUC)0.5~0.7表明具有较低准确性,>0.7~0.9具有一定准确性,>0.9具有较高准确性。以P<0.05为差异有统计学意义。
2 结果
2.1 病理结果 54个经过病理检查的肺结节中,恶性肺结节47个,其中不典型腺瘤样增生4个,原位腺癌5个,微浸润腺癌4个,浸润性腺癌34个;良性肺结节7例,均为结核球。
2.2 两种阅片方式诊断GGN情况比较 AI阅片诊断GGN的阳性率(87.2%)高于医师阅片(68.8%),差异有统计学意义(χ2=10.686,P=0.001;见表1),两种诊断方法的吻合度较弱,Kappa系数为0.019。
2.3 两种阅片方式对恶性肺结节的诊断价值 以病理检查结果为“金标准”,AI阅片提示低中危肺结节8个中,经病理证实后良、恶性肺结节各4个;AI提示高危肺结节46个中,病理证实良、恶性肺结节分别为3、43个;医师阅片提示可能良性肺结节12个中,病理证实后良、恶性肺结节各6个;医师阅片提示可疑肺结节42个中,病理证实良、恶性肺结节分别为1、41个。医师阅片与AI阅片诊断恶性肺结节的AUC分别为0.845 、0.743,均>0.7(见表2、图2)。
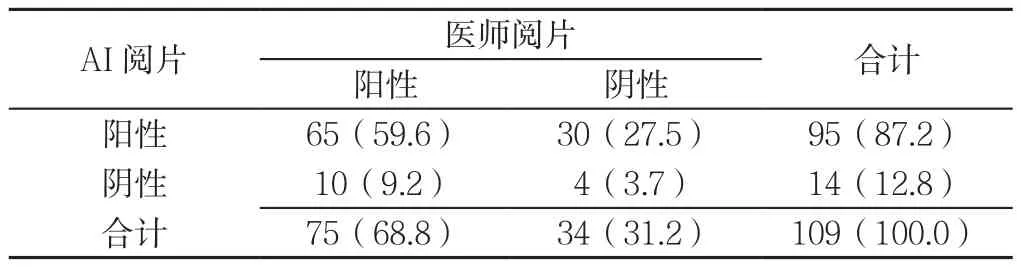
表1 两种阅片方式诊断GGN情况对比〔n(%)〕Table 1 Comparison of the diagnosis results of GGN by two methods of reading
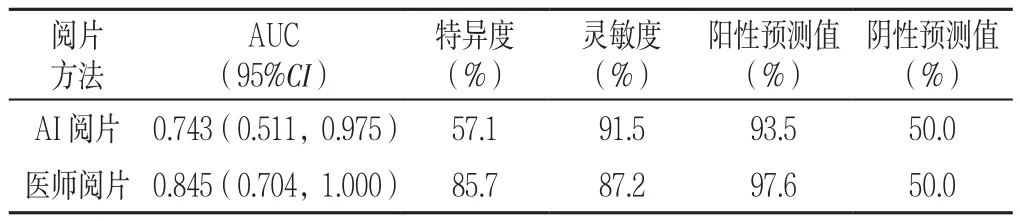
表2 两种阅片方法诊断恶性肺结节的临床价值比较Table 2 Comparison of clinical value of two methods in the diagnosis of malignant pulmonary nodules
3 讨论
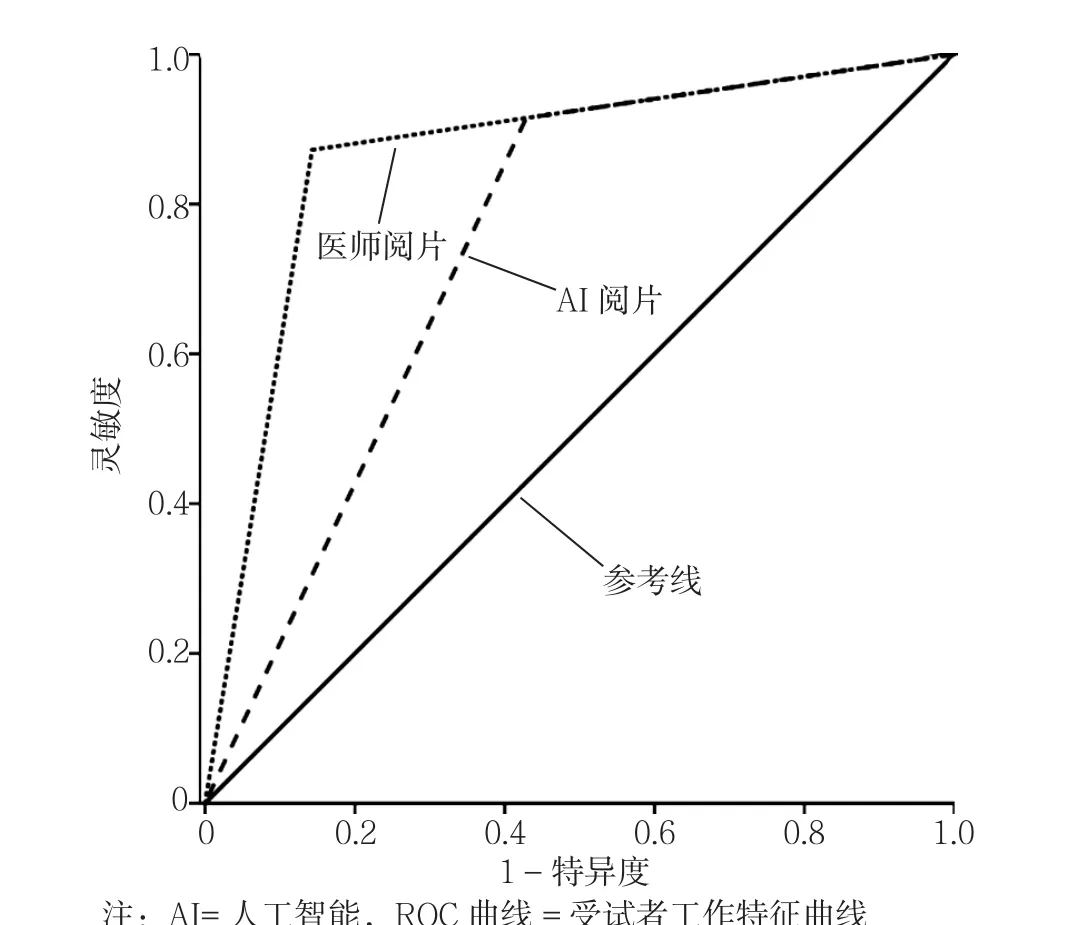
图2 AI阅片与医师阅片诊断恶性肺结节的ROC曲线Figure 2 ROC curves of the diagnosis results of malignant pulmonary nodules by AI reading and physician reading
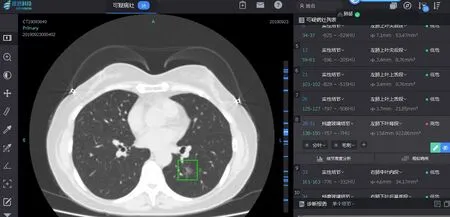
图 1 InferRead CT Lung 肺癌智能筛查系统Figure 1 InferRead CT Lung intelligent screening system for lung cancer
目前,肺癌是全球癌症相关死亡的主要原因[6],70%~80%的患者出现临床症状就诊时已为中晚期,失去手术治疗的最佳时机[7]。但相关研究结果表明,Ⅰ期肺癌经过手术切除后5年生存率可接近100%[8],提示早发现、早诊断及早治疗可明显提高肺癌患者的生存率。肺结节是肺癌早期的影像学表现之一,目前国内外相关指南建议年龄≥40岁且有吸烟史、环境或高危职业暴露史、肺部基础疾病等高危人群完善胸部低剂量CT进行肺结节筛查[4]。面对筛查人群增加和影像医师逐年短缺的现状,尤其在三级甲等医院单独靠人工阅片无法满足当今肺结节的筛查工作。伴随5G时代的来临,AI应用于多个领域,尤其在医学放射影像领域较成熟。肺结节筛查系统能够有效挖取肺癌的核心特征,协助医师发现早期肺癌并鉴别其良恶性,基于此,本研究结合病理和随访结果,对比AI阅片与放射科医师阅片在GGN中的诊断阳性率,分析不同阅片方式下良恶性肺结节的判断情况。
GGN是指高分辨率CT(HRCT)上呈模糊、似磨玻璃样的密度增高影,可清晰显示病灶内的支气管和血管走形。研究表明其病理表现遵循不典型腺瘤样增生→原位癌→微浸润性腺癌→浸润性腺癌的生长演变规律[9],故GGN的筛查尤为重要。本研究纳入的256个肺结节中,GGN共计109个,AI诊断GGN的阳性率高于医师阅片,可能原因为:(1)薄层LDCT作为早期筛查肺结节主要手段,辐射量相当于普通CT的1/4~1/5[10],但在肺结节的定量检测、小结节图像显示率等方面增加了阅片难度[11]。(2)肺结节筛查工作量大,医师相对短缺,受视力、精力等影响,直径较小、密度较低的GGN容易被漏诊。(3)肺结节筛查系统通过原始数据的建立、图像的分割、特征提取、亚型分类、数据集训练等多个流程对肺结节病变特征深度学习[12],可在数秒内发现肺结节,缩短了阅片时间,尤其在GGN的筛查中,可明显降低假阴性结果的发生,为经验不足的医师提供帮助,提高了判读胸部CT影像学的效率[13]。虽然AI阅片结果中出现了部分假阳性结节,但医师可在AI阅片的基础上对疑似病灶上下层面进行逐层分析,对肺结节进行选择性剔除,降低肺结节的误诊率。
肺结节的良恶性鉴别仍是目前放射科医师、临床医师共同面临的挑战,早期识别恶性肺结节,并及时给予临床积极干预,可挽救患者的生命,减少我国肺癌的死亡率。本研究发现AI阅片和医师阅片诊断恶性肺结节的灵敏度相似,前者特异度弱于后者,影响其结果的主要原因考虑:(1)由于肺脏的血管、支气管、肺组织等结构复杂,肺结节的位置和形态多样,肺内局部实变影、支气管内痰液栓,局灶性间质纤维化、肺内淋巴结、血管等均可误诊为中高危肺结节[14];(2)AI阅片未能准确预测部分GGN肺结节的恶性概率。本研究中有4个肺结节,AI阅片提示为低中危结节,而手术切除病理检查证实1个为微浸润性腺癌、3个为浸润性腺癌。故为提高AI阅片诊断准确率,需要进一步加强软件数据集的质量管理,扩大数据集训练数量,以进一步减少误诊、提升恶性概率的准确性[15]。虽然医师阅片特异度高于AI阅片,AUC更大,但人工阅片也存在一些缺陷,如对于病灶小、密度低的肺结节,医师在阅片过程中由于视力疲乏、精力有限等因素,易出现漏诊。本研究纳入的2例浸润性肺癌患者,术前43个月、3个月影像学均提示存在肺结节,而影像报告提示胸部CT未见异常。此外早期肺癌缺乏特异性影像学表现,即使部分病灶出现毛刺征、分叶征、空泡征、胸膜凹陷征、血管集束征等其中1个或几个恶性征象,但病理结果也未必是恶性。为克服两种阅片方式单独使用带来的不便,可采取AI联合医师阅片方式,一方面AI阅片可在短时间内标记出结节的位置、形态、大小及恶性征象等信息,避免了人工阅片的主观因素偏差[16],减少漏诊率;另一方面医师可对AI疑似的肺结节进行薄层原始图像和多平面重建、曲面重建、表面阴影成像、容积再现等图像处理和重建,以观察病灶的大小、密度、形状、病灶与支气管、病灶与血管、病灶与胸膜之间的关系[17],有助于肺结节的早期定性。
但是,本研究也存在一定的局限性,受恶性病灶样本量的限制,由于浸润前病变有发展为浸润性肺癌的潜在危险性,故本文将浸润前病变(原位癌、微浸润性腺癌)纳入恶性组中,分组存在一定偏倚。有待进一步搜集并扩大样本量,减少偏倚导致的误差。
综上所述,AI技术在肺结节的筛选过程中起着至关重要的作用,与人工阅片比较,可降低GGN漏诊率,值得推广应用。AI在肺结节筛查领域取得了突破性进展,但从临床诊断学角度分析,单一的肺结节筛查并不能完全满足临床诊疗的需求,临床医师需要根据患者病情全面评估以做出明确诊断。因此,倡导“AI﹢人工”模式应用于临床工作。
作者贡献:李甜负责文章的构思与设计,研究的实施与可行性分析,论文撰写;李甜、李晓东负责数据收集与整理,统计学处理;李甜、刘敬禹负责结果的分析与解释;刘敬禹负责论文的修订,文章的质量控制及审校,并对文章整体负责,监督管理;李甜、李晓东、刘敬禹负责英文的修订。
本文无利益冲突。
