瓣膜置换同期改良迷宫射频消融术治疗瓣膜性心脏疾病合并房颤的临床效果评价
2020-04-16郭志祥张成鑫葛圣林
郭志祥,张成鑫,葛圣林
房颤是一种人类常见的心律失常,在普通人群中的发生率约为1.5%~2.0%。与无心律失常的病人相比,房颤(atrial fibrillation,AF)病人的脑卒中的发生率增高5倍、心力衰竭(heart failure,HF)的发生率增加3倍,同时可导致病人死亡风险的增高[1]。对于此类药物难治性房颤,建议采用手术或经皮消融的非药物治疗[2]。最初的房颤手术消融尝试可以追溯到20世纪80年代,包括左房隔离和走廊手术;然而直到1987年Cox-Maze手术的发展,才可靠地实现了手术消融的成功[3]。传统迷宫手术主要基于切割缝合,虽治疗房颤效果可靠,但操作难度大、时间长、创伤较大,一直未能在临床广泛推广使用。近年来,随着射频消融技术及设备的不断进步,改良双极射频消融迷宫术得到临床越来越多的认可。本研究拟分析安徽医科大学第一附属医院收治的心脏瓣膜疾病合并房颤的病人,总结其手术治疗经验,以提高临床治疗效果。
1 资料与方法
1.1 一般资料 选取安徽医科大学第一附属医院2016年1月至2018年12月行心脏瓣膜手术同期行双极射频消融迷宫术治疗AF的病人66例,术前常规行超声心动图确诊,年龄50岁以上者均行冠脉血管成像或冠脉造影排除冠心病。其中男20例,女46例;年龄(51.8±6.7)岁,体质量(58.0±9.7)kg,同时合并中度以上三尖瓣关闭不全39例。术前合并疾病包括高血压病、II型糖尿病、脑梗死等,见表1。先前研究的多元回归分析结果显示左心房内径(LAD)>60.0 mm可作为AF复发的独立危险因素[4],为消除混杂因素的影响,本研究排除了术前超声心动图显示LAD>60.0 mm的病人,其他排除标准包括术前合并冠心病的病人,术前心功能分级(NYHA)Ⅳ级的病人,以及其他研究人员认为不适合纳入研究的病人。病人或其近亲属知情同意,本研究符合《世界医学协会赫尔辛基宣言》相关要求。
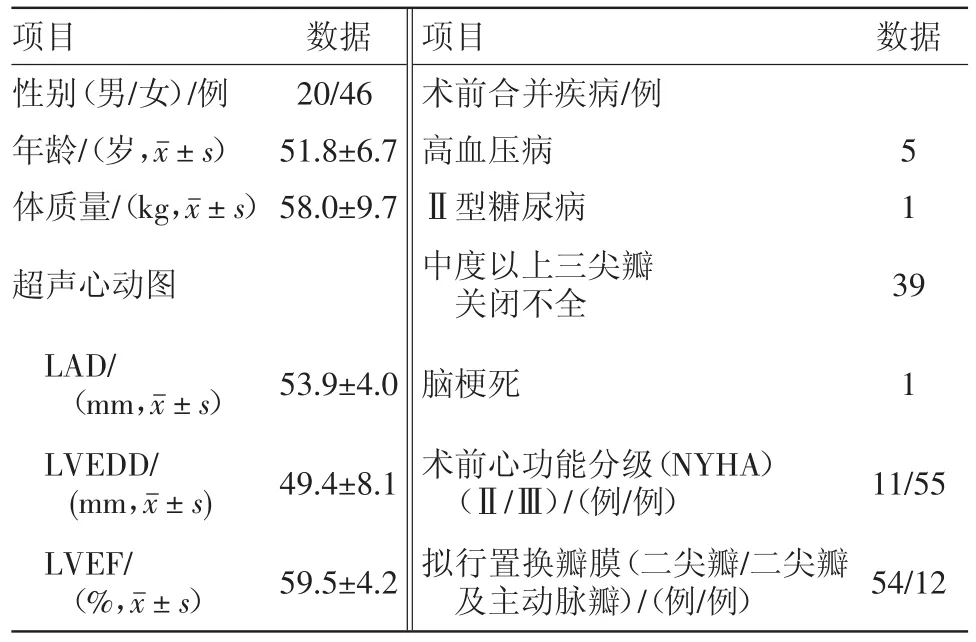
表1 心脏瓣膜手术同期行双极射频消融迷宫术治疗房颤66例一般情况
1.2 方法 手术方法手术均在全麻气管插管、中度低体温、体外循环下进行。麻醉满意后,常规胸骨正中切口,建立体外循环;“I”形切开心包,游离上、下腔静脉并套绕阻断套带。升主动脉近心包反折处双重缝合对口同心主动脉插管荷包,近心端缝合灌注插管荷包,上、下腔静脉缝插管荷包。经升主动脉根部直接灌心肌保护液,心脏自动停搏,心包腔内置冰泥;右肺静脉前庭做左房切口,手术采用美国AtriCure公司的双极射频消融系统,左右肺静脉前庭予以消融钳隔离消融,如探查见左心房存在陈旧性血栓,则予以清除,并予以大量清水冲洗;行左房平行房室沟切口;左房后壁行上下消融,与肺静脉隔离线形成“box”,行右肺静脉后壁至二尖瓣后瓣P2处消融;左心耳切除,切断marshall韧带,消融肺静脉处部自主神经节;左心耳至左肺静脉消融,形成“box”;切除右心耳,做心耳至三尖瓣环消融线;右房中段纵切口,界中段至上下腔静脉、右肺静脉及冠状静脉窦消融,三尖瓣峡部消融。消融完毕后,按常规行瓣膜置换术。所有病人术中全部安置心表面临时起搏导线。
1.3 术后治疗及随访 术后监测心率,若血流动力学稳定,则常规静脉泵入胺碘酮0.6~0.8 g/d,控制心率在70~100次/分,心率低于70次/分,停用胺碘酮。进食后改为口服胺碘酮每次0.2 g,一天两次,持续1周,然后改为每天0.2 g至术后6个月,并根据病人心律情况具体调整,控制心率在(70~100次/分,注意定期复查心电图。术后心率慢者可以使用临时起搏器,使心率维持在70次/分以上;术后3~5 d心率仍<60次/分者,可停用胺碘酮,必要时给予提升心率药物。于术后即时、出院时及术后6个月时,复查12导联心电图。
本研究观察的主要终点为术后的房颤转为窦性心律的例数,次要终点为术后病人心功能改善情况,包括心功能分级和超声心动图结果。
1.4 统计学方法 本研究为单臂观察性研究,采用SPSS10.0统计学软件进行治疗前后的差异性检验,两两时点间的比较为配对t检验;其中的计数资料,采用χ2检验,P<0.05为差异有统计学意义。
2 结果
本组行二尖瓣置换及三尖瓣成型合并射频消融50例,同期双瓣置换及三尖瓣成型合并射频消融9例,余瓣膜置换同期行射频消融7例。升主动脉阻断时间(99.2±30.8)min,体外循环时间(140.4±32.4)min,ICU住院时间(48.8±36.5)h。术后12导联心电图结果显示:术后即时转为窦性心律的例数66例,转窦率为100%,出院时为60例,转窦率90.9%,术后6个月时为56例,转窦率84.8%。无Ⅲ度房室传导阻滞发生,无因出血二次开胸,无围手术期死亡。术后7 d复查超声心动图,结果显示病人左房、左室减小明显,射血分数明显升高,心功能明显改善(结果见表2)。
3 讨论
房颤是心脏瓣膜病变的常见合并症,不仅明显影响心功能,且增加继发血栓、卒中等风险,严重影响病人的生存质量和远期生存率[5]。心脏手术同期行外科消融治疗房颤可以提高病人生存质量,降低卒中率,延长生存时间,同时不增加手术风险[6]。目前美国心脏协会(AHA)、美国心脏病学会(ACC)的指南中均指出,在择期行其他类型心脏手术的房颤病人中建议同期房颤射频消融术,但指南中也说明了由于数据有限,这一建议仅为C级证据推荐[7]。Gillinov等的研究表明,在持续性房颤的病人中,心内直视下二尖瓣手术同期行房颤射频消融术能够显著提高术后1年的房颤治愈率[8]。截至2008年,北美已有超过一半的二尖瓣疾病伴发房颤的病人同时接受二尖瓣置换和房颤射频消融手术[9]。而在我国目前仍远远低于这个数字。
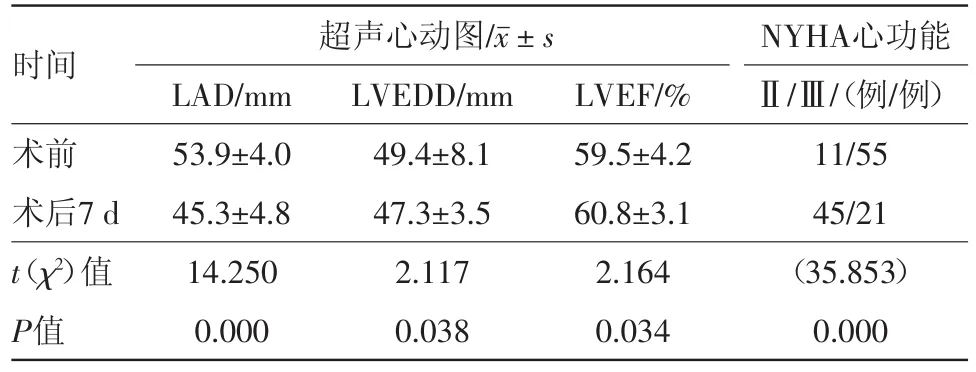
表2 心脏瓣膜手术同期行双极射频消融迷宫术治疗房颤66例随访结果
已有研究表明二尖瓣病变及左心房增大是房颤发病的危险因素。二尖瓣病变的病人常常伴发房颤。二尖瓣返流的病人即使术前是窦性心律,但如果病人术前左心房较大,那么在二尖瓣置换术后也可能转变为房颤心律,尤其是术前左心房内径≥50mm的病人[10-12]。由于二尖瓣疾病的病人心房容积或压力增加,血流动力学超负荷导致左心房扩张,房室扩张导致心房壁变薄、细胞间纤维化和脂肪浸润,左心房结构性增大,增加房颤的发生率[13]。因为随着左心房内径增加,折返径路增多,需要增加左右肺静脉间消融线,才能彻底打断折返环路,从而破坏房颤的维持机制[14]。
经典的迷宫Ⅲ型手术是外科治疗房颤的“金标准”,但由于其操作较复杂、时间长、创伤大、对心功能影响明显等并,一直未能广泛推广[15]。射频消融可使得心房壁线状凝固坏死,避免了大量“切和缝”的操作,达到简化流程,缩短时间,减少术后出血的目的[16]。近期研究结果显示[17],风湿性心脏瓣膜病合并房颤的病人行瓣膜置换同期行改良迷宫手术对心功能的改善优于仅行瓣膜置换手术,明显降低远期死亡率及脑梗发生率,提高生活质量。本研究心内直视下瓣膜置换同期采用双极射频消融迷宫术治疗房颤,术后即时转为窦性心律的例数66例,转窦率为100%,无死亡病例,出院时为60例,转窦率90.9%,术后六个月时为56例,转窦率84.8%,治疗效果满意;术后7日复查超声心动图,结果显示病人左房、左室减小明显,射血分数明显升高,心功能明显改善(见表2),结果显示通过改良消融路径,合理规划步骤,缩短阻断时间,能达到治疗房颤、保护心肌、改善左心功能的作用,具有很高的实用价值,值得推广[18]。
通过本组治疗,我们体会:①手术采用美国AtriCure公司的双极射频消融系统,安全、操作简便、使用方便。②双极射频消融系统虽能透壁自动提示,但局部点状透壁仍可触发应答,因此一般同部位消融次数2~3次,组织较厚位置可适当增加消融次数且每次消融前注意把消融钳上焦痂擦拭干净。③在消融双侧肺静脉环时可用导尿管牵引消融钳,简单易行,不额外增加住院费用,且消融线尽可能靠近左心房前庭以避免肺静脉狭窄。④对于部分左房间沟暴露困难病人,可采用右上下肺静脉小切口消融左房后壁,再经房间隔入路置换二尖瓣。⑤左心耳结扎及内口缝闭,左房-左心耳残余分流发生率高,易发生血栓及脑卒中,因此建议切除左心耳。⑥消融过程中避免损伤冠状动脉。⑦右房消融时远离房室结,避免传导阻滞。⑧注意避免损伤二尖瓣瓣环及三尖瓣瓣环。⑨消融中,注意消融线完全连接,尽可能形成“box”,增加房颤治愈率。⑩常规缝置起搏导线,避免心脏不良事故的发生。⑪术后常规应用胺碘酮,减少心律失常的发生。
