甲磺酸阿帕替尼治疗晚期胃癌的不良事件分析
2020-04-13柏峰高熙方献英宋波张宇王全祥
柏峰,高熙,方献英,宋波,张宇,王全祥
(1.信阳市中心医院 肿瘤内科二病区,河南 信阳 464000;2.河南科技大学医学院,河南 洛阳 471023)
肿瘤的增殖和转移依赖肿瘤血管的形成,甲磺酸阿帕替尼高选择性结合血管内皮生长因子受体-2(vascular endothelial growth factor receptor-2,VEGFR-2),抑制肿瘤血管生成进而抑制肿瘤的增殖和转移[1-2]。作为中国独立开发的第一种口服小分子VEGFR-2酪氨酸激酶抑制剂,甲磺酸阿帕替尼在胃癌Ⅱ/Ⅲ临床试验中有良好疗效[3-4],在肺癌、乳腺癌、肝癌等Ⅱ期临床试验中显示了良好疗效,并进行了Ⅲ期临床试验。基于此2014年被CFDA批准上市。尽管已经证实甲磺酸阿帕替尼临床效果及安全性良好,但该药上市时间短,临床医生尚不能充分认识该药的毒副反应,特别是一些毒副反应虽发生率低却是致命的。本研究总结回顾了在临床中应用甲磺酸阿帕替尼的不良事件情况及处理情况,以供参考,以避免严重不良事件的发生。
1 资料与方法
1.1 研究对象收集2016年1月至2017年9月信阳市中心医院收治的采用甲磺酸阿帕替尼治疗的晚期胃癌患者52例作为研究组。纳入标准:(1)临床分期为Ⅳ期;(2)均经病理学诊断;(3)Karnofsky评分≥60分或ECOG评分≤2分;(4)年龄≥18岁;(5)心电图、肝、肾功能无明显异常;(6)预期生存大于3个月。排除标准:(1)严重高血压;(2)活动性出血。使用回顾性调查方法,逐一审查医疗记录,记录患者基本信息、既往史、诊断、肿瘤病理、联合其他用药情况、患者住院期间实验室检查及影像学检查,病历记录的不良反应情况等。由2位研究者按上述内容自行提取资料,然后交叉核对,具有争论的,与第3人讨论出最终结果。筛选出同时期未使用甲磺酸阿帕替尼化疗的50例晚期胃癌患者作为对照组。所有患者及家属均签署知情同意书。本研究经信阳市中心医院医学伦理委员会审核批准。
1.2 治疗方案研究组患者口服甲磺酸阿帕替尼(江苏恒瑞医药股份有限公司,国药准字H20140103)联合化疗或单药口服甲磺酸阿帕替尼。甲磺酸阿帕替尼用法为口服0.75~0.85 g,每日1次,28 d为1个周期,如不能耐受或病情进展则停药。若出现Ⅲ级或Ⅳ级不良反应,暂停用药或减量至0.5 g口服,每日1次。对照组患者应用化疗不联合甲磺酸阿帕替尼,化疗方案有FOLFOX4、卡培他滨、替吉奥等。
1.3 观察指标不良事件(AE)的认定由2位研究者依据事件发生时间、药物使用以及疾病相关症状等综合判定,具有争论的与第3人讨论最终结果。所有不良事件有客观检查数据的,以发生最严重级别评价,需主观评价的以病历记录情况评价,分级评价标准采用CTCAE V4.0。不良事件的分级由2位研究者评定,具有争论的与第3人讨论最终结果。通过RESCIST V1.1评估药物效果。
1.4 统计学方法采用SPSS 17.0统计软件进行数据处理分析。一般资料、不良反应发生率、有效率以频数和率(%)表示,组间比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 一般资料本研究共筛选出102例患者。两组一般资料比较,差异无统计学意义(均P>0.05)。见表1。
2.2 甲磺酸阿帕替尼不良事件发生率所有不良事件限于从治疗开始到治疗时间结束后的8周。52例患者总不良事件发生率为90.4%,其中3/4级不良事件发生率为28.8%。甲磺酸阿帕替尼联合化疗不良事件发生率高于单药甲磺酸阿帕替尼,差异有统计学意义(P<0.05)。见表2。
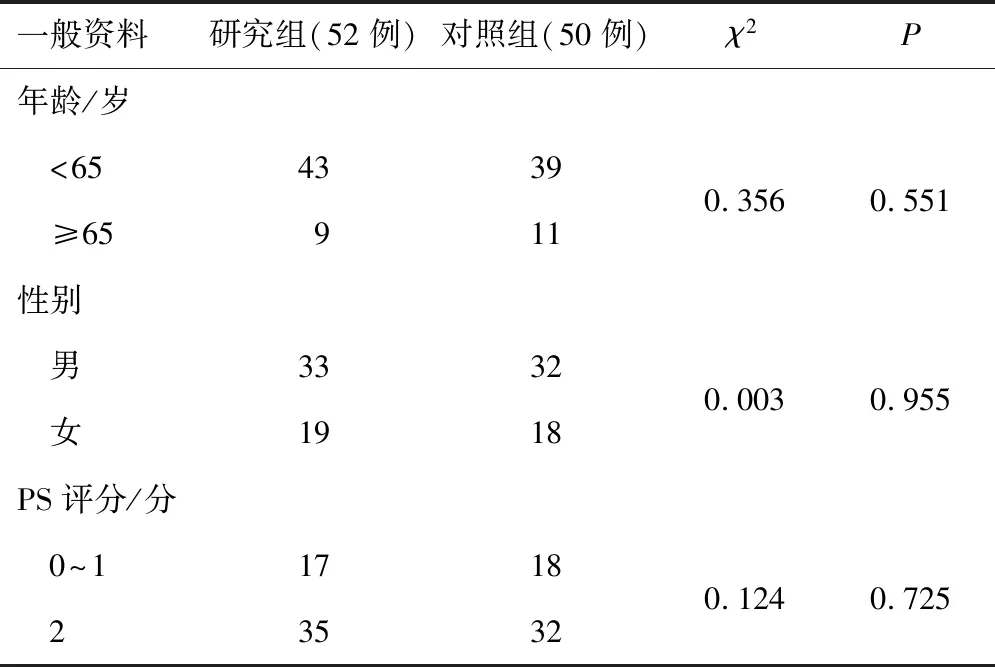
表1 两组一般资料比较(n)
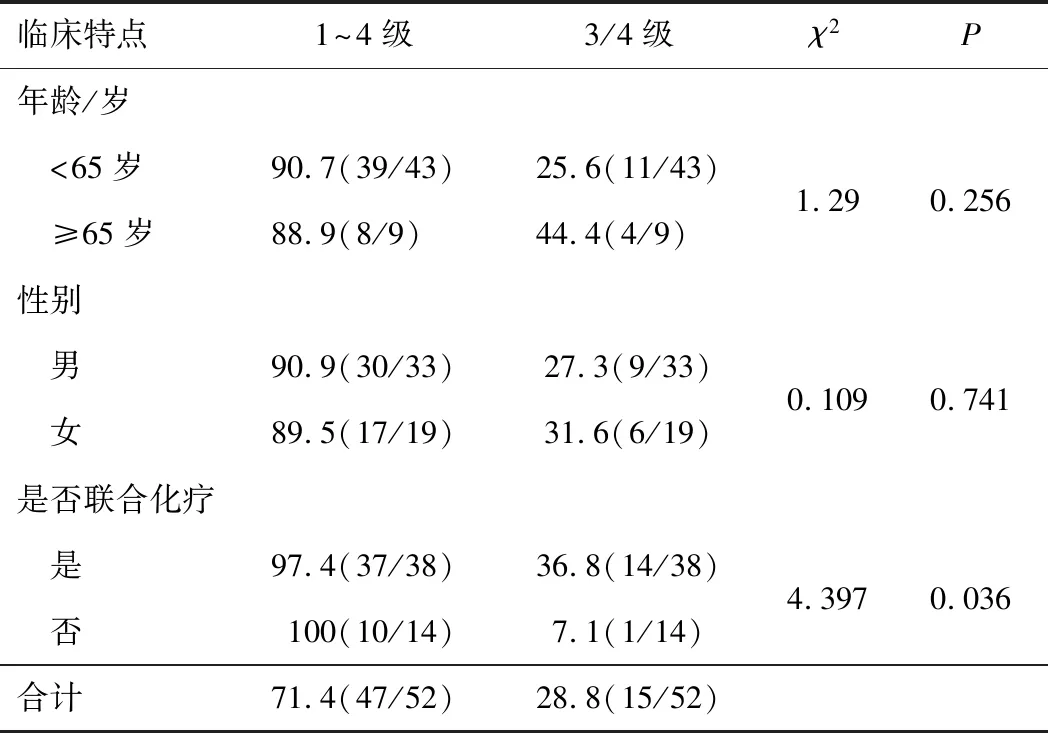
表2 甲磺酸阿帕替尼相关不良事件发生率
2.3 甲磺酸阿帕替尼各种不良反应发生情况及处理甲磺酸阿帕替尼治疗胃癌的主要不良反应为中性粒细胞减少等血液学毒性及手足综合征、恶心呕吐、高血压等非血液学毒性,大多为1/2级不良事件,少数3级不良事件,经对症处理后好转,患者耐受性良好。见表3。
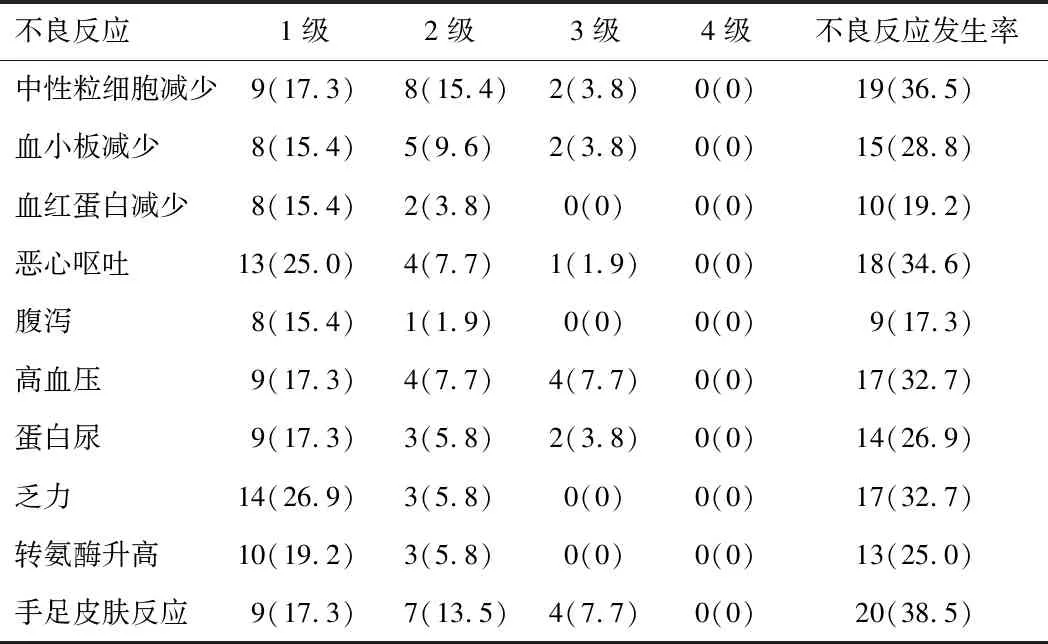
表3 甲磺酸阿帕替尼各种不良反应发生率[n(%)]
2.3.1血液学毒性 本研究中中性粒细胞减少发生率为36.1%,其中2例患者发生3级不良事件,均发生在联合化疗组,未发生中性粒细胞减少性发热及感染,在应用粒细胞集落刺激因子治疗后恢复正常。血小板减少发生率为27.9%,其中3例患者发生3级不良事件,当血小板计数低于50×109L-1时,予以白介素-11升血小板治疗,同时给予止血敏预防出血,血小板均恢复正常且未发生出血。血红蛋白减少多为1/2级,予以加强营养治疗。
2.3.2非血液学毒性 本研究中手足综合征发生率为39.3%,其中4例发生3级不良事件,予以外用尿素软膏及抗真菌、抗生素软膏,必要时口服止痛药物,待不良反应下降1个级别,予以下调甲磺酸阿帕替尼剂量口服。恶心呕吐发生率为34.4%,其中2例3级不良事件,予以五羟色胺3受体拮抗药联合糖皮质激素对症处理后不良反应可控。乏力发生率为32.8%,嘱患者注意休息,适度参与活动,加强营养,给予康复运动治疗及心理治疗,同时针对引起乏力的贫血、缺氧等因素对症支持治疗。高血压发生率为32.8%,4例发生3级不良事件,予以钙离子拮抗剂联合利尿剂口服后血压可控。蛋白尿发生率为26.2%,2例发生3级不良事件,暂停用药,予以密切监测24 h尿蛋白定量,直至24 h尿蛋白低于3.5 g,下调甲磺酸阿帕替尼剂量继续口服。
2.4 两组不良反应比较研究组和对照组不良反应经对症处理后均可以控制,两组血液学毒性、消化道反应、乏力以及转氨酶升高不良反应发生率比较,差异无统计学意义(均P>0.05)。研究组高血压、蛋白尿以及手足皮肤反应发生率高于对照组,差异有统计学意义(均P<0.05)。见表4。
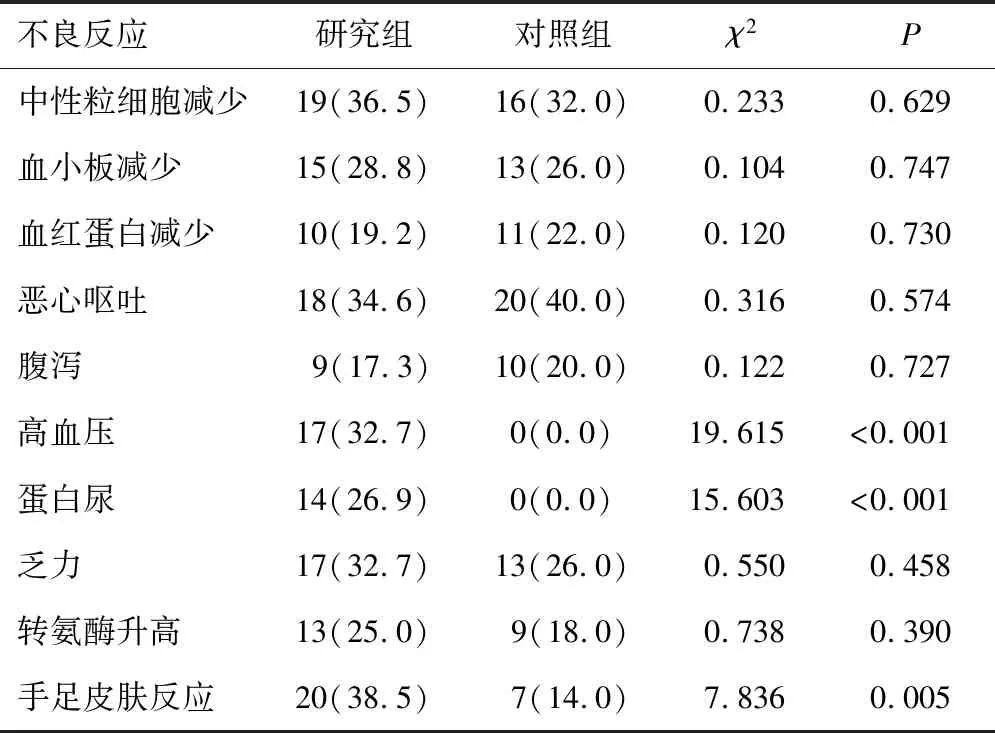
表4 两组不良反应比较[n(%)]
2.5 两组疗效比较及亚组疗效分析研究组疾病控制率(57.7%)高于对照组(36.0%),差异有统计学意义(P<0.05)。见表5。在研究组内甲磺酸阿帕替尼单药14例,甲磺酸阿帕替尼联合化疗38例。14例单药患者CR 0例、PR 0例、SD 4例、PD 10例,疾病控制率为28.6%;38例联合化疗患者CR 0例、PR 6例、SD 20例、PD 12例,疾病控制率为68.4%,甲磺酸阿帕替尼联合化疗疾病控制率高于单药甲磺酸阿帕替尼,差异有统计学意义(χ2=6.656,P<0.05)。
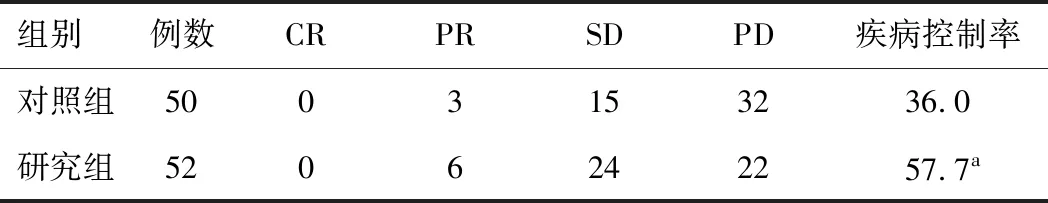
表5 两组疗效比较(n,%)
注:与对照组比较,aχ2=4.814,P=0.028。
3 讨论
甲磺酸阿帕替尼是中国独立开发的第1种口服小分子VEGFR-2酪氨酸激酶抑制剂,得到了国家“十一五”和“十二五”重大新药创建基金的支持。另一种大分子抗VEGFR-2酪氨酸激酶抑制剂,同时期在国外开发,经美国食品药品管理局批准优先上市,并于2015年纳入NCCN临床实践指南,证实了针对VEGFR-2靶点药物的疗效[1]。本研究总结了52例甲磺酸阿帕替尼治疗晚期胃癌的情况,近期疗效显示疾病控制率达到57.7%,优于对照组,与多个临床试验数据一致[4-7]。甲磺酸阿帕替尼在治疗胃癌中显示了良好的效果,同时其在多种肿瘤中也有良好疗效[7-12],是近年来少有的具有广谱疗效的靶向药物。
甲磺酸阿帕替尼的不良事件主要为1/2级,3/4级不良事件较少。年龄和性别亚组的不良事件发生率无统计学差异,但年龄组65岁及以上患者仅9例,可能存在统计学偏倚,实际应用中仍建议考虑高龄因素。甲磺酸阿帕替尼联合化疗的不良事件发生率高于单药口服甲磺酸阿帕替尼,和对照组不良反应相似,但联合化疗组疗效优于单药甲磺酸阿帕替尼组以及对照组,且不良事件多为1/2级,经对症处理可控,如患者一般情况可,无化疗禁忌,仍建议甲磺酸阿帕替尼联合化疗用药。
血液学毒性(中性粒细胞减少、血小板减少)和非血液学毒性(手足综合征、恶心和呕吐、高血压、乏力和蛋白尿)是甲磺酸阿帕替尼的主要不良反应,和多个临床研究报道数据一致[13-15]。其中大多数为1/2级不良反应,3/4级不良反应可通过暂停用药、减少剂量和对症治疗来控制。依据临床应用的专家共识[1],高血压、蛋白尿和手足皮肤反应是需要较为重视的不良反应。应用甲磺酸阿帕替尼时,若出现血压升高,建议应用血管紧张素转换酶抑制剂及血管紧张素受体拮抗剂控制血压,不建议应用非二氢吡啶类钙离子通道阻滞剂,高血压危象患者应永久停药[16]。因甲磺酸阿帕替尼引发的蛋白尿,目前还没有明确的治疗方法,可以适当应用血管紧张素转换酶抑制剂和血管紧张素受体拮抗剂,发现肾功能损伤或肾病综合征,应立即停药,并予以支持治疗[1]。出现手足皮肤反应患者需避免手足皮肤机械性损伤和摩擦,外用尿素软膏和糖皮质激素软膏,根据病情应用抗真菌药物和抗生素,也可以适当口服B族维生素和非甾体类止痛药。随着用药时间延长手足皮肤反应症状会逐渐减轻,如出现3级不良反应无缓解或加重,应永久停药[1]。
本研究是回顾性研究,反映了临床应用甲磺酸阿帕替尼的实际情况,由于实际应用中对患者的主观选择,对某些高危因素的回避,以及因患者治疗间歇不在院对不良反应的观察疏漏,病例中对轻度无需处理的不良反应的遗漏记录,有存在降低某些不良反应发生率的可能。晚期恶性肿瘤患者多具有合并症、并发症,以及多种药物联合使用,比如化疗药,则可能增加不良事件的发生率。另本研究数据提取及判定过程中虽有多人按照既定方案操作,仍不能避免主观选择偏倚及观察偏倚。
总而言之,在甲磺酸阿帕替尼临床应用中,根据适应证选择患者并注意监测不良反应,不良反应可控,耐受性好,疗效确切。由于该药上市时间短,前瞻性的临床研究仍在进一步探索中,对不良反应的观察和防治仍需要更多临床数据的积累。
