腹腔镜下直肠癌前切除术中保留左结肠动脉的意义
2020-03-26周志翔龚光伟赵丹李胜文
周志翔,龚光伟,赵丹,李胜文
(武汉科技大学附属孝感医院胃肠外科,湖北 孝感 432600)
在我国直肠癌的发病率逐年增高[1],手术仍然是其主要治疗方式,全直肠系膜切除(total mesorectal excision,TME)作为直肠癌前切除术的重要原则,已经得到国内外专家的肯定,使越来越多的病人从中获益[2],而在处理肠系膜下动脉(inferior mesenteric artery,IMA)过程中是否保留左结肠动脉(left colonic artery,LCA),目前仍然存在争议[3]。因此,笔者回顾性分析了2017年3月至2018年7月期间在武汉科技大学附属孝感医院胃肠外科行腹腔镜下直肠癌前切除术中129例病人的临床资料,比较其中行IMA高位结扎病人和IMA低位结扎保留LCA病人的围手术期临床资料,探讨在腹腔镜下直肠癌前切除术中IMA低位结扎保留LCA病人的临床疗效,现报告如下。
资料与方法
一、一般资料
纳入2017年3月至2018年7月期间我院收治并确诊的129例实施腹腔镜直肠癌前切除术的病人,根据术中是否保留LCA分为两组:保留LCA组(观察组,51例)与不保留LCA组(对照组,78例)。观察组中男性29例,女性22例;≤65岁27例,>65岁24例;体质量指数为(21.25±2.11) kg/m2;吻合口距齿状线距离为(3.21±0.23) cm。对照组中男性43例,女性35例;≤65岁40例,>65岁38例;体质量指数为(22.36±1.81) kg/m2;吻合口距齿状线距离为(3.46±0.11) cm。两组病人的年龄、性别、体质量指数、吻合口距齿状线距离等一般资料比较,差异均无统计学意义(均P>0.05),具有可比性。
二、纳入标准与排除标准
纳入标准:①病历资料记录完整;②病理确诊为直肠癌;③无远处转移;④肿瘤未侵犯周围组织。排除标准:①急诊合并肠梗阻或穿孔;②肝肾功能严重不全;③合并其他恶性疾病;④腹腔镜手术中转开腹。
三、手术方法[4-5]
观察组采取头侧中间入路方式,病人取头低脚高右倾截石位,采用常规腹腔镜直肠手术五孔穿刺法,推开Treitz韧带处空肠,游离附着该处的韧带及筋膜,将小肠推至右上腹,助手辅助显露Treitz韧带、腹主动脉及左侧结肠系膜;打开IMA头侧腹主动脉表面腹膜进入左结肠后间隙,向尾侧清扫IMA根部淋巴结;另于骶骨岬水平打开直乙结肠系膜并进入乙状结肠后间隙,清扫IMA下方淋巴结,完成乙状结肠后间隙与左结肠后间隙会师。于IMA根部向左侧裸化血管,显露IMA、肠系膜下静脉和左结肠血管、乙状结肠血管等相关血管,在IMA发出LCA的远侧1 cm左右离断IMA并保留LCA。对照组采用中间入路方式,于骶骨岬水平打开直乙结肠系膜并进入乙状结肠后间隙,清扫第253组淋巴结至IMA根部,在腹主动脉发出IMA约1 cm处结扎IMA。两组均按照TME原则[6-7]行Dixon术式常规切除直肠癌病灶,重建肠道,留置引流管。
四、观察指标
比较两组病人的手术时间、术中出血量、分离脾区数、预防性回肠造瘘数、吻合口漏数、术后肛门首次排气时间、第253组淋巴结清扫数等,其中排除预防性回肠造口病例术后通气时间的统计。
五、统计学方法
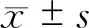
结 果
两组病人均顺利完成手术,术中无明显并发症。观察组与对照组在手术时间及术后肛门首次排气时间方面,差异均具有统计学意义(P值分别为0.008和0.004)。观察组有1例出现吻合口漏,2例因肿瘤较大切除肠管较多,需游离脾区;对照组6例出现吻合口漏,4例因近端肠管血运欠佳而切除肠管变短游离脾区,2例因吻合后血运较差行预防性末端回肠造瘘术,两组间差异均无统计学意义(均P>0.05)。在术中出血量、清扫第253组淋巴结数方面,差异无统计学意义(P>0.05)。具体结果详见表1、表2。
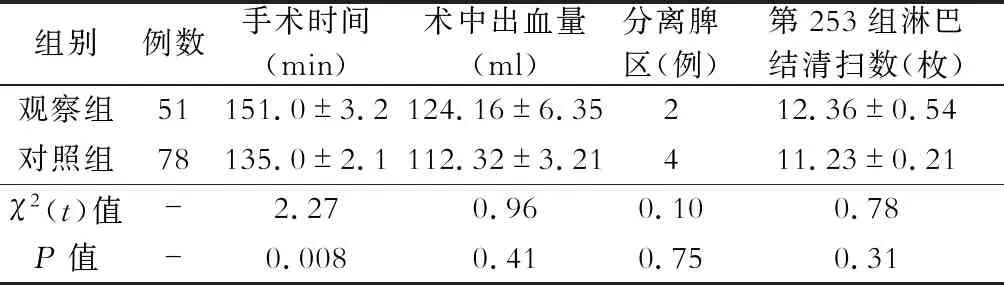
表1 两组病人术中情况比较
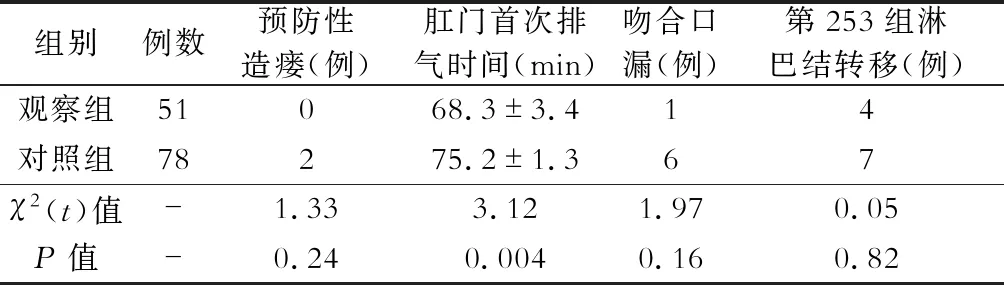
表2 两组病人术后情况比较
讨 论
腹腔镜下直肠癌前切除术已日趋成熟和规范,相比保留LCA,部分文献认为不保留LCA可以使第三站(第253组)淋巴结得到更彻底清扫,有利于对肿瘤正确分期及预后评估,减少吻合口张力,操作更简便[8]。而保留LCA则可以改善吻合口血供。因而,争论的焦点主要集中在吻合口血供和淋巴结清扫的彻底性上。
研究表明,吻合口漏的发生,在术中与肠管血供、吻合口张力及手术者因素密切相关,其发生率为2.7%~19.0%[9-11]。不保留LCA后,吻合口近端的血供主要来自Drummond边缘动脉弓和Riolan动脉弓,Drummond边缘动脉弓在脾区通常存在吻合不全(Griffiths′点),中结肠左支的血供通过Griffiths′点后才能供给吻合口。肠系膜动脉造影报道差异性较大,Griffiths′点缺失或薄弱的发生率为9%~43%,正常存在的为48%。一般情况下,Riolan动脉弓血流少且缓慢,可改善结肠的侧支循环,国人Riolan动脉弓的出现率为10%~40.3%[12]。因此,如Riolan动脉弓缺如或Griffiths′点缺失,则可影响吻合口血供。GessLer等[13]研究显示通过单因素分析和多因素分析证实保留LCA可显著降低吻合口漏发生率。黄俊等[14]研究116例腹腔镜下直肠前切除术病人,Riolan弓缺如率为60.3%,8例发生吻合口漏,全部是Riolan弓缺如。而Cirocchi等[15]通过Meta分析,结果显示保留LCA组与不保留LCA组的吻合口漏发生率差异并无统计学意义。本研究中,不保留LCA组4例因近端肠管血运欠佳而切除肠管,吻合距离不够而游离脾区,2例吻合后,考虑吻合口血运不佳,行预防性末端回肠造瘘术,6例出现术后吻合口漏;而保留LCA组仅1例出现吻合口漏。虽然两组差异无统计学意义,但笔者认为从临床角度考虑,保留LCA组1例与不保留LCA组6例比较是有差别的,影响了治疗效果。此外,随着人口老龄化的加速,合并糖尿病、高脂血症、动脉粥样硬化等慢性病的病人增多,可导致全身动脉的狭窄和闭塞,势必导致吻合口血供更差,有研究者通过术中分别夹闭IMA后,利用激光多普勒血流检测直肠断端血供,发现直肠断端血供明显下降,老年病人下降更明显[16]。笔者统计的7例术后吻合口漏病人,有5例为65岁以上合并高血压或糖尿病病人。研究报道[17]缺血性肠病的好发人群是老年合并糖尿病、动脉粥样硬化群体,好发部位是左半结肠,以脾区为中心,导致肠壁供血不足。因此,笔者认为保留LCA,尤其是合并老年糖尿病、动脉粥样硬化的病人,可以改善吻合口血供,降低吻合口漏的风险。另外本研究中保留LCA组病人术后肛门首次排气时间明显短于不保留LCA组[(68.3±3.4) min比(75.2±1.3) min,P=0.004],考虑术后吻合口处灌注更加充足,减少了肠道缺血导致的肠痉挛、蠕动慢等因素。
直肠癌最常见的转移途径之一是淋巴结转移,其淋巴引流第三站为IMA根部区域淋巴结(第253组淋巴结),第253组淋巴结转移的发生率为0.3%~8.6%[18-19],清扫第三站是直肠癌的标准术式,清扫范围为IMA根部、LCA发出部和肠系膜下静脉内侧。文献报道[18-19]腹腔镜下直肠癌根治术中,保留LCA组与不保留LCA组在淋巴结清扫数目上差异无统计学意义[20-21]。本研究显示第253组淋巴结检出率中不保留LCA组为(11.23±0.21)枚,保留组为(12.36±0.54)枚,淋巴结转移检出率分别为8.97%、7.84%,差异无统计学意义。国内外的大量回顾性研究[22-24]显示,保留LCA与不保留LCA的5年生存率差异无统计学意义,笔者认为保留LCA不影响第三站的淋巴结清扫。
有研究报道[25],实施保留LCA的直肠癌根治术,能获得与不保留LCA一样的游离结肠距离;还有研究报道[23],同时保留LCA有助于肠管保持下垂的松弛状态,保障吻合口血运。本研究中,保留LCA组中,有2例因肿瘤浸润,切除肠管较多,需游离脾区;不保留组4例因血运较差,切除肠管较多,需游离脾区,两者比较差异无统计学意义。笔者认为近端肠管的适当保留和结肠侧腹膜的充分游离,保留LCA组与不保留LCA组比较,前者不会增加吻合口张力。
术中出血量和手术时间影响手术方式的接受度[26]。本研究中,保留LCA组手术时间为(151.0±3.2) min,术中出血量为(124.16±6.35) ml,比不保留LCA组时间长、出血量略高,考虑为寻找LCA的分叉有关。有研究[21]认为,保留LCA的直肠癌根治术不会增加手术时间及术中出血量。笔者认为,这些术者因素会随着手术学习曲线的增加,得到改善,保留LCA组头侧中间入路更容易进入正确的层面,显露及裸化血管更容易,便于有效清扫第三站淋巴结,为保留LCA的直肠癌根治术增加了可操作性, 随着腔镜技术的提升,特别是3D腹腔镜的逐渐开展,IMA相关血管显露更加清楚,立体感更强,血管的游离难度相对降低,保留LCA的术式越来越多地被接受。
