原发性甲状旁腺功能亢进伴急性肾损伤
2019-12-31郭锦洲许书添李世军
郭锦洲 许书添 李世军
病史摘要
病史68岁女性患者,因“干呕、纳差3周,关节痛2周,发现血清肌酐(SCr)升高3d”于2015-07-03入院。
2015-06-12患者上呼吸道感染后出现干呕、食欲下降,伴口干、多饮、多尿,未予重视。6月19日出现双侧踝关节、膝关节、髋关节疼痛,不影响行走,6月27日出现双下肢乏力,偶有头晕,无尿量减少。6月30日就诊于我院门诊,查血白蛋白40.4 g/L,球蛋白35.6 g/L,钾2.5 mmol/L,钠135 mmol/L,氯97 mmol/L,总二氧化碳24 mmol/L,钙5.10 mmol/L,尿素15.3 mmol/L,SCr 190 μmol/L,尿酸538 μmol/L,体液免疫IgA、IgG、IgM正常,抗核抗体(ANA)+,抗中性粒细胞胞质抗体(ANCA)阴性,给予口服补钾等治疗,症状无缓解。7月2日我院急诊科就诊,查血钙5.20 mmol/L,磷1.6 mmol/L,SCr 198 μmol/L,钾2.5 mmol/L,钠127.7 mmol/L,动脉血气示离子钙2.39 mmol/L,乳酸2.5 mmol/L,尿常规示尿蛋白(-)、隐血(-)、酮体(-)、pH 7.5,给予补钾、补液、鲑降钙素注射剂及鼻喷剂等降钙治疗。7月3日由急诊以“高钙血症、急性肾损伤”收住我科。病程中,患者精神、食欲、睡眠差,近1周便秘,小便如上所述,体重、体力均明显下降。
既往史10多岁时曾患“肾炎”,具体不详。2005年被自行车撞伤致右侧髌骨骨折,行手术治疗(具体不详),术后恢复良好。2015-05-23摔倒后出现右侧桡骨远端骨折,在我院骨科门诊行石膏外固定术,当时未行血液及尿液检查。
个人史、月经及婚育史、家族史无特殊。
体格检查体温37.3℃,脉搏85次/min,呼吸20次/min,血压111/61 mmHg。急性面容,神志清楚,精神差。皮肤干燥、弹性差。右侧甲状腺区可触及包块,大小约4 cm×3 cm,包块表面光滑,可随吞咽上下移动,左侧甲状腺未触及明显包块,双侧颈部及双侧锁骨上淋巴结未及肿大。心肺腹部查体无特殊。右前臂石膏固定,右侧膝关节可见陈旧性手术疤痕。双下肢无浮肿,关节活动正常。
实验室检查
尿液 蛋白质-,隐血±,葡萄糖-。尿蛋白定量1.36 g/24h,尿量2 600 ml。尿沉渣红细胞1万/ml,白细胞0~1/HP。C3 32 mg/L,α2巨球蛋白 20 mg/L,N-乙酰-β-葡萄糖苷酶(NAG) 185.8 U/(g·Cr)(参考值≤16.5),视黄醇结合蛋白(RBP)36.3 mg/L(参考值<0.5),溶菌酶(Lyso)1.3 mg/L(参考值<0.5),NGAL 29.57 μg/L,KIM-l 0.00 μg/L,白细胞介素18(IL-18)8.83 ng/L。24h尿钙526 mg,尿钙排泄分数13.8%,24h尿磷246.6 mg。
血液 血红蛋白97g/L,红细胞计数3.05×1012/L,网织红细胞计数33.9×109/L,白细胞计数14.7×109/L,中性粒细胞比84.8%,淋巴细胞比例6.3%,血小板计数283×109/L,C反应蛋白107.5 mg/L。血清白蛋白36.6 g/L,球蛋白22.9 g/L,尿素氮53.9 mg/dl,SCr 215.70 μmol/L,尿酸407 μmol/L,碱性磷酸酶169 U/L,乳酸脱氢酶424 U/L,总胆固醇4.13 mmol/L,三酰甘油1.09 mmol/L,钾2.78 mmol/L,钠135.6 mmol/L,氯95.8 mmol/L,总二氧化碳26.2 mmol/L,钙4.40 mmol/L,磷1.55 mmol/L,降钙素原0.440 μg/L,IL-6 184.90 ng/L。D-二聚体1.78 mg/L。空腹血糖5.61 mmol/L。骨代谢指标:全段甲状旁腺激素(iPTH) 374.9 pmol/L(参考值1.3~9.3),总25(OH)D37.82 ng/ml(参考值>30)。静脉血气分析:离子钙 2.45 mmol/L。
免疫学 ANA 1∶ 128,A-dsDNA阴性。抗核抗体谱阴性。补体C3 0.91 g/L,C4 0.104 g/L。外周血淋巴细胞亚群:CD3+633个/μl,CD4+385个/μl,CD8+207个/μl。血游离轻链κ 68.8 mg/L,λ 33.1 mg/L,κ/λ 2.1。免疫固定电泳图谱未见明显异常。
甲状腺功能 FT3 4.09 pmol/L,FT4 13.8 pmol/L,T3 1.0 nmol/L,T4 143.5 nmol/L,TSH 0.02 mIU/L。降钙素7.19 ng/L。甲状腺相关抗体均阴性。
贫血相关检查 血清叶酸10.8 nmol/L,维生素B12>1 107 pmol/L。直接抗人球蛋白试验、间接抗人球蛋白试验、血清酸化溶血试验阴性,结合珠蛋白、游离血红蛋白正常。
肿瘤标志物 血β2微球蛋白 5.98 mg/L,鳞状细胞癌相关抗原1.7 ng/ml,AFP、CEA、CA19-9、CA125、CA15-3、CA72-4、CA50、CA24-2正常。
骨髓 细胞学:浆细胞占1.5%。骨髓活检病理:骨髓轻度增生低下。
辅助检查
头颈部CT 甲状腺多发病变,结节性甲状腺肿并右叶腺瘤可能(图1A)。
甲状腺及甲状旁腺彩超 (1)甲状腺内低回声团块,TI-RADS超声分级3级,考虑结节性甲状腺肿(图1B);(2)甲状腺右叶下方囊实性肿块,考虑来源于甲状旁腺,甲状旁腺瘤囊性变?(3)双侧甲状旁腺区声像图未见占位。
胸部CT (1)两肺散在炎症;(2)主动脉粥样硬化;(3)纵隔及双侧腋窝多发小淋巴结;双侧胸膜增厚;(4)甲状腺多发低密度灶;(5)肝内多发囊肿。
四肢脊柱平片 右侧尺、桡骨远端骨折外固定术后。
骨密度检查(正位脊柱、双股骨) L1-L4 T值:-3.6,左股骨T值:-4.0。结论:严重骨质疏松症。
ECT全身骨显像 全身骨骼弥漫性摄取亚甲基二膦酸盐(99Tcm-MDP)增加,尤以双下肢骨皮质明显,双肺、胃弥漫性示踪剂异常浓聚(图1C)。
心脏彩超 左室舒张功能减低。
心电图 窦性心律;T波改变,心率84次/min。
肾脏超声 左肾124 mm×45 mm×62 mm,右肾122 mm×41 mm×61 mm,皮质厚度不清,皮质回声增强,皮髓界限欠清楚,集合系统正常。左肾见数个强回声光团,较大的约3mm,未见后声影。双肾轮廓规则,包膜连续完整,结构欠清楚。双肾内未见肾盂肾盏扩张(图1D)。

图1 影像学检查A:甲状腺CT示甲状腺多发病变,结节性甲状腺肿并右叶腺瘤可能(→);B:甲状腺超声示甲状腺内低回声团块(→);C:ECT全身骨显像示全身骨骼弥漫性摄取99Tcm-MDP增加,尤以双下肢骨皮质明显,双肺、胃弥漫性示踪剂异常浓聚;D:肾脏超声示左肾见数个强回声光团,较大的约3 mm,未见后声影()
诊疗分析患者系老年女性,病程短,起病急,临床表现为多系统损害,包括胃肠道症状(干呕、纳差、便秘)、骨关节疼痛(桡骨骨折、骨质疏松、双下肢多关节疼痛)、泌尿系统(少量蛋白尿伴非少尿型急性肾损伤,无镜下血尿,双肾体积增大,高尿钙,左肾钙质沉着)、水电解质紊乱(脱水貌、高钙血症、低钾血症、低钠血症)。
明确病因该患者以干呕、口干、多饮、多尿等胃肠道症状起病,首先考虑2型糖尿病,但急诊及住院期间查血糖正常,且尿常规示尿糖、酮体均阴性,可排除糖尿病。无酸中毒,无严重氮质血症,不能用肾功能衰竭解释胃肠道症状。急诊科查血清总钙5.20 mmol/L,离子钙2.39 mmol/L,符合高钙危象诊断标准血清总钙>3.75 mmol/L。高钙危象可解释该患者的多系统受累表现:(1)胃肠道:高血钙可引起厌食、胃肠道蠕动减慢,出现恶心、呕吐、便秘。(2)泌尿系统:高血钙可导致肾小管损害,肾小管浓缩功能受损,引起多尿、烦渴、多饮,同时该患者反复干呕、食欲下降,导致低钾血症和低钠血症。全身皮肤干燥,血乳酸升高,提示严重脱水,存在循环衰竭风险。尿钙排泄增多导致肾钙质沉着。(3)神经肌肉系统:高钙血症可导致乏力、倦怠、四肢近端为主的肌力下降。(4)软组织异位钙化:钙可沉积于关节周围和软骨,导致关节疼痛、关节功能障碍。
高钙血症病因分析:
(1)恶性肿瘤:肿瘤是高钙血症的常见原因,在住院患者中占首位,约20%~30%的晚期肿瘤患者出现高钙血症。最常见的肿瘤是乳腺癌、肺癌和肾癌,其次是血液系统肿瘤,尤其是多发性骨髓瘤。肿瘤导致高钙血症的机制包括体液性(80%)、局部骨质破坏(20%)、1,25(OH)2D3分泌增多(0.1%)和异位性甲状旁腺功能亢进(<0.1%)。体液性高钙血症(HHM)多发生在鳞癌(头颈部、食道、肺、宫颈)、肾癌、膀胱癌、乳腺癌、非霍奇金淋巴瘤和卵巢癌。甲状旁腺激素相关蛋白(PTHrp)是HHM的主要机制,其N端氨基端序列与PTH相似,可作用于靶器官上的PTH-1受体,促进骨质吸收和尿钙吸收,但PTHrp不能刺激1,25(OH)2D3合成增多。如肿瘤患者发现高钙血症,但是PTH、1,25(OH)2D3是低的,此时需检测PTHrp。本例患者入院后完善肿瘤指标及胸部CT、ECT全身骨显像等检查,可排除乳腺癌、肺癌等实体肿瘤,同时骨穿结果可排除多发性骨髓瘤。
(2)结节病:结节病患者(尤其是暴露于阳光下)可出现高钙血症,与肉芽肿内巨噬细胞含1α羟化酶、不断产生活性维生素D有关。本例患者肺部CT示纵隔及双侧腋窝多发小淋巴结,但查体未触及浅表淋巴结肿大,临床无发热、厌食等一般表现,无结节性红斑、虹膜睫状体炎、肝脾肿大、关节炎、肌肉肿痛、心律失常等多系统受累表现,因此考虑结节病可能性不大。
(3)药物:大量补钙、维生素D或其衍生物、维生素A、雌激素、噻嗪类利尿剂、阿米洛利、锂剂等均可导致医源性高钙血症。该患者未服用相关药物,故不考虑药物因素。
(4)继发性/三发性甲状旁腺功能亢进(简称甲旁亢):慢性肾功能不全患者肾脏合成活性维生素D减少和尿磷排泄减少,导致低钙血症、高磷血症,刺激甲状旁腺过量分泌PTH,称为继发性甲旁亢。如甲状旁腺受到持久刺激,部分增生组织转变为腺瘤,自主性分泌过多PTH,此时可出现高钙血症,称为三发性甲旁亢。该患者既往无慢性肾脏病史,肾脏超声示双肾体积增大,不符合慢性肾功能不全,故可排除三发性甲旁亢导致的高钙血症。
(5)原发性甲旁亢(pHPT):门诊患者中90%的高钙血症是由pHPT引起的。PTH的分泌主要受血浆离子钙浓度影响,低血钙常伴PTH升高,而高血钙常伴PTH降低。pHPT时这一平衡被打破,甲状旁腺腺瘤、增生或罕见的甲状旁腺癌引起PTH分泌过多,临床出现高钙血症、高钙尿症、低磷血症和高磷尿症。由于尿钙和尿磷排出增加,磷酸钙、草酸钙等钙盐沉积而形成肾结石、肾钙化。本例患者查iPTH明显升高,甲状旁腺超声提示甲状腺右叶下方囊实性肿块,结合高钙血症、高钙尿症、高磷尿症,左肾钙质沉着,符合pHPT临床特点。
治疗及随访经补液扩容、促进尿钙排泄(呋塞米)、抑制骨破坏(降钙素鼻喷剂及注射剂、唑来膦酸注射剂4 mg×1次)等治疗,患者尿量3 500~4 000 ml/d,血钙逐渐下降,肾功能好转,7月13日复查血钙2.25 mmol/L,SCr 88 μmo/L。7月16日转至外科行“部分甲状旁腺切除术备癌根治术”,术中右侧甲状腺可触及一实性包块,大小约8 cm×8 cm,质地硬,边界不清楚,与周围组织无黏连,快速病理结果显示甲状腺癌,遂行双侧甲状腺全切除术。右侧甲状旁腺可触及一囊实性包块,大小约4 cm×4 cm,质地柔软,边界清楚,与周围组织无黏连。术后病理示:(1)右侧甲状腺:乳头状癌(肿物2个,直径为0.9和0.3 cm);(2)右侧甲状旁腺:甲状旁腺腺瘤;(3)左侧甲状腺:结节性甲状腺肿(图2)。术后第1天查PTH降至正常(1.7 pmol/L)。定期门诊随访(末次随访时间2019年3月),血iPTH波动在0.1~0.5 pmol/L,长期服用碳酸钙维生素D3片,血钙维持在正常范围,SCr波动于100 μmol/L左右。
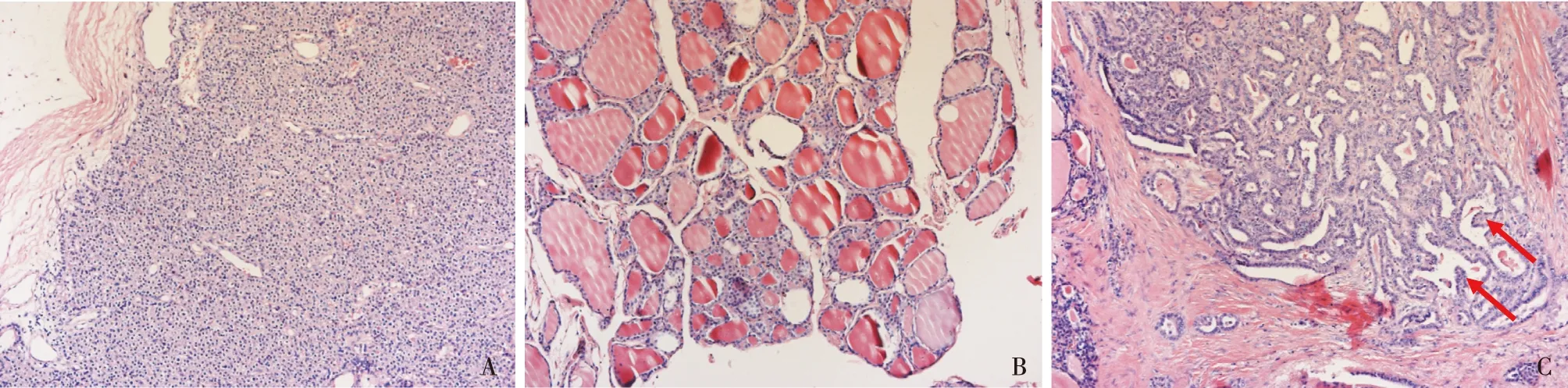
图2 甲状腺及甲状旁腺组织病理A:右侧甲状旁腺:甲状旁腺腺瘤,可见肿瘤细胞呈巢状分布,以主细胞为主,包膜完整,细胞核呈圆形,染色质浓密;B:左侧甲状腺:结节性甲状腺肿,甲状腺滤泡大小不等;C:右侧甲状腺:乳头状癌,肿瘤呈乳头状浸润性生长(→),周围纤维结缔组织环绕,细胞核呈毛玻璃状,核大,核浆比例增加,核排列紊乱、拥挤、重叠
最后诊断(1)右侧甲状旁腺腺瘤,原发性甲状旁腺功能亢进症;(2)高钙危象,急性肾损伤2期;(3)右侧甲状腺乳头状癌(PTC,Ⅰ期 T1N0M0);(4)骨质疏松症;(5)右侧桡骨远端骨折外固定术后;(6)右侧髌骨骨折术后。
讨 论
pHPT与急性肾损伤研究显示,13%~19%pHPT患者存在基础慢性肾脏病[1-3],同时17.3%~18.1%患者出现急性肾损伤[4-5]。峰值血钙水平是发生急性肾损伤的独立预测因素[5]。对比健康人群,无症状pHPT患者观察3年后出现肾衰竭和肾结石的概率分别增加13.83倍和5.15倍[6]。pHPT患者出现肾功能损伤的机制包括:(1)高血钙抑制肾小管细胞膜上的ATP酶,干扰抗利尿激素作用,同时患者常有食欲不振、呕吐,导致血容量下降,如未及时补液可出现肾前性急性肾损伤;(2)高钙血症导致肾血管收缩、肾小球滤过率下降;(3)长期高钙尿症导致的微结晶可引起肾小管阻塞;(4)输尿管结石导致尿路梗阻,而反复肾盂肾炎又可导致慢性间质性肾炎。早期及时治疗,肾功能可恢复正常,如病情迁延,肾功能将逐渐恶化。一项回顾性研究显示,高钙危象组患者的术前SCr明显高于无高钙危象组,但两组患者在甲状旁腺切除术(PTX)后肾功能均恢复正常[7]。国内曾报道1例pHPT患者,PTX术前查SCr 389 μmol/L,肾穿刺病理示急性肾小管坏死,肾小管上皮细胞及管腔内钙质沉着,术后4个月复查SCr 125 μmol/L,重复肾穿刺示慢性肾小管损伤[8]。本例患者表现为非少尿型急性肾损伤,入院时有明显容量不足表现;尿蛋白定量为1.36 g/24h,但尿常规示蛋白质阴性,提示非白蛋白尿,可能是肾小管性蛋白尿或溢出性蛋白尿,骨髓穿刺及活检排除多发性骨髓瘤及B细胞肿瘤;尿NAG、RBP明显升高,提示肾小管损伤较重。综上,考虑急性肾小管坏死。经补液扩容、降钙、虫草制剂、EPO等处理,肾功能恢复正常。
pHPT的诊断与治疗高钙血症伴iPTH升高,同时排除三发性甲旁亢、异位性甲旁亢,可基本确诊pHPT,如血磷正常低值或轻度下降、血碱性磷酸酶升高、高氯性代谢性酸中毒,则进一步支持诊断。如有高钙血症家族史,需完善遗传学基因检测。定性诊断明确后,可通过超声、99mTc-甲氧基异丁基异睛(MIBI)双时相显像等定位检查明确甲状旁腺病变部位。临床疑诊pHPT可参考《原发性甲状旁腺功能亢进症诊疗指南》进行鉴别诊断[9]。pHPT 的治疗包括手术治疗和药物治疗。pHPT首选手术治疗,如出现严重高钙血症甚至高钙危象时需及时处理。治疗原则包括扩容、促进尿钙排泄、抑制骨吸收等。低钙血症是PTX术后常见的并发症之一。术后低钙血症的原因主要是相对的、暂时性甲状旁腺功能不足,待术前功能受抑制的正常甲状旁腺逐渐恢复功能,血钙可恢复正常。本例患者术后半个月出现肌肉抽搐,检查示严重低钙血症(1.42 mmol/L),经静脉及口服补钙后血钙升至正常,但在术后长期随访中血iPTH水平持续低下,提示左侧甲状旁腺功能未能恢复,故该患者需长期服用活性维生素及钙剂来维持血钙稳定。
pHPT与甲状腺癌首诊为pHPT的患者最常见并发甲状腺癌[10]。甲状旁腺腺瘤常与甲状腺髓样癌并存(多见于多发性内分泌瘤2A型),因其都源自滤泡旁细胞,而PTC来源于滤泡细胞,因此甲状旁腺腺瘤与PTC很少合并存在,其发生率在1.3%~17.6%[11]。在一项纳入228例pHPT手术患者的回顾性研究中,86例(37.7%)合并甲状腺疾病,其中6例(2.6%)为PTC[12]。pHPT合并甲状腺疾病的危险因素包括:颈部射线暴露、高钙血症导致甲状腺肿及有丝分裂活性增加[13]。研究发现,PTH具有肿瘤促进效应,可引起新发肿瘤的遗传倾向[14]。Nilsson等[13]对1958~1997年在pHPT确诊前、确诊时或PTX术后1年内罹患其他肿瘤的患者进行分析,发现PTX术后肿瘤风险持续存在,手术只能延缓肿瘤的发生,作者认为PTH影响了遗传基因易感性或者降低了人体对外界刺激的耐受性。
甲状腺癌与高钙血症少量文献报道甲状腺癌通过分泌PTHrp引起高钙血症。Ito等[15]于1993年首先报道2例PTC患者血液中PTHrp水平升高。Nakashima等[16]利用原位杂交及逆转录聚合酶链反应技术检测82例原发性甲状腺癌、9例甲状腺腺瘤和16例腺瘤性甲状腺肿的组织标本,以甲状腺癌周围正常组织为对照,结果显示97.6%的甲状腺癌组织表达PTHrp,1例甲状腺腺瘤组织表达PTHrp,而甲状腺肿及对照组不表达。需注意的是,该研究所有患者均无高钙血症,提示肿瘤细胞表达PTHrp并不一定引起血液中PTHrp升高。Hiroshi等[17]在2004年报道一例有多部位转移的老年女性患者,甲状腺细针穿刺示乳头状癌,同时血液PTHrp升高,死后尸检报告显示甲状腺肿块为未分化癌,气管部位肿瘤为乳头状癌,其周围为鳞状细胞癌,而原发灶和转移瘤细胞抗PTHrp染色均阳性。肿瘤病人出现高钙血症还需排除是否合并pHPT。Lee等[18]检测178例高钙血症住院患者的血液PTH和PTHrp,93例(52.24%)为肿瘤相关(71例PTHrp升高),28例(15.7%)由pHPT引起,7例(3.9%)同时存在肿瘤(3例PTHrp升高)和pHPT,其中1例为PTC合并pHPT,PTX术后血钙降至正常,提示高钙血症是由pPHT引起的。本例患者未检测血液中PTHrp,甲状腺癌组织未做抗PTHrp染色,不能排除是否合并甲状腺癌相关高钙血症。
小结:临床医师应熟知高钙血症的临床表现,遇到烦渴多尿、骨关节疼痛、反复泌尿系结石、肾功能受损等多系统受累时需检测血钙水平。pHPT和肿瘤是高钙血症的最常见病因,iPTH是鉴别的关键,有条件应完善PTHrp。pHPT首选手术治疗,如有严重高钙血症应首先内科处理。PTX术后应密切监测iPTH和血钙水平。如能早期发现并积极治疗,pHPT导致的急性肾损伤可完全恢复。
