阿帕替尼用于铂类耐药复发性卵巢癌的疗效与安全性
2019-12-30陈蜜王锡恩张静
陈蜜 王锡恩 张静
[摘要] 目的 探讨阿帕替尼用于铂类耐药复发性卵巢癌的疗效与安全性。 方法 选取宁波大学附属鄞州医院2017年1月~2018年1月间诊断及治疗的铂类耐药复发性卵巢癌患者72例,采用随机数表法分为阿帕替尼组(36例)及吉西他滨组(36例),阿帕替尼组采用口服阿帕替尼方案,0.25 g,bid;吉西他濱组采用静滴吉西他滨方案,每日剂量1000 mg/m2,比较两组患者的疗效、总生存、无进展生存以及不良反应。 结果 阿帕替尼组ORR显著高于吉西他滨组(47.22% vs 22.22%;χ2=4.963,P=0.025);阿帕替尼组中位无进展生存时间为8.0(5.0~10.5)个月,吉西他滨组中位PFS为5.0(3.0~8.8)个月,阿帕替尼组疾病进展风险显著低于吉西他滨组[HR=0.631,95%CI(0.382,1.043),P=0.046];阿帕替尼组未达到中位生存时间,吉西他滨组中位生存时间为6.0(3.8~12.0)个月,阿帕替尼组死亡风险显著低于吉西他滨组[HR=0.556,95%CI(0.300,1.030),P=0.049];阿帕替尼组3级及以上不良反应发生率显著低于吉西他滨组(30.56% vs 47.22%;χ2=6.769,P=0.009)。 结论 阿帕替尼具有较好的治疗铂类耐药复发性卵巢癌的疗效与安全性。
[关键词] 阿帕替尼;铂类耐药复发性卵巢癌;吉西他滨;生存时间
[中图分类号] R737.31 [文献标识码] B [文章编号] 1673-9701(2019)31-0074-04
Efficacy and safety of apatinib in platinum-resistant recurrent ovarian cancer
CHEN Mi WANG Xien ZHANG Jing
Department of Integrated Chinese and and Western Medicine Oncology, Affiliated Yinzhou Hospital of Ningbo University, Ningbo 315000, China
[Abstract] Objective To investigate the efficacy and safety of apatinib in platinum-resistant recurrent ovarian cancer. Methods 72 patients with platinum-resistant recurrent ovarian cancer who were diagnosed and treated from January 2017 to January 2018 in Affiliated Yinzhou Hospital of Ningbo University were selected. The random number table method was used to divide the patients into apatinib group(36 cases) and gemcitabine group(36 cases). The apatinib group was orally given apatinib, 0.25 g, bid; the gemcitabine group was given intravenous infusion of gemcitabine at a daily dose of 1000 mg/m2. The efficacy, overall survival, progression-free survival, and adverse reactions were compared between the two groups. Results The ORR in the apatinib group was significantly higher than that in the gemcitabine group(47.22% vs 22.22%; χ2=4.963, P=0.025); the median progression-free survival time in the apatinib group was 8.0(5.0-10.5) months. The median PFS in the gemcitabine group was 5.0(3.0-8.8) months. The risk of disease progression was significantly lower in the apatinib group than in the gemcitabine group[HR=0.631, 95%CI(0.382, 1.043), P=0.046); the apatinib group did not reach the median survival time. The median survival time in the gemcitabine group was 6.0(3.8-12.0) months. The risk of death was significantly lower in the apatinib group than in the gemcitabine group[HR=0.556, 95%CI(0.300, 1.030), P=0.049]; the incidence rate of adverse reactions of grade 3 and above in the apatinib group was significantly lower than that in the gemcitabine group(30.56% vs 47.22%; χ2=6.769, P=0.009). Conclusion Apatinib has a good efficacy and safety in the treatment of platinum-resistant recurrent ovarian cancer.
[Key words] Apatinib; Platinum-resistant recurrent ovarian cancer; Gemcitabine; Survival time
卵巢癌是女性死亡率最高的肿瘤[1],使用肿瘤细胞减灭术后辅助以铂类为基础的化疗是当前标准的治疗方案[2]。虽然大多数卵巢癌对化疗敏感,但仍具有较高的复发及铂类耐药率,据统计约75%的晚期卵巢癌患者会复发,这其中约30%对铂类敏感[3],此类铂类耐药性复发性卵巢癌多数预后不良,治疗目的为改善患者症状及提高生活质量,因此治疗首选非铂类药物,包括吉西他滨、多西他赛、依托泊苷、紫杉醇等。阿帕替尼作为血管生成抑制的靶向药物,可有效抑制血管内皮生长因子受体,进而发挥抑制癌细胞生长的作用,研究[4]显示其可有效且安全的提高晚期难治性胃癌患者的总生存期(overall survival,OS)及无进展生存期(Progression-free survival,PFS),但其对于铂类耐药复发性卵巢癌患者的疗效及安全性与其他化疗药物的对比报道较少,为此本研究对我院72例铂类耐药复发性患者进行一项前瞻性研究,现报道如下。
1 资料与方法
1.1 一般资料
选取宁波大学附属鄞州医院2017年1月~2018年1月间诊断及治疗的铂类耐药复发性卵巢癌患者,纳入标准:(1)卵巢癌诊断均经病理明确且符合《卵巢恶性肿瘤诊断与治疗指南(第四版)》[5],经一线含铂类化疗方案治疗且缓解期<6个月;(2)复发定义为影像学可测量的肿瘤病灶;(3)患者必须至少2种标准化疗方案失败;(4)体力情况符合ECOG评分≤2;(5)预计生存期>15周;(6)心、肺、肝等重要脏器及骨髓造血功能基本正常。排除标准:(1)合并其他原发肿瘤;(2)已出现中枢神经系统转移;(3)存在胃肠疾病异常可能影响到药物的服用者;(4)6个月内存在如心脏血管成形术或支架植入术、心肌梗死、不稳定心绞痛、心力衰竭等心血管疾病;(5)伴有血尿、出血性疾病或原因不明的血压异常。共纳入72例患者,采用随机数字表法分为阿帕替尼组及吉西他滨组,每组36例,两组一般资料无明显差异(P>0.05),具有可比性,见表1。本研究所有患者均签署知情同意书及化疗同意书,并已通过我院伦理委员会审批。
1.2 治疗方案
1.2.1 阿帕替尼组 使用阿帕替尼(商品名:艾坦,江苏恒瑞医药股份有限公司,国药准字H20140105,0.25 g/片),起始剂量0.25 g,po,bid,治疗中发生手足症候群使用局部干预,如皮质类固醇、角化剂、保湿剂或光疗,发生白细胞减少使用集落刺激因子,发生高血压使用血管紧张素受体阻滞剂或钙拮抗剂治疗。若发生3级及以上血液不良事件、高血压、手足症候群或其他有必要减量的副作用时减量至0.25 g,qd,若发生疾病进展、减量后仍有不可接受的毒性作用、开始治疗周期后因毒性累积需单次停药>14 d或停药>2次则终止使用阿帕替尼并改用其他化疗方案。
1.2.2吉西他滨组 使用吉西他滨(商品名:健择,Eli Lilly and Company,国药准字H20110535,200 mg/支),起始剂量1000 mg/m2,单次静滴时间>30 min,每周1次,连续3周,休息1周,每4周为1个周期,若发生3级及以上血小板或红细胞减少进行相应的成分输血。
1.3 评价指标
阿帕替尼组在用药2个月吉西他滨组在用药2个周期后评价疗效,疗效评价依据实体瘤疗效评价标准[6],分为:完全缓解(complete remission,CR):瘤体完全消失;部分缓解(partial remission,PR):瘤体长径总和缩小≥30%;疾病稳定(stable disease,SD):瘤体长径总和有缩小,但未达PR标准;疾病进展(progressive disease,PD):瘤体长径总和增加或出现新发病灶;总缓解率(overall response rate,ORR)=(CR+PR)。無进展生存是指从入组开始到发生任何事件的时间,包括死亡、疾病进展、改换化疗方案、改为化疗、加用其他治疗、发生致死性或不能耐受的副作用等事件,总生存时间是指患者从开始治疗至死亡或随访截止的时间。不良反应根据常见不良反应术语评定标准[7](Common Terminology Criteria for Adverse Events,CTCAE)4.0版进行评估和统计,分为:1级(轻度),无症状或轻微;2级(中度),需要小、局部、非侵入性治疗;3级(重度),严重或医学上有重要意义但不会立即危及生命;4级,危及生命需紧急治疗;5级,不良反应相关的死亡。主要比较3级及以上不良反应发生情况。
1.4 随访
于门诊每个月进行随访,检查患者生命体征、血常规、肝肾功能、血清肿瘤标记物水平,必要时使用增强CT评估进展情况,同时统计不良反应发生情况,随访截止日期2019年1月31日。
1.5统计学处理
采用SPSS18.0和GraphPad Prism 7.0进行数据处理,计数资料用[n(%)]表示,使用χ2检验进行比较,等级变量采用秩和检验;不服从正态分布的计量资料采用中位数(四分位间距)的形式表示,Kruskal-Wallis秩和检验比较组间差异,服从正态分布计量资料用均数±标准差(x±s)表示,使用t检验进行比较,使用Kaplan-Meier法绘制生存曲线,应用Log rank检验计算风险比(Hazard ratio, HR)及其95%置信区间。P<0.05为差异有统计学意义。
2 结果
2.1 随访结果
本研究中阿帕替尼组未出现停药患者,阿帕替尼组中位随访时间为9个月,吉西他滨组中位随访时间为7个月。
2.2 兩组近期疗效对比
阿帕替尼组ORR显著高于吉西他滨组(47.22% vs 22.22%;χ2=4.963,P=0.025),见表2。
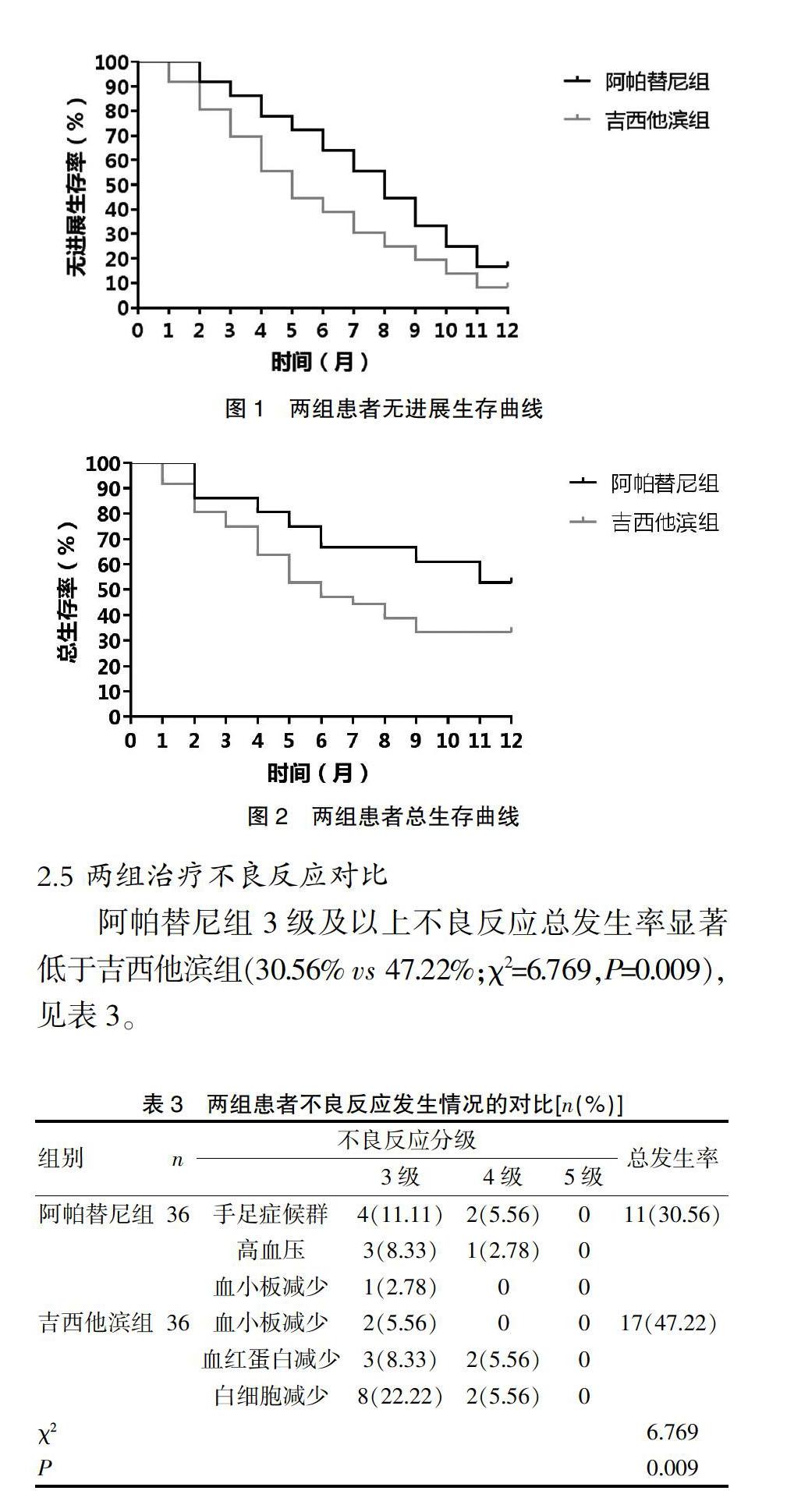
2.3 两组无进展生存对比
阿帕替尼组中位PFS为8.0(5.0~10.5)个月,吉西他滨组中位PFS为5.0(3.0~8.8)个月,阿帕替尼组疾病进展风险显著低于吉西他滨组[HR=0.631,95%CI(0.382,1.043),P=0.046],见图1。
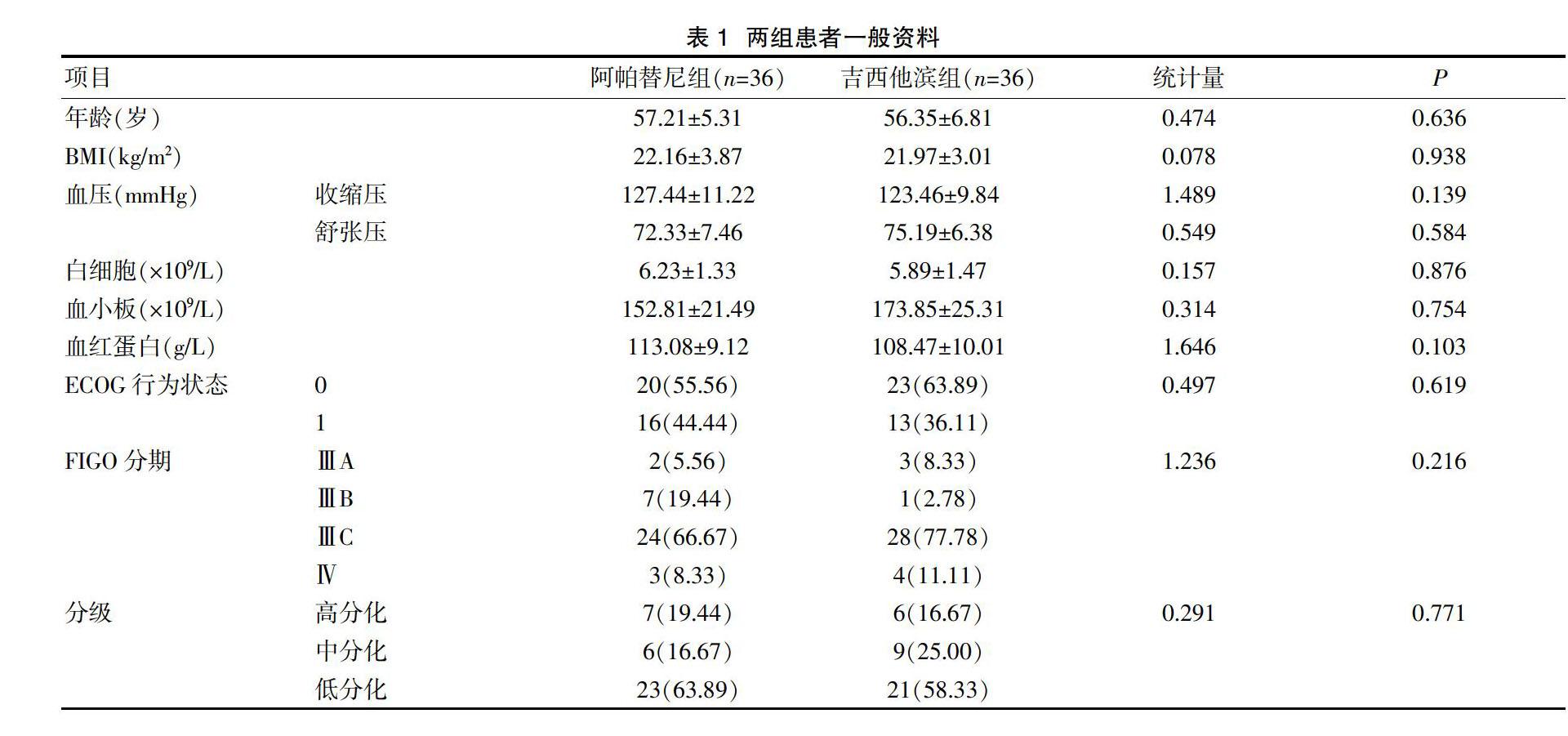
2.4 两组患者总生存对比
阿帕替尼组未达到中位OS,吉西他滨组中位OS为6.0(3.8~12.0)个月,阿帕替尼组死亡风险显著低于吉西他滨组[HR=0.556,95%CI(0.300,1.030),P=0.049],见图2。
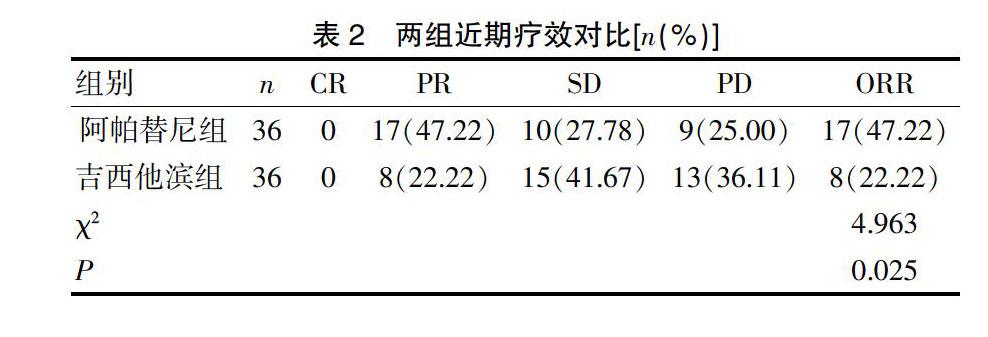
2.5 两组治疗不良反应对比
阿帕替尼组3级及以上不良反应总发生率显著低于吉西他滨组(30.56% vs 47.22%;χ2=6.769,P=0.009),见表3。
3 讨论
在铂类耐药复发性卵巢癌的发生和进展中,新生血管的生成在其中具有重要作用,其中血管内皮生长因子受体[8](vascular endothelial growth factor receptor,VEGFR)是当前研究热点,同时针对VEGFR信号通路的靶向治疗也被证实是卵巢癌有前景的治疗策略之一,也因此开发了多种VEGFR抑制剂,包括索拉非尼[9]、凡德他尼[10]、西地尼布[11]等,均具有较好的抗癌效果。吉西他滨是NCCN推荐的用于铂类耐药复发性卵巢癌治疗的化疗药物,同时阿帕替尼作为新型抗血管生成的VEGFR抑制剂,两者在铂类耐药复发性卵巢癌间的治疗疗效及安全性的对比相关报道较少,为此,本研究进行一项前瞻性对照研究。
本研究显示,阿帕替尼组总缓解率显著高于吉西他滨组,当前研究[12]表明吉西他滨的抗癌机制主要为:其在体内经核苷激酶作用下生成具有活性的二磷酸及三磷酸核苷,二磷酸核苷可抑制核苷酸还原酶活性,减少DNA合成所必须的三磷酸脱氧核苷的生成;三磷酸核苷可与DNA或RNA合成中所必须的三磷酸脱氧核苷竞争掺入至DNA及RNA链,起到阻止DNA及RNA合成作用,表现为DNA合成期的细胞中G1期/S期交接点细胞进展受到抑制。因此普遍认为吉西他滨是治疗铂类耐药复发性卵巢癌的有效药物[13]。本研究中吉西他滨组的ORR为22.22%,与之前报道[14]相近,也证实了吉西他滨对于铂类耐药复发性卵巢癌的治疗效果,而本研究中阿帕替尼的ORR为47.22%,显著高于吉西他滨,显示出阿帕替尼在铂类耐药复发性卵巢癌的短期治疗优势。
此外,本研究结果还显示阿帕替尼组疾病进展风险及死亡风险均显著低于吉西他滨组,表明阿帕替尼对铂类耐药复发性卵巢癌的预后也优于吉西他滨。提高患者的无进展生存期和总生存时间以改善患者的预后是铂类耐药复发性卵巢癌治疗最终目的,VEGFR根据酪氨酸激酶活性的不同分为VEGFR-1、VEGFR-2及VEGFR-3[15],其中VEGFR-2是最重要的通过VEGF途径介导新生血管生成的信号分子[16],阿帕替尼能够特异性结合并抑制细胞内VEGFR-2,其活性是同类药物瓦他拉尼和索菲拉尼的10倍,有效防止磷酸化并阻断随后的下游信号,进而发挥降低卵巢癌新生微血管密度,达到减缓或停止瘤体生长的作用[17],赖章超等[18]研究也证实阿帕替尼对于铂类耐药复发的卵巢癌具有较好的缓解临床症状及增加生存时间的作用。
在治疗安全性方面,阿帕替尼的主要不良反应为手足症候群、高血压及血小板减少,其发生机制尚不明确[19],但经对症处理后均能有所缓解,未出现不能耐受进而停药的患者,其3级以上不良反应的总发生率也显著低于吉西他滨组,证实了其治疗耐受性及安全性。阿帕替尼Ⅱ期及Ⅲ期临床试验也显示,不良事件的发生情况与已上市同类药物相似[20],同时李琪等[21]研究指出阿帕替尼还能有效减轻卵巢癌患者恶性腹腔积液,有效解除因腹腔积液造成的腹部症状及呼吸困难。
综上所述,阿帕替尼具有较好的治疗铂类耐药复发性卵巢癌的疗效与安全性,值得进一步深入研究。
[参考文献]
[1] Dvm AJ,Bray F,Center MM,et al. Global cancer statistics[J]. Ca A Cancer Journal for Clinicians,2013,65(2):87-108.
[2] Banerjee S,Kaye SB. New strategies in the treatment of ovarian cancer:current clinical perspectives and future potential[J]. Clinical Cancer Research An Official Journal of the American Association for Cancer Research,2013, 19(5):961-968.
[3] Galanis E,Atherton PJ,Maurer MJ,et al. Oncolytic Measles Virus Expressing the Sodium Iodide Symporter to Treat Drug-Resistant Ovarian Cancer[J]. Cancer Res,2015,75(1):22.
[4] Li J,Qin S,Xu J,et al. Randomized,Double-Blind,Placebo-Controlled Phase III Trial of Apatinib in Patients With Chemotherapy-Refractory Advanced or Metastatic Adenocarcinoma of the Stomach or Gastroesophageal Junction[J]. J Clin Oncol,2016,34(13):1448-1454.
[5] 周琦,吴小华,刘继红,等. 卵巢恶性肿瘤诊断与治疗指南(第四版)[J]. 中国实用妇科与产科杂志,2018,34(7):739-749.
[6] Ronot M,Bouattour M,Wassermann J,et al. Alternative Response Criteria(Choi,European association for the study of the liver,and modified Response Evaluation Criteria in Solid Tumors[RECIST])Versus RECIST 1.1 in patients with advanced hepatocellular carcinoma treated with sorafenib[J]. Oncologist,2014,19(4):394-402.
[7] Smith TL,Sarto G,Helow K,et al. Impact of Change From CTCAE Version 3 to CTCAE Version 4 on Urologic Toxicity Scores in Prostate Cancer-International Journal of Radiation Oncology·Biology·Physics[J]. Int J Radiat Oncol Biol Phys,2014,90(1):S419.
[8] Mi SP,Dong SM,Kim BR,et al. Thioridazine inhibits angiogenesis and tumor growth by targeting the VEGFR-2/PI3K/mTOR pathway in ovarian cancer xenografts[J]. Oncotarget,2014,5(13):4929-4934.
[9] Maggiore ULR,Menada MV,Venturini PL,et al. Sorafenib for ovarian cancer[J]. Expert Opin Investig Drugs,2013, 22(8):1049-1062.
[10] Song WS,Yuan YE. Inhibitory effect of Vandetanib on human ovarian cancer cells and its mechanism[J]. Chinese Journal of Cancer Prevention & Treatment,2014,21(20):1589-1593.
[11] Ledermann JA,Embleton AC,Raja F,et al. Cediranib in patients with relapsed platinum-sensitive ovarian cancer(ICON6):a randomised,double-blind,placebo-controlled phase 3 trial[J]. Lancet,2016,387(10023):1066-1074.
[12] Toyota Y,Iwama H,Kato K,et al. Mechanism of gemcitabine-induced suppression of human cholangioc-ellular carcinoma cell growth[J]. Int J Oncol,2015,47(4):1237-1241.
[13] Chanpanitkitchot S,Tangjitgamol S,Khunnarong J,et al. Treatment outcomes of gemcitabine in refractory or recurrent epithelial ovarian cancer patients[J]. Asian Pacific Journal of Cancer Prevention Apjcp,2014,15(13):5215-5221.
[14] 袁瓊,何跃东. 吉西他滨联合铂类治疗铂类耐药复发性卵巢癌的疗效和安全性[J]. 中华妇幼临床医学杂志(电子版),2018,14(5):542.
[15] Sun Q,Zhou J,Zhang Z,et al. Discovery of fruquintinib,a potent and highly selective small molecule inhibitor of VEGFR 1,2,3 tyrosine kinases for cancer therapy[J]. Cancer Biol Ther,2014,15(12):1635-1645.
[16] Zhao D,Pan C,Sun J,et al. VEGF drives cancer-initiating stem cells through VEGFR-2/Stat3 signaling to upregulate Myc and Sox2[J]. Oncogene,2015,34(24):3107-3119.
[17] Zhang M,Tian Z,Sun Y. Successful treatment of ovarian cancer with apatinib combined with chemotherapy:A case report[J]. Medicine(Abingdon),2017,96(45):e8570.
[18] 赖章超,梁仁佩,吴清木,等. 甲磺酸阿帕替尼对二线治疗失败的晚期卵巢癌的近期疗效观察[J]. 实用肿瘤杂志,2018,33(4):26-29.
[19] 郎丰平,赵毓毅,范鹏. 甲磺酸阿帕替尼治疗晚期胃癌的疗效及安全性分析[J]. 实用癌症杂志,2017,32(6):996-998.
[20] Blaser AR,Starkopf L,Deane AM,et al. Comparison of different definitions of feeding intolerance:A retrospective observational study[J]. Clin Nutr,2015,34(5):956-961.
[21] 李琪,赵峻峰,史晓宇,等. 阿帕替尼联合化疗用于二线治疗失败晚期卵巢癌的临床观察[J]. 河北医科大学学报,2017,38(12):1384-1387.
(收稿日期:2019-07-12)
