强筋祛湿液药效学研究
2019-11-08郑立肯叶世芸殷少文2孙济平
郑立肯 叶世芸* 殷少文2 孙济平 王 维
1.贵州中医药大学,贵州 贵阳 550000;2.贵阳市第三人民医院,贵州 贵阳 550006
痹者,闭也。《素问·痹证》中记载:“风寒湿三气杂至,合而为痹也”[1],早在《黄帝内经》中就有收录运用“醪酒”治疗痹证[2]。中医理论下由邪气侵犯人体肌表经络引起的痛痹、行痹、着(湿)痹等合称为“痹证”,以筋骨肌肉酸胀疼痛、麻痹、沉重甚至关节肿胀变形等为主要临床表现。现代医学中所认为的慢性自身免疫性疾病,如风湿关节炎、类风湿关节炎、风湿多肌痛、风湿热、神经痛等关节炎症与疾病均属于“痹证”范畴[3]。常规治疗风湿病症的药物有非甾体消炎止痛药、糖皮质激素、改善风湿病情药物(DMARDs)和α肿瘤坏死因子(TNF-α)抑制剂等新型生物制剂[4-5],除单用常规合成药外,亦采用csDMARD三联疗法(向甲氨蝶呤中加入羟氯喹和柳氮磺胺吡啶)、MTX-TNFi(甲氨蝶呤加入肿瘤坏死因子α抑制剂)联合治疗[6],上述药物除易产生药物依赖性外亦可能引起心血管疾病、骨质疏松以及高血压等不良反应[7-8]。中医治疗痹证常辨明风寒湿热,疾病新久,区分标本虚实方进行扶正、祛邪、通络等治疗[9],以补虚药、祛风湿药、解表药、活血化瘀药等相互配伍使用[10],配合针灸、敷贴等外治法[11]或同生物制剂联合使用,综合治疗达到良好的治疗效果。
强筋祛湿液为贵州中医药大学孙济平教授的经验方,该方中含有防己、川牛膝、寻骨风等三十余味药材,以祛风除湿、活血化瘀为主要功效,临床上常用于治疗风湿关节痛、关节肿胀,皮下损伤瘀血,皮肤擦伤溃破等。在前期研究基础上,已初步建立强筋祛湿液质量标准,现从强筋祛湿液对抗炎、消肿、镇痛方面进行主要药效学与急性给药毒性研究,以期为强筋祛湿液临床应用提供依据,并为后续深入研究奠定基础。
1 仪器与材料
1.1 试剂与药品 二甲苯(批号:20140908,重庆茂业化学试剂有限公司);2,4-二硝基氯苯(批号:T20150905,西亚试剂);完全弗氏佐剂(批号:F58810nl;USA);强筋祛湿液(批号:20150501,贵州中医药大学实验中心);消肿止痛酊(批号:20150302,广西壮族自治区花红药业股份有限公司)。
1.2 实验动物 KM小鼠,SPF级,体重18~22 g,雌性,购于长沙天勤生物技术有限公司,许可证号:SCXK(湘)2014-0011;SD大鼠,SPF级,体重180~220g,雄性,购于长沙市天勤生物技术有限公司提供,许可证号:SCXK(湘)2014-0011;家兔,Ⅰ级实验动物,体重2.1~2.5kg,雌雄各半,购于贵州医科大学实验动物中心,许可证号:SCXK(黔)2012-0001。
1.3 仪器 MNT50游标卡尺(上海美耐特实业有限公司);AB204-S分析天平(上海);YLS-3E电子压痛仪(济南益延科技发展有限公司);CT10R离心机(上海天美科学仪器有限公司)。
2 方法[2]
2.1 强筋祛湿液皮肤给药急性毒性试验 取健康家兔18只,雌雄各半,随机分为3组,即空白组、溶媒组、强筋祛湿液组,每组6只。以背脊为中线脱除背部脊柱两侧毛,约160 cm2(10 cm×16 cm),温水擦洗,24 h后检查脱毛区域皮肤无损伤。各组受试家兔均按1.34 g·kg-1皮肤涂抹给药,24 h后温水洗去受试物,局部观察家兔毒副反应情况。如试验中出现死亡的家兔需进行解剖,记录组织的颜色和体积改变等。
2.2 对二甲苯致急性耳肿胀小鼠模型消肿作用 健康小鼠随机分为6组,每组12只:空白组、溶媒组、消肿止痛酊组、强筋祛湿液组(强筋祛湿液低、中、高剂量组给药剂量按人体等效给药量的5、10、20倍计算)。空白组给予生理盐水10 mL/kg、溶媒组给予同体积的溶剂,给药组分别给予消肿止痛酊0.65 g/kg、强筋祛湿液高、中、低剂量1.86,0.93,0.47 g/kg涂于小鼠右耳廓0.2 mL,每次间隔12 h,连续给药14 d,于末次给药后30 min,每鼠右耳廓涂二甲苯0.1 mL;1 h后颈椎脱臼处死小鼠,打孔器取下左耳和右耳同一部位的圆片,称重,计算耳廓肿胀度。公式如下:
肿胀度(mg)= 右耳片重-左耳片重
2.3 对角叉菜胶致足跖肿胀大鼠模型消肿作用 取SD大鼠60只,雄性,按体重随机分为6组,即空白组、溶媒组、消肿止痛酊组、强筋祛湿液组(强筋祛湿液低、中、高剂量组给药剂量按人体等效给药量的3.5、7、14倍计算),每组10只。空白组给予同体积生理盐水,给药组分别给予消肿止痛酊0.46 g/kg、强筋祛湿液高、中、低剂量1.30,0.65,0.33 g/kg涂于右后足跖,每次给药间隔12 h,连续给药14 d。末次给药后0.5 h分别于大鼠右后足跖皮内注射1%角叉菜胶混悬液0.1 mL/只致炎;末次给药前和给药后2、3、4、5、6、8 h分别用游标卡尺测右后足跖厚度,计算足跖肿胀率。
2.4 对佐剂性关节炎大鼠模型消炎作用 取SD大鼠70只,雄性,180~220 g,按体重随机分为7组:空白组、模型组、溶媒组、消肿止痛酊组、强筋祛湿液低、中、高剂量组,游标卡尺测定右后足跖厚度。空白组右后足跖皮内注射生理盐水10 mL/kg,其余6组右后足跖皮内注射完全弗氏佐剂0.1 mL致炎。次日,空白组和模型组于生理盐水涂抹于足跖,溶媒组涂抹同体积的高粱酒,其余4组分别给消肿止痛酊0.46 g/kg、强筋祛湿液高、中、低剂量1.3,0.65,0.33 g/kg,药液涂于右侧足跖。每天间隔12 h,连续给药13 d。
观察指标:测量致炎第1 天、第7 天和第13 天右后足跖肿胀度和压痛值。给药第14 天,取股动脉取血5 mL,3000 r/min离心15 min,离心后取血清-20 ℃冷藏,采用IL-6和TNF-α定量酶联检测放射免疫试剂盒检测血清中白介素-6(IL-6)和肿瘤坏死因子(TNF -α)炎症因子;取关节滑膜HE染色病理检测。
2.5 对小鼠热板疼痛反应的影响 每次取1只18~22 g雌性小鼠放在已预热10 min(55±0.5 ℃)的热板上,自放在热板上至出现舔后足所需时间(秒)作该鼠的痛阈值。选择痛阈值范围为5~30 s的小鼠。将合格小鼠随机分为6组,每组12只分为:空白组、溶媒组、消肿止痛酊组、强筋祛湿液低、中、高剂量组(强筋祛湿液低、中、高剂量组给药剂量按人体等效给药量的5倍、10倍、20倍计算),分别给生理盐水10 mL/kg、高粱酒10 mL/kg、消肿止痛酊0.65 g/kg、强筋祛湿液高、中、低剂量1.86、0.93、0.47 g/kg药液涂于双后足跖,每次给药间隔12 h,连续给药14 d。末次给药后2 h 用热板法测痛阈值,计算痛阈变化率;在测试中如60 s仍无反应,将小鼠取出,以免烫伤,其痛阈值以60 s计算。

3 结果
3.1 强筋祛湿液皮肤给药急性毒性试验 由表1、2可知,给药后观察14 d,期间动物未出现中毒及死亡,用温水洗去皮肤上的受试物,未观察到皮肤红斑、水肿等反应。给药期间动物体重均有增长,给药组、溶媒组与空白组统计无统计学差异(P<0.05)。
3.2 对二甲苯至急性耳肿胀小鼠模型消肿作用 致炎后,各组小鼠右耳高度红肿。与空白组比较,消肿止痛酊组与强筋祛湿液低、中、高剂量组给药后肿胀度显著低于空白组,而溶媒组无明显差异。表明强筋祛湿液对二甲苯致小鼠耳廓肿胀具有抑制作用,差异具有统计学意义(P<0.05)。见表3。

表1 家兔急性毒性试验观察结果 (1~14d)
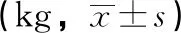

组别0 d7 d14 d空白组2.31±0.092.35±0.102.39±0.10溶剂组2.29±0.112.33±0.122.37±0.14强筋祛湿液组2.24±0.122.31±0.112.36±0.10

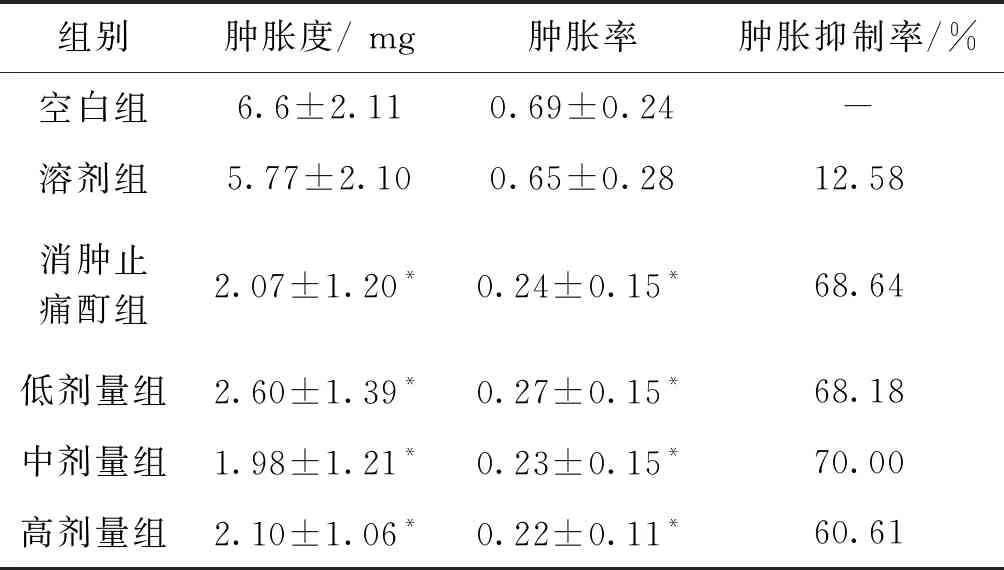
组别肿胀度/ mg肿胀率肿胀抑制率/%空白组6.6±2.110.69±0.24-溶剂组5.77±2.100.65±0.2812.58消肿止痛酊组2.07±1.20*0.24±0.15*68.64低剂量组2.60±1.39*0.27±0.15*68.18中剂量组1.98±1.21*0.23±0.15*70.00高剂量组2.10±1.06*0.22±0.11*60.61
注:与空白组比较,*P<0.05。
3.3 对角叉菜胶致足跖肿胀大鼠模型消肿作用 由表4可知,同空白组比较,注射角叉菜胶后测量所有组别大鼠足趾肿胀率减弱,同时消肿止痛酊组、强筋祛湿液各剂量组大鼠足趾肿与空白组比较有明显差异。表明强筋祛湿液对角叉菜胶致大鼠的足趾肿胀具有抑制作用。
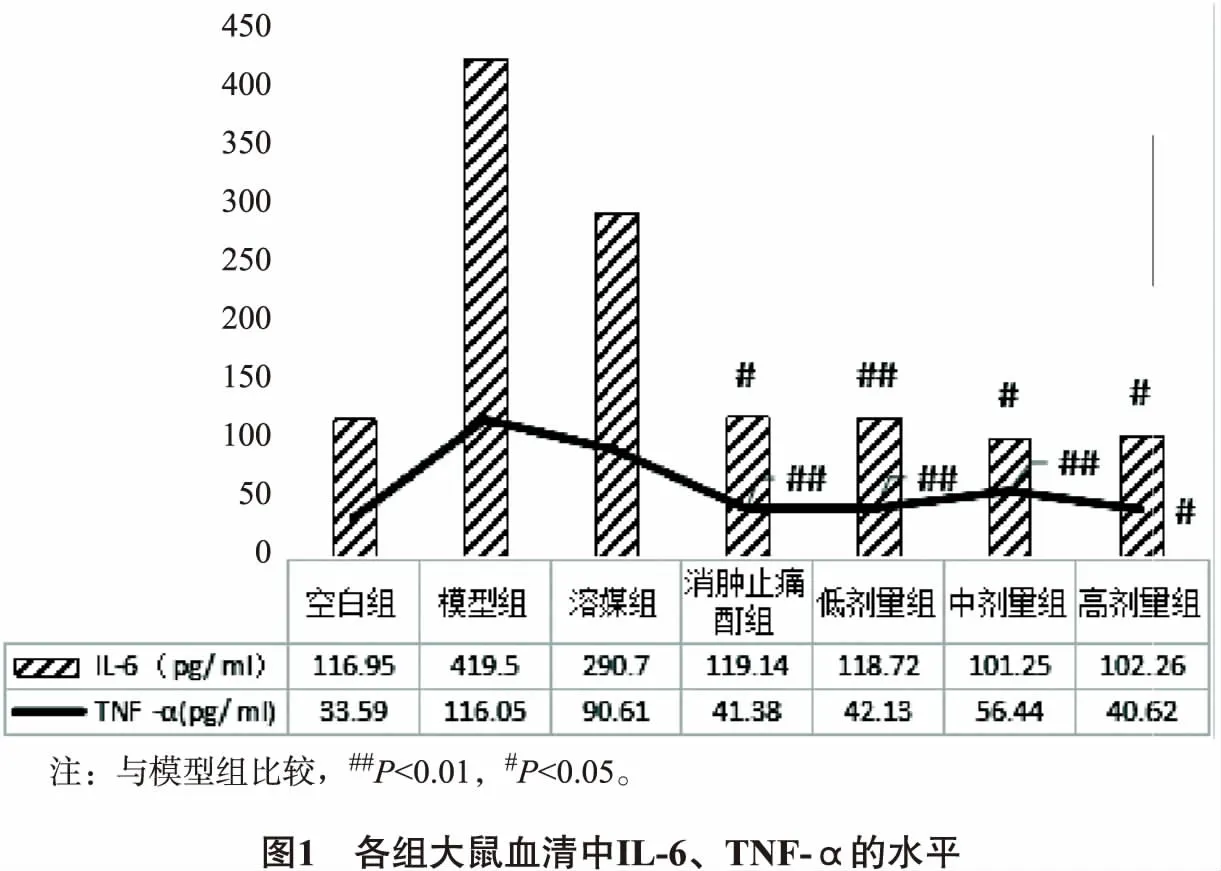
3.4 对佐剂性关节炎大鼠模型消炎作用 由表5可知,在连续给药7 d至13 d后,消肿止痛酊组与强筋祛湿液药酒的高、中、低剂量组在致炎后大鼠的足趾肿胀度减弱,与模型组比较有明显差异。继续给药至第13 天后,阳性对照药物消肿止痛酊与强筋祛湿液的低、中、高剂量组在致炎后大鼠的足趾压痛值提高,并存在统计学差异(P<0.05),而溶媒组仍无统计学差异(P>0.05),说明强筋祛湿液可有效减轻炎症同时消肿止痛。由图1可知,造模14 d佐剂性关节炎模型组大鼠血清中TNF -α、IL-6的浓度显著性增加,消肿止痛酊组和强筋祛湿液组可显著性降低TNF -α、IL-6的浓度。
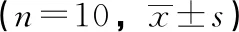

致炎后不同时间足跖肿胀率组别2 h3 h4 h5 h6 h8 h空白组0.60±0.120.51±0.110.39±0.100.40±0.110.39±0.100.35±0.08溶媒组0.51±0.080.48±0.070.37±0.060.36±0.120.42±0.100.32±0.10消肿止痛酊0.48±0.070.38±0.08*0.27±0.06*0.26±0.08*0.25±0.09*0.20±0.11*低剂量0.46±0.110.44±0.150.32±0.080.30±0.06*0.26±0.08*0.25±0.11中剂量0.43±0.160.37±0.160.22±0.09*0.22±0.09*0.14±0.09*0.12±0.09*高剂量0.50±0.110.26±0.08*0.18±0.07*0.15±0.07*0.12±0.08*0.13±0.04*
注:与空白组比较,*P<0.05。
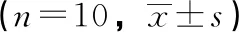
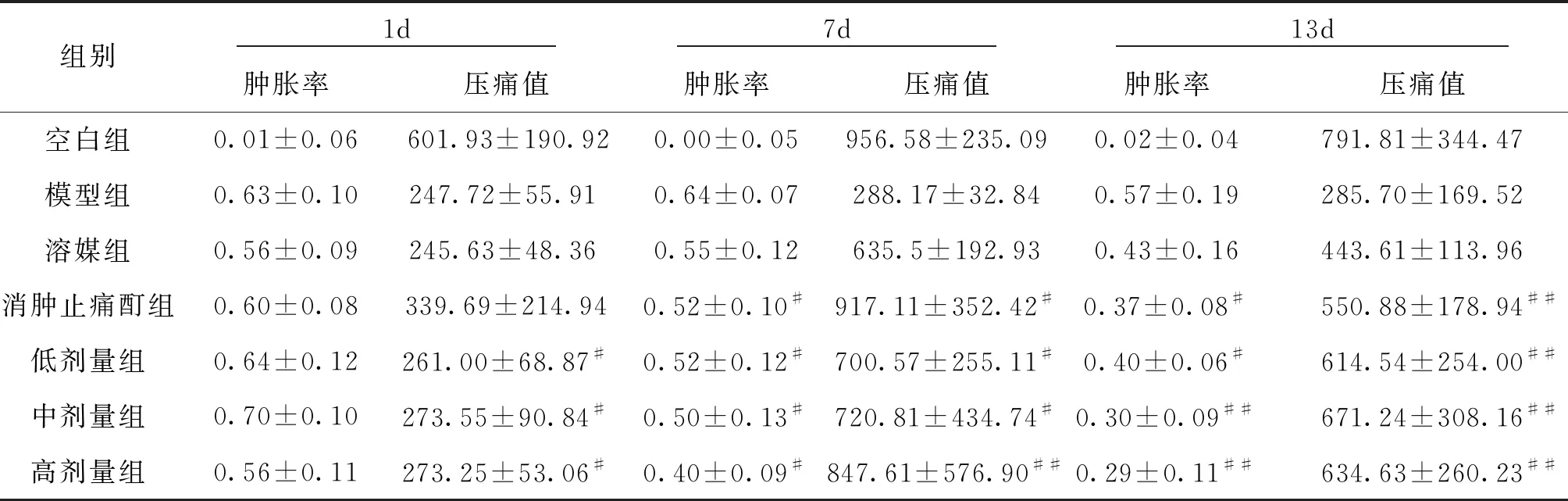
组别 1d 7d 13d 肿胀率压痛值肿胀率压痛值肿胀率压痛值空白组0.01±0.06601.93±190.920.00±0.05956.58±235.090.02±0.04791.81±344.47模型组0.63±0.10247.72±55.910.64±0.07288.17±32.840.57±0.19285.70±169.52溶媒组0.56±0.09245.63±48.360.55±0.12635.5±192.930.43±0.16443.61±113.96消肿止痛酊组0.60±0.08339.69±214.940.52±0.10#917.11±352.42#0.37±0.08#550.88±178.94##低剂量组0.64±0.12261.00±68.87#0.52±0.12#700.57±255.11#0.40±0.06#614.54±254.00##中剂量组0.70±0.10273.55±90.84#0.50±0.13#720.81±434.74#0.30±0.09##671.24±308.16##高剂量组0.56±0.11273.25±53.06#0.40±0.09#847.61±576.90##0.29±0.11##634.63±260.23##
注:与模型组比较,#P<0.05,##P<0.01。
由图2可知,处死实验大鼠,取右后肢关节滑膜固定于10%的甲醛溶液中,脱钙后常规石蜡包埋,切片并HE染色后,空白组滑膜上皮细胞形态正常,呈单层排列,滑膜细胞无水肿;模型组滑膜上皮细胞严重增生,滑膜细胞水肿明显,大量炎性细胞浸润;消肿止痛酊组滑膜上皮细胞轻微增生,滑膜细胞水肿不明显;强筋祛湿液组滑膜上皮细胞少量增生,滑膜下见少量炎性细胞浸润,滑膜细胞轻度水肿。表明强筋祛湿液对佐剂致大鼠关节炎病变有明显改善作用。

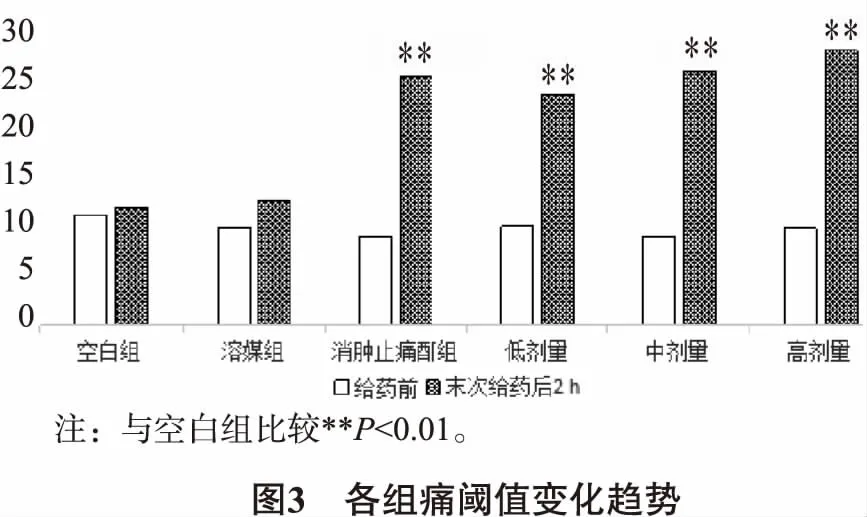
3.5 对小鼠热板疼痛反应的影响 由图3可知,在不同时间内的痛域值有显著性差异,各个药物组之间的痛域值差异有显著性意义。与空白对照组相比较,消肿止痛酊组、强筋祛湿液低、中、高剂量组的痛域值呈现上升趋势,在第14 天时,痛域值具有显著性差异,表明强筋祛湿液对热板所致的非特异性疼痛具有一定抑制作用。
4 讨论
强筋祛湿液由防己、川牛膝、杜仲、红花等35味中药制备而成,主药防己称为“祛风湿要药”,有效成分粉防己碱用于治疗水肿、风湿性疾病和炎性疾病[13],研究表明粉防己碱可通过抑制NF-κB/ COX-2通路有效降低RA大鼠血清中TNF-α,IL-1β和IL-6的浓度[14-15],通过依赖芳烃受体(AhR)相互调节STAT3和STAT5活性[16]以恢复Th17/ Treg平衡发挥其抗关节炎功效[17]。川牛膝甾酮类化合物、杜仲提取物等亦可减少促炎细胞因子与环氧合酶-2的分泌,改善软骨代谢保护关节软骨[18-20]。因此,实验以足跖肿胀度、TNF -α、IL-6以及痛阈值为指标,对强筋祛湿液镇痛抗炎活性进行评价,为其临床用药的有效性提供实验依据。
本实验急性毒性试验显示,家兔给予强筋祛湿液后未出现皮肤红斑、水肿等反应,提示强筋祛湿液安全性良好;从抗炎、镇痛以及对大鼠佐剂关节炎模型等方面评价了强筋祛湿液的药理作用,结果表明其可有效抑制炎症并增加受试动物痛阈值。强筋祛湿液对二甲苯致小鼠耳廓肿胀、对角叉菜胶致大鼠足跖肿胀具有不同程度的抑制作用,给药后3 h高剂量组大鼠足趾肿胀率减弱,同空白组比较出现明显差异,表明强筋祛湿液具有抗炎作用。给药组在不同时间内痛域值呈现上升趋势,表明强筋祛湿液对热板所致的非特异性疼痛具有一定抑制作用。同时,强筋祛湿液可显著性降低佐剂性关节炎模型组大鼠血清中IL-6和TNF-α的浓度与水平,提示强筋祛湿液抗类风湿的机理或与调节炎性细胞因子有关。各组大鼠关节滑膜经HE染色后结果表明强筋祛湿液对佐剂致大鼠关节炎病变有明显改善作用。
综上所述,强筋祛湿液对完全佐剂、对角叉菜胶所导致足趾肿胀度与二甲苯致小鼠耳廓肿胀具有极显著的抑制作用,急性毒性试验结果显示安全性较好,且对皮肤无明显皮肤过敏反应,可显著下调佐剂关节炎模型血清中炎性细胞因子水平,显著提高痛阈值。故强筋祛湿液对于痹证有良好的作用效果,作为院内制剂具有良好的开发价值和应用前景。
