当归调经颗粒(无糖型)的质量标准研究
2019-11-08唐靖雯卢礼平李娇娇
唐靖雯 卢礼平 李娇娇 杨 桃 潘 梅
贵州威门药业股份有限公司,贵州 贵阳 550018
当归调经颗粒由当归、熟地黄、川芎、党参、白芍、甘草、黄芪等7味药材组成,收载入《中国药典》2015年版。具有补血助气、调经的功效,用于贫血衰弱、病后、产后血虚以及月经不调、痛经。本研究在当归调经颗粒含糖型基础上,完成了其无糖型产品的质量标准研究并建立了企业内控质量标准,为广大患者提供了一个治疗痛经的产品。为保证临床用药的安全、有效以及更好地控制产品质量,本研究采用薄层色谱法对制剂中当归、川芎、甘草、黄芪、白芍等5味药材进行定性鉴别;建立了以制剂中白芍的主要活性成分芍药苷为指标性成分的HPLC含量测定方法。
1 仪器与材料
1.1 仪器 Agilent 1260高效液相色谱仪,包括二极管阵列检测器、ChemStation色谱工作站、1200型自动进样器(美国Agilent公司);AG135型电子天平(瑞士Mettler-Toledo公司);CH-250型超声波清洗机(天津恒奥科技公司,功率:250W,频率:40KHz);硅胶G(青岛海洋化工厂分厂,批号:20150701)。
1.2 药品与试剂 无糖型当归调经颗粒(批号:170501、170502、170503,贵州威门药业股份有限公司);芍药苷对照品(批号:110736-201741,中国食品药品检定研究院);磷酸(批号:10015408,国药集团化学试剂有限公司);乙腈为色谱纯;乙酸乙酯、三氯甲烷、冰醋酸、环己烷、无水乙醇均为分析纯;水为超纯水。
2 方法与结果
2.1 定性鉴别
2.1.1 当归、川芎的鉴别 取本品10 g,研细,加水30 mL使溶解,用乙醚振摇提取2次(水液备用),每次使用20 mL,将两次乙醚提取液合并,挥干乙醚提取液,残渣加l mL甲醇使完全溶解,作为供试品溶液。分别取当归、川芎药材,按照供试品溶液的制备方法分别制成当归、川芎对照药材溶液。另按制剂的处方比例称取适量缺当归、川芎药材的其他各味药材,按该制剂的制备工艺制成颗粒,取颗粒适量,按上述制备供试品溶液的操作方法制成缺当归、川芎药材的阴性样品。照薄层色谱法(2015年版中国药典四部,通则0502),分别依次吸取上述当归对照药材、川芎对照药材、阴性样品、供试品溶液各4 μL,分别依次点于同一硅胶G薄层板,选用正己烷-二氯甲烷-乙酸乙酯-甲酸(4∶1∶1∶0.1)的溶液为展开剂进行展开,取出硅胶板后放置晾干,将晾干的硅胶G薄层板置紫外光灯(365 nm)下检视。结果,当归的TLC图中,不同批次供试品溶液所呈现的斑点完全一致,在与对照药材色谱相应的位置上显相同颜色的荧光斑点,且阴性无干扰。如图1所示。
2.1.2 甘草的鉴别 取本品10 g,研细,加乙醚40 mL,超声处理30 min,滤过,弃去乙醚液,残渣挥干乙醚,加水40 mL使溶解,用水饱和的正丁醇振摇提取2次,每次30 mL,合并正丁醇液,用正丁醇饱和的水洗涤2次,每次20 mL,分取正丁醇液,回收溶剂至干,残渣加甲醇l mL使溶解,作为供试品溶液。另取甘草药材及缺甘草的阴性样品适量,按上述供试品溶液的制备方法分别制成甘草对照药材溶液、缺甘草的阴性样品溶液。照薄层色谱法(2015年版中国药典四部,通则0502),分别吸取上述甘草对照药材、阴性样品、供试品溶液各6 μL,分别依次点于同一硅胶G薄层板,选用乙酸乙酯-甲酸-冰醋酸-水(15∶1∶1∶2)的溶液为展开剂进行展开,取出硅胶板后放置晾干,将晾干的硅胶G薄层板置紫外光灯(365 nm)下检视。结果,当归的TLC图中,不同批次供试品溶液所呈现的斑点完全一致,且阴性无干扰。如图2所示。


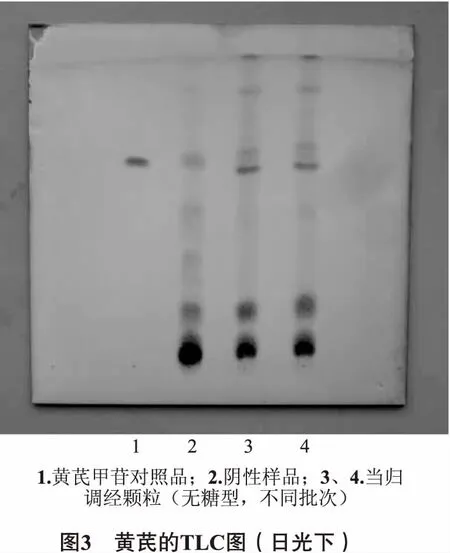
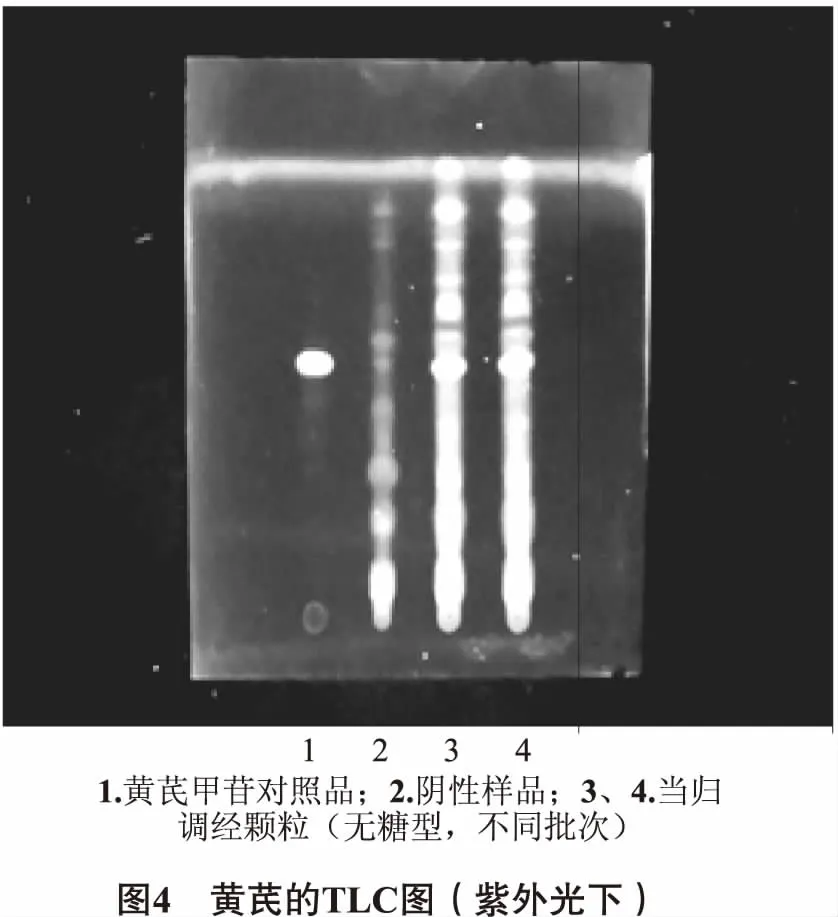
2.1.3 黄芪的鉴别 取“2.1.1”项下的备用水溶液,用水饱和的正丁醇振摇提取2次,每次30 mL,合并正丁醇提取液,用氨试液洗涤2次,每次20 mL,分取正丁醇液,回收溶剂至干,残渣加甲醇l mL使溶解,作为供试品溶液。取黄芪甲苷对照品,加甲醇制成每l mL含0.5 mg的溶液,作为对照品溶液。另取缺黄芪的阴性样品适量,按上述供试品溶液的制备方法制成缺黄芪的阴性样品溶液。照薄层色谱法(2015年版中国药典四部,通则0502),分别吸取上述黄芪苷对照品、阴性样品、供试品溶液各6 μL,分别依次点于同一硅胶G薄层板,选用三氯甲烷-甲醇-水(13∶7∶2)的下层溶液作为展开剂,取出硅胶板后放置晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,分别在日光及紫外光(365 nm)下检视。结果,黄芪的TLC图中,不同批次供试品溶液所呈现的斑点完全一致,日光下显相同颜色的斑点,紫外光下显相同颜色的荧光斑点,且阴性无干扰。如图3、图4所示。
2.1.4 白芍的鉴别 取本品10 g,加乙醇10 mL,振摇5 min,滤过,滤液蒸干,残渣加乙醇l mL使溶解,作为供试品溶液。取芍药苷对照品,加乙醇制成每l mL含l mg 的溶液,作为对照品溶液。另取缺白芍的阴性样品适量,按上述供试品溶液的制备方法制成缺白芍的阴性样品溶液。照薄层色谱法(2015年版中国药典四部,通则0502),分别吸取上述芍药苷对照品、阴性样品、供试品各10 μL,分别依次点于同一硅胶薄层板,选用三氯甲烷-乙酸乙酯-甲醇-甲酸(40∶5∶10∶0.2)为展开剂进行展开,取出硅胶板后放置晾干,喷以5%香草醛硫酸溶液,加热至斑点显色清晰。结果,白芍的TLC图中,不同批次供试品溶液所呈现的斑点完全一致,与芍药苷对照品相应的位置上,显相同的斑点,且阴性无干扰。如图5所示。

2.2 芍药苷的含量测定
2.2.1 色谱条件 色谱柱:Agilent TC-C18(250 mm×4.6 mm,5 μm);乙腈-0.1%磷酸溶液(12∶88,V/V);流速:1.0 mL/min;检测波长:230 nm;柱温:25 ℃;进样量:10 μL。
2.2.2 溶液的制备
2.2.2.1 供试品溶液[2]取装量差异项下的本品,研细,从中取约2.5 g药物粉末,精密称定,置具塞锥形瓶中,精密加入70%乙醇10 mL使溶解,密塞,称定重量,超声处理(功率250 W,频率50 kHz)30 min,放冷,再称定重量,用70%乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.2.2.2 对照品溶液 取芍药苷对照品适量,精密称定,用甲醇配制成每1 mL含35 μg的溶液,既得。
2.2.2.3 缺白芍的阴性样品 按处方称取缺白芍的群药,按上述供试品溶液的制备方法制成缺白芍的阴性样品溶液。
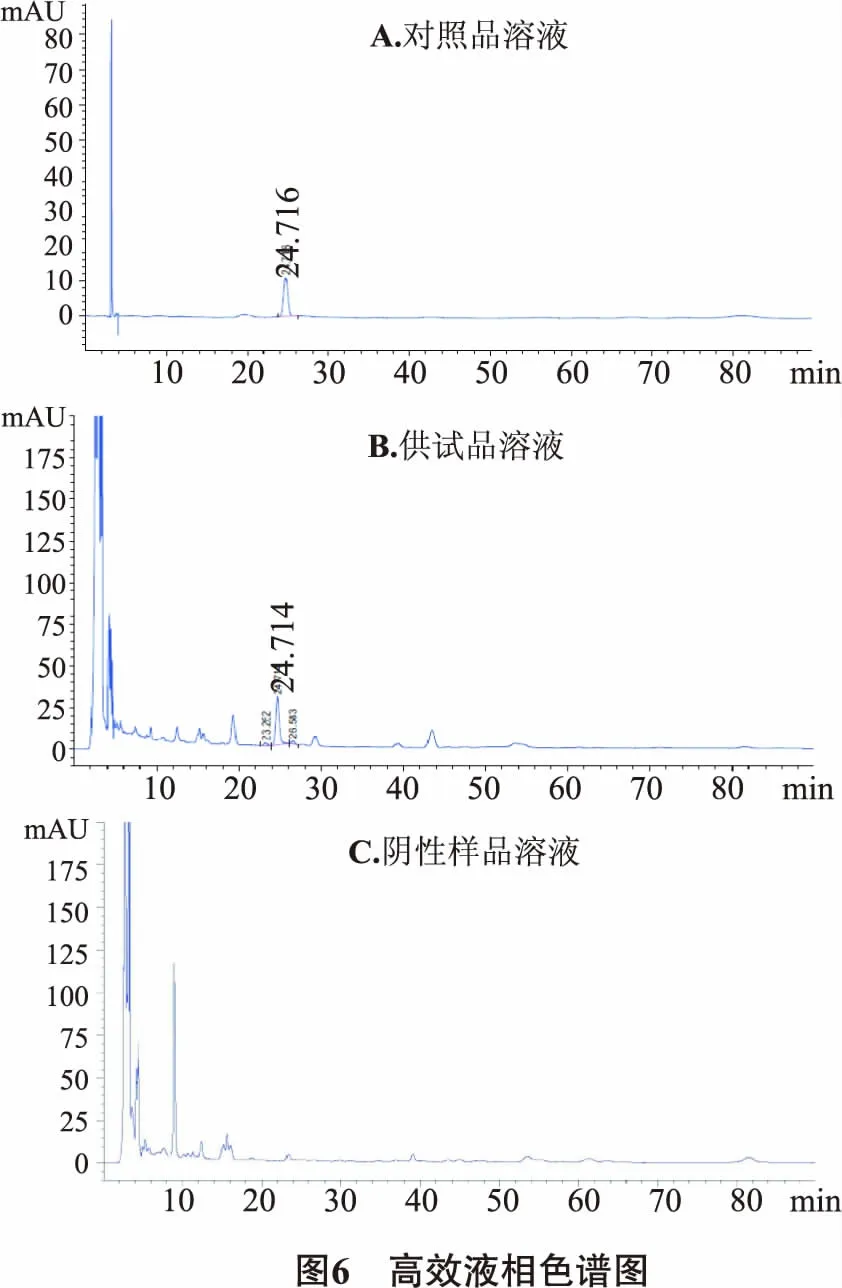
2.2.3 系统适用性试验[3-5]精密吸取“2.2.2”项下对照品溶液、供试品溶液、缺白芍的阴性样品溶液各10 μL,按“2.2.1”项下色谱条件进行测定。理论板数按芍药苷峰计算>3000,分离度>1.5。色谱如图6所示。
2.2.4 线性关系 取芍药苷对照品适量,精密称定,用甲醇溶解并稀释制成0.2192 mg/mL的溶液,分别精密量取0.5、1、2、4、8、16 μL至25 mL的容量瓶中,加甲醇稀释刻度。按“2.2.1”项下色谱条件,各进样10 μL,记录峰面积,以各对照品溶液的浓度为横坐标,峰面积为纵坐标绘制标准曲线,进行线性回归。回归方程:A= 14.254C-25.694,r=0.9998。结果表明,对照品溶液浓度在(4.38~140.16)μg/mL范围内,与峰面积呈良好的线性关系。
2.2.5 精密度试验 取样品(批号170501),按“2.2.2”项下方法制成供试品溶液,精密吸取10 μL,按“2.2.1”项下色谱条件重复进样6次,记录芍药苷的峰面积。结果,峰面积RSD为0.28%,表明仪器精密度较好。
2.2.6 稳定性试验 取样品(批号170501),按“2.2.2”项下方法制成供试品溶液,按“2.2.1”项下色谱条件,分别于0、2、4、6、8、10 h进样测定记录色谱峰。结果,峰面积的RSD为1.72%,表明供试品溶液在10 h内稳定。
2.2.7 重复性试验 取同一批样品(批号170501)6份,精密称定,按“2.2.2”项下方法制成供试品溶液,按“2.2.1”项下色谱条件进行测定,以外标一点法计算芍药苷的含量。结果,含量的RSD为1.96%,表明本方法的重复性良好。
2.2.8 加样回收率试验 取已知芍药苷含量的当归调经颗粒(无糖型,批号:170501,含量为0.3427 mg/g),采用加样回收法,测定本方法的回收率。精密称取本批次当归调经颗粒1.25 g,分别精密吸取芍药苷对照品溶液(35.20 μg/mL)10 mL,按“2.2.2”项下的方法制成供试品溶液,按“2.2.1”项下色谱条件,计算白芍苷的加样回收率,结果详见表1。
2.2.9 样品含量的测定 取3批样品(批号170501、170502、170503)各适量,按 “2.2.2”项下方法制成供试品溶液,精密吸取10 μL注入HPLC仪,按“2.2.1”项下色谱条件记录色谱图;另取“2.2.2”项下对照品溶液,同法测定。按外标法以峰面积计算供试品的含量,结果详见表2。
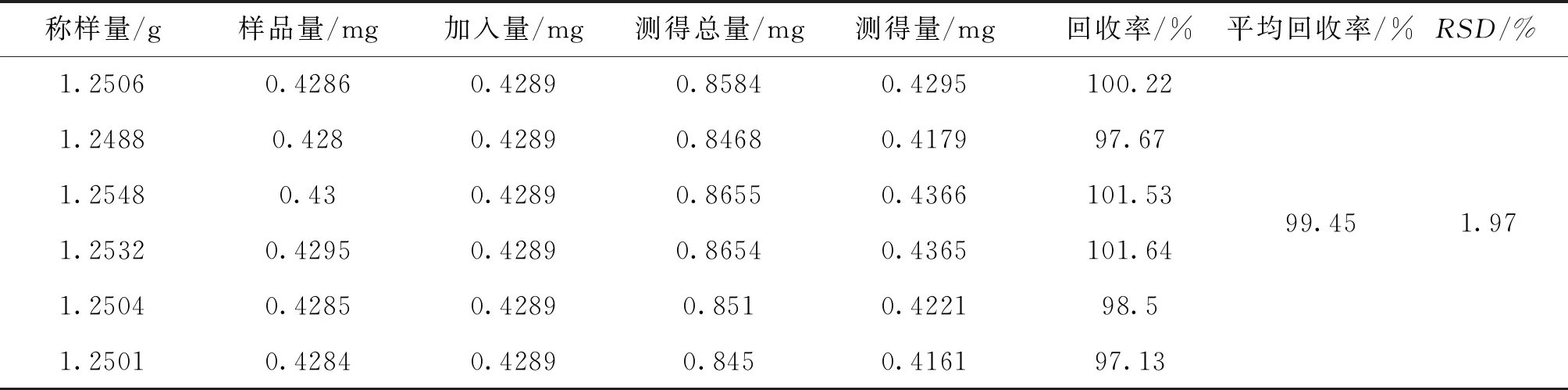
表1 加样回收率试验结果 (n=6)
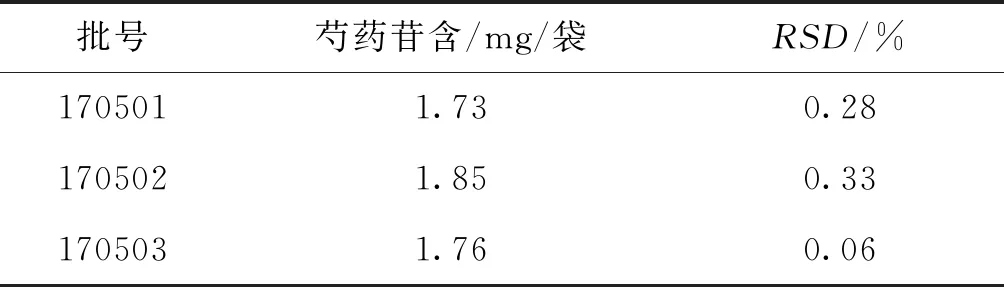
表2 样品含量测定结果 (n=3)
3 讨论
研究对制剂中当归、川芎进行TLC 定性鉴别时,按照文献方法:分别用正己烷-乙酸乙酯(9∶1)、正己烷-乙酸乙酯(4∶1)作为展开剂进行TLC定性鉴别,结果供试品色谱中均未显示斑点。在多次尝试的基础下发现,以两种溶剂作为展开剂时始终无法获得理想的展开效果,故最终选择采用正己烷-二氯甲烷-乙酸乙酯-甲酸(4∶1∶1∶0.1)的4种溶剂作为展开剂,所得的供试品色谱中斑点也较为清晰。
制剂中当归、白芍的主要活性成分分别为阿魏酸、芍药苷,在含量测定的指标性成分如何选取过程中,考虑到君药当归中阿魏酸含量较低,故选择含量较高、成分较稳定的活性成分芍药苷作为指标性成分,采用高效液相色谱法测定白芍中芍药苷的含量。但由于中药制剂成分复杂且该制剂中白芍所占比例小等因素,仅以白芍中芍药苷作为指标性成分来控制该制剂质量明显不足,因此在后续的研究中,应优化臣药中阿魏酸的提取方法,增加制剂中阿魏酸提取量,建立多指标性成分的含量测定方法,以更有效地控制该制剂的质量。
综上,本研究建立的质量控制分析方法,经过对多批产品的验证,结果表明该质量控制方法简便、准确,可用于当归调经颗粒(无糖型)生产过程质量控制,能有效地保证产品临床用药的安全性、有效性和可控性。
