复方九节茶颗粒微生物限度检查方法的建立与验证
2019-10-30广西桂林市食品药品检验所541012覃晓李夏林
广西桂林市食品药品检验所(541012)覃晓 李夏林
广西医科大学第一附属医院(530021)王仁生
复方九节茶颗粒是广西医科大学研制的中药制剂,处方由肿节风等三味中药组成。根据其给药途径、成分和制法,应按《中国药典》2015年版四部(1107)“非无菌药品微生物限度标准”附表1口服给药固体制剂要求进行需氧菌、霉菌和酵母菌数的测定及控制菌——大肠埃希菌检查。现按照《中国药典》2015年版四部(1105、1106)的有关规定,建立微生物限度检查方法并加以验证。
1 仪器与材料
1.1 仪器设备 电子天平(METTLER TOLEDO公司)、电热干燥箱(160~250℃)(上海沪越实验仪器有限公司沪越科学实验仪器厂)、高压蒸汽灭菌锅(ZEALWAY公司)、生物安全柜(ESCO )、恒温培养箱(30~35 ℃)(BINDER公司)、生化培养箱(20~25℃)(BINDER公司)、微生物鉴定药敏分析系统(BIONERIEUX公司)等。
1.2 培养基 胰酪大豆胨液体培养基;胰酪大豆胨琼脂培养基;沙氏葡萄糖液体培养基;沙氏葡萄糖琼脂培养基;麦康凯液体培养基;麦康凯琼脂培养基;MUG培养基,以上培养基均来源于北京陆桥技术有限责任公司。
1.3 试剂与试药
1.3.1 试剂 靛基质试剂;0.1%苯扎溴铵溶液(供洗手、擦拭操作台面用); 75%乙醇溶液;碘伏溶液。
1.3.2 稀释剂 0.9%无菌氯化钠溶液、0.05% (ml/ml)聚山梨酯80的0.9%无菌氯化钠溶液,均自己配制。
1.4 菌种 大肠埃希菌(Escherichia coli)[CMCC(B) 44 102]、金黄色葡萄球菌(Staphylococcus aureus)[CMCC(B) 26 003]、枯草芽孢杆菌(Bacillus subtilis)[CMCC(B) 63 501]、铜绿假单胞菌(Pseudomonas aeruginosa) [CMCC(B) 10 104]、白色念珠菌(Candida albicans)[CMCC(F) 98 001]、黑曲霉(Aspergillus niger) [CMCC(F) 98 003],以上菌种均购自中国食品药品检定研究院。

附表1 需氧菌总数常规法预试验结果(样品批号:20170701)

附表2 霉菌和酵母菌总数常规法预试验结果(样品批号:20170701)

附表3 金黄色葡萄球菌稀释法预试验结果(样品批号:20170701)
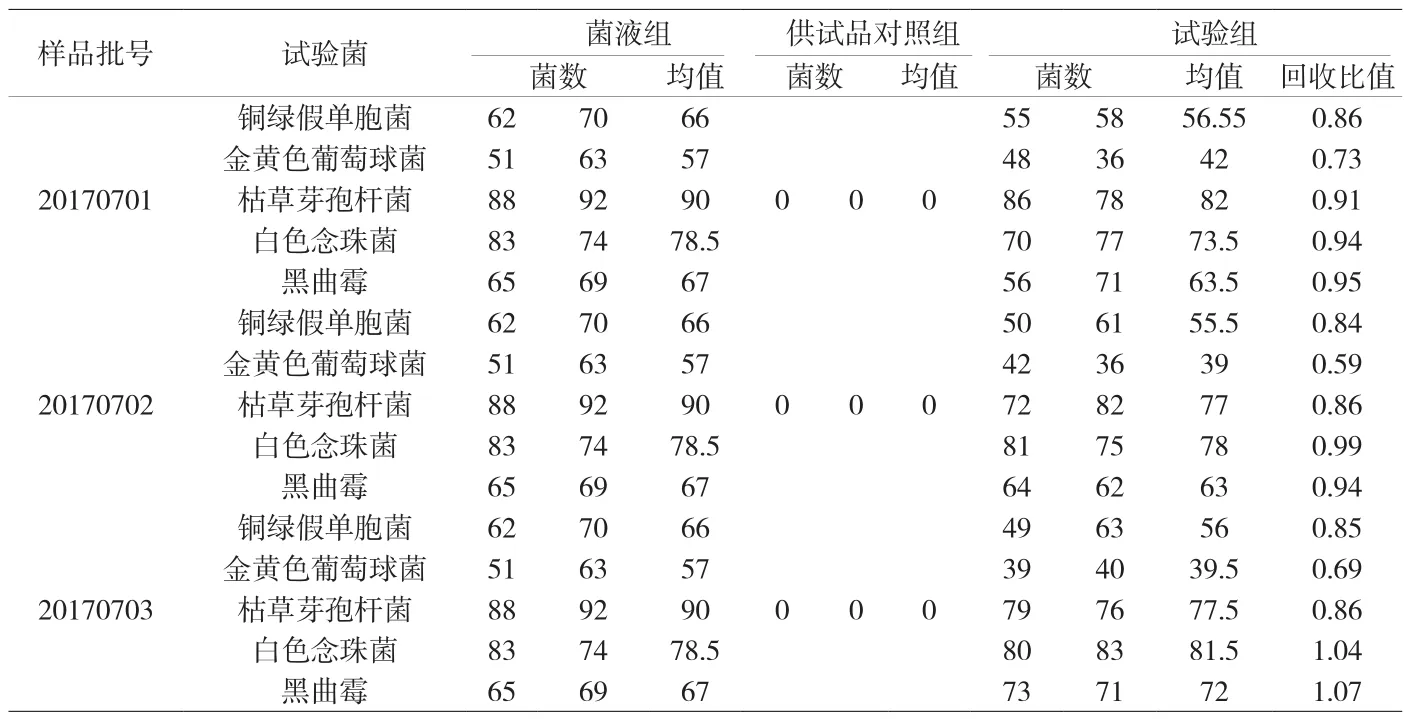
附表4 需氧菌计数方法的验证试验结果

附表5 霉菌和酵母菌计数方法的验证试验结果

附表6 大肠埃希菌检查预试验结果

附表7 大肠埃希菌检查法验证试验结果

附表8 复方九节茶颗粒微生物限度检查结果
1.5 样品 名称:复方九节茶颗粒。批号:20170701;20170702;20170703。样品来源:广西医科大学。
2 方法与结果
2.1 菌液制备 所用菌种均为第三代。取金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、白色念珠菌的新鲜培养物用0.9%无菌氯化钠溶液制成适宜浓度的菌悬液。接种黑曲霉的新鲜培养物至沙氏葡萄糖琼脂斜面培养基上,25℃培养7天,加人5ml含0.05% (ml/ml)聚山梨酯80的0.9%无菌氯化钠溶液,将孢子洗脱。然后吸出孢子悬液至无菌试管内,用含0.05% (ml/ml)聚山梨酯80的0.9%无菌氯化钠溶液制备成适宜浓度的孢子菌悬液。
2.2 供试液的制备 取供试品10g,加胰酪大豆胨液体培养基至100ml,混匀,作为1∶10供试液。
2.3 需氧菌总数、霉菌和酵母菌总数计数方法的建立及验证
2.3.1 预试验 ①试验组:取上述制备好的供试液9.9ml于灭菌试管中,加入0.1ml的试验菌液,混匀,使每1ml供试液中含菌量不大于l00cfu,然后取1ml注入平皿中,立即倾注培养基(需氧菌倾注胰酪大豆胨琼脂培养基,霉菌、酵母菌倾注沙氏葡萄糖琼脂培养基),每株试验菌平行制备2个平皿,待凝固后,需氧菌置33℃培养3天,霉菌、酵母菌置25℃培养5天,点计结果。测定结果见附表1~3。②供试品对照组:取制备好的供试液于灭菌试管中,以稀释液代替菌液同试验组操作,测定供试品本底菌数。③菌液对照组:取相应稀释液替代供试液于灭菌试管中,按试验组操作加入试验菌液并进行微生物回收试验。④回收比值计算:试验组的菌回收比值现行标准规定,若各试验菌的回收试验的回收比值在0.5~2.0范围内,则所采用的方法方可行。⑤ 结果判断 预试验结果表明,本品采用平皿法(1ml/皿)时,只有金黄色葡萄球菌试验组的试验菌回收比值不在0.5~2.0范围内,因此需氧菌总数不适合采用平皿法(1ml/皿)测定,霉菌和酵母菌总数可采用平皿法(1ml/皿)测定。用试验菌金黄色葡萄球菌采用培养基稀释法(0.5ml/皿)重新做回收试验,其试验结果见附表3。
从附表3中的结果看,金黄色葡萄球菌回收比值在0.5~2.0范围内,符合标准规定的要求,故可采用培养基稀释法(0.5ml/皿)作为本品的需氧菌总数测定是可行的。
2.3.2 需氧菌、霉菌和酵母菌计数方法的验证 取3批样品,对上述预试验方法进行验证,结果见附表4、附表5。根据3次独立的平行试验结果表明,各试验组的试验菌回收比值均在0.5~2.0,确定本品的需氧菌总数检查为采用平皿法(培养基稀释0.5ml/皿),霉菌和酵母菌总数检查为平皿法(1ml/皿)。
2.4 控制菌检查方法的建立和验证 供试液的制备同2.2项下;菌液制备同2.1项下。
2.4.1 大肠埃希菌 ①试验组:取1∶10供试液10ml接种至100ml胰酪大豆胨液体培养基中,同时加入不大于100cfu的大肠埃希菌,33℃培养24h。取上述培养物lml接种至100 ml麦康凯液体培养基中,42℃培养48小时。取麦康凯液体培养物划线接种于麦康凯琼脂培养基平板上,33 ℃培养72小时,观察其菌落形态。取麦康凯琼脂培养基平板上的菌落经纯化后培养物,接种至5mlMUG培养基中,培养,于5h、24h在366nm紫外线下观察,同时用未接种MUG培养基作本底对照。若管内培养物呈现荧光,为MUG阳性;反之,则为MUG阴性。沿管壁加入数滴靛基质试液,液面呈现玫瑰红色,为靛基质阳性;呈试液本色则为靛基质阴性。同时挑取经纯化后的新鲜培养物制成一定菌液浓度后上微生物鉴定药敏分析系统进行培养鉴定,概率在85%以上可以接受。试验结果见附表6。②阳性对照组:取不大于100cfu的大肠埃希菌,接种至100ml胰酪大豆胨液体培养基中,方法同试验组。③阴性对照组:以稀释液代替供试品溶液,接种至100ml胰酪大豆胨液体培养基中,方法同试验组。
结果表明,采用常规法进行大肠埃希菌检验,结果可行。
2.4.2 控制菌检查方法的验证 取3批样品对上述预试验方法进行验证。结果见附表7。根据3次独立的平行试验结果表明,确定大肠埃希菌检查方法为常规法。
3 供试品的微生物限度检查
取三批供试品,按上述确定的微生物限度检查法进行检验,结果见附表8。
4 结果与讨论
4.1 样品预试验中,采用平皿法(1ml/皿)反复做了三次,每次金黄色葡萄球的回收比值低于0.5,说明样品对该菌有轻微的抑制作用,改为培养基稀释法(0.5ml/皿)降低每个皿中的药物浓度来降低其抑菌能力以提高回收比值。故本试验采用培养基稀释法(0.5ml/皿)作为该品种需氧菌计数。
4.2 白色念珠菌及黑曲霉预试验中,采用平皿法(1ml/皿)回收比值均在0.5~2之间,故可采用平皿法作为该品种霉菌和酵母菌计数。
4.3 控制菌大肠埃希菌检查的验证,结果试验组及阳性对照组细菌生长良好,阴性对照组未长菌,为确保检测结果的可靠性,用2010年版药典方法及微生物鉴定药敏分析系统验证,结果确证检出的是大肠埃希菌。因此,确认可以采用该方法进行大肠埃希菌检查。
