儿童噬血细胞性淋巴组织细胞增多症的胸部CT及实验室检查
2019-10-19莫潼干芸根曾伟彬王晓玉龙庆玲曾洪武
莫潼,干芸根,曾伟彬,王晓玉,龙庆玲,曾洪武*
1.深圳市儿童医院放射科,广东深圳 518038;2.深圳市儿童医院血液肿瘤科,广东深圳 518038; *通讯作者 曾洪武.homerzeng@126.com
噬血细胞性淋巴组织细胞增多症(hemophagocytic lymphocytosis,HLH)是一组在多种细胞因子,如粒细胞-巨噬细胞集落刺激因子(granulocyte-macrophage colony-stimulating factor,GM-CSF)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、白介素(interleukin,IL)等作用下,以免疫系统过度刺激、淋巴细胞及巨噬细胞的病理性活化为特点的系统性炎症的临床综合征[1]。既往研究表明,未经治疗的HLH患儿平均存活时间仅约2个月[2]。HLH常见的临床征象及辅助检查异常包括发热、外周血细胞减少、骨髓涂片发现噬血细胞、肝功能损害、肝脾淋巴结肿大、凝血功能障碍等[3]。王旖旎等[4]研究发现,约63.9%的HLH患者有咳嗽、咳痰、气促、干湿啰音等呼吸系统症状。崔云等[5]研究表明,约40%的重症EB病毒感染患儿可合并肺损害,临床表现包括发热、咳嗽、气促、喘息、呼吸衰竭等。目前国内外尚缺乏儿童HLH胸部CT特征的影像学研究。本研究回顾性分析18例HLH患儿的胸部CT特征,以期为提高本病的诊断水平提供参考。
1 资料与方法
1.1 研究对象 回顾性分析2015年7月—2018年1月在深圳市儿童医院住院并确诊为HLH患儿的临床及影像学资料,18例HLH患儿中,男10例,女8例;男女比为1.25∶1,年龄 0.5~15.8岁,中位年龄2.5岁。记录血常规、病原学检查、肝功能、凝血功能等实验室检查结果及临床特征。纳入标准:①符合2004年国际组织细胞协会制订的HLH诊断标准[6];②年龄小于18岁。排除标准:①患有心、肝、肾、内分泌、血液系统等严重躯体疾病者;②不能配合检查者。根据影像学诊断结果是否存在异常征象,将HLH患儿分为正常组6例及异常组12例。
1.2 胸部 CT检查方法 18例患儿均行胸部 CT平扫,扫描仪为64排容积CT(Optima CT680 Quantum,GE)。患儿取仰卧位,两臂上举抱头,扫描范围自胸廓入口处至肺下界膈面。扫描参数:管电压100 kV,管电流250 mA,螺距0.984,层厚7.5 mm,间隔7.5 mm,重建层厚及间隔均为0.625 mm。患儿年龄过小不配合者待熟睡后检查,或检查前30 min给予10%水合氯醛0.5 ml/kg灌肠镇静,最大剂量10 ml。
1.3 影像学诊断 由2名从事儿童呼吸系统影像诊断工作的放射科副主任医师以上者采用双盲法进行阅片,观察肺内的实变、间质性改变、支气管充气征、磨玻璃样改变、空洞、胸水、胸膜增厚、纵隔腋窝淋巴结是否肿大等,并统计病灶分布。实变定义为肺实质内的均匀高密度影,掩盖肺纹理;磨玻璃样变定义为仍能见到其内肺纹理的模糊密度增高影[7]。若2人意见不一致时协商达成一致意见。
1.4 统计学方法 应用 SPSS 18.0软件,利用偏度-峰度检验法及Shapiro-Wilk检验法(W检验)对数据进行正态性检验。比较CT正常组及异常组各项实验室指标,符合正态分布的计量资料以±s表示,组间比较采用成组资料t检验;不符合正态分布者采用非参数秩和检验,描述参数采用中位数(四分位间距)。将单因素分析中P<0.1的变量纳入多因素分析,采用二元Logistic回归分析HLH患儿肺部CT异常表现的相关因素。P<0.05表示差异有统计学意义。
2 结果
2.1 临床资料与实验室检查结果 18例HLH患儿中,16例与感染相关、2例病因未明。其中单纯EB病毒感染10例、单纯肺炎支原体感染3例、EB病毒+肺炎支原体混合感染1例、葡萄球菌感染2例。实验室检查结果见表1。本组18例HLH患儿均有持续性发热症状,热峰39.0~40.4℃,多为急性起病,对抗生素反应较差,胸部CT表现正常组热峰为39.2(39.5)℃,异常组热峰为40.0(40.1)℃,组间比较差异有统计学意义(Z=-2.268,P=0.024)。白细胞计数、血红蛋白、血小板、白蛋白、纤维蛋白原、三酰甘油、骨髓细胞学检查、血清铁蛋白等组间差异均无统计学意义(P>0.05)。见表1。
2.2 影像学特征分析 12例CT异常征象HLH患儿中,10例表现为大片状肺实变影,8例伴有支气管充气征,病变分布较广泛,9例累及两肺,其中两肺上叶最常受累,1例仅累及右肺。10例可见少量胸水,其中3例为单侧,7例为双侧。8例存在间质性改变,分布部位与肺实变相似,多为胸膜下小叶间隔增厚。5例可见磨玻璃样改变,表现为模糊的密度增高影,仍见其内肺纹理,多累及两肺上叶。仅1例患儿病情较重,右肺中叶大片实变影中出现一小空洞影,内壁光整。见图1~3。
多因素分析结果显示,年龄、热峰、白细胞计数、血红蛋白、血小板、血清白蛋白、纤维蛋白原、三酰甘油、血清铁蛋白等均非HLH患儿胸部CT异常的影响因素(P>0.05)。见表2。
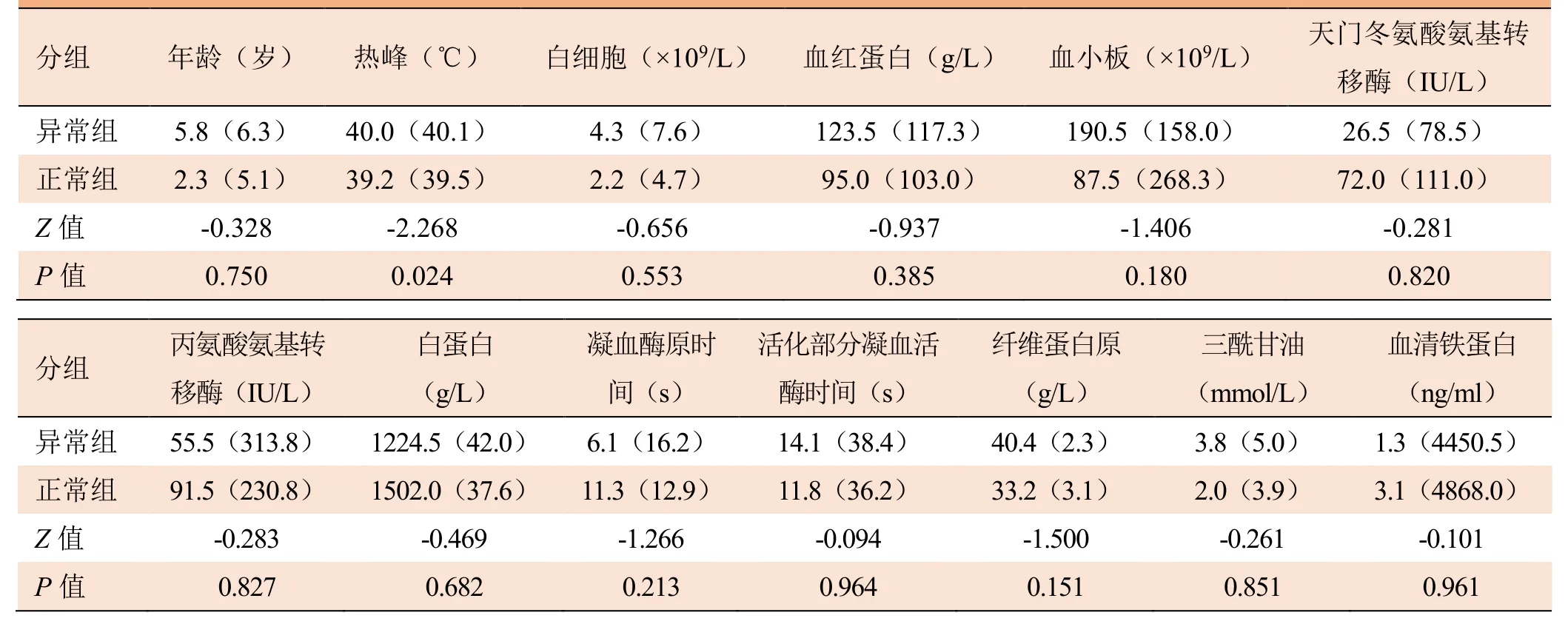
表1 两组HLH患儿临床及实验室检查结果比较
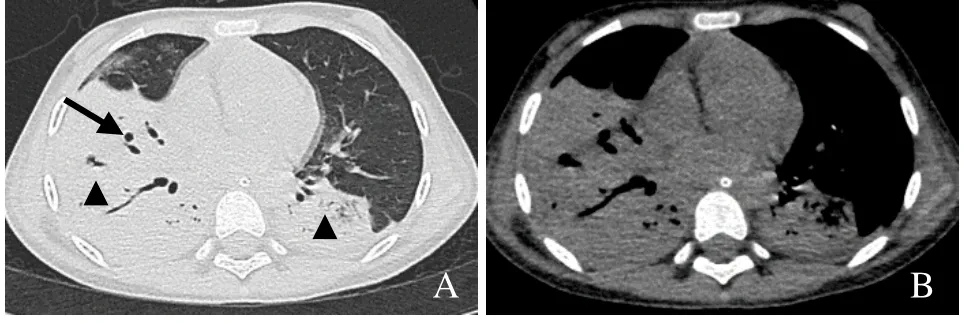
图1 女,8.6岁,间断发热、咳嗽15 d。两肺见大片状实变影(箭头),伴有支气管充气征,右肺中叶见少量磨玻璃样变,及空洞形成(箭,A);纵隔窗示左侧胸腔少量积液,肺炎支原体感染(B)
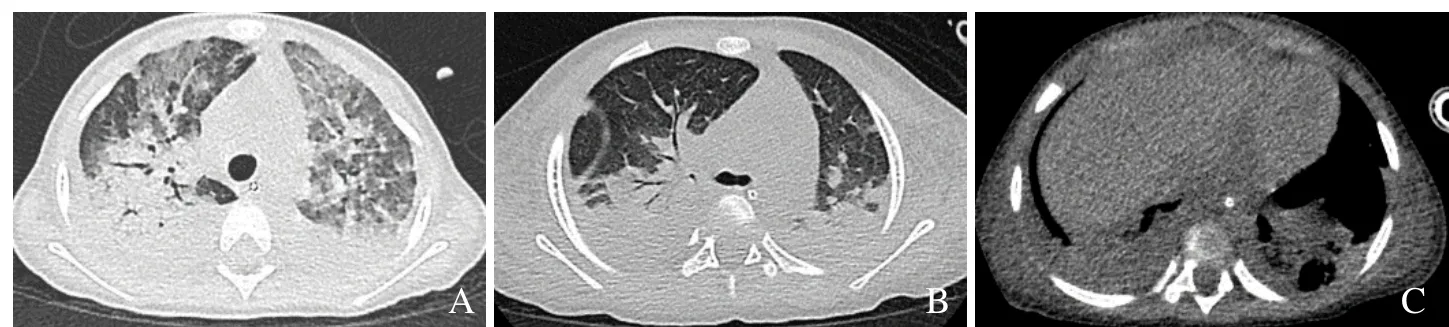
图2 女,1.8岁,发热7 d,躯干散在出血0.5 d。肺窗,两肺可见大片状实变影伴支气管充气征,可见磨玻璃样变及间质性改变(A、B);纵隔窗示双侧胸腔积液,EB病毒感染(C)
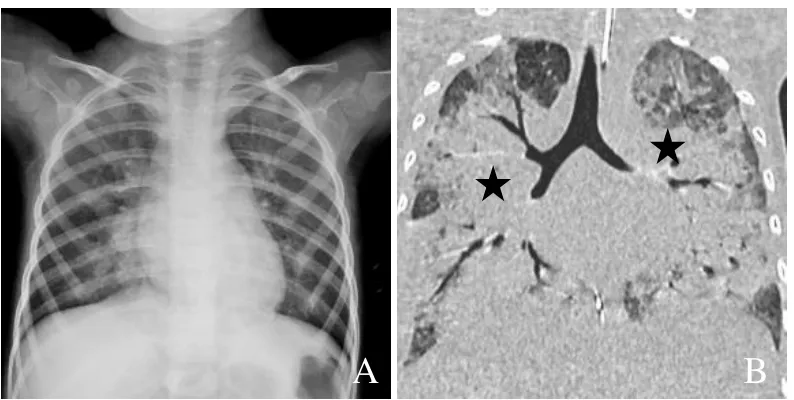
图3 男,2.5岁,发热1 d。入院第2天胸片,两肺下野中内带见少量斑片状致密影,右心缘稍模糊(A);入院后第18天胸部CT,两肺门区见对称性蝶翼状实变影(星号),内见支气管充气征,考虑肺水肿,葡萄球菌感染(B)
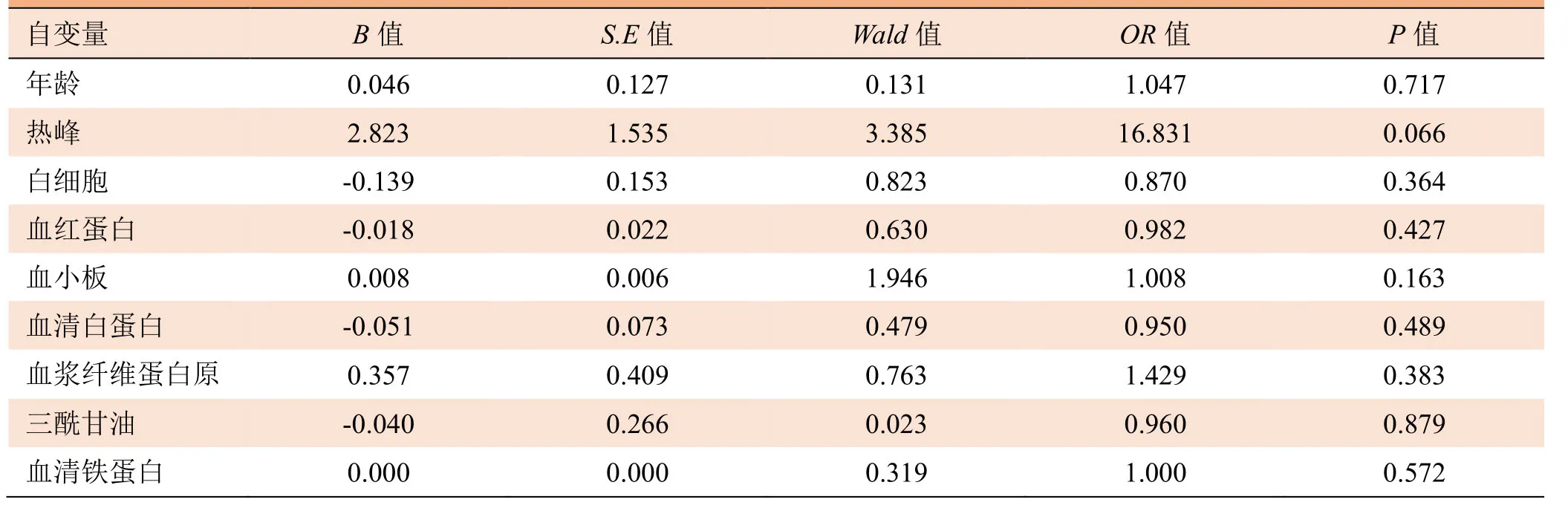
表2 胸部CT征象的多因素Logistic回归分析结果
3 讨论
3.1 HLH的概述及临床特点 Farquhar等[8]于1952年首次提出HLH的概念,并认为这是一种“家族性噬血细胞性网状细胞增生症”的遗传性免疫异常疾病。国际组织细胞协会于1999年将其划分为巨噬细胞相关的组织细胞增生症一类,并将其分为原发性(家族性)和继发性两大类[9]。研究认为,HLH与基因突变、感染、自身免疫性疾病、恶性肿瘤、血液系统疾病等相关,其中绝大部分为继发性,特别是EB病毒感染相关的HLH[10-13]。90%以上的原发性HLH发生于患儿2岁以内,为常染色体隐性遗传,确诊依赖于STX1和PRF1等基因检测[14]。常见的临床症状及实验室检查异常包括发热、肝脾肿大、外周血细胞减少、皮疹等[15]。其中伴有肺部感染者可出现咳嗽、咳痰、呼吸困难等呼吸系统症状。
本研究中,11例患儿确诊年龄低于5岁,其中8例于2岁内发病,无明显阳性家族史。治疗前,18例患儿均出现不同程度的发热,热峰39.0~40.4℃,其中16例患儿C反应蛋白明显升高,结合相关病原学检查,提示与感染相关,其中以EB病毒感染居多。本研究共10例EB病毒感染,与既往报道相符[10-13];其余感染包括肺炎支原体感染3例,EB病毒+肺炎支原体混合感染1例,葡萄球菌感染2例。获得性HLH是多种病因启动免疫系统的活化机制引起的一种疾病,使体内组织细胞增生且过多地吞噬血细胞。本组接受骨髓穿刺的17例患儿中,15例患儿骨髓细胞学检查可发现噬血细胞现象,与上述机制相符合。
HLH患者血清铁蛋白升高的机制尚不明确,可能因免疫反应活化,幼红细胞无法利用铁生成血红蛋白,故血清铁蛋白含量增高、血红蛋白含量降低[16];也有学者认为血清铁蛋白增高由于肝脏受损,储存在网状内皮系统的血清铁蛋白增加[17]。本研究中15例HLH患儿丙氨酸氨基转移酶及天门冬氨酸氨基转移酶增高,7例总胆红素增高,4例白蛋白降低,提示HLH患儿可能存在肝功能受损,但仍有3例患儿肝功能未见异常;而血清铁蛋白增高,故此结论无法完全解释HLH患儿血清铁蛋白增高的机制。其他解释还包括细胞因子的作用或铁蛋白受体下降导致血清铁蛋白升高[18]。Allen等[19]研究认为,血清铁蛋白≥10 000 ng/ml对于诊断HLH具有较高的特异性。本研究中,14例患儿的血清铁蛋白>500 ng/ml,诊断符合率达82%,其中3例血清铁蛋白>10 000 ng/ml,最高达 86 900.9 ng/ml。高水平的血清铁蛋白可能反映了机体内剧烈的细胞因子风暴和炎症反应,提示可能是HLH引起的免疫异常的结果。本研究中3例HLH患儿的血清铁蛋白<500 ng/ml,可能与患儿检测时处于疾病早期,炎症反应未到达顶峰有关。
3.2 HLH的肺部CT特征 HLH患儿的胸部CT表现不尽相同。部分患儿影像学表现较重,表现为两肺弥漫分布的大片状实变影伴支气管充气征,当肺组织坏死时,还可出现空洞征象,少量胸腔积液;表现较轻者两肺正常,可能与患儿HLH免疫系统活化是否累及肺脏、合并肺部感染、抗感染治疗等有关。EB病毒是疱疹病毒科可引起人类感染的淋巴滤泡病毒,主要作用靶细胞为表皮细胞和B淋巴细胞,可累及全身多个系统,与呼吸道感染、传染性单核细胞增多症、川崎病、特发性血小板减少性紫癜等关系密切[20]。本组10例HLH患儿与EBV感染相关,其中3例两肺可见实变影及支气管充气征,2例仅见右侧少量胸水,2例仅见纵隔腋窝淋巴结肿大,3例未见任何异常。
Mcmanus等[21]报道1例成人EBV感染性肺炎,其肺部CT表现以两肺弥漫性的磨玻璃样变及小叶间隔增厚为主,给予阿昔洛韦抗病毒治疗后,肺部表现明显好转。但本组患儿除上述征象外,还出现肺实变及胸腔积液等渗出征象。因此,EBV感染性相关HLH的胸部CT表现可能是感染性肺炎与免疫异常状态下渗出表现共同作用的结果。当病情发展为多器官功能衰竭时,常可危及患儿生命。王旖旎等[4]研究认为,经治疗的HLH患者15周总体生存率为46.8%。卢志威等[22]报道的3例患者中,1例死于多器官功能衰竭。本研究中,2例患儿经治疗及抢救无效死亡,死因分别为感染性休克合并急性肺水肿,肺出血伴呼吸衰竭及肝功能衰竭。因此,临床怀疑患有HLH,而胸部CT表现较重、进展较快时,病情凶险,应积极治疗,避免发展为多器官功能衰竭而致死。
总之,HLH患儿的肺部 CT表现多样,可能是HLH免疫系统活化累及肺脏以及肺部感染的共同结果。两肺弥漫性磨玻璃样变及小叶间隔增厚,同时伴有两肺实变影及胸腔积液的肺部CT征象,对EBV感染相关的HLH有一定的诊断意义。当胸部CT表现急速进展时,临床应提高警惕,避免患儿出现多器官功能衰竭而致死。本研究样本量较少,增加样本量和进行多中心研究有助于进一步证实肺部CT对于HLH诊断及预后评估的临床意义。
