枯草芽孢杆菌发酵玉米肽供体的筛选
2019-09-11刘奇,张智
刘 奇,张 智
(东北林业大学林学院,黑龙江哈尔滨 150040)
玉米肽(Corn Peptide,CP)是一种由氨基酸通过肽键以不同的连接方式而形成的具有特定空间结构和功能活性的短肽聚合物[1-2]。研究表明CP具有抑制血管紧张素转换酶[3]、降低血压[4]、促进乙醇代谢、醒酒护肝[5]以及抗氧化[6-8]、缓解疲劳[9]、抗癌[10]等功能。张智等[11]以CP为参照研究玉米肽锌(CP-Zn)螯合物的结构表征和体内抗氧化活性变化,结果表明CP-Zn的抗氧化活性优于CP,且能显著降低小鼠血清、肝脏中丙二醛含量,提高超氧化物歧化酶的活力。
目前常用的制备玉米肽螯合物的方法有酶解法、微生物发酵法和化学合成法[12]。枯草芽孢杆菌发酵制备玉米肽螯合物是利用微生物发酵产生的胞外酶将供体镶嵌在两个肽分子之间形成一种稳定的连接形式,可以提高CP功能活性的同时改善其适口性[13],降低肽的苦味和抗营养因子含量。目前我国利用CP制备玉米肽-葡萄糖(CP-G)并研究其体内体外抗氧化活性的研究相对较少。为充分开发利用CP,提高玉米副产物附加值,本研究以CP为底物,通过添加酸类、糖类和金属离子等供体,利用枯草芽孢杆菌(Bacillussubtilis)ls-45为发酵菌种,以DPPH转化率为指标进行供体的筛选和体内抗氧化活性的研究,为后续探讨CP修饰产物细胞免疫功能试验等提供数据支持。
1 材料与方法
1.1 材料与仪器
种子培养基(葡萄糖0.5%、酵母膏1%、蛋白胨0.5%、氯化钠0.2%) 本实验室自制;雄性SPF小鼠(体重为(20±2) g,合格证号:SCXK黑2013-004) 由黑龙江省中医药大学药物评价中心提供;CP 齐齐哈尔大学食品与生物工程学院提供;枯草芽孢杆菌(Bacillussubtilis)ls-45 东北林业大学食品微生物实验室保藏;蛋白胨、酵母膏、乳糖、半乳糖、甘露糖、果糖、葡萄糖 北京华美生科生物技术有限公司;DPPH、琥珀酸酐、乙二胺四乙酸(EDTA)、乙酸酐、乙酸、草酸、硫酸铁、硫酸铜、硫酸镁、硫酸锌、硫酸锰、硫酸钙 上海浩洋生物技术有限公司;超氧化物歧化酶(SOD)测试盒、谷胱甘肽过氧化物酶(GSH-Px)测试盒、丙二醛(MDA)测试盒 苏州卡尔文生物技术有限公司。
722S可见分光光度计 上海精密科学仪器有限公司;TU-1810紫外分光光度计 北京普析通用仪器有限公司;5030-PVL程控压力蒸汽灭菌器 长春百奥生物仪器有限责任公司;SW-CJ-IFD超净台 苏州安泰空气技术有限公司;AR2140型分析天平、S220型pH计 瑞士梅特勒-托利多仪器有限公司;ZD-85双功能气浴恒温振荡器 江苏金怡仪器科技有限公司;TgL16B型台式离心机 上海安亭科学仪器厂制造;Dgg-9053A型电热鼓风干燥箱 上海森信实验仪器有限公司。
1.2 实验方法
1.2.1 枯草芽孢杆菌发酵CP供体修饰方法 通过Sephadex G-25分级得到CP段,其平均分子质量为572 Da,肽含量为75.83%,将CP段配制成底物浓度为4%的溶液,调节pH至7;取50 mL CP溶液,按CP与不同供体(见表1)体积比为10∶1的比例加入供体,再次调节pH至7;121 ℃高压蒸汽灭菌20 min,冷却至室温(20 ℃);在无菌条件下接入枯草芽孢杆菌菌液进行发酵,枯草芽孢杆菌接种量4%,发酵时间48 h;得到的发酵液再次灭菌,冷却后4500 r/min离心10 min;流水透析24 h,过滤后冷冻干燥得到最终修饰产物[11]。

表1 各类修饰供体选择Table 1 Selection of different modified donors
1.2.2 枯草芽孢杆菌发酵CP供体筛选 以枯草芽孢杆菌为菌种发酵,利用酸类的酰基化、糖类的糖基化和金属离子的螯合作用分别对CP进行修饰,以产物DPPH·清除能力为依据,转化率为指标进行CP供体体外抗氧化能力的筛选。
1.2.2.1 CP修饰产物DPPH·清除能力的测定 将1.2.2制得的CP修饰产物配制成3 mg/mL的乙醇溶液备用。用95%的乙醇溶解DPPH粉末,配成0.2 mmoL/L的DPPH溶液。取待测样品溶液和DPPH各2 mL混匀,室温(20±2) ℃下避光放置30 min后,于517 nm处测吸光度值,记为OD1;对照组用95%的乙醇代替DPPH溶液,同样条件下室温避光放置30 min后,于517 nm处测吸光度值,记为OD2;空白组用蒸馏水代替样液,于517 nm处测定吸光值,记为OD0。
式(1)
式中:OD1为样液加DPPH溶液的吸光度值;OD2为样液加乙醇溶液的吸光度值;OD0为乙醇加DPPH溶液的吸光度值。
1.2.2.2 CP修饰产物DPPH·转化率的测定 利用酸类、糖类和金属离子对CP进行修饰,得到修饰产物的DPPH·转化率,并与CP的DPPH·转化率进行比较,得出DPPH·清除率提高的百分比,即转化率。
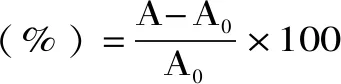
式(2)
式中:A为修饰产物的DPPH·清除率;A0为CP的DPPH·转化率。
1.2.3 CP修饰供体比例的确定 按CP与供体投料质量比1∶1、2∶1、3∶1、4∶1、8∶1和10∶1加入筛选后的供体,其余过程采用1.2.1 微生物法CP供体修饰方法,最终以产物的转化率为评价指标,考察投料比对修饰产物DPPH转化率的影响,从而确定最佳供体比例,转化率计算见式(2)。
1.2.4 动物实验模型建立与饲养 健康雄性SPF小鼠适应性饲养7 d后,称量小鼠体重,将小鼠按照体重指标随机分为7组,每组12只,采用基础饲料饲喂,自由饮水,室温环境(20±2) ℃,相对湿度45%±3%,光照12 h/d。空白组采用生理盐水灌胃,各组均每天上午9时灌胃,连续灌胃给药30 d。给药剂量根据《保健食品功能学评价程序和检验方法-2003》拟定[14],实验分组见表2。
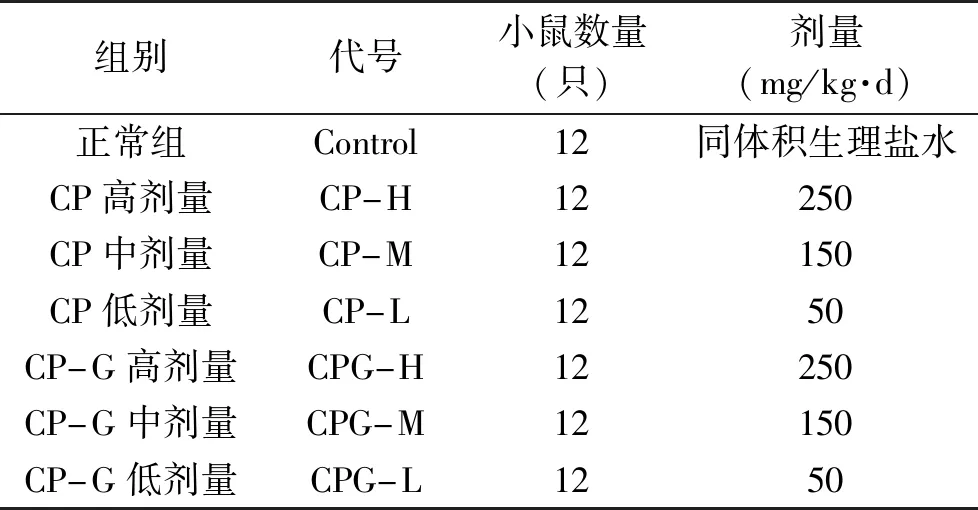
表2 功能实验分组 Table 2 Groups of function test
1.2.5 抗氧化酶活性的测定 末次灌胃给药并禁食24 h后,称量实验小鼠体重并记录,处死实验小鼠后,摘取脾脏、胸腺,利用氧化物歧化酶(SOD)试剂盒、谷胱甘肽过氧化物酶(GSH-Px)试剂盒测定小鼠血清和肝脏组织匀浆中超氧化物歧化酶(SOD)活性和谷胱甘肽过氧化物酶(GSH-Px)活性水平。
1.3 统计学分析
数据采用SPSS 20统计学软件进行比较分析,p<0.05差异显著,p<0.01差异极显著,Origin软件绘制相关图表。
2 结果与分析
2.1 CP修饰供体筛选
由图1~图3可知,利用枯草芽孢杆菌发酵CP供体的修饰结果中,酸类、糖类和金属离子修饰后产物的DPPH·转化率都大幅度提高。从酸类供体修饰效果来看,乙酸酐>柠檬酸>琥珀酸酐>草酸>乙酸>EDTA,乙酸酐DPPH·转化率达到65.95%,修饰效果最好;从糖类供体修饰效果来看,葡萄糖>乳糖>半乳糖>甘露糖>果糖,修饰供体葡萄糖的DPPH·转化率达到79.95%,是所有修饰供体中效果最佳的;从金属离子类供体修饰效果来看,Fe2+>Mg2+>Cu2+>Mn2+>Ca2+>Zn2+,其中经Fe2+修饰后的DPPH转化率达到78.26%。综合图1~图3可知,三类供体对C修饰效果整体表现为:糖类>酸类>金属离子,因此本研究选取葡萄糖作为CP修饰的最佳供体。
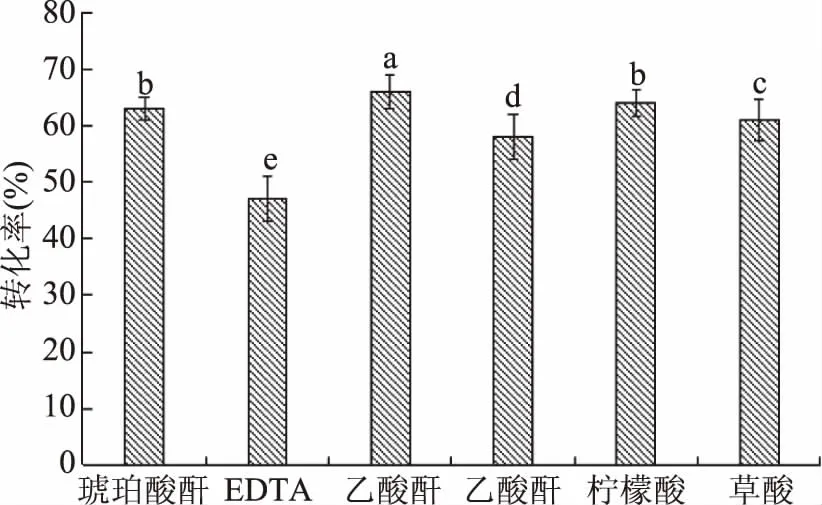
图1 酸类供体筛选Fig.1 Screening the modified donors from acid groups注:不同小写字母表示差异显著(p<0.05);图2、图3同。
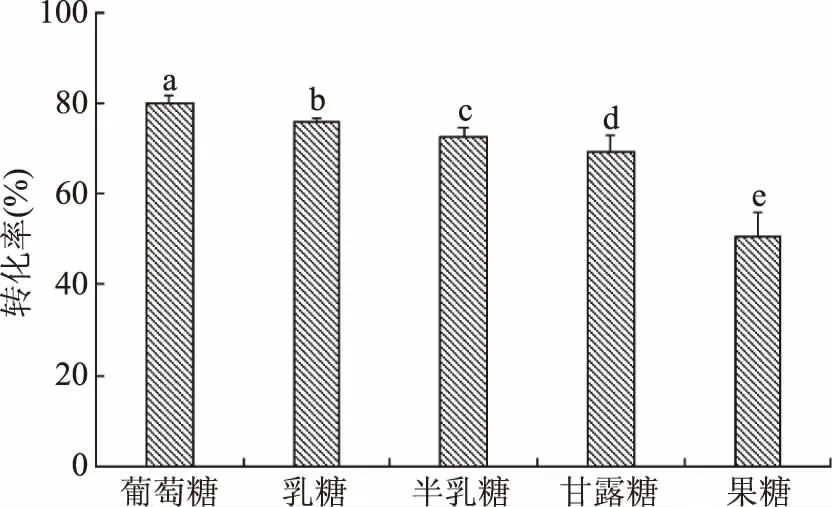
图2 糖类供体筛选Fig.2 Screening the modified donor from saccharides groups
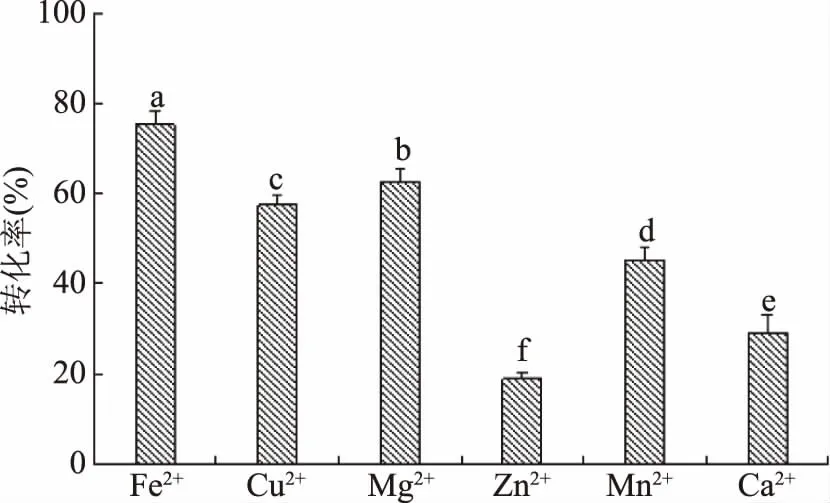
图3 金属离子供体筛选Fig.3 Screening the modified donor from metal ion groups
2.2 CP修饰供体比例的确定
由图4可以看出,随着CP与葡萄糖供体投料比的增加,即供体所占比例减少时,转化率整体呈先上升后平缓的趋势,这说明投料比对CP的DPPH转化率有一定影响。在投料比为8∶1时,转化率达到79.84%,因此从实际生产的角度考虑本研究选择投料比为8∶1作为CP与葡萄糖的最佳配比。
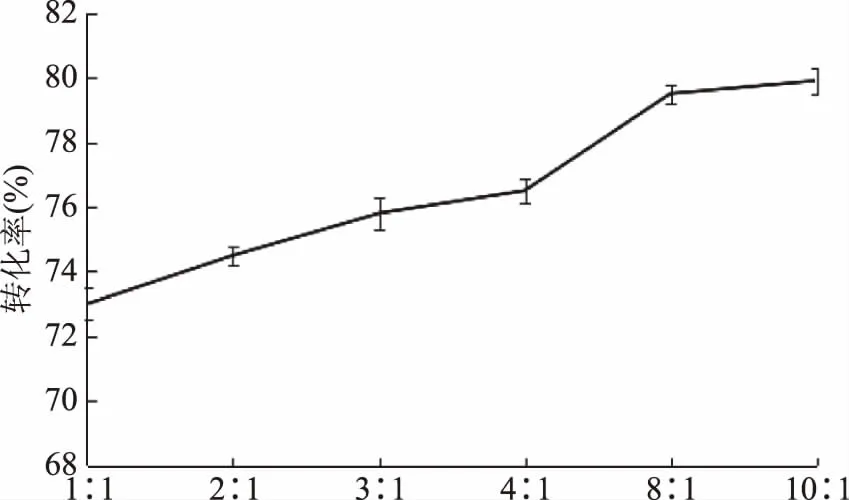
图4 葡萄糖比例的确定Fig.4 Determination of proportion of donors to glucose
2.3 小鼠体内抗氧化活性实验结果
2.3.1 血清、肝脏中SOD活性 CP和CP-G对小鼠血清、肝脏中SOD活性的影响见图5。SOD是体内重要的抗氧化酶,能有效清除氧自由基,降低或阻止其对机体细胞和组织的损害[15]。超氧化物歧化酶对机体的氧化与抗氧化平衡起着至关重要的作用,超氧化物歧化酶能清除机体内氧自由基,抑制脂质过氧化反应,保护细胞免受自由基损伤。由图5可知,与正常组相比CP中、高剂量组和CP-G低、中、高剂量组均显著(p<0.05)提高血清和肝脏中的SOD活性。

图5 CP、CP-G对小鼠血清、肝脏中SOD活性的影响Fig.5 Influence of CP、CP-G on activity of SOD in serum and liver of mice注:不同大写字母表示各组血清指标差异显著(p<0.05), 不同小写字母表示各组肝脏指标差异显著(p<0.05);图6同。
2.3.2 血清、肝脏中GSH-Px活性 CP和CP-G对小鼠血清、肝脏中GSH-Px活性的影响见图6。谷胱甘肽(GSH)是由谷氨酸、半胱氨酸和甘氨酸组成的一种三肽,是甘油醛磷酸脱氢酶的辅基,又是乙二醛酶及磷酸丙糖脱氢酶的辅酶。而GSH-Px是机体广泛存在的一种重要的催化过氧化氢分解的酶,它能特异催化还原型谷胱甘肽过氧化氢进行还原反应,清除体内低分子自由基、过氧化氢和脂质过氧化物等,进而起到保护细胞膜结构和功能完整的作用,减少氧自由基对机体细胞或组织的损伤[16]。因此血清和肝脏中SOD和GSH-Px是评价机体抗氧化应激能力的重要指标[17]。由图6可知,与正常组相比,CP和CP-G低、中、高剂量组均显著(p<0.05)提高血清中的GSH-Px活性;CP低、中、高剂量组,CP-G中、高剂量组均显著(p<0.05)提高肝脏中的GSH-Px活性。
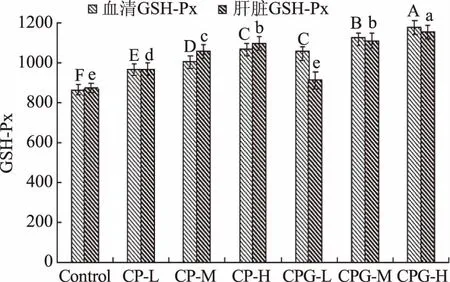
图6 CP、CP-G对小鼠血清、肝脏中GSH-Px活性的影响Fig.6 Influence of CP、CP-G on activity of GSH-Px in serum and liver of mice
3 结论
枯草芽孢杆菌发酵三类供体,分别为酸类(琥珀酸酐、乙二胺四乙酸(EDTA)、乙酸酐、乙酸、柠檬酸、草酸)、糖类(葡萄糖、乳糖、半乳糖、甘露糖、果糖)和金属离子(硫酸铁、硫酸铜、硫酸镁、硫酸锌、硫酸锰、硫酸钙),得到的CP修饰供体整体抗氧化效果为:糖类>酸类>金属离子,经筛选CP的最佳修饰供体为葡萄糖,当投料比为8∶1时,DPPH转化率达到79.84%。体内抗氧化实验表明,同对照组相比CP中、高剂量组和CP-G低、中、高剂量组均显著(p<0.05)提高血清和肝脏中的SOD活性;CP和CP-G低、中、高剂量组均显著(p<0.05)提高血清中的GSH-Px活性;CP低、中、高剂量组和CP-G中、高剂量组均显著(p<0.05)提高肝脏中的GSH-Px活性。由此说明CP-G较CP而言可以更有效提高体内SOD和GSH-Px含量,增强机体的自由基清除能力。本文为后续研究CP-G修饰产物细胞免疫机制提供理论及数据支持。
