色谱-质谱联用技术鉴定环孢素A的有关物质
2019-08-28倪悦泠杭太俊
倪悦泠,韩 兴,宋 敏,杭太俊
(中国药科大学药物分析系,南京210009)
环孢素 A(cyclosporin A,环[[(E)-(2S,3R,4R)-3-羟基-4-甲基-2-(甲氨基)-6-辛烯酰]-L-2-氨基丁酰-N-甲基甘氨酰-N-甲基-L-亮氨酰-L-缬氨酰-N-甲基-L-亮氨酰-L-丙氨酰-D-丙氨酰-N-甲基-L-亮氨酰-N-甲基-L-亮氨酰-N-甲基-L-缬氨酰],图 1),是从真菌代谢产物中提取得到含11个氨基酸残基的环肽免疫抑制剂。临床上主要用于肝、肾以及心脏移植的抗排异反应,预防及治疗骨髓移植时发生的移植物抗宿主反应[1],也是目前眼科应用最多的一种免疫抑制剂类可供眼表使用的抗炎药物,可治疗干眼症、结膜炎,抑制角膜移植排异反应[2-4]。此外,环孢素还可用于重症肌无力、类风湿性关节炎、全身性红斑狼疮、特发性血小板减少性紫癜、溃疡性结肠炎、慢性肾炎和肾病综合症等多种自身免疫性疾病[5-8]。
中国及主要发达国家现行药典已收载环孢素A及其制剂的质量标准,欧洲药典还列出其A、B、C 3类共12个杂质和结构。已有文献报道了环孢素 A制剂质量研究[9-11]及药代动力学研究[12-14],但是,环孢素A原料药有关物质的系统研究与鉴定未见文献报道。

Figure 1 Chemical structure of cyclosporine A
本研究建立了适用于环孢素A有关物质检查的色谱-质谱联用分析方法,通过TOF/MS测定了环孢素A各有关物质的准确分子质量及分子式,结合MS/MS的子离子特征,综合解析鉴定其有关物质的结构,可用于环孢素A的发酵工艺和成品的质量控制。
1 材 料
1.1 药品与试剂
环孢素A原料药(批号180301HB,江苏九阳生物制药有限公司);环孢素 A粗品(批号WCP180101,江苏九阳生物制药有限公司);环孢素A对照品(EP);环孢素色谱分离度对照品(USP,环孢素 U-环孢素,1∶100)。
乙腈、甲基叔丁基醚(美国Tedia公司);甲酸(AR,南京化学试剂股份有限公司)。自制纯净水。
1.2 仪 器
Agilent 1290 Infinity液相色谱-6224飞行时间质谱仪(美国 Agilent公司);Thermo Dionex Ulti-Mate 3000高效液相色谱-TSQQuantum Ultra型LCMS/MS联用仪(美国 Thermo-Fisher公司);BS 21S分析天平(德国Sartorius公司)。
2 方 法
2.1 色谱及质谱条件
Thermo Scientific BDS Hypersil C18(100 mm×4.6 mm,2.4μm)色谱柱;乙腈-水-甲基叔丁基醚-甲酸(430∶520∶50∶1)流动相等度洗脱,流速0.8 mL/min,柱温80℃,检测波长为210 nm,进样量20μL。
电喷雾正离子化,TOF/MS测定喷雾电压3.5 kV,雾化氮气压力 275 kPa,流量 10 L/min,温度350℃,碎片电压200 V,参比离子m/z121.050 8(质子化嘌呤,C5H5N4+)和m/z922.009 8(质子化氟代膦嗪HP-921,C18H19O6N3P3F24+),质量数扫描范围m/z100~1 300。MS/MS测定的喷雾电压4 kV,雾化气压力300 kPa,辅助气压力35 kPa,毛细管温度350℃,二级质谱扫描碰撞氩气压力0.16 Pa,碰撞能量30~60 eV。
2.2 供试品溶液的制备
取环孢素A约25 mg,精密称定,置于10 mL量瓶中,加乙腈-水(70∶30)稀释剂溶解并稀释至刻度,摇匀,配制成质量浓度为2.5 mg/mL的供试品溶液。精密量取上述溶液适量,加稀释剂定量稀释,配制0.1%的自身对照溶液。
2.3 对照品溶液的制备
取环孢素A对照品约25 mg,精密称定,加稀释剂溶解并定量稀释成质量浓度约为2.5 mg/mL的溶液作为环孢素A对照品溶液。
取环孢素色谱分离度对照品(含环孢素U-环孢素,1∶100)25 mg,精密称定,置10 mL量瓶中,加稀释剂溶解并稀释制成含环孢素A和环孢素U的质量浓度分别约为2.5 mg/mL和25μg/mL的混合溶液,用于供试品中环孢素U的定性。
2.4 强制降解试验溶液
取环孢素A约25 mg两份,加入稀释剂0.5 mL溶解后,分别经1 mol/L盐酸溶液0.5 mL 60℃水浴4 h、或1mol/L氢氧化钠溶液0.5mL 60℃水浴1 h处理后,分别中和后加稀释剂稀释至10 mL,配制成质量浓度约为2.5 mg/mL的酸、碱强制降解试验溶液。
取环孢素A约25 mg,经30%过氧化氢1 mL 60℃水浴52 h,然后加稀释剂溶解并稀释至10 mL,配制成质量浓度约为2.5 mg/mL的氧化强制降解试验溶液。
取环孢素A约25 mg,经120℃烘箱放置5 d,加稀释剂溶解并稀释至10 mL,配制成质量浓度约为2.5 mg/mL的高温强制降解试验溶液。
同时进行空白试验,制备空白对照。
3 结果和讨论
3.1 有关物质检查
建立的环孢素A有关物质挥发性流动相HPLC检查方法适用于质谱联用鉴定。现行药典所使用的乙腈-甲基叔丁基醚-水流动相体系分离效果较好,尝试将甲基叔丁基醚更换为甲醇,或使用四氢呋喃,对分离度及柱效均无改善。色谱条件中柱温是影响分离的关键因素,低于80℃柱温,环孢素A及各有关物质的保留时间均增加,峰展宽严重,分离变差。本研究优化了流动相中有机相种类、比例,尝试添加三氟乙酸和缓冲盐体系,分离均未改善。最终确立的色谱条件可尽早洗脱出各有关物质,色谱分离较好。
图2为环孢素A原料药、粗品及其强制降解溶液的HPLC-UV谱图。采用0.1%自身对照法估算有关物质的含量,按保留时间由小到大顺序对含量大于0.1%主要杂质进行识别和编号,共检出分离效果较好的29个主要有关物质,其中有关物质9、10、12、14、15、16、17、18、19、20、23、24和 27与EP中列出的9个已知结构杂质(或其光学异构体)相应。
环孢素A原料药供试品共检出2个有关物质(21、23,图2-c)。环孢素A粗品共检出9个有关物质(9、10、12、15、19、21、23、24和 28,图 2-h)。强制降解试验结果表明,本品对强酸、强碱、氧化、高温条件均具有一定敏感性,对光照条件较为稳定。酸破坏形成3个主要降解产物(13、25和26,图2-d);碱破坏形成4个主要降解产物(2、11、16和19,图2-e);氧化破坏形成2个主要降解产物(4和8,图2-f);高温破坏形成15个主要降解产物(1、3、4、5、6、7、8、14、17、18、19、20、22、27和 29,图2-g)。
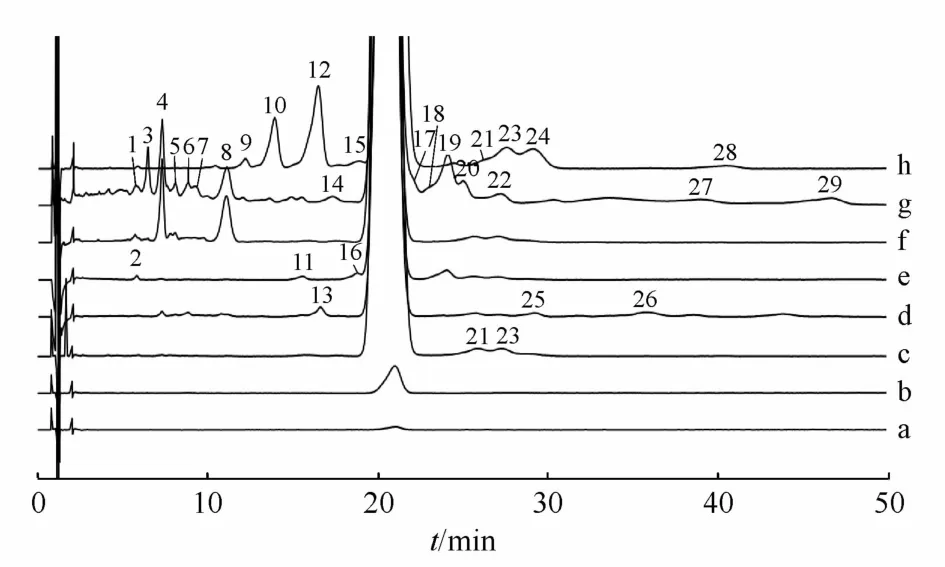
Figure2 HPLC-UV chromatograms of cyclosporin A(a.Reference solution of0.1%;b.Reference solution of1.0%;c.API)and its stressed solutions(d.Acid;e.Alkaline;f.Oxidation;g.Thermal;h.Crude)
3.2 有关物质的结构鉴定
采用LC-TOF/MS测得各有关物质母离子的准确质量和离子组成,三重四极质谱测得它们的二级质谱特征碎片,并通过与环孢素A和环孢素U的质谱特征的对比分析,鉴定各主要有关物质的结构。结果见表1和图3。
3.2.1 环孢素质谱裂解规律 通过对环孢素A对照品及色谱分离度对照品中环孢素A、环孢素U进行一级质谱母离子准确质量(图4)、二级质谱特征碎片离子进行分析,总结出环孢素母核一般裂解规律(图5~图7),从而辅助未知有关物质结构的推断。

Table 1 Related substances of cyclosporin A identified by LC-MS
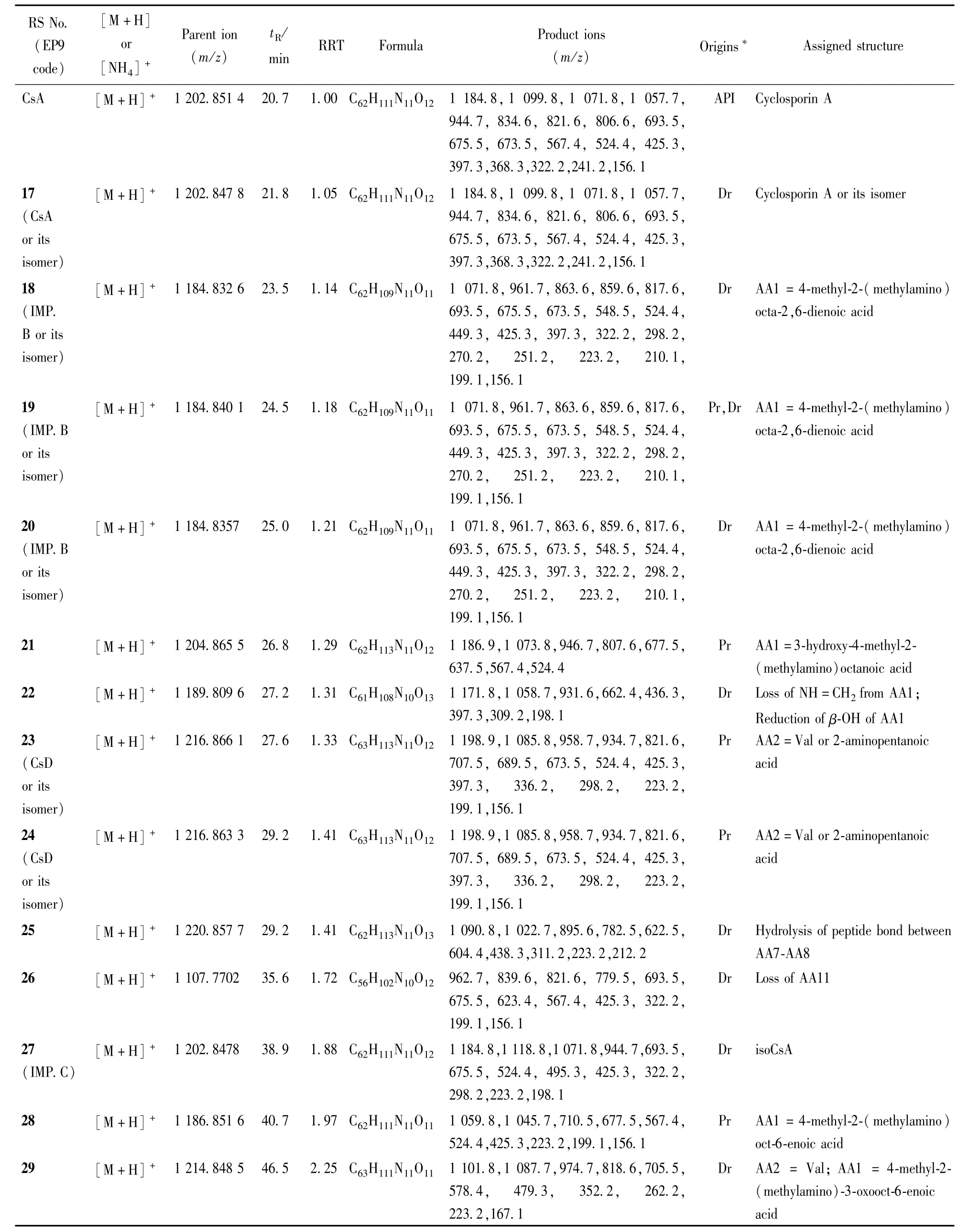
(Continued)
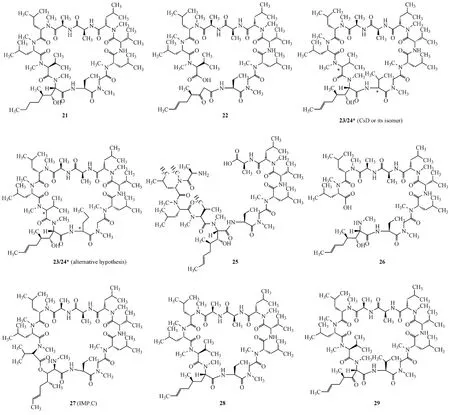
Figure 3 Chemical structures of the related substances(RSs1 29)of CsA
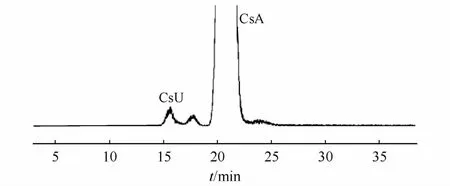
Figure 4 ESI-MSTIC chromatogram obtained from cyclosporine A resolution mixture(2.5 mg/mL)
环孢素A ESI+-TOF/MS测得环孢素A的[M+H]+准确质量为 1 202.851 4,与离子式C62H112N11O12+相应,相对分子质量为1 202.6。测得[M+H]+的ESI+-MS/MS主要特征碎片离子m/z1 184.8、1 099.8、1 071.8、1 057.7、944.7、834.6、821.6、806.6、693.5、675.5等。m/z1184.8与母离子脱水生成的[P-H2O]+特征碎片离子相应;m/z834.6、821.6和806.6由母离子b/Y裂解丢失AA5(Val)+AA6(MeLeu)+AA7(Ala)+AA8(D-Ala)、AA2(Abu)+AA3(MeGly)+AA4(MeLeu)+AA5(Val)和AA7(Ala)+AA8(D-Ala)+AA9(MeLeu)+AA10(MeLeu)产生;m/z637.5由m/z821.6离子b/Y裂解丢失 AA1产生;m/z1 099.8、1 071.8、944.7、693.5、675.5和 567.4分别由m/z1 184.8离子 b/Y裂解丢失 AA2(Abu)、AA11(MeVal)、AA10(MeLeu)+AA11(MeVal)、AA1+AA2(Abu)+AA10(MeLeu)+AA11(MeVal)、AA2(Abu)+AA3(MeGly)+AA4(MeLeu)+AA5(Val)+AA6(MeLeu)和 AA1+AA2(Abu)+AA9(MeLeu)+AA10(MeLeu)+AA11(MeVal)产生。环孢素 A的二级质谱图及推断裂解途径分别见图5。

Figure5 MS/MSspectrum of[M+H]+ion and fragmentation pathways of CsA(m/z1 202.8)
环孢素U ESI+-TOF/MS测得环孢素U的[M+H]+准确质量为 1 188.831 8,与离子式C61H110N11O12+相应,相对分子质量为1 188.6。测得[M+H]+的 ESI+-MS/MS主要特征碎片离子m/z1 170.8、1 157.7、1 085.8、1 057.7、930.6、679.5、675.4、661.5、383.3等。环孢素 U的裂解规律与环孢素A相似,m/z1 170.8与母离子脱水形成的碎片离子相应;m/z679.5由母离子b/Y裂解丢失 AA7(Ala)+AA8(D-Ala)+AA9(MeLeu)+AA10(MeLeu)+AA11(MeVal)产生;m/z661.5为m/z679.5离子脱水生成的质量数为[M-18]+的特征碎片离子;m/z1 086.7、1 057.7和675.4分别由m/z1 170.8离子 b/Y裂解丢失 AA2(Abu)、AA11(MeVal)和 AA2(Abu)+AA3(MeGly)+AA4(MeLeu)+AA5(Val)+AA6(MeLeu)产生。环孢素U的二级质谱图及推断裂解途径分别见图6。

Figure 6 MS/MS spectrum of[M+H]+ion and fragmentation pathways of CsU(m/z1 188.8)
环孢素母核裂解规律如下:(1)键开裂的方式主要有 a/X、b/Y、c/Z 3种,由于所使用碰撞能较大,3种开裂产物均可能出现,氨基酸残基上化学键也可能发生断裂,因此环孢素A及其有关物质的质谱图较为复杂。(2)环孢素A及其有关物质在AA1残基β-OH易脱水生成质量数为[M-18]+碎片离子。(3)环孢素 A较易在 AA1-AA2、AA5-AA6、AA8-AA9、AA9-AA10和 AA11-AA1间肽键发生b/Y型断裂。(4)环孢素A、环孢素U及其他有关物质的二级质谱大多产生相同质荷比的小于m/z650的碎片离子。根据肽类化合物氨基酸残基裂解规律,推断它们均为相同结构(图7),提示这些有关物质与环孢素A有大致相同的氨基酸组成及多肽片段。但是,由于不同有关物质中价键能量的差异、二级质谱测定时碰撞电压的不同,可能会使这些碎片离子峰簇的相对丰度此消彼长[15]。此类碎片离子只宜用于验证结构推断的正确性,而不能作为判定氨基酸序列的决定性依据。
3.2.2 有关物质的结构鉴定 ESI-MS总离子流色谱图中,主成分及各有关物质均产生[M+H]+、[M+NH4]+、[M+Na]+单电荷分子离子峰,及[M+H+NH4]2+、[M+H+Na]2+等双电荷峰(图8)。本研究中,ESI-MS/MS均选择[M+H]+或[M+NH4]+作母离子,以便二级质谱解析。
测得各有关物质母离子的准确质量和离子组成(表1),及它们的二级质谱特征碎片(图9),并通过与环孢素A和环孢素U的质谱特征的对比分析,鉴定各主要有关物质的结构(表1,图3)。
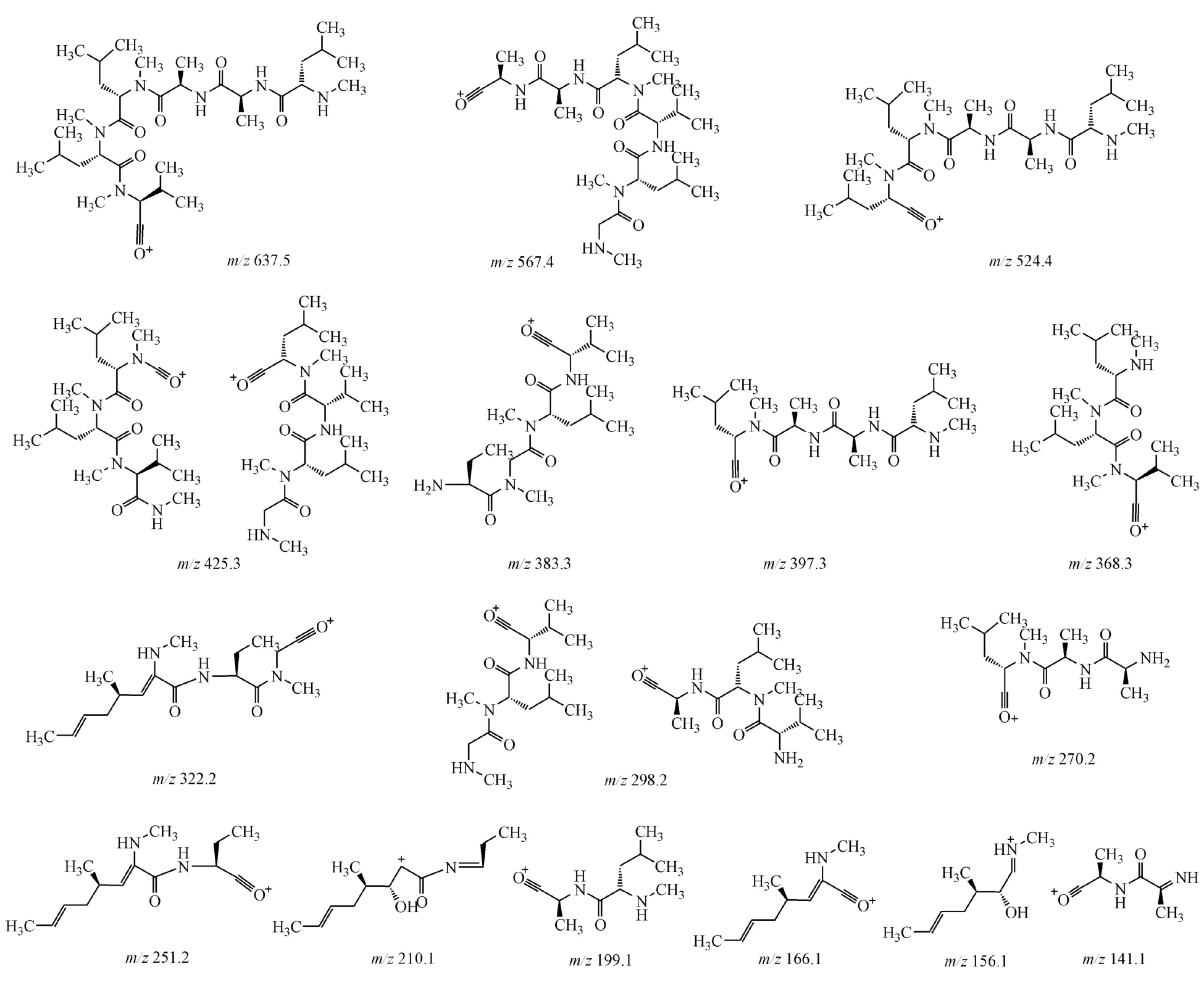
Figure 7 MS/MS common fragments(m/z<650)of CsA and its typical RSs
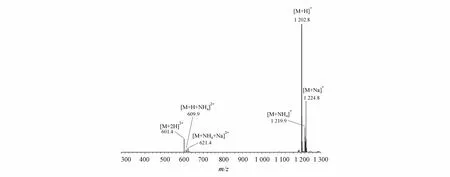
Figure 8 ESI-MS full scan spectrum of CsA
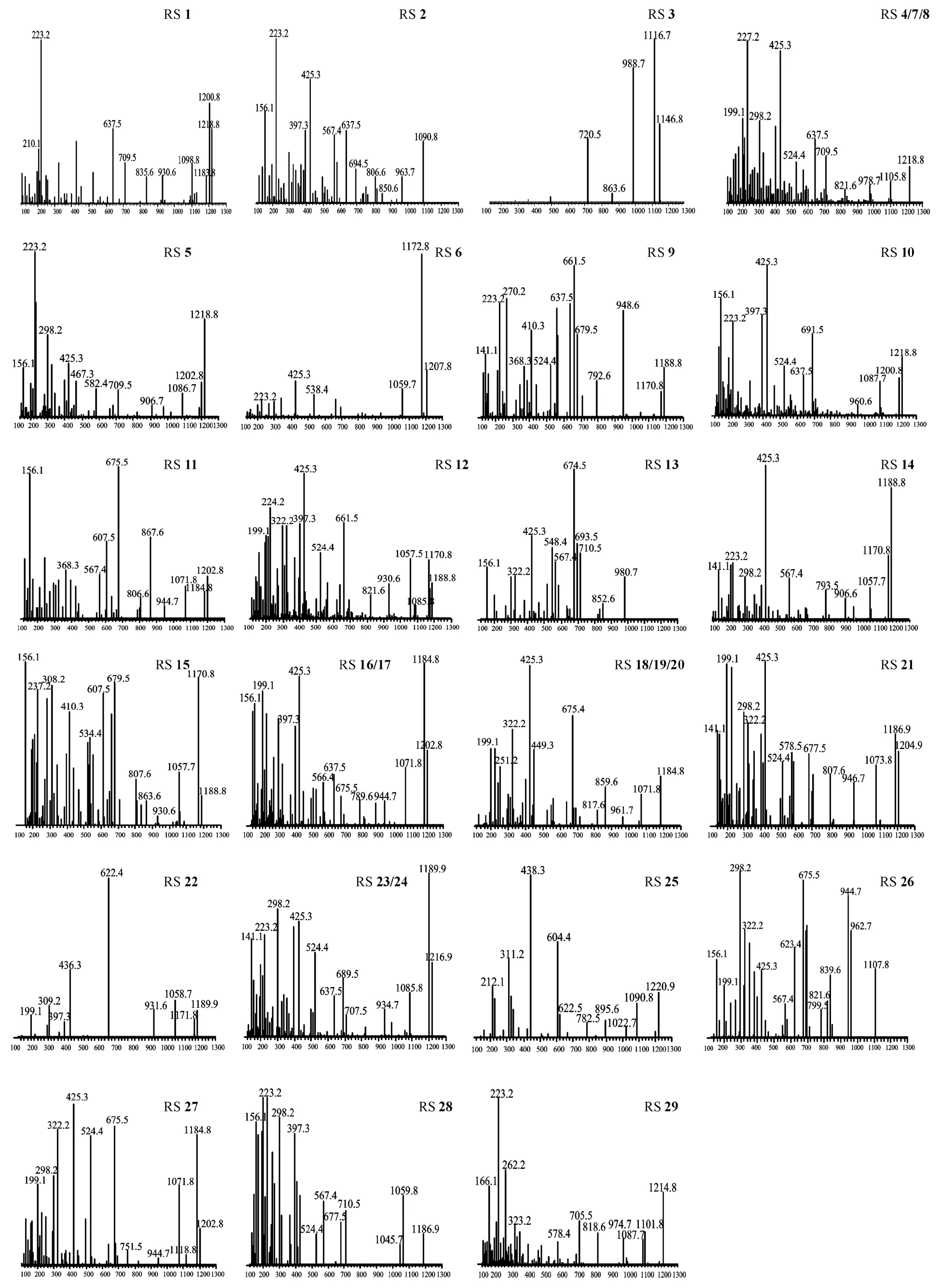
Figure 9 MS/MS spectra of typical RSs of CsA
通过有关物质HPLC保留时间及质谱定性,确证有关物质12与色谱分离度对照品中环孢素U对应。检测出的29个有关物质均与环孢素A有相似母核,根据结构将其大致分为以下几类:
(1)环孢素家族及其立体异构体
有关物质9、10、12、14和15的结构分别与环孢素L、环孢素C、环孢素U、环孢素T和环孢素B相应;16和17与环孢素A/H及其光学异构体相应;27与异环孢素A相应;23和24与环孢素D及其光学异构体相应。
有关物质9 质量数比环孢素A少14,元素组成少 CH2。特征碎片离子m/z1 170.8、930.6、679.5和661.5均与环孢素Am/z1 184.8、944.7、693.5和675.5相差14。推断其甲基丢失在AA1的N上,与欧洲药典收载的杂质环孢素L相应,为发酵工艺中产生。
有关物质10 质量数比环孢素A多16,元素组成多一个 O,与一个羟基相应。m/z1 200.8、1 087.7、960.6和 691.5均与环孢素 Am/z1 184.8、1 071.8、944.7和675.5相差16。确证其羟基带在AA2上,为苏氨酸(Thr)。该杂质与欧洲药典收载的环孢素C结构相应,为发酵工艺中产生,含量较大。
有关物质12 其保留时间、准确质量、元素组成及特征碎片离子均与已知杂质环孢素U的基本相同。确证有关物质12即为环孢素U。
有关物质14 质量数比环孢素A少14,元素组成少CH2。特征碎片离子m/z1 170.8、1 057.7和679.5与环孢素 Am/z1 184.8、1 071.8和693.5相差14,其甲基丢失在AA10的N上。推断为环孢素A在高温条件下,失去AA10上N-甲基产生,与欧洲药典收载的杂质环孢素T相应。
有关物质15 质量数比环孢素A少14,元素组成少CH2。特征碎片离子m/z1 170.8、1 057.7、930.6、679.5、308.2和 237.2均比环孢素 Am/z1 184.8、1 071.8、944.7、693.5、323.2和 251.2小14;m/z862.6和806.6也为环孢素A碎片。推断甲基丢失在AA1或AA2上,当其AA2为少一个甲基的丙氨酸(Ala)时,与欧洲药典收载的杂质环孢素B相应,为发酵工艺中产生。
有关物质16/17 为环孢素A在碱性或高温强制破坏条件下。质量数、主要特征碎片离子及裂解途径与环孢素A均相同,推断为环孢素A母核碳原子发生构型反转产生的差向异构体。当AA11为D-甲基缬氨酸(D-MeVal)时与欧洲药典收载的杂质环孢素H相应。
有关物质23/24 质量数比环孢素A大14,元素组成多 CH2。主要特征碎片离子m/z933.7、821.6、637.5等与环孢素A特征碎片离子相同;m/z1 198.9、1 085.8、958.7、707.5和 336.2比环孢素 Am/z1 184.8、1 086.7、944.6、693.5和322.2多14,推断AA2残基多一个甲基,为缬氨酸(Val)或2-氨基丁酸(Abu),但可能存在构型翻转,故有不同保留。其中当AA2为L-缬氨酸(L-Val)时,为欧洲药典收载的杂质环孢素D。均为发酵工艺中产生。
有关物质27 为环孢素A的同分异构体,其保留较强,极性较小。而环孢素AA1残基上β-OH是其极性的重要影响因素,根据其主要特征碎片离子推测,其为环孢素A在高温条件下AA1上β-OH与AA1-AA11间酰胺键羰基发生亲核置换,缩合成酯产生。m/z1 184.8与母离子AA11-AA1间酯键水解后脱水形成的特征碎片离子相应;m/z1 118.8为母离子AA1残基脱去一分子C6H12形成;m/z751.5为母离子裂解失去AA9(MeLeu)+AA10(MeLeu)+AA11(MeVal)形成。推断其结构与欧洲药典收录的杂质C相同,为异环孢素A。其产生过程如图11所示。
(2)肽键水解或丢失部分氨基酸
有关物质1为环孢素A在高温条件AA1-AA11间肽键水解产生;有关物质13、25和26均由环孢素A在酸性条件下水解后丢失部分氨基酸片段产生。
有关物质1 质量数比环孢素A大16,元素组成多O,保留很弱,极性较大。m/z1 200.8比母离子m/z1 218.8小18,与母离子脱水相应,推测为环孢素A环状结构开环水解含有游离羧基产物。m/z835.6为母离子脱去一分子HCOOH和AA1+AA2(Abu)+AA3(MeGly)产生;m/z710.6为m/z835.6 b/Y裂解丢失 AA4(MeLeu)产生。推断该杂质为环孢素A在高温条件下,AA1-AA11间肽键水解产生。
有关物质13 质量数比环孢素A少222,不饱和度减少3,其保留较弱,极性较大。碎片离子中m/z674.5、567.4、548.4、425.3、322.2、297.2、198.1、156.1等也为环孢素A的特征碎片离子,故杂质AA1~8与环孢素A相同;m/z710.5比环孢素Am/z693.5大17,与一个羟基相符,故其AA9存在游离羧基。推断为环孢素A在强酸条件下水解,脱去AA10和AA11产生。
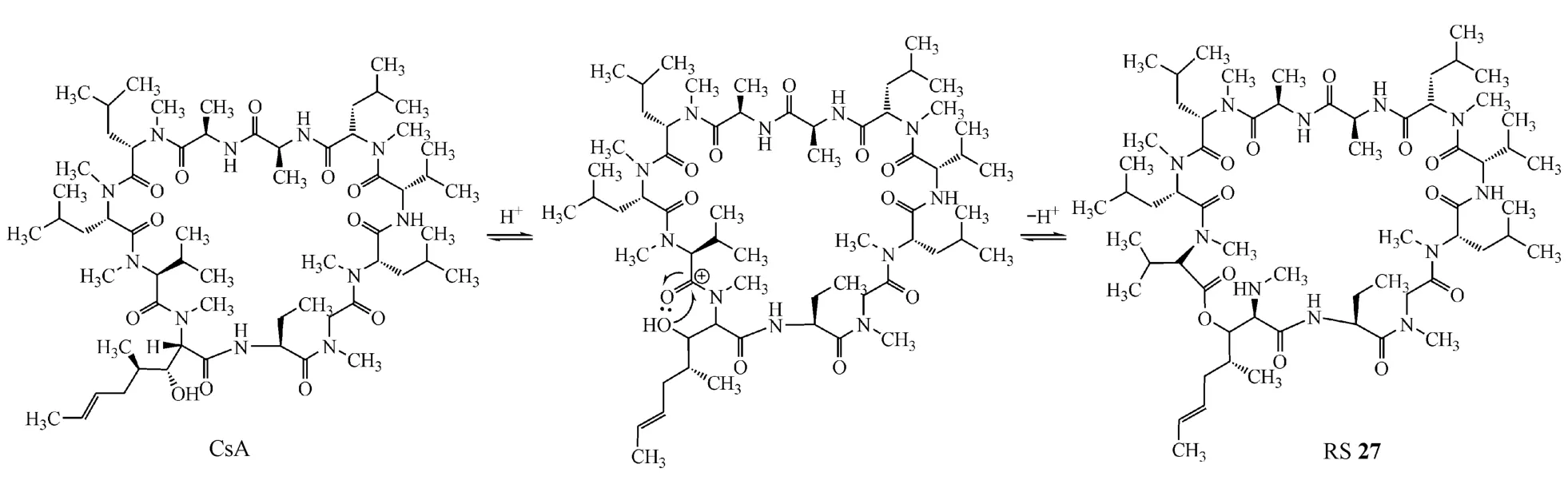
Figure 10 Formation reaction of RS 27
有关物质25 质量数比环孢素A大18,元素组成多H2O,不饱和度减1。特征碎片离子m/z1 022.7、895.6和782.5表明AA7存在游离羧基。推断为环孢素A在强酸条件下,AA7-AA8间肽键水解形成。
有关物质26 质量数比环孢素A少95。主要特征碎片离子中m/z962.7、944.7、821.6、779.5、675.5、566.3等与环孢素 A相同;m/z839.6比环孢素Am/z821.6多18,证明 AA10存在游离羧基。推断为环孢素A在强酸条件下水解,脱去AA11产生。
(3)N-去甲基化
有关物质9、12和14质量数比环孢素 A少14,元素组成少CH2,不饱和度不变。在粗品中存在,或在高温条件下产生,均由环孢素A在氨基酸N位发生去甲基化产生。
(4)侧链修饰
有关物质2 质量数比环孢素A少了112,不饱和度减1。特征碎片离子m/z963.7、850.6和581.4均比环孢素A特征碎片m/z1 157.7、944.7和675.5少94,与AA1残基脱水后相对分子质量相应。推断为环孢素A在碱性条件下AA1-α碳原子上残基全部脱去产生。
有关物质3 质量数比环孢素A少56。推测AA1为2-氨基-3-酮戊酸。m/z1 116.7为母离子AA1残基上脱去一分子C2H6产生。由于环孢素AA1-β-OH的存在,高温条件下γ碳发生断裂,丢失一个丁烯,羟基氧化成羰基形成该杂质。
有关物质4/7/8 其分子式及主要特征碎片离子相同,质量数均比环孢素A多16,元素组成多O,不饱和度不变。m/z1 200.8比环孢素A特征碎片m/z1 184.8多 16,与一个羟基相应;m/z1 105.8和978.7均比环孢素 Am/z1 071.8和944.7多34,与两个羟基相应。为环孢素A在高温或者强氧化条件下,AA1残基烯键被氧化成ε-羰基产生(在此过程中母核易发生构型翻转,因此有多种立体结构)。m/z1 188.8为母离子AA1残基上开裂脱去一分子C2H6产生,进一步确证结构中羰基的位置。推断有关物质4、7和8为环孢素A在氧化或高温条件下产生。
有关物质5 质量数均比环孢素A多16,元素组成多O,不饱和度不变。m/z709.5和582.4均比环孢素Am/z675.5和566.4多16,与一个羟基相应,其AA1残基与有关物质4/7/8有相同的羰基结构;m/z1 174.8为母离子AA1残基丢失一分子CH2=CHOH产生。推断其羰基位置在ζ位,为环孢素A在高温条件下产生。
有关物质18/19/20 质量数均比环孢素A小18,元素组成少H2O,与脱一分子水对应。其中,有关物质19在粗品中存在,在高温和强碱强制降解溶液中显著增加。3个杂质主要特征碎片离子基本相同,也都是环孢素A的特征碎片离子,推断均为环孢素A上AA1-β-OH脱去一分子水成烯键形成。在此过程中母核可能发生构型反转,因此有多种立体结构,但三者的具体构型无法确证。当其碳原子构型与环孢素A完全相同时,为欧洲药典收载的杂质B
有关物质21 质量数比环孢素A大2,元素组成多2H,不饱和度减1。其主要特征碎片离子m/z1 186.9、1 073.8、946.7和 677.5均比环孢素 Am/z1 184.8、1 071.8、944.7和 675.5大 2,m/z567.4、524.4等碎片离子与环孢素 A相同,证明AA1残基上双键还原。在环孢素粗A品及原料药中均存在,为发酵工艺中产生。
有关物质28 质量数比环孢素A小16,与一个O对应,不饱和度不变。其保留比环孢素A强很多,极性较弱。主要特征碎片离子中没有母离子脱水生成的[P-H2O]+离子,说明结构中无游离羟基。推断其AA1为2-氨基-4-甲基-6-烯辛酸,在发酵工艺中产生。
有关物质29 质量数比环孢素A多12,不饱和度减少1,保留较强,极性很弱。主要特征碎片离子m/z1 101.8、974.7、818.6、705.5、578.4和479.3比环孢素 Am/z1 089.8、963.5、806.6、693.5、567.4和 467.3均大12,m/z352.2比环孢素Am/z322.2大30。推断AA2残基比环孢素A多一个甲基,且AA1-β-OH氧化成羰基。为高温条件下产生降解杂质。
(5)缩酮反应
有关物质11 缩醛(酮)具有类似于醚的结构,在碱性介质中化学稳定性很好[16]。根据特征碎片离子,推断为碱性强制破坏条件下,环孢素A肽键上羰基可与AA1支链上羟基发生半缩酮反应,产生有关物质11。其产生过程如图12所示。

Figure 12 Formation reaction of RS 11
(6)其 他
有关物质6 质量数比环孢素A多5,不饱和度减1。推断为环孢素A在高温条件下,AA2-β碳氧化带上羟基,同时AA5-AA6间肽键水解并失去一分子NH==CH2产生。
有关物质22 质量数比环孢素A小13,不饱和度不变,保留较强。根据分子式,其结构比环孢素A少一个C和一个N,多一个O,其主要特征碎片离子m/z1 171.8为母离子丢失一个羟基形成;m/z1 058.7正好为m/z1 171.8失去一个甲基缬氨酸(MeLeu)形成;m/z662.4比环孢素 A的m/z693.5少31,与脱去一分子NH==CH2同时出现双键相符。推断有关物质22为环孢素A高温条件下脱去第1位氨基酸上NH==CH2,且羟基被氧化成羰基形成。
4 结 论
本研究建立了能有效检测和分离环孢素A发酵过程及其强制降解产生29个有关物质的挥发性流动相LC-MS方法,并对这些有关物质进行了结构推测,对发酵工艺质量控制、评估药物内在稳定性及制定存储条件具有一定意义。
检测出的有关物质根据来源可分为发酵工艺杂质和降解杂质,其产生途径见图13。环孢素A在发酵工艺过程中产生了9个有关物质(有关物质9、10、12、15、19、21、23、24和 28);原料药中两个有关物质(有关物质21和23),含量均未超过药典规定限度。
强制降解实验表明,环孢素A在强酸条件下易发生肽键的水解反应,丢失部分氨基酸片段生成链状多肽(有关物质13、25和26);在强碱条件下,环孢素A可脱去残基,肽键可与邻近残基上羟基发生缩酮反应,或降解成保留极弱的氨基酸片段(有关物质2、11、16和19);在氧化和高温条件下,环孢素A易发生N-脱甲基、残基脱羟基等反应(有关物质 1、3、4、5、6、7、8、14、17、18、19、20、22、27和29);环孢素A对光较为稳定,强光照射几乎没有新的杂质产生。故环孢素需于密封干燥处储存。
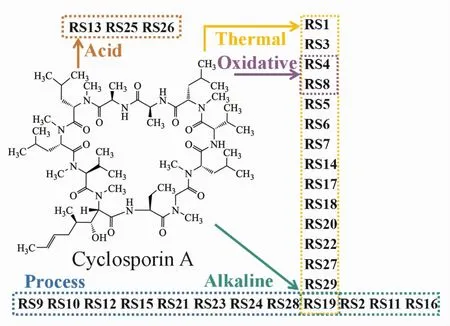
Figure13 Generation of themain RSs of CsA
