淫羊藿苷在不同条件下的降解动力学行为
2019-08-26陶俊烨丁选胜吴正红丁雨寅宋征宇
陶俊烨, 丁选胜*, 吴正红, 丁雨寅, 宋征宇, 王 勤
(1. 中国药科大学基础医学与临床药学学院, 江苏 南京211100; 2. 中国药科大学药学院, 江苏 南京211100)
淫羊藿苷是从淫羊藿干燥叶中提取出的有效成分之一, 具有促进骨代谢[1]、 增强生殖功能[2-3]等多种药理作用, 近年来该成分对心血管疾病的改善作用逐渐被人们所重视[4], 同时它对糖尿病及其并发症也有一定疗效[5]。 但淫羊藿苷在水中的溶解性较低[6], 故在一定程度上限制了相关新药的开发。
目前, 已有关于淫羊藿苷稳定性和溶解度的报道[6-7], 但对其降解动力学的研究还比较少。由于人体胃肠道中具有不同的pH 和化学环境[8],本实验将探究淫羊藿苷在不同pH 缓冲液中的稳定性, 以及在不同pH、 温度、 缓冲液中的降解动力学行为, 以期为该成分进一步开发应用提供参考。
1 材料
SPD20-A 高效液相色谱仪(配置LC-20AT 溶剂输送泵、 UV-VIS 检测器、 Rheodyne 7725i 手动进样阀、 LC Solution 工作站, 日本岛津公司);RPL-D2000 柱温箱(大连日普利科技仪器有限公司); PHS-3C 雷磁PH 计(上海仪电科学仪器股份有限公司); CPA225D 电子天平[赛多利斯科学仪器(北京) 有限公司]; ZYC-200B 恒温摇床(上海溪乾仪器设备有限公司); 80-2 电动离心机(常州国宇仪器制造有限公司); DF-101SA-H 集热式恒温加热磁力搅拌器(南京科尔仪器设备有限公司); 超声波清洗机 (上海比朗仪器制造有限公司)。
淫羊藿苷原料药(陕西锦泰生物工程有限公司, 批号JT171010, 含有量>98%); 淫羊藿苷对照品(中国食品药品检定研究院, 批号110737-201516, 含有量94.2%)。 盐酸(南京化学试剂股份有限公司, 批号170320098H, 含有量36% ~38%); 氢氧化钠(西陇化工股份有限公司, 批号1112021); 十二水合磷酸氢二钠(西陇科学股份有限公司, 批号171221); 磷酸二氢钠 (批号030210109)、 一水合枸橼酸(批号150505182K)、三水合枸橼酸三钠 (批号160306063U)、 乙酸(批号171012355F) (南京化工试剂股份有限公司;无水乙酸钠(国药集团化学试剂有限公司, 批号20170301); 甲醇(批号21171001)、 乙腈(批号011370501) 为色谱纯(上海星可高纯溶剂有限公司)。
2 方法与结果
2.1 淫羊藿苷含有量测定
2.1.1 色谱条件 Hedera ODS-2 色谱柱(250 mm×4.6 mm, 5 μm); 流动相乙腈-水(3.4 ∶6.6); 检测波长270 nm; 体积流量1.0 mL/min; 柱温30 ℃; 进样量20 μL。
2.1.2 溶液制备 精密称取淫羊藿苷对照品20 mg于小烧杯中, 少量甲醇溶解后移入100 mL 量瓶中,甲醇定容至0.2 mg/mL, 即得对照品溶液。 精密称取淫羊藿苷原料药20 mg, 甲醇制成每1 mL 含0.4 mg该成分的溶液, 即得供试品溶液。
2.1.3 线性关系考察 按照2015 年版《中国药典》[9]方法, 精密量取对照品贮备液2.5、 5.0、10.0、 20.0 mL, 置于50 mL 量瓶中, 流动相稀释并定容, 摇匀, 得10、 20、 40、 80 μg/mL 对照品溶液, 将10 μg/mL 溶液分别稀释2、 4 倍, 得到2.5、 5 μg/mL, 0.45 μm 有机系滤头过滤, 取中间段续滤液, 在“2.1.1” 项色谱条件下进样20 μL测定, 每个质量浓度进行3 次。 以溶液质量浓度为横坐标(X), 峰面积为纵坐标(Y) 进行回归,得方程为Y=51 919X+49 687 (r=0.999 8), 在2.5~80 μg/mL 范围内线性关系良好。
2.1.4 专属性考察 取流动相、 供试品溶液、 对照品溶液, 在“2.1.1” 项色谱条件下进样20 μL测定, 再取配制好的400 μL 母液, 稀释1 倍后加入人工肠液和大鼠回肠液以加速其降解, 在选定时间取20 μL, 在“2.1.1” 项色谱条件下进样测定,结果见图1。 由图可知, 淫羊藿苷峰型良好, 溶剂峰不产生干扰, 降解产物无干扰[10]。

图1 淫羊藿苷HPLC 色谱图Fig.1 HPLC chromatograms of icariin
2.1.5 精密度试验 取对照品溶液, 在“2.1.1”项色谱条件下进样测定6 次, 测得淫羊藿苷峰面积RSD 为0.6%, 表明仪器精密度良好。
2.1.6 加样回收率试验 精密称取对照品1.6、2.0、 2.4 mg, 置于10 mL 量瓶中, 甲醇溶解并稀释至刻度, 量取5 mL 至50 mL 量瓶中, 流动相稀释至20、 40、 80 μg/mL, 在“2.1.1” 项色谱条件下进样测定3 次, 测得淫羊藿苷平均加样回收率为99.86%, RSD 为1.59%。
2.1.7 检测限考察 对照品溶液用流动相逐步稀释, 在“2.1.1” 项色谱条件下进样测定, 以峰高接近基线噪音3 倍时的质量浓度为检测限, 测得其为1.25 μg/mL。
2.1.8 缓冲液配制[10-12]
2.1.8.1 磷酸盐缓冲液(调节pH 用) 磷酸二氢钠溶液: 精密称取磷酸二氢钠24.00 g, 加水溶解后置于1 000 mL 量瓶中, 定容至刻度, 即得(0.2 mol/L)。
磷酸氢二钠溶液, 精密称取十二水合磷酸氢二钠71.63 g, 加水溶解后置于1 000 mL 量瓶中, 定容至刻度, 即得(0.2 mol/L)。
然后, 将2 种溶液按照一定比例混合, 再用盐酸和氢氧化钠溶液调节pH (微量, 几乎不影响体积), 即得(0.2 mol/L)。
2.1.8.2 磷酸盐缓冲液(测定动力学参数用)磷酸二氢钠溶液, 精密称取磷酸二氢钠1.2、 3.6、6.0 g, 加水溶解后置于100 mL 量瓶中, 定容至刻度, 即得(0.1、 0.3、 0.5 mol/L)。
磷酸氢二钠溶液, 精密称取十二水合磷酸氢二钠3.58、 10.74、 17.91 g, 加 水 溶 解 后 置 于100 mL量瓶中, 定容至刻度, 即得 (0.1、 0.3、0.5 mol/L)。
然后, 将2 种溶液按照一定比例混合, 氢氧化钠或盐酸调pH, 即得(0.1、 0.3、 0.5 mol/L)。
2.1.8.3 醋酸盐缓冲液 醋酸钠溶液, 精密称取醋酸钠0.82、 2.46、 4.10 g, 加水溶解后置于100 mL量瓶中, 定容至刻度, 即得 (0.1、 0.3、0.5 mol/L)。
醋酸溶液, 精密量取冰醋酸0.57、 1.7、2.85 mL, 加水溶解后置于100 mL 量瓶中, 定容至刻度, 即得(0.1、 0.3、 0.5 mol/L)。
然后, 将2 种溶液按照一定比例混合, 氢氧化钠溶液调pH, 即得(0.1、 0.3、 0.5 mol/L)。
2.1.8.4 枸橼酸盐缓冲液 枸橼酸溶液, 精密称取一水合枸橼酸2.10、 6.30、 10.5 g, 加水溶解后置于100 mL 量瓶中, 定容至刻度, 即得 (0.1、0.3、 0.5 mol/L)。
枸橼酸钠溶液, 精密称取三水合枸橼酸钠3.12、 9.36、 15.6 g, 加水溶解后置于100 mL 量瓶中, 定容至刻度, 即得(0.1、 0.3、 0.5 mol/L)。
然后, 将2 种溶液按照一定比例混合, 氢氧化钠或盐酸调pH, 即得(0.1、 0.3、 0.5 mol/L)。
2.2 淫羊藿苷稳定性研究 取淫羊藿苷适量, 甲醇溶解并定容至刻度, 制成每1 mL 含400 μg 该成分的溶液, 精密量取8 份, 每份1 mL, 置于10 mL量瓶中, 0.2 mol/L 磷酸盐缓冲液稀释至刻度, 调pH 为1、 2、 3、 4、 5、 6、 7、 8, 摇匀, 避光, 在25 ℃下放置。 然后, 于第0、 2、 4、 6、 8、 12、24 h 取样, 在“2.1.1” 项色谱条件下进样测定,计算保留率, 公式为保留率=Ct/C0×100%, 其中Ct为淫羊藿苷处理后质量浓度, C0为淫羊藿苷初始质量浓度。 结果见图2。
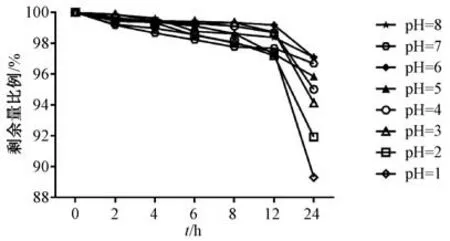
图2 淫羊藿苷保留率Fig.2 Retention rates of icariin
由图可知, 12 h 内淫羊藿苷在pH 1 ~8 磷酸盐缓冲液中的稳定性相对良好, 保留率都在97% 以上, 并随着pH 增大呈逐渐上升的趋势; 24 h 后,淫羊藿苷保留率均有所下降, 在酸性条件下更明显。
2.3 淫羊藿苷降解动力学研究
2.3.1 pH 值 取淫羊藿适量, 甲醇溶解并定容至刻度, 制成每1 mL 含400 μg 该成分的溶液, 精密量取1 mL 至10 mL 量瓶中, 0.2 mol/L 磷酸盐缓冲液稀释至刻度, 调pH 为1、 3、 4.5、 6、 6.8、 7、8 (由于胃肠道中pH 不同, 故选取几个与人体胃肠道中不同部位pH 相似的点), 摇匀, 分装于6 mL 西 林 瓶 中, 密 封, 于0、 6、 12、 36、 60、72 h取样。 然后, 以降解一定时间后淫羊藿苷剩余浓度对数(lnC) 对时间(t) 作图, 再按反应动力学方法计算反应级数及表观降解速率常数(K),结果见图3、 表1。
由图3 可知, 降解曲线具有线性, 基本符合一级动力学降解过程(R2>0.860 0); 由图3、 表1可知, 淫羊藿苷在pH 6.8 时降解速率最小, 稳定性最强。

图3 淫羊藿苷在不同pH 下的降解曲线Fig.3 Degradation curves for icariin under different pH values
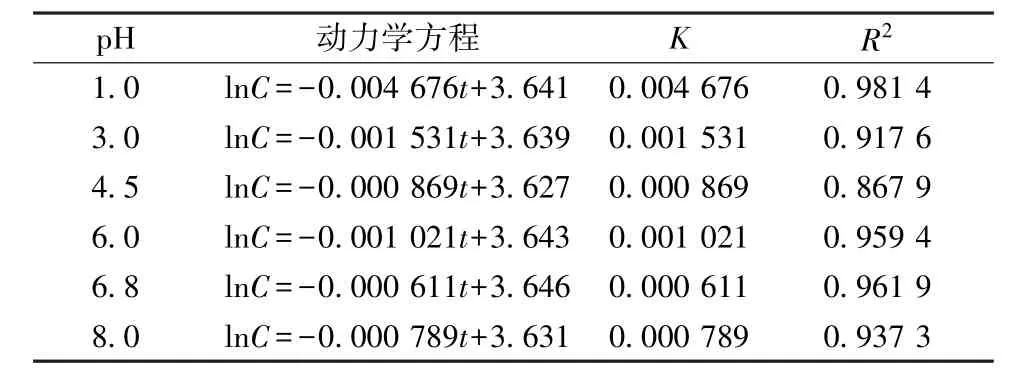
表1 淫羊藿苷在不同pH 下的动力学参数Tab.1 Kinetic parameters for icariin under different pH values
2.3.2 温度 取淫羊藿苷适量, 甲醇溶解并定容至刻度, 制成每1 mL 含400 μg 该成分的溶液, 精密量取1 mL至10 mL 量瓶中, 0.2 mol/L 磷酸盐缓冲液定容至刻度, 调节pH 为6.8, 密封, 在4、25、 37、 60 ℃恒温 水 浴 中 加 热, 于0、 12、 24、36、 48、 60 h取样。 然后, 将峰面积代入标准曲线计算质量浓度, 以某温度降解一定时间后淫羊藿苷剩余浓度对数(lnC) 对时间(t) 作图, 结果见图4、 表2。
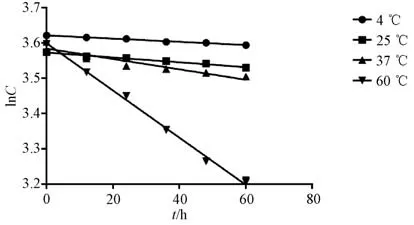
图4 淫羊藿苷在不同温度下的降解曲线Fig.4 Degradation curves for icariin under different temperatures
由此可知, pH 为6.8 时, 淫羊藿苷在不同温度下的降解均为一级反应, 而且温度越高, 降解速率越快。
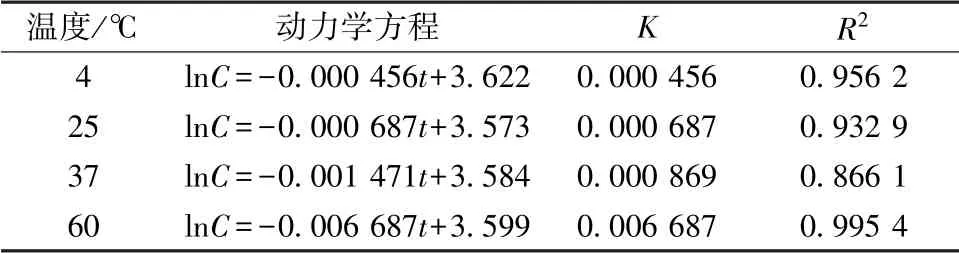
表2 淫羊藿苷在不同温度下的动力学参数Tab.2 Kinetic parameters for icariin under different temperatures
2.3.3 缓冲液 精密称取淫羊藿苷适量, 甲醇溶解并定容至刻度, 制成每1 mL 含400 μg 该成分的溶液, 精密量取1 mL 至10 mL 量瓶中, 0.1、 0.3、0.5 mol/L 磷酸盐、 柠檬酸盐、 醋酸盐缓冲液定容至刻度, 调pH 为6.8, 摇匀, 分装入6 mL 西林瓶中, 密封。 然后, 将峰面积带入标准曲线计算质量浓度, 以降解一定时间后淫羊藿苷的剩余浓度对数(lnC) 对时间(t) 作图, 再将缓冲降解所对应的K 值绘图, 结果见图5~6、 表3。
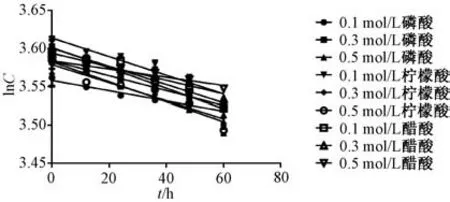
图5 淫羊藿苷在不同缓冲液中的降解曲线Fig.5 Degradation curves for icariin in different buffers

图6 不同缓冲液对淫羊藿苷降解速率的影响Fig.6 Effects of different buffers on the degradation rate of icariin

表3 淫羊藿苷在不同缓冲液中的动力学参数Tab.3 Kinetic parameters for icariin in different buffers
由图5、 表3 可知, 淫羊藿苷在不同缓冲液中的降解行为均为一级动力学, 而且速率不同; 由图6 可知, 淫羊藿苷的降解速率在磷酸盐缓冲液中随着盐浓度升高而升高, 在柠檬酸盐缓冲液中无明显变化, 在醋酸盐缓冲液中随着盐浓度升高而下降。
3 讨论
大多数单体成分在贮存过程中可能会受到环境因素的影响而发生降解, 其动力学行为基本符合零级或一级模型[13]。 淫羊藿苷属于中药单体成分,其降解动力学研究结果表明, 它在不同pH 下的降解曲线呈线性, R 在0.9 以上[14-15](≥0.81), 即符合一级动力学特征; 在酸性环境下, 该成分降解速率大于弱酸性、 中性条件下, 在pH 6.8 时最小,即此时稳定性最强; 随着温度上升, 该成分降解速率增大, 在人体体温(37 ℃) 下其降解速率K 值是室温下的2 倍。 本实验选用了3 种常见缓冲液,每种3 个浓度, 发现在25 ℃、 pH 6.8 时, 磷酸盐缓冲液中淫羊藿苷降解速率与盐浓度呈正比, 柠檬酸盐缓冲液中无明显变化, 醋酸盐缓冲液中与盐浓度呈反比。
另外, 本实验虽然模拟了人体胃肠道的pH,但并无酶参与, 与内环境有一定差异, 这也是今后需要进一步研究的方向。
