胸部CT特征对克唑替尼治疗晚期非小细胞肺癌疗效及预后的预测价值*
2019-08-07王一棣王化韩丽珠韩颖马菊香叶兆祥
王一棣 王化 韩丽珠 韩颖 马菊香 叶兆祥
目前,肺癌是许多国家发生率及死亡率最高的恶性肿瘤,其中80%为非小细胞肺癌(non-small cell lung cancer,NSCLC),且确诊时多为晚期[1-2]。传统铂类为基础的化学治疗方法5年生存率较低。针对表皮生长因子受体(epidermal growth factor receptor,EGFR)基因突变的酪氨酸激酶抑制剂(tyrosine kinase inhibitors,TKIs)对NSCLC 的 治 疗 具 有 一 定 的 影响[3]。Soda 等[4]及Rikova 等[5]研究相继表明,肺腺癌细胞中EML4 基因与间变性淋巴瘤激酶(anaplastic lymphoma kinase,ALK)基因重排(EML4-ALK)可促进肿瘤的发生。ALK 重排在NSCLC 中发生率约2%~7%,多发生于较年轻、不吸烟或轻度吸烟者中[5-7]。克唑替尼(crizotinib)为一种小分子多靶点ATP 竞争性TKI,其整体客观缓解率(objective response rate,ORR)及中位无进展生存期(median progression-free survival,mPFS)均 明 显 优 于 化 疗 药物[7-10]。尽管克唑替尼有良好的治疗效果,仍有部分患者疗效或预后不佳。能够在治疗前对疗效或预后进行预测对临床治疗方案的选择尤为重要。目前,各类计算机成像相关技术应用广泛,其对组织结构的密度、间质的成份或肿瘤内部组织是否均匀等均有较好的显像效果。其中,CT检查由于便捷、无创等特点,在肿瘤的诊断、病情评估、治疗方案选择及疗效评价等方面具有重要的作用。许多研究表明影像特征与肿瘤的病理特征或基因表达息息相关[11-13]。然而,关于治疗前CT 特征与克唑替尼治疗疗效或预后的研究相对较少[14-15]。本研究对晚期NSCLC 常见胸部CT 特征进行分析,探究其在预测克唑替尼治疗晚期ALK 重排阳性NSCLC 患者的疗效及预后中的价值。
1 材料与方法
1.1 临床资料
分析天津医科大学肿瘤医院2014年1月至2017年3月门诊或住院的经病理证实为ALK 重排阳性47例NSCLC患者的临床及影像资料。所有患者均为Ⅲ~Ⅳ期未行手术治疗的NSCLC 患者,在接受克唑替尼治疗前4 周内均进行胸部CT 平扫检查。其中,男性20例(42.6%),女性27例(57.4%);年龄26~74岁,中位年龄49 岁;吸烟患者13 例(27.7%);Ⅲ期患者13 例(27.7%),Ⅳ期患者34 例(72.3%);10 例(21.3%)患者于治疗前发现脑转移;27 例(57.4%)患者接受过含铂方案化疗。
1.2 方法
1.2.1 胸部CT扫描 所有胸部CT检查采用下列3台CT机之一进行扫描:GE Healthcare Discovery CT750 HD、Light speed 16(美国,GE Healthcare 公司)、Siemens Somatom Definition AS(德国,Siemens公司)。扫描参数如下:1)GE Healthcare Discovery CT750 HD和GE Light speed 16 CT机:电压120 kVp,管电流150~200 mA(自动),螺距0.984:1,扫描旋转时间0.6 s/周,重建层厚及层距1.25 mm;2)Siemens Somatom Definition AS CT机:电压120 kVp,管电流自动,螺距1.375:1,扫描旋转时间0.6 s/周,重建层厚及层距1.25 mm。扫描范围为胸廓入口至膈平面。纵隔窗设置:窗宽320 HU,窗位35 HU;肺窗设置:窗宽1 200 HU,窗位-500 HU。所有图像均为胸部轴位平扫CT图像。
1.2.2 治疗、随访及疗效评价 患者口服克唑替尼250 mg,每日1 次至病情进展,或至因不良反应而停药。每1~3个月进行胸部CT检查,并定期复查腹部B 超/CT 及头颅CT/MRI。根据实体瘤疗效评价标准(RECIST)1.1[16]对治疗后效果进行随访评价,使用电话随访及电子病历系统对随访记录进行补充,根据随访资料评价患者最佳总体疗效,记录为完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病进展(progressive disease,PD)及疾病稳定(stable disease,SD),并将其分为缓解组(CR+PR)及未缓解组(SD+PD),随访终点为:1)疾病进展;2)失访,但随访时间已满12 个月;3)虽疾病未进展,但至2018年12月随访时间已达12 个月。无进展生存期(PFS)记为从服用药物开始至首次确认病情进展或患者死于疾病进展的时间。
1.2.3 胸部CT图像分析 从本研究影像归档和通信系统(picture archiving and communication system,PACS)内调取图像,由两名放射科医师分别对图像进行评价,当两名医师意见不一致时协商得出统一结论。对胸部CT特征评价主要包括以下内容:1)病灶大小:测量病灶最大截面的最长径,并分为≤3 cm和>3 cm组;2)病变位置:分为中心型及周围型组;3)肿瘤形态特征:包括有无毛刺征,有无分叶征,有无空泡/空洞征,有无钙化,有无空气支气管征,有无胸膜牵拉,有无胸膜附着;4)肿瘤周围血管征象:包括有无血管集束征,有无周围支气管血管束增粗;5)有无胸腔积液;6)有无心包积液;7)有无周围肺野实变;8)有无其它存在恶性可能的肺结节:按结节发生位置,分为无、原发病灶同侧肺叶结节、原发病灶对侧肺叶结节;9)有无癌性淋巴管炎。
1.3 统计学分析
采用SPSS 23.0 软件进行统计学分析。应用GraphPad Prism 7.0软件绘制生存曲线。各组之间率的比较采用χ2检验及Fisher精确检验,连续变量采用Mann-Whitney U检验进行分析。使用Kaplan-Meier法进行单因素生存分析并使用Log-rank 法进行显著性检验,Cox单因素比例风险回归模型对各因素的风险比(HR)进行计算;将单因素分析中具有统计学差异的特征纳入Cox 多因素比例风险回归模型进行分析。以P<0.05 为差异具有统计学意义。
2 结果
2.1 临床特征
截止至2018年12月,34 例患者进展,12 例至截止时间为PR 或SD,mPFS 为10 个月。缓解组30 例(PR 30例,66.7%),未缓解组15例(SD 7例,PD 8例,33.3%),无CR 患者,另外2 例患者(含2 例脑转移患者)最佳疗效不可评价。各临床特征在缓解组及未缓解组中差异均无统计学意义(P>0.05)(表1)。单因素生存分析结果显示,PFS与各临床特征之间无相关性(表2)。

表2 经克唑替尼治疗患者临床特征与预后的关系
2.2 胸部CT特征与疗效
单因素分析显示,各胸部CT 特征与疗效之间的关系差异无统计学意义(P>0.05,表3)。
2.3 胸部CT特征与预后
使用Kaplan-Meier法及Log-rank检验进行单因素生存分析,结果表明,在CT特征中,患者PFS与肿瘤的大小(HR=2.486,95%CI:1.201~5.145;P=0.009)、位置(HR=3.219,95%CI:1.517~6.833;P=0.002)、肺实变(HR=2.962,95%CI:1.413~6.209;P=0.002)、胸腔积液(HR=3.180,95%CI:1.484~6.812;P=0.001)及癌性淋巴管炎(HR=2.674,95%CI:1.109~6.447;P=0.019)相关。肿瘤较大(>3 cm)、中央型、存在实变、存在胸腔积液或存在癌性淋巴管炎提示患者PFS相对较短(图1)。将上述特征纳入Cox多因素比例风险回归模型,结果显示,病变位置(HR=3.219,95%CI:1.517~6.833;P=0.002)为克唑替尼治疗晚期NSCLC的唯一独立预后预测因素(表4,图2)。
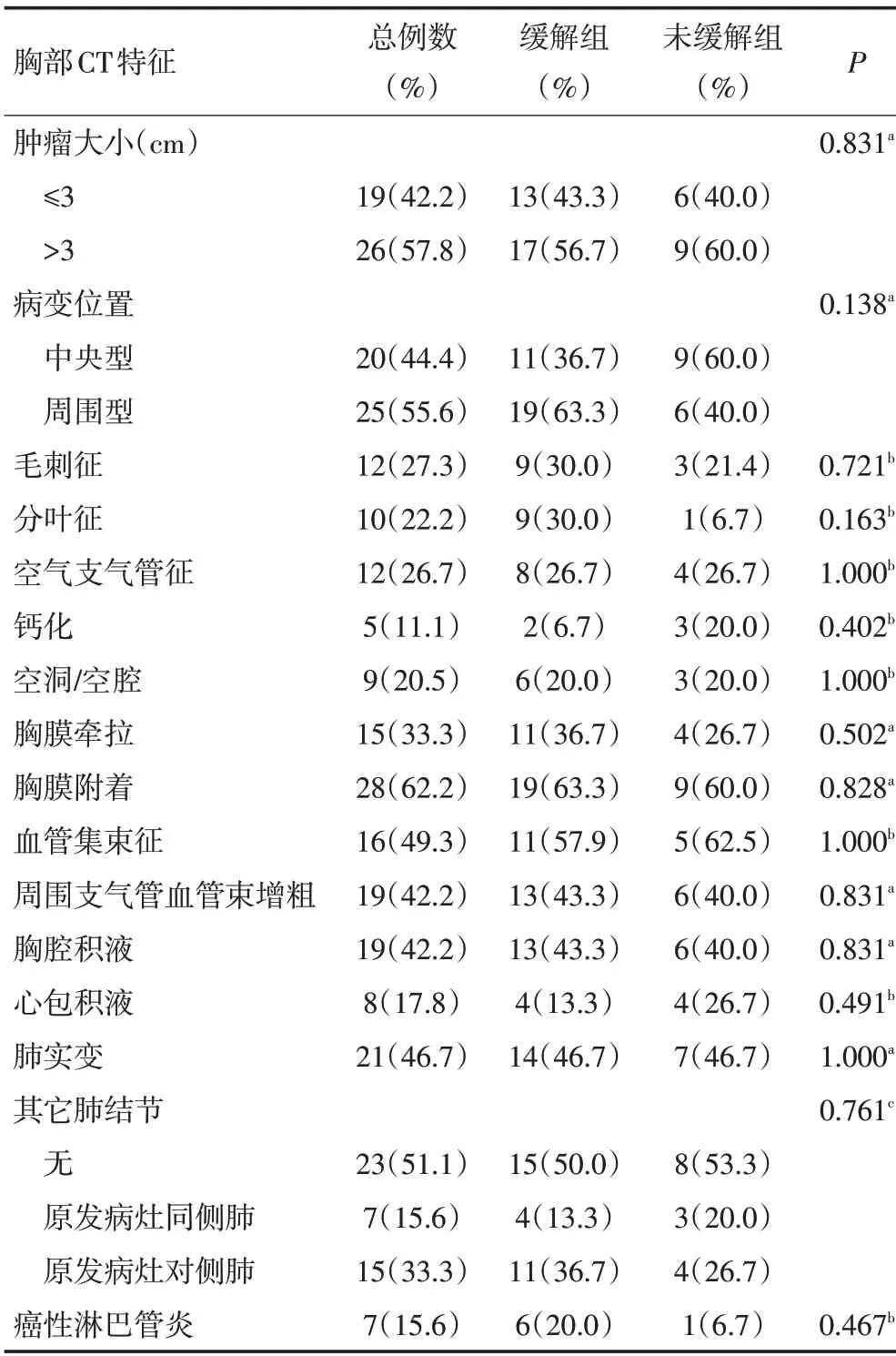
表3 克唑替尼治疗NSCLC疗效与胸部CT特征的关系
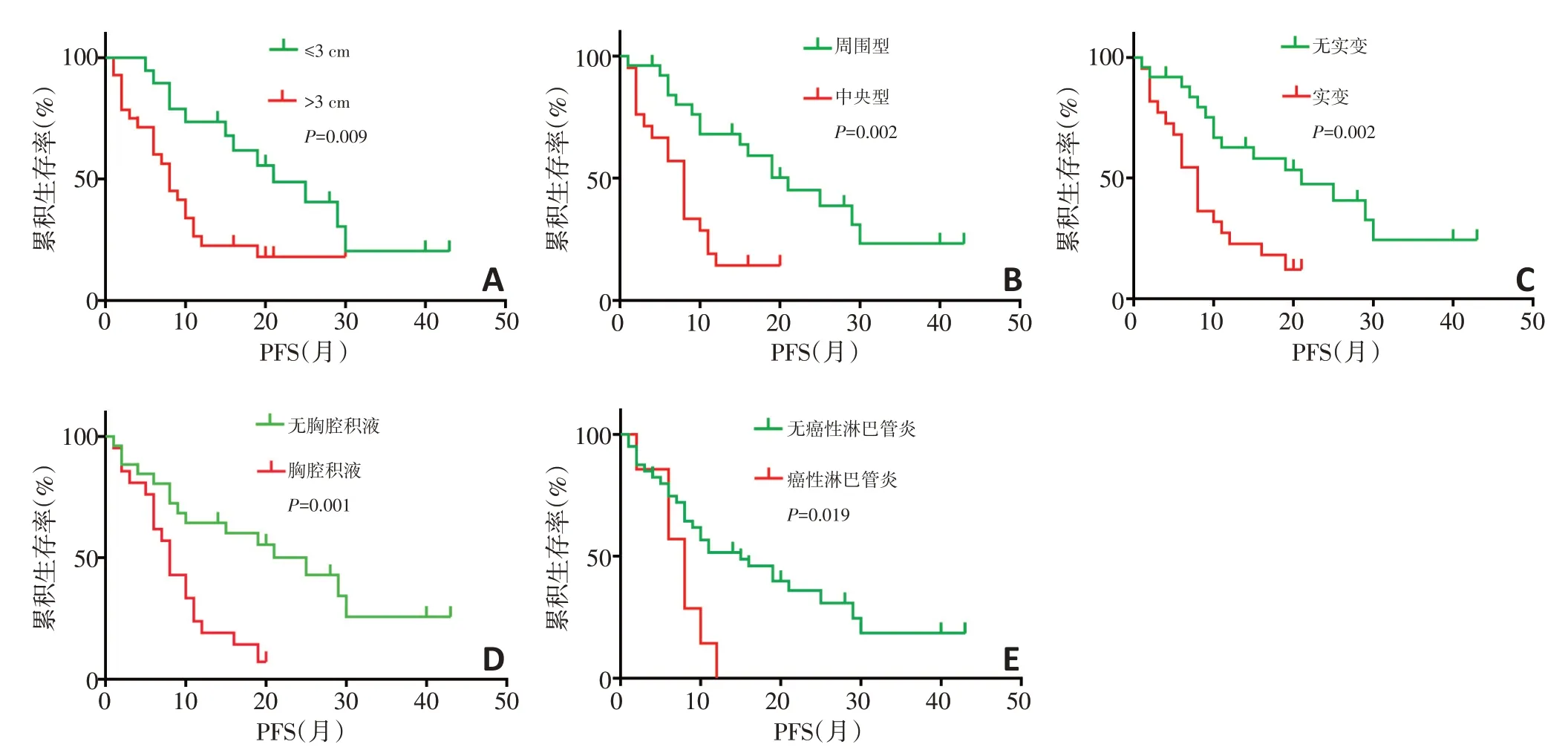
图1 各胸部CT特征与患者PFS的关系
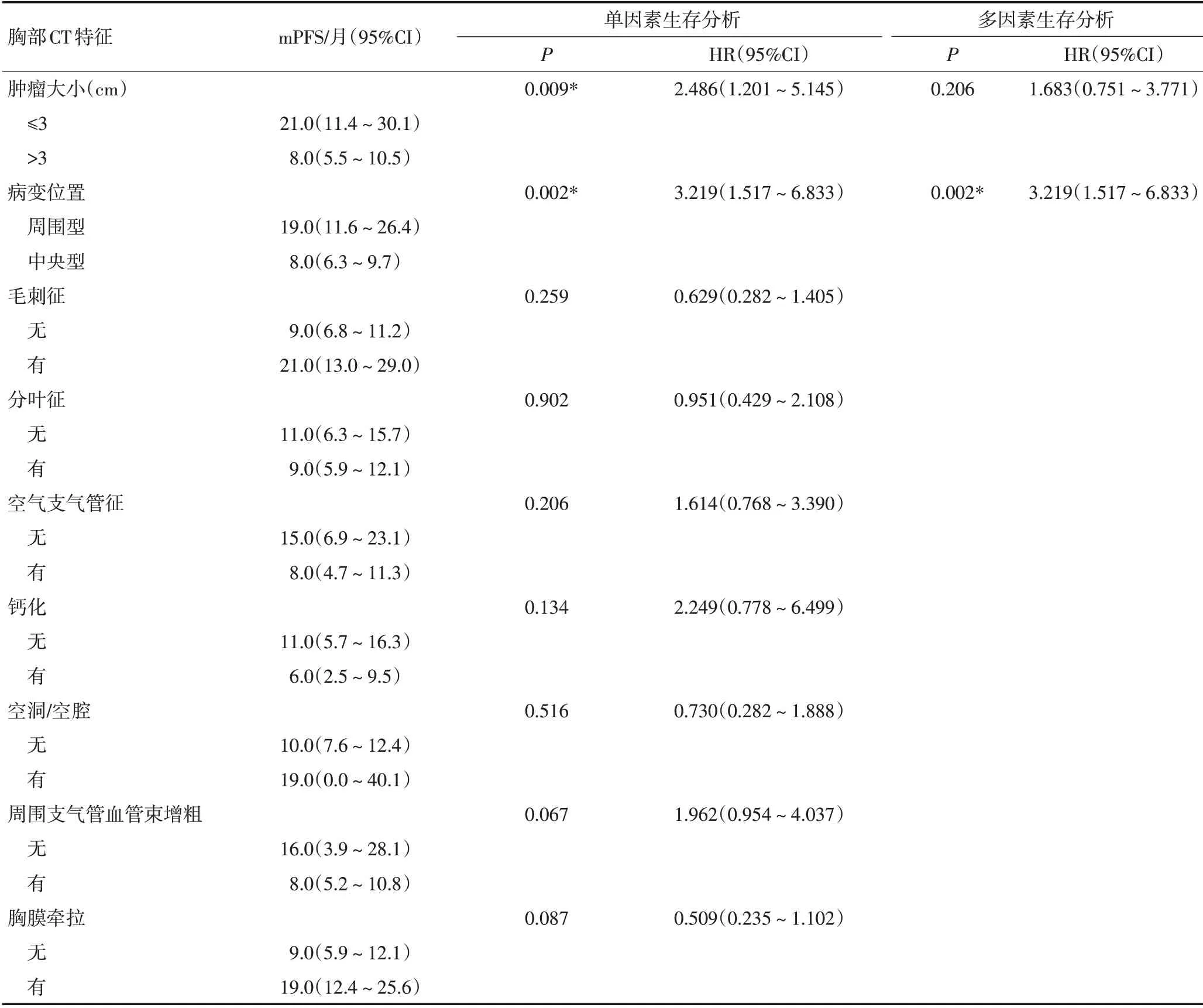
表4 克唑替尼治疗NSCLC预后与胸部CT特征的关系

表4 克唑替尼治疗NSCLC预后与胸部CT特征的关系(续表4)
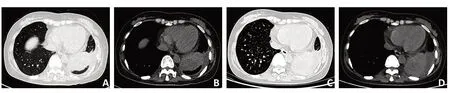
图2 1例中央型非小细胞肺癌胸部CT图像
3 讨论
克唑替尼于2011年通过美国食品药品监督管理局(FDA)批准上市,是第一代治疗ALK 重排阳性NSCLC 的靶向药物。临床试验表明,尽管克唑替尼治疗ALK重排阳性的晚期NSCLC患者PFS明显优于化疗,但两者治疗后的总生存期(overall survival,OS)无显著差异(P=0.978)[17]。能够在治疗前对疗效进行预测,判断患者是否可以获得较长的PFS,对临床治疗方案的选择具有重要意义。目前已有多项研究认为影像特征对肿瘤的治疗及预后具有一定的预测价值,但关于CT 特征与克唑替尼疗效及预后关系的研究较少,目前尚处于初步研究阶段[14,18-20]。
本研究中,临床特征对克唑替尼治疗ALK 重排阳性晚期NSCLC 的疗效及预后均不具有预测价值。在一项I期临床实验中,Camidge等[8]研究结果表明患者客观反应与性别、年龄及一线、二线治疗无关,与本研究结果相一致。中枢神经系统是晚期NSCLC常见的转移部位,据报道,20%~30%NSCLC 患者在初诊时已发生脑转移[21-22]。研究认为,克唑替尼的血脑屏障通过率较低,因此在治疗过程中极易发生中枢神经系统进展[23]。为了探究用药前脑转移是否影响克唑替尼治疗的疗效和预后,将脑转移这一因素纳入研究。结果表明,存在脑转移患者与无脑转移患者的疗效差异无统计学意义(P=0.491)。尽管有脑转移者与无脑转移者相比mPFS较短,但两者间差异无统计学意义(8个月vs.11个月,P=0.865)。Costa等[21]研究中分析了临床试验PROFILE 1005 和1007 中的888例经克唑替尼治疗的ALK重排型NSCLC患者,包含275 例(31%)脑转移患者,其研究结果显示,治疗前有无脑转移在疾病控制率、ORR以及PFS等方面差异均无统计学意义。
目前,尚缺乏针对CT 特征与克唑替尼疗效之间关系的研究报道。王毓洲等[24]研究显示,在37 例含有EGFR 突变的晚期NSCLC 患者中,有胸腔积液、肺转移灶数量在3 个以上及病灶呈中等以上强化者经EGFR-TKIs 治疗后疗效更优。而本研究认为,单独使用胸部CT形态特征对克唑替尼疗效尚不具有提示或预测的价值。治疗前胸部CT特征对靶向药物治疗NSCLC 的疗效是否具有预测价值尚需进一步研究。
有研究提示,中央型肺癌在ALK 重排型NSCLC中的发生率比ALK阴性更高[14,25]。在本研究中,病变位置可作为预后的独立预测因素,中央型是预后的危险因素。另外,病灶大小、肺实变、胸腔积液及癌性淋巴管炎等CT征象均与患者PFS具有相关性。在Choi等[15]研究中,肿瘤较小(≤3 cm;HR=1.02,95%CI:1.01~1.03;P<0.01)、结节型(HR=0.55,95% CI:0.34~0.88;P=0.01)、周围型(HR=0.62,95% CI:0.42~0.93;P=0.02)提示EGFR-TKIs 治疗后具有较长PFS,与本研究结果相近。Yamamotco等[14]对37例ALK阳性NSCLC胸部CT特征进行分析,单因素生存分析显示肿瘤周围杂乱的血管征象提示预后不良(HR=2.437,95%CI:1.00~5.85;P=0.041)。本研究中分析了血管集束征和周围支气管血管束增粗两个血管特征,单因素生存分析显示两者均非预后预测因子,尽管具有周围支气管血管束增粗的患者有预后较差的趋势,然而此差异具有统计学意义(8 个月vs.16 个月,P=0.067)。另外,部分研究显示,相较于ALK重排阴性或EGFR突变NSCLC患者,大量胸腔积液、癌性淋巴管炎在ALK 阳性者胸部CT 中更常见[14,26-27],但上述研究未涉及CT特征与预后相关性研究。胸腔积液及癌性淋巴管炎提示癌症胸膜转移及肺内淋巴管转移,也许是导致PFS较短的原因。
综上所述,治疗前胸部CT 特征对克唑替尼治疗ALK 重排阳性的晚期NSCLC 预后具有一定预测价值,病变位置为预后的独立预测因素。
