恩诺沙星及其代谢物在方正银鲫组织中的代谢及消除规律
2019-07-13罗晶晶邹荣婕韩典峰李佳蔚任传博薛敬林刘慧慧
罗晶晶,邹荣婕,宋 怿,黄 会,韩典峰,李佳蔚,任传博,薛敬林,刘慧慧
(1. 山东省海洋资源与环境研究院,山东省海洋生态修复重点实验室,山东烟台 264006;2. 烟台市福山区农业农村局,山东烟台 265500;3. 中国水产科学研究院,农业农村部水产品质量安全控制重点实验室,北京 100141)
恩诺沙星(Enrofloxacin)属于第3代喹诺酮类药物(quinolone)——氟喹诺酮类(ftuoroquinolones)之一,又名乙基环丙沙星,具有低毒和高效等特点[1-5],1996年10月获美国食品药品监督管理局(FDA)批准,成为畜禽和水产专用抗菌药物。因其具有抗菌谱广、渗透性强、无交叉耐药等优点,被广泛应用于细菌性疾病和支原体感染的治疗[1,6]。在水生动物中,恩诺沙星主要用于治疗鱼类细菌性败血症、烂鳃病、赤皮病、肠炎病、白头白嘴病、打印病和弧菌病等细菌性疾病及甲鱼溃疡病等[2,7-8]。据统计,恩诺沙星用量在2013年兽用抗菌药物中排名第四[9]。2015年9月,我国规定禁止在食品动物中使用洛美沙星、培氟沙星、诺氟沙星和氧氟沙星4种原料药后,恩诺沙星在养殖生产中更受青睐[10]。与此同时,恩诺沙星在动物中的残留情况也备受关注。目前,恩诺沙星体内代谢和消除研究的水产动物种类有鲆鳎类[11-13]、鳗鲡(Anguilla)[14-16]、乌鳢(Ophicephalus argus)[17]、黑鮶(Gymnocorymbus ternetzi)[18]、 罗 非 鱼(Eriocheir sinensis)[19]、 泥鳅(Oriental weather fish)[20]、异育银鲫(Carassius auratus gibelio)[21-23]、 虾(Litopenaeus vanname)[24]和蟹(Eriocheir sinensi)[25],给药方式有投喂药饵和肌注两种。以上研究多采用《恩诺沙星水产养殖使用规范》[26]推荐剂量开展研究,但由于恩诺沙星药物使用频率高,致病菌药物敏感性降低[22],实际生产中存在大剂量用药现象。
本研究采用鱼类养殖中常用的口灌方式,对方正银鲫(Carassius auratus gibelio)以60 mg/kg.b.w剂量灌服恩诺沙星,分析方正银鲫各组织中恩诺沙星及其代谢物的代谢及消除规律,以期为鲫实际养殖生产中恩诺沙星给药及药物代谢周期提供参考数据。
1 材料与方法
1.1 试验用鱼
试验用方正银鲫取自山东省济宁市泉林镇水库,体质量(250±10)g,体表完整无外伤,健康状况良好;置于半径2 m、水深0.8 m的水泥池中养殖。养殖用水为山泉水,水温范围为12~15 ℃。试验期间,通过投放冰水和加热棒对水温进行辅助调节。每天按鱼体质量的3%投喂饲料。经检测,试验用鱼、养殖用水及饲料中均不含氟喹诺酮类药物。
1.2 试剂及药品
盐酸恩诺沙星:购自浙江国邦药业有限 公 司( 批 号 兽 药 字(2013)110132337,纯度98.0%);恩诺沙星标准品:购自德国Dr.Eherestorfer公司(纯度99.0%);环丙沙星标准品:购自德国Dr.Eherestorfer公司(纯度94.0%);氘代恩诺沙星标准品:购自TRC公司(纯度97.9%);氘代环丙沙星标准品:购自TRC公司(纯度98.0%);肝素钠注射液:购自天津生物化学制药有限公司(1.25万单位);无水硫酸钠:购自阿拉丁公司(农残级);乙腈、甲醇和正己烷均为色谱纯,甲酸为优级纯,试验用水为超纯水。
1.3 主要仪器
超高效液相色谱-串联质谱仪:TSQ Endura,美国Thermo公司;超纯水仪:Milli-Q Gradient,法国Millipore公司;高速离心机:TGL-10C,上海安亭科学仪器厂;超声波清洗器:KQ-600E,昆山市超声仪器有限公司;旋转蒸发仪:R-100,瑞士BUCHI公司。
1.4 药液配制
称取9 g盐酸恩诺沙星,加入800 mL水充分溶解后,再加入适量淀粉和少许红色食用色素,用水定容配制成1 L恩诺沙星混悬液,混悬液中恩诺沙星含量为9 mg/mL,红色食用色素作为回吐指示剂。
1.5 试验设计
给药剂量为60 mg/kg.b.w。用2 mL注射器连接软导管伸入方正银鲫胃部给药,给药后静置3~5 s放入水中,无回吐者用于试验。每个时间点灌喂6尾方正银鲫,分别于给药后15、30 min,1、3、6、9、12、24、48、72 和 96 h,5、7、9、11、14、17、20、25、30、35、40、45、50、55、60、70、80、90、100和120 d等31个取样点取样,取其肌肉、皮肤、肝脏、肾脏和鳃5种组织样品,充分匀浆后,分别置于封口袋中,于-18 ℃保存待检。
血浆样品采集:注射器事先用1%肝素钠处理,于尾静脉抽取血液,每尾鱼不少于3 mL,收集于5 mL离心管内,经6 000 r/min离心后取上层血浆,-18 ℃保存。
1.6 检测方法及色谱、质谱条件
1.6.1 检测方法 参照农业农村部1077号公告《水产品中17种磺胺类及15种喹诺酮类药物残留量的测定 液相色谱-串联质谱法》,称取(2.0±0.1)g试样,加入50 μL氘代恩诺沙星和氘代环丙沙星混合溶液(10 μg/mL),混匀后静置10 min;加入10 g无水硫酸钠,用20 mL酸化乙腈(含1%甲酸)提取;将提取液收集于50 mL梨形瓶中,重复提取1次;合并2次提取液,于40 ℃水浴旋转蒸发至干;用1 mL甲醇溶液(体积分数为20%)复溶,正己烷去脂;过0.22 μm滤膜,供高效液相色谱-串联质谱仪测定。
1.6.2 色谱、质谱条件 色谱柱为Hypersil GLOD(100.0 mm×2.1mm);柱温为35 ℃;进样量10 μL。流动相A相为甲醇,B相为水(含0.1%甲酸),流速为0.25 mL/min。梯度洗脱程序见表1。质谱条件:离子化模式采用H-ESI,正离子模式;正离子电压3 500 V,负离子电压 2 500 V,离子传输杆温度325 ℃,雾化温度300 ℃,鞘气(Sheath Gas)40 Arb,辅助气(Aux Gas)10 Arb,质谱扫描方式为SRM,扫描母离子、子离子和碰撞能量见表2。

表1 流动相梯度洗脱程序

表2 选择反应监测母离子、子离子和碰撞能量
1.7 数据处理
采用Microsoft Excel 2010数据处理;采用Origin 8.0绘制曲线;采用DAS 2.0进行药动学参数计算。
2 结果与分析
2.1 标准曲线、相关系数、方法检测限及回收率
本试验条件下,恩诺沙星、环丙沙星检出限为2.0 μg/kg,平均回收率为84%~103%;恩诺沙星、环丙沙星在0.10~1 000.00 ng/mL范围内,线性良好,线性方程分别为Y= -0.011 +0.001 8x(r= 0.999 2)和Y=-0.002 7+0.001 2x(r= 0.999 8)。
2.2 恩诺沙星及其代谢产物在鲫体内的代谢及消除情况
2.2.1 恩诺沙星 如图1所示,口灌给药后,血药浓度最早达到峰值,达峰时间(tmax)为9 h,其次是肌肉(tmax为18 h),肝脏、鳃(tmax为24 h),肾脏和皮肤(tmax为48 h);达峰浓度以肾脏最高,cmax为30.490 mg/kg;其次是肝脏、肌肉、血浆、鳃、皮肤,cmax依次为21.372、18.715、16.636、15.157、11.663 mg/kg。达峰值后的恩诺沙星含量迅速下降,各组织中恩诺沙星代谢趋势相似,药时曲线如图1所示。血浆中恩诺沙星消除最快,给药后30 d无检出,鳃、肌肉和皮肤中恩诺沙星分别于50、60和100 d后无检出,肝脏和肾脏消除最慢,100 d时仍有检出,残留量接近限量值 100 μg/kg。
2.2.2 环丙沙星 给药后15 min,方正银鲫各组织均检出环丙沙星,其代谢和消除趋势与恩诺沙星大致相同,达峰时间较恩诺沙星延后(图2)。血浆中环丙沙星最早产生达峰值,达峰时间tmax为18 h,其次是肌肉(tmax为1 d),肝脏、鳃(tmax为2 d),肾脏、皮肤(tmax为3 d);达峰浓度以肾脏最高,cmax为547.26 μg/kg,其他依次为血浆、肝脏、鳃、皮肤和肌肉,cmax分别为214.04、202.60、65.26、62.23 和 50.081 μg/kg。
2.3 药物代谢动力学参数
恩诺沙星在鲫各组织中的药物代谢动力学参数见表3。
3 讨论
药动学中用房室模型模拟人体,把接受或消除药物速率相似的部位,归入一个房室[27]。房室模型的划分由药物的动态分布特征所决定。本研究数据经DAS2.0拟合得出。口灌给药后,恩诺沙星在鲫体内各器官状态均符合二室模型。给药后,药物立即分布到分布速率常数α相对较大的血浆和肌肉组织中,α分别为0.181和0.174,之后再缓慢分布到分布速率常数α较小的肝脏、鳃、肾和皮肤中,α范围为0.058~0.026。恩诺沙星在异育银鲫血浆中的药时数据符合二室模型[21];肌注给药时,恩诺沙星在眼斑拟石首鱼(Sciaenops ocellatus)[28]血浆内的药时数据也可拟合为二室模型。
3.1 恩诺沙星在鲫体内的吸收、分布及消除
cmax、tmax是反映药物吸收快慢程度的重要药物代谢动力学参数[23,28]。本研究中血浆tmax为9 h,表明口灌给药后,恩诺沙星从胃部吸收进入血液后,9 h时达到峰值,cmax为16.636 mg/kg。各研究组织中血浆tmax最小,说明血浆对恩诺沙星的吸收速度最快。同样口灌给药后,恩诺沙星在杂交鲟[7]血浆、肌肉和肝脏中的tmax分别为2.01、1.51和 0.99 h, 鲤(Cyprinus carpio)[29]、 牙 鲆(Paralichthys olivaceus)[30]血浆tmax分别为4 h、0.5 h,且26 ℃和20 ℃条件下鲤血浆tmax分别为0.75 h和4 h,说明口灌给药后,恩诺沙星进入鱼血浆或肌肉等组织中的速度受鱼的种类、水温等因素影响。肾脏cmax最高,为30.490 mg/kg,肝脏次之,为21.372 mg/kg,鳃和皮肤较低分别为15.157 mg/kg和11.663 mg/kg。肾脏、肝脏中药物浓度高,说明恩诺沙星在方正银鲫肾脏和肝脏中组织结合率高。
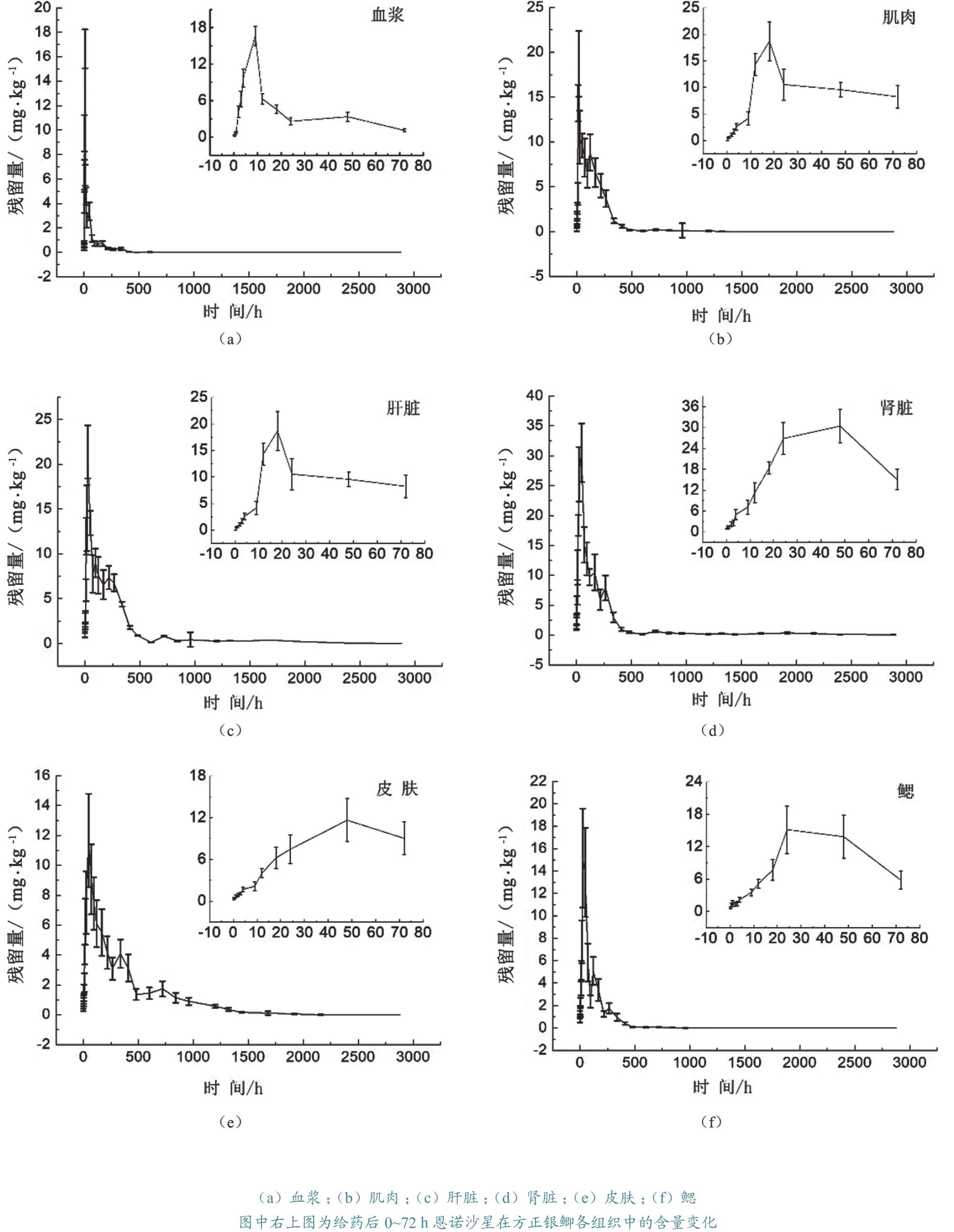
图1 口灌给药后恩诺沙星在方正银鲫各组织中的含量变化趋势

图2 口灌给药后环丙沙星在方正银鲫各组织中的含量变化趋势
药时曲线下面积(AUC)、表观分布容积(V1/F)是反映药物在体内分布的主要药动学参数。V1/F指药物在体内分布达到动态平衡时体内药量和血药浓度的比值,其大小可反映药物在体内分布的广泛程度以及组织结合程度,通常以0.8和1.0 L/kg为临界值:大于0.8 L/kg则认为药物在体内广泛分布或组织蛋白对药物结合力强;大于1.0 L/kg则说明该组织中药物浓度高于血浆中浓度[7,31-32]。恩诺沙星在方正银鲫肝脏、肾脏、皮肤、肌肉、鳃中的V1/F分别为1.335、0.898、0.633、1.582和1.496 L/kg。除皮肤外,恩诺沙星在肝脏、肾脏、肌肉和鳃中分布广泛,药物达到动态平衡时,肝脏、肌肉和鳃中药物浓度高于血药浓度。
AUC表明药物在体内的暴露量,是衡量药物在体内被利用程度的一个重要参数[31]。一般认为AUC值越大,药物穿入组织越多,分布越广[32]。恩诺沙星在方正银鲫各组织AUC值以肾脏最高4 455.889 mg·h/L,肝脏次之 3 672.847 mg·h/L,血浆最低433.414 mg·h/L。将红笛鲷(Lutjanus sanguineus)[33]以5 mg/kg的剂量口灌恩诺沙星后,其肌肉、肝脏和肾脏中AUC值以肾脏最高为58.692 mg·h/L;对杂交鲟[7]单次口灌恩诺沙星10 mg/kg后,肌肉、血浆和肝脏中AUC值以肝脏最高为462.21 mg·h/L。假设组织中AUC值与给药量成正比,以60 mg/kg.b.w的给药量,红笛鲷肾脏和杂交鲟肝脏中AUC分别为704.30和2 773.26 mg·h/L,低于本研究方正银鲫肾脏和肝脏AUC值。可见口灌给药后,恩诺沙星在方正银鲫肾脏和肝脏中分布更广。
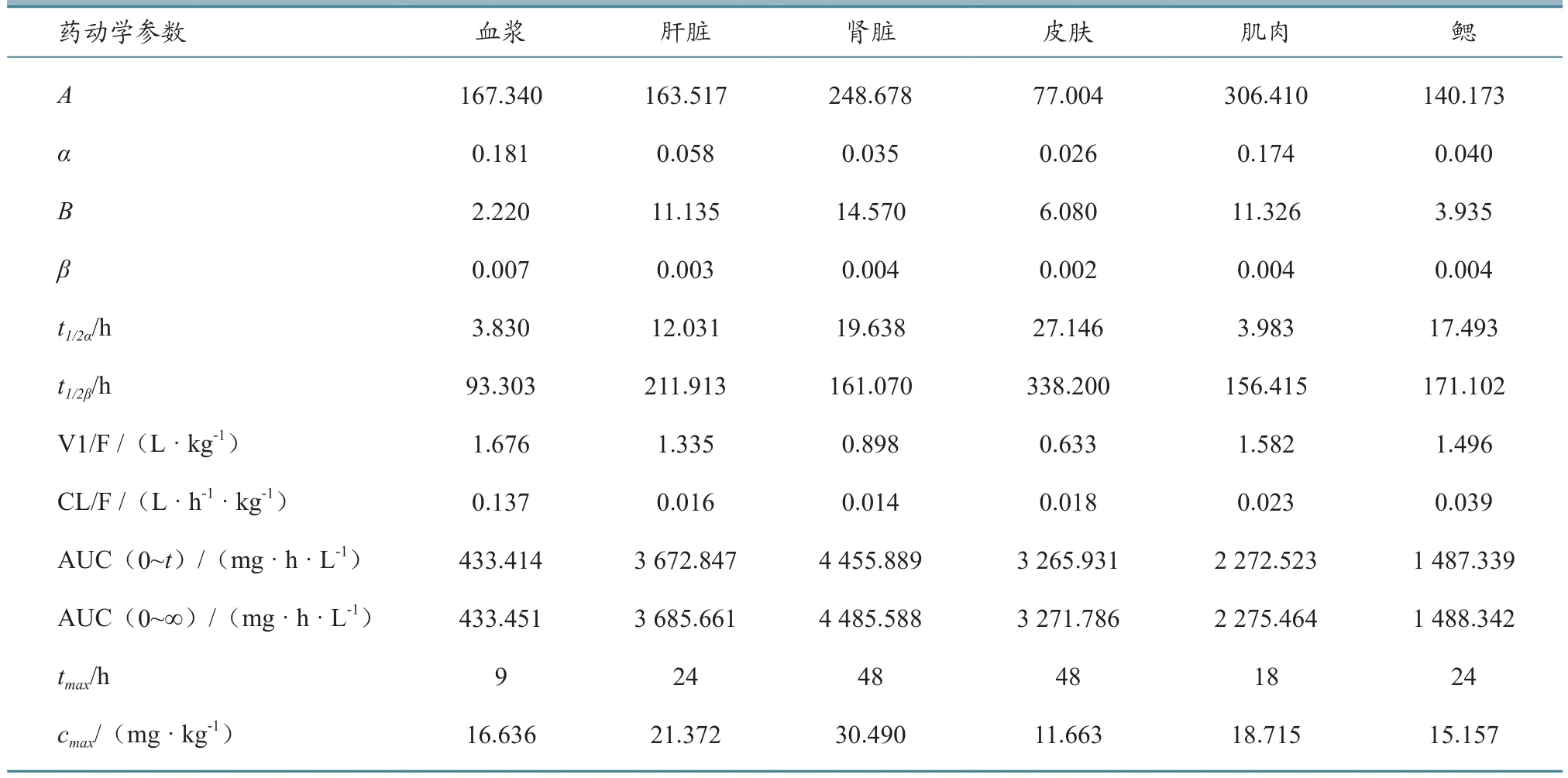
表3 口灌给药后恩诺沙星在方正银鲫体内各组织中的药代动力学参数
3.2 恩诺沙星代谢产物环丙沙星在方正银鲫体内的代谢情况
目前多数研究认为,恩诺沙星进入水生动物机体后,98%的恩诺沙星以原药形式存在,脱乙基后产生的环丙沙星是其在水生动物体内的主要代谢产物,但含量不足 2%[16,19,22-23,34-35],或未检测到[36]。牙鲆[30]口灌恩诺沙星后,对血浆、肝脏、肾脏、肌肉和鳃进行检测,仅在血浆、肝脏和肾脏中检出环丙沙星。本研究中,给药后15 min,各组织中均检出环丙沙星,且血浆、肌肉、肝脏、肾脏、皮肤和鳃中环丙沙星与恩诺沙星总含量比值分别为2.27%、0.36%、1.09%、3.17%、0.82%和0.80%。可见,恩诺沙星在方正银鲫体内主要以原药恩诺沙星形式存在,同时有小部分脱乙基后代谢成环丙沙星,各组织中环丙沙星平均含量为1.60%,与多数对水生动物的报道[37]一致。
3.3 代谢周期
本试验对恩诺沙星在方正银鲫肌肉、血液、鳃和肝脏、肾脏、皮肤中的消除规律做了研究,为制定恩诺沙星在方正银鲫中的休药期提供数据支持。t1/2β反映药物在体内的消除速度。恩诺沙星在方正银鲫各组织的t1/2β值以皮肤最高,为338.20 h;血浆最低,为93.303 h。恩诺沙星在牙鲆[30]肌肉中的t1/2β为67.759 h,在红笛鲷[33]血浆、肌肉、肝脏和肾脏的t1/2β分别为 9.18、83.32、94.47和21.81 h,在凡纳滨对虾[24]肌肉、肝脏中t1/2β分别为30.30 h和34.80 h,在欧洲鳗鲡[15]血浆、肌肉、肝脏和肾脏中的t1/2β分别为908.07、901.24、59.32和761.81 h。相比而言,本研究恩诺沙星在方正银鲫体内消除速度较牙鲆、红笛鲷和凡纳滨对虾慢,而较欧洲鳗鲡快。按5个t1/2后体内药物基本消除干净计算,药物消除量达97%[38]。本试验条件下,恩诺沙星在方正银鲫皮肤和血浆中的消除半衰期分别为1 691 h 和466.5 h,即给药70.5 d 和19.4 d后,药物基本消除干净。根据农业部235号公告-2002《动物性食品中兽药最高残留限量》规定,恩诺沙星和环丙沙星在组织中的最高残留总量不得超过0.1 mg/kg。本试验条件下,可食性组织中皮肤中恩诺沙星和环丙沙星残留总量降低到0.1 mg/kg以下的时间最长,为1 200度日,与理论值基本符合。恩诺沙星在方正银鲫可食组织中的残留量经1 200度日后可降至检测限以下。
4 结论
本研究探讨了恩诺沙星在方正银鲫体内的代谢及消除特征,对恩诺沙星在方正银鲫肌肉、血浆、肝脏、肾脏、鳃和皮肤中不同时间点的含量进行跟踪分析。恩诺沙星在方正银鲫各组织中的最高浓度由大到小依次为肾脏、肝脏、肌肉、血浆、鳃和皮肤。各组织中恩诺沙星在皮肤中的消除半衰期最长。本试验条件下,恩诺沙星以60 mg/kg.b.w剂量单次口灌给药后,可食性组织中,皮肤中的恩诺沙星和环丙沙星残留总量降低到0.1 mg/kg以下的时间最长,为1 200度日。总体来说,方正银鲫对恩诺沙星的消除较缓慢。本研究为今后恩诺沙星在方正银鲫养殖中的合理使用及休药期制定提供了数据支持。
