HPLC法同时测定不同产地甘西鼠尾草及丹参中8种主要成分的含量
2019-05-15王亚峰王生彪朵德龙王爱霞岗桑卓玛严英俊
王亚峰,王生彪,朵德龙,王爱霞,岗桑卓玛,严英俊
(青海省人民医院,西宁 810007)
甘西鼠尾草(SalviaprzewalskiiMaxim)为唇形科鼠尾草属弧隔鼠尾草亚属毛地黄鼠尾草,是优良的传统中草药,其主要有效成分与丹参类似,包括水溶性的酚酸类成分和脂溶性的丹参酮类成分[1-2],作为其代用品在临床上发挥重要作用[3-5]。研究表明,甘西鼠尾草具有保护心肌缺血细胞和心肌缺血再灌注损伤细胞、改善血液流变学、保护神经细胞、利尿、抗菌、抗病毒、抗氧化、抗血栓、抗抑郁和抑制黄嘌呤氧化酶等作用[6-16],还可抑制乳腺癌、肺癌、肝癌、白血病和胃癌等多种肿瘤细胞株的生长[17-19]以及结肠癌细胞的侵袭和迁移[20]。此外,有报道称甘西鼠尾草还具有抗缺氧作用,因此甘西鼠尾草在治疗心血管疾病、抗癌、抗炎和高原病方面具有广阔的应用前景。
甘西鼠尾草还未收载入《中国药典》,只收载于《甘肃省中药材质量标准》和《云南省药品标准》等地方标准中[5]。青海甘西鼠尾草主产于尖扎、同仁以及民和等县区,生于海拔1 900~3 800 m的山谷、林下、山坡和河滩[21]。质量标准无章可循,因此急需在这方面进行研究。本文建立了可同时测定甘西鼠尾草中8种化学成分的HPLC法,通过比较不同产地甘西鼠尾草与丹参中8种成分的含量,为建立和完善青海甘西鼠尾草的质量标准,挖掘青海甘西鼠尾草药材以及进一步研究其抗缺氧活性提供了依据。
1 仪器与试药
1.1仪器 Waters 600分析型高效液相色谱仪(包括Waters 2998 PAD检测器、Waters 2707自动进样器和Empower色谱工作站),色谱柱SunFire C18(250 mm×4.6 mm,5 μm)(美国Waters公司);XP205型分析天平(美国梅特勒-托利多公司);KJ-11030AL型超声波清洗仪(深圳市科洁超声科技有限公司)。
1.2试药 乙腈、甲醇为色谱纯(德国Merck公司);丹参酮ⅡA对照品(批号 110766-201721)、隐丹参酮对照品(批号110852-200806)、丹参酮Ⅰ对照品(批号110867-201607)、丹酚酸B对照品(批号111562-201716)、迷迭香酸对照品(批号111871-201706)和丹参素钠对照品(批号110855-201614),均购自中国食品药品检定研究院;紫草酸对照品(批号CAS 28831-65-4)和二氢丹参酮Ⅰ对照品(批号CAS 87205-99-0),均购自北京莱耀生物科技有限公司(质量分数≥98%)。甘西鼠尾草样品均采自10月份花期后,丹参样品均购自成都睿智中药材有限责任公司,所有样品经青海师范大学生命科学学院院长、博士生导师陈志教授鉴定为唇形科植物甘西鼠尾草及丹参。
2 方法与结果
2.1溶液的制备
2.1.1混合对照品溶液 精密称取丹参素钠、迷迭香酸、紫草酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA对照品,置于同一量瓶中,加体积分数为80%的甲醇配制成质量浓度分别为218.27,137.10,264.50,164.20,138.50,157.40,296.00和150.50 μg·mL-1的混合对照品溶液,置于2~8 ℃冰箱中用锡箔纸避光保存。
2.1.2供试品溶液 取不同产地采集的甘西鼠尾草根,在阴凉处晾干、粉碎,过3号筛,精密称取过筛后的粉末1.0 g,置于100 mL具塞锥形瓶中,加入50 mL体积分数为80%的甲醇,超声(功率180 W,频率40 kHz)提取50 min,以3 000 r·min-1离心30 min,过滤。过滤后以同样方法用50 mL甲醇提取2次。合并滤液作为供试品溶液,置于2~8 ℃冰箱中用锡箔纸避光保存。
2.2方法学考察
2.2.1色谱条件与系统适用性 色谱柱:SunFire C18(250 mm×4.6 mm,5 μm)色谱柱;流动相:乙腈(A)-0.8 mL·L-1的甲酸超纯水溶液(B),梯度洗脱(0~19 min,20%A~60%A;19~49 min,60%A~81%A;49~53 min,81%A~91%A;53~57 min,95%A),流速:1.0 mL·min-1;检测波长:270 nm;柱温:26 ℃;进样量:2 μL。在上述色谱条件下,理论塔板数均大于4 000,样品中8个被测组分的色谱峰与相邻峰的分离度R>1.5,拖尾因子符合要求,混合对照品及甘西鼠尾草样品色谱图见图1。
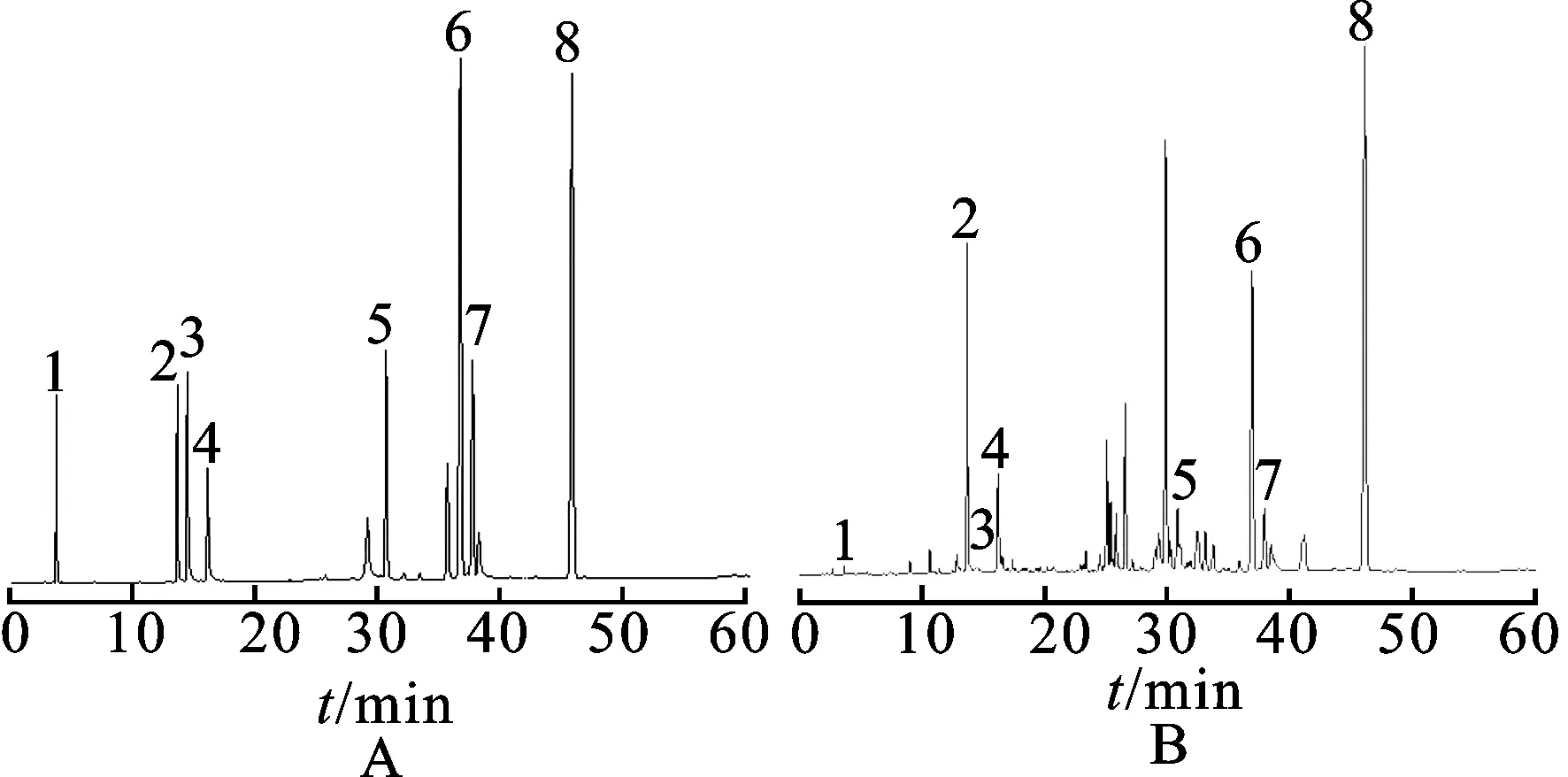
图1 HPLC图
A.混合对照品溶液;B.供试品溶液;1.丹参素钠;2.迷迭香酸;3.紫草酸;4.丹酚酸B;5.二氢丹参酮Ⅰ;6.隐丹参酮;7.丹参酮Ⅰ;8.丹参酮ⅡA。
Fig.1 HPLC chromatograms
A.mixed reference substance;B.sample solution;1.sodium danshensu;2.rosmarinic acid;3.lithospermic acid;4.salvianolic acid B;5.dihydrotanshinquinone-Ⅰ;6.cryptotanshinone;7.tanshinoneⅠ;8.tanshinone ⅡA.
2.2.2线性范围考察 将2.1.1项下制备的混合对照品溶液,用体积分数为80%的甲醇稀释成系列质量浓度的混合对照品溶液,用高效液相色谱仪进行分析,进样时用棕色进样瓶,记录峰面积。以各对照品质量浓度为横坐标(x)、峰面积为纵坐标(y),用origin软件绘制标准曲线,结果见表1,表明各化合物在相应范围内线性关系良好。
表1 8个待测化合物的回归方程和线性范围
Tab.1 Regression equations and linear ranges of the 8 active compounds analyzed by HPLC
2.2.3精密度实验 精密吸取2.1.2项下制备的供试品溶液,按照2.2.1项下色谱条件,连续进样6次,测定8种待测组分的峰面积,结果丹参素钠、迷迭香酸、紫草酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA峰面积的RSD(n=6)值分别为0.7%,0.5%,1.4%,0.9%,1.1%,1.3%,1.7%和0.3%,表明该方法精密度良好。
2.2.4重复性实验 取同一批样品6份,按照2.1.2项下方法制得供试品溶液,按照2.2.1项下色谱条件进样分析,测定8种待测组分的含量,结果丹参素钠、迷迭香酸、紫草酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA含量的平均值(n=6)为0.103%,3.375%,0.009%,2.399%,0.727%,1.500%,1.033%和2.354%。RSD值分别为0.6%,0.4%,1.5%,1.1%,1.2%,0.7%,1.7%和0.1%,表明该方法重复性良好。
2.2.5加样回收率实验 精密称取已知含量的甘西鼠尾草粉末6份,每份1.0 g。分别加入2.1.1项下制备的混合对照品溶液,按照2.1.2项下方法制备供试品溶液,进样分析,记录峰面积,计算丹参素钠、迷迭香酸、紫草酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA的平均回收率分别为98.8%,101.8%,98.8%,97.9%,99.8%,101.3%,100.2%和100.2%,RSD值分别为2.1%,1.1%,1.4%,1.7%,0.5%,2.3%,1.6%和0.2%,表明该方法回收率良好。
2.3样品的测定 取不同产地的丹参及甘西鼠尾草,按照2.1.2项下方法制备供试品溶液,按照2.2.1项下色谱条件进行分析,通过峰面积,用外标法计算丹参素钠、迷迭香酸、紫草酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA的含量,进行对比。测定结果见表2。
表2 样品含量测定结果
Tab.2 Results of the content determination of samples (n=3)

编号产地含量/%丹参素钠迷迭香酸紫草酸丹酚酸B二氢丹参酮Ⅰ隐丹参酮丹参酮Ⅰ丹参酮ⅡA1青海黄南种植0.3736.7500.3712.6420.6110.7920.7991.1942青海黄南野生0.4224.7310.3301.0630.3220.6390.3411.4283青海民和前河0.1093.9370.4192.4100.7251.5191.0922.5984青海民和西沟0.1462.8400.2350.7710.3510.5980.1911.0135云南迪庆0.0761.3790.1790.0610.0480.2320.0070.5846陇南野生0.1911.4830.1941.1440.2860.4260.3770.8577西藏朗县0.1593.9580.1950.4790.0900.2520.5961.2008西藏加查0.3552.6420.4990.4460.0860.2140.4601.1409陇南丹参0.5630.253—8.7910.1210.2230.1350.30010陕西丹参0.7820.6060.63617.7700.1060.4000.0090.62411山东丹参0.2410.1760.4714.7930.3960.6080.4600.847
注:—表示未检测到。
3 讨论
以8种化合物的含量作为考察指标,采用单因素法,参考程沛等[21]及胡伟慧等[22]研究报道,考察了在提取溶剂为50 mL的超声提取下,提取溶剂为体积分数为50%,60%,70%,80%及90%的甲醇,提取次数为1,2和3次,提取时间为25,35,45,55和60 min对提取效率的影响,最终确定甘西鼠尾草样品的提取方法为50倍体积分数为80%的甲醇超声提取2次,每次45 min,此条件提取率高,干扰杂质少。
由表2测定结果可知,不同产地甘西鼠尾草同一样品中,水溶性成分主要为迷迭香酸,其次为丹酚酸B,丹参素钠和紫草酸含量较少,脂溶性成分主要为丹参酮ⅡA,其次为隐丹参酮。对比可知,1号(青海黄南种植)样品的水溶性成分最高,迷迭香酸含量达到了6.750%,除丹参酮ⅡA和丹参素钠外,1号样品中其他6种成分均高于2号(青海黄南野生)样品。3号(青海民和前河)样品中4种脂溶性成分含量最高,二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA含量分别为0.725%,1.519%,1.092%和2.598%。4号(青海民和西沟)样品采自温度较低、光照较弱的河边树林地区,6种成分含量均小于1,2和3号,故甘西鼠尾草中8种成分的含量可能与生长适宜的光照和温度关系较大。比较青海地区甘西鼠尾草与5号(云南迪庆)、6号(陇南野生)、7号(西藏朗县)和8号(西藏加查)样品,8号样品紫草酸含量最高,为0.499%,但低于陕西丹参的0.636%。
比较青海甘西鼠尾草和不同产地丹参的测定结果可知,青海甘西鼠尾草与丹参(9,10和11号)相比,水溶性成分中,陕西丹参在丹参素钠和紫草酸含量上均高于其他样品,丹参样品中的丹酚酸B含量较高,其中10号(陕西丹参)样品高达17.770%,为1号样品的6.5倍,而青海甘西鼠尾草迷迭香酸的含量较丹参样品高,其中1号样品中迷迭香酸含量为10号样品的10倍。除4号样品外,4种脂溶性成分中隐丹参酮和丹参酮ⅡA的含量青海甘西鼠尾草均高于丹参样品。3种丹参样品中陕西丹参的水溶性成分较高,山东丹参的脂溶性成分较高。
不同来源的甘西鼠尾草水溶性和脂溶性成分含量差异显著,青海不同产地甘西鼠尾草较其他产地甘西鼠尾草脂溶性成分和水溶性成分均有较好的优势。甘西鼠尾草作为丹参的替代品,虽已在临床广泛应用,但与丹参相比主要的差别在于丹酚酸B和迷迭香酸的含量,青海不同产地甘西鼠尾草,除丹酚酸B的含量较丹参样品低,4种脂溶性成分均优于丹参样品。本文建立的HPLC法可同时测定甘西鼠尾草及丹参中的8种成分,保留时间稳定,分离度高,测定结果准确,方法精密度高,所得结果能为建立和完善青海甘西鼠尾草的质量标准、挖掘青海甘西鼠尾草药材及进一步研究其抗缺氧活性提供依据。
致谢:感谢青海师范大学生命科学学院陈志院长的悉心教导,感谢硕士研究生宋道光和熊元治对本实验的帮助和支持。
