腹腔镜下脾门血管精细解剖+超声刀钳夹法在脾部分切除术中的应用
2019-04-29李毅
李 毅
(德阳市人民医院,四川 德阳,618000)
随着对脾脏功能认识的加深,保脾手术在儿童中的应用显得尤为重要。由于脾脏质脆,血供丰富,止血困难,脾部分切除理念未得到普及,加之技术原因,基层医院主要以脾切除为主,因此保脾率一直较低[1]。为探索安全、有效的保脾方式,笔者在熟练掌握开腹与腹腔镜脾切除技术后,尝试采用多种方式进行保脾,如缝合、网膜包裹、射频止血[2-3]等,取得了一定效果,但在实际操作中也发现脾脏切除后的断面止血有一定困难。受到肝切除技术的启发,自2013年起采用腹腔镜下脾门血管精细解剖+超声刀钳夹法技术行腹腔镜下脾部分切除术,效果良好。现将体会报道如下。
1 资料与方法
1.1 临床资料 2013年3月至2016年12月笔者行腹腔镜脾部分切除17例,其中男10例,女7例;17~59岁,平均(32.1±11.3)岁。外伤性脾破裂11例(美国创伤外科协会分级Ⅱ~Ⅲ级),脾脏良性肿瘤6例(脾脏错构瘤2例,脾脏血管瘤1例,脾脏淋巴管瘤1例,脾囊肿1例,脾脏炎性肉芽肿1例)。
1.2 手术方法 患者取平卧位,常规五孔法建立气腹及操作通道。首先探查腹腔情况,游离脾周韧带,解剖出脾脏动脉分支、静脉属支(图1),理清脾门二、三级血管分支的分布关系(图2),采用腔镜下血管夹阻断血管分支使脾脏处于部分缺血状态,观察缺血区域与预切除脾脏部分的关系,调整阻断血管的支数、位置,使缺血区域大部分覆盖于切除部分后完全离断,采用超声刀钳夹法沿预切线切除脾脏(图3、图4),其断面采用滴水电凝止血(图5)。如创面出血明显,采用压迫止血、滴水电凝止血无效后,进一步离断脾脏保留侧分支血管后再采用上述方式止血。对于外伤性脾破裂患者,术中探查无消化道损伤后常规使用血液回收系统,探查脾脏时注意保留脾周血凝块,吸去腹腔积血后单独统计术中出血量。首先用分离钳钝性分离出脾后隧道,腔镜血管阻断钳阻断脾蒂后尽快解剖出脾动静脉,如术中脾脏断面持续活动出血则在阻断脾动静脉主干后进行余下操作,确定血管支配区域时可间断开放脾动脉。切除部分脾脏后,残余脾脏创面使用止血材料覆盖,冲洗术区及腹腔,吸净冲洗液,脾窝放置腹腔引流管。
2 结 果
16例患者成功完成腹腔镜脾部分切除术;1例外伤性脾破裂患者,由于裂口靠近脾门,残余脾脏断面渗血,缝合止血后见残脾变色,考虑残脾血供差,遂改为全脾切除。手术时间平均(85.2±45.3)min;术中出血量平均(285.5±67.0)mL;术后引流2~5 d,平均(3.0±1.2)d,引流量10~290 mL,平均(50.7±36.4)mL。术后无活动性出血、腹腔感染、切口感染等并发症发生,脾周可见少量积液,无脾静脉血栓,血小板一过性升高,未特殊处理。术后1周行增强CT,见保留血管支通畅,脾周少量积液,脾脏边缘少部分缺血坏死,无脾脓肿、脾周脓肿形成。保留的脾脏与术前相比,有血供的区域CT测量面积大于30%(图6)。经过22个月的随访,残余脾脏血供良好,白细胞、血小板计数正常。
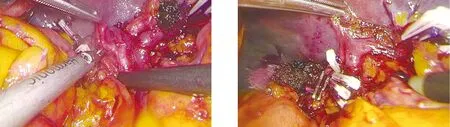
图1 全程解剖出脾门血管走向 图2 离断其二、三级分支

图3 超声刀钳夹法断脾 图4 显露脾实质内管道
3 讨 论
脾脏是人体最大的免疫器官,脾脏中的T淋巴细胞在机体特异性免疫应答、免疫调节中具有重要作用。研究表明,全脾切除对机体的免疫功能有一定影响[4-6],但这种影响能否通过其他免疫途径进行代偿或是否在某些疾病中成为决定性因素尚且未知。目前唯一可肯定的是儿童时期行全脾切除后可能发生脾切除术后凶险性感染,6岁以下儿童的脾切除术后凶险性感染发病率是其他年龄的两倍,因此多数学者认为应尽可能避免对6岁以内的患儿行全脾切除。而对于成年人,终身面临脑膜炎奈瑟菌、肺炎链球菌、B型流感嗜血杆菌等特殊细菌感染的风险,同时肺动脉高压、动脉硬化、血栓形成等不良事件也与脾脏缺失有关[7-9]。越来越多的证据支持保留25%~30%的脾实质,以维持对特定抗原刺激的免疫反应[10-12]。对于良性脾脏疾病、外伤性脾破裂,部分脾切除已成为临床上比较常用的术式。由于具有一定难度,且无固定的手术模式,因此大多数的报道仍是在开腹下进行的。腹腔镜具有视野放大、术后切口疼痛轻、胃肠道功能恢复快等特点,因此,腹腔镜脾切除的效果完全优于开腹脾切除[13]。但同时腹腔镜手术由于操作复杂,需要团队配合,操作时间可能长于开腹手术。因此,腹腔镜下行部分脾切除被认为是脾脏外科的亮点[14]。腹腔镜部分脾切除具有两个难点:(1)脾脏是实质性器官,不同于空腔脏器可在镜下使用直线切割器直接离断;(2)脾脏血供丰富,质地脆,又不同于肝脏可缝合其中的管道,脾脏断面止血尤为困难。在既往针对脾部分切除的报道中,断面止血多采用如射频止血、缝合、压迫、网膜填塞等方式[15];脾脏血管采用间断阻断或部分离断的方式,总体而言,效果不尽如人意。

图5 滴水电凝止血,保持创面新鲜,少留痂壳 图6 保留的脾脏血供良好
笔者回顾了肝切除与腹腔镜肝切除的发展历程,觉得其中的部分理念、技巧值得借鉴。根据脾动脉分支情况可将脾脏划分为2~3个叶与上极段、下极段两个段。相邻脾段间动静脉的吻合较少,形成一个近乎无血管区的平面,这一解剖特点构成了脾部分切除术的解剖学基础[16-17],沿着无血管平面解剖离断脾实质,不仅可减少术中、术后出血,还可减少残留缺血坏死脾脏的可能。但脾脏血管的二级分支无明显分布规律,其供血区域变化较大,这是影响脾脏部分切除的一个重要因素[18]。本报道主要有两个特点:精细解剖与超声刀钳夹法。(1)精细解剖:既往报道中多在离断上下极血管后观察脾脏的缺血带,如缺血带已包含了需要切除的部分,则距缺血带1 cm以内切除;如缺血带未完全包含预切除部分,则继续向保留侧离断血管。而笔者认为,仅解剖出上下极血管是不够的,因为在继续离断血管过程中“断”、“留”是基于脾门血管的大体分布具有盲目性,应进一步解剖至脾门血管的二级甚至三级分支,以达到精确阻断的目的,而且精细化解剖后对于需保留的血管显露更加清晰,利于保持残脾血供。(2)超声刀钳夹法:既往认识中,切除实质器官时应使用超声刀夹持一片组织,尽可能凝固后再切断,但在腹腔镜肝切除术中此方法有一定缺点,处理小的血管没有问题,如果夹持组织中包含大血管或靠近大血管容易引起出血,尤其大片钳夹时撕裂肝静脉分支是切肝过程中静脉出血的主要原因。因此,目前比较推崇的超声刀使用方式是“小步快走”,即每次钳夹一小部分组织,采用快档迅速打开组织,既借鉴了小钳夹法的压榨作用又充分利用了超声刀的止血功能。本研究结果表明,此方式利于暴露脾内血管、减少脾实质出血,尤其切除界面与脾脏无血管平面不一致时可显露其中的血管单独用可吸收夹夹闭。由于脾脏血管不像肝内管道那样清晰,钳夹遇到阻力时也将当前组织压榨后当作血管处理。经此方式处理后的脾脏断面需要处理的出血部位少,且更容易止住。
切除脾脏时,以往的观念与研究热点是如何使用电外科工具、能量平台使脾脏断面出血物理凝固[19],这是基于脾脏实质较脆、脾脏内血管难以显露而做出的无奈之举。但操作中我们也发现,有时较小的出血点也难以电凝止血,多次凝固后的一大片焦痂下仍有活动性出血,这估计与小血管缩回脾实质电外科能量难以传达到血管断端有关,这也是部分脾切除的难点、决定手术成功的关键之一。笔者认为,与其被动止血不如主动预防出血,其核心手段即精细化的血管解剖、采用超声刀钳夹法。术中两者相辅相成。钳夹法主动发现脾实质内小血管,减少脾门离断血管的数量而保持残脾血供;如果断面出现活动性出血又不能直接凝固止血时,可将脾门处靠近断面的三级血管分支阻断,达到减少出血的目的。当然,脾门血管的精细解剖需要对脾门结构充分认识,镜下各种器械应用合理,我们解剖的目的不是淋巴结清扫而是显露,因此,暴露血管的二三级分支走行而无需“骨骼化”,这在腔镜下经过短期训练是完全可以做到的。本组术后随访2年左右,增强CT显示残余脾脏血供良好,血管无栓塞,白细胞、血小板指标正常,表明精细解剖以保留部分脾蒂血管从而保留脾脏血供的重要性。
进行本研究前,笔者团队曾为1例脾占位患者行“L”形切除,即在切除下极后未发现病灶(由于经验不足,实际切缘与术前规划有较大偏差),术中超声定位发现包块位于脾门后方边缘的实质内,遂在未进一步解剖血管的情况下,于脾门后方平行脾脏长轴切取部分组织,使切除断面呈“L”形,术中出血少于200 mL,成功保脾。这也是本研究的前身与灵感来源。本研究收治的外伤性脾破裂病例中,入组患者血流动力学均稳定,术前影像学评估为Ⅱ~Ⅲ级脾破裂,进入腹腔后采用隧道法钝性掏通脾蒂后方,采用镜下血管阻断钳阻断脾蒂,待游离出脾动静脉后将阻断钳换至脾动静脉主干,其余操作不变。由于外伤性脾破裂对保留脾脏的形态、部位无硬性要求,因此在满足保留约30%脾组织、血供后可灵活设计切取范围。
综上所述,对于适合保脾的患者,腹腔镜下脾门血管精细解剖+超声刀钳夹法较以往做法具有一定优势,应用于脾脏部分切除术安全、可行。
