阿帕替尼治疗小细胞肺癌的临床疗效及安全性*
2019-04-18金钊宋蕾崔建琦赵艳滨
金钊 宋蕾 崔建琦 赵艳滨
小细胞肺癌是肺癌的一种病理亚型,占肺癌的15%~20%[1-2]。化疗联合放疗仍为小细胞肺癌的主要治疗手段[3]。尽管初始化放疗疗效明显,但多数患者短期内出现复发及转移,且复治后的治疗有效率大幅降低,使得局限期小细胞肺癌的中位生存期不超过24 个月,广泛期不超过12 个月[4],5年生存率不足5%[5]。近10余年分子靶向药物明显改善了非小细胞肺癌的预后,但针对小细胞肺癌的靶向治疗却未见突破,因此寻找一种不良反应轻、疗效好的新药尤为重要。血管生成在肿瘤生长和转移过程中发挥重要作用。在癌基因的激活诱导下,趋使肿瘤内血管生成,使得内外部肿瘤细胞均可得到充足氧气和营养物质,肿瘤体积迅速增大。因此,阻断肿瘤血管生成过程中的任一环节均可使肿瘤生长受到限制[6]。血管内皮生长因子是其中作用最强、最重要的血管生成因子[7]。阿帕替尼作为中国自主研发的抗血管生成药物,通过与VEGFR-2结合,竞争性抑制VEGF与VEGFR-2结合及VEGFR-2自动磷酸化,从而发挥强有力的抗肿瘤作用[8],目前批准用于胃癌二线及以上治疗[9],但对于小细胞肺癌的研究仍在探索中。本研究收集2016年1月至2017年12月哈尔滨医科大学附属肿瘤医院收治41例多线治疗失败后的小细胞肺癌患者临床资料,探讨使用阿帕替尼在晚期小细胞肺癌患者治疗中的应用,以延长晚期小细胞肺癌患者的生存期。
1 材料与方法
1.1 病例资料
选取2016年1月至2017年12月哈尔滨医科大学附属肿瘤医院收治并经病理学确诊的41例小细胞肺癌患者,其中男性24 例,女性17 例。所有患者均接受2 线及以上化疗或放射治疗。其中脑转移10例。所有病例信息完整,诊疗过程详实。
1.2 方法
1.2.1 治疗方法 对多线治疗失败的晚期小细胞肺癌患者给予阿帕替尼靶向治疗。患者口服阿帕替尼500 mg/d,直至病情进展或出现不可耐受的不良反应。若出现3~4 级阿帕替尼相关不良事件,则减量至250 mg/d,每2个周期进行1次疗效评估。
1.2.2 疗效评定标准 按照RECIST 1.1 版标准进行疗效评价,分为完全缓解(completely response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD)。CR+PR 为客观缓解率(objective response rate,ORR)。CR+PR+SD为疾病控制率(disease control rate,DCR)。
1.2.3 不良反应 口服阿帕替尼可能出现的不良反应包括手足综合征、出血、高血压、蛋白尿、疲乏。观察不良反应与患者疗效之间的关系,并对相关不良反应给予对症治疗,不良反应严重时需要停药。采用NCICTCAE 4.0版标准评价不良反应,分级1~4级。
1.2.4 随访 患者每周监测血压1 次,每2 周复查血常规、尿常规、肝肾功和心电图,每6 周进行CT 扫描。随访截至2018年5月。无进展生存时间(progression free survival,PFS)定义为首次服用阿帕替尼至肿瘤进展或死亡时间。
1.3 统计学分析
采用SPSS 22.0软件进行统计学分析。频数资料用百分率(%)表示,频数资料组间比较采用χ2检验,计量资料采用描述,生存分析采用Kaplan-Meier法绘制生存曲线。生存期组间比较采用Log-rank法。以P<0.05为差异具有统计学意义。
2 结果
2.1 临床疗效分析
本研究共纳入41例小细胞肺癌患者口服阿帕替尼(表1)。至随访截止,ORR 为12.19%(5/41),DCR为80.48%(33/41)(表2),中位PFS 为4.1 个月(图1)。其中10例脑转移患者中2例疗效达到PR。
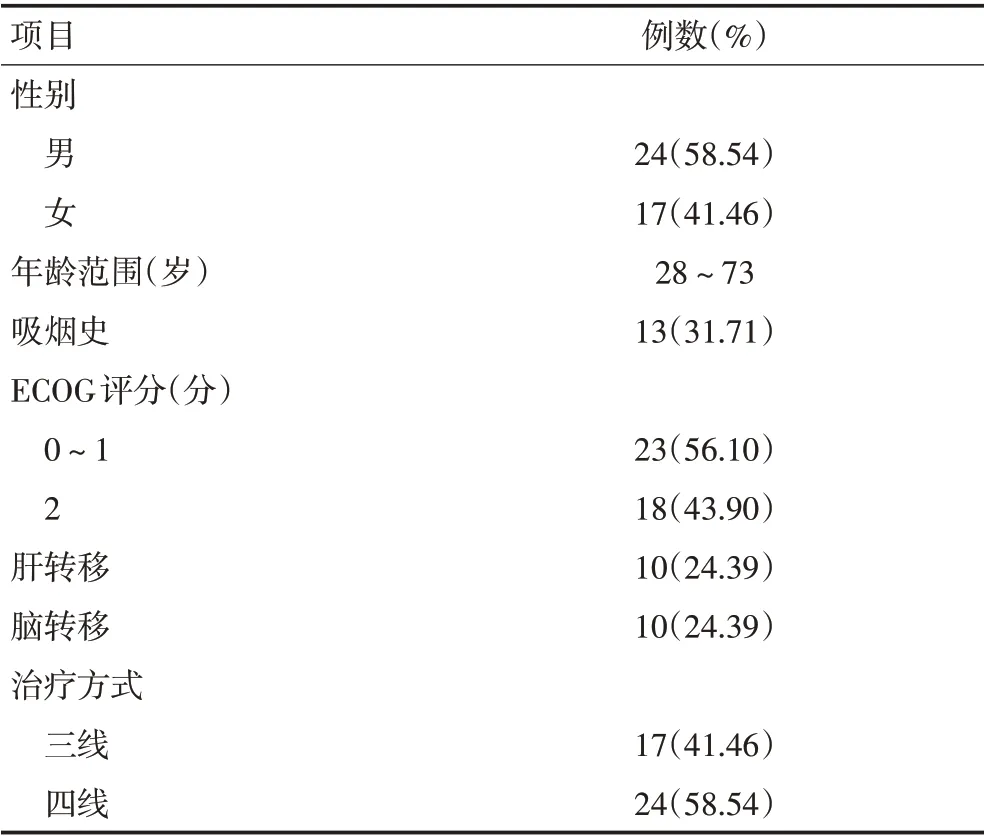
表1 41例小细胞肺癌患者临床资料

表2 不同组患者对阿帕替尼的临床反应 例
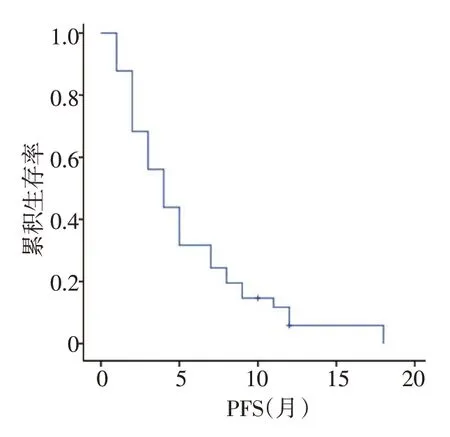
图1 41例小细胞肺癌患者PFS生存曲线
2.2 不良反应及安全性分析
不良反应中高血压21 例(51.21%),其中Ⅰ级10例(24.39%),Ⅱ级5例(12.19%),Ⅲ级6例(14.63%),无Ⅳ级。手足综合征13 例(31.70%),其中Ⅰ级7 例(17.07%),Ⅱ级5例(12.19%),Ⅲ级1例(2.43%)。蛋白尿12 例(29.26%),其中Ⅰ级9 例(21.95%),Ⅱ级3例(7.31%),无Ⅱ级以上蛋白尿。疲乏9例(21.95%),其中Ⅰ级7 例(17.07%),Ⅱ级2 例(4.87%)。转氨酶升高3 例(7.31%),均为Ⅰ级。其他少见不良反应有恶心、呕吐、头晕、血液学毒性等,其中头疼、恶心呕吐症状主要发生在脑转移患者,主要为Ⅰ~Ⅱ级,多无需特殊处理(表3)。

表3 阿帕替尼治疗41例小细胞肺癌患者的不良反应 例
3 讨论
小细胞肺癌是恶性程度高、侵袭性强、易复发转移的难治性恶性肿瘤。虽经10 余年,小细胞肺癌的发病机制、驱动基因、新药研发等领域研究有所进展,但治疗模式和疗效未见突破。近年抗血管生成治疗在各大肿瘤的治疗中取得一定的疗效,为探索抗血管生成治疗在小细胞肺癌中的疗效,基于ALTER 1202 临床研究[10]中安罗替尼的优异表现,安罗替尼治疗后患者总生存期(overall survival,OS)显著延长2.4个月,死亡风险下降47%,已被批准作为小细胞肺癌三线及以上治疗的Ⅱ级推荐。
对小细胞肺癌的研究显示,细胞在乏氧状态下,VEGFR表达显著增加,而阿帕替尼是一个强效VEGFR-2 的抑制剂。因此,近年有研究探索阿帕替尼作为广泛期小细胞肺癌维持治疗的效果。一项关于阿帕替尼用于难治性广泛期小细胞肺癌的单臂多中心Ⅱ期前瞻性研究[11],招募40例经过2次或3次化疗的广泛期小细胞肺癌患者,1 次/d 接受初始剂量为500 mg的阿帕替尼。中位PFS和OS分别为3.0个月和5.8个月。最常观察到的3 级或以上与治疗相关的不良事件为高血压、手足综合征、L-γ-谷氨酰转移酶升高。另一项关于难治性小细胞肺癌患者的回顾性研究[12],选取22例二线治疗失败的小细胞肺癌患者,口服阿帕替尼的初始剂量为500 mg/d,直至疾病进展或出现不可耐受的不良反应。中位PFS 为135 d,DCR为86.4%。主要的3 级或4 级不良反应是高血压(22.7%)、手足综合征(13.6%)和蛋白尿(9.1%)。另一项单中心回顾性研究[13]广泛期小细胞肺癌的治疗,23例患者的PFS为4.1个月,OS为12.5个月,常见不良反应为手足综合征、高血压、疲乏等。有研究[14]探索了阿帕替尼作为广泛期小细胞肺癌的维持治疗。对1 例在4 线化疗失败后接受了阿帕替尼的挽救治疗的小细胞肺癌患者进行评估,1 个月后达到PR,最终获得了5 个月的PFS,阿帕替尼作为多线治疗后的挽救方案有一定疗效。上述研究均表明,阿帕替尼有可能适用于小细胞肺癌三线治疗方案,甚至是标准二线治疗方案。
本研究通过对接受阿帕替尼治疗的41例晚期小细胞肺癌患者临床资料进行分析,ORR为12.19%(5/41),DCR为80.48%(33/41),中位PFS为4.1个月。研究结果显示在二线及以上治疗情况下,阿帕替尼治疗小细胞肺癌治疗有一定有效率。最常见的不良事件为高血压(51.21%)、手足综合征(31.70%)、蛋白尿(29.26%)、疲乏(21.95%),其中3~4级不良反应为高血压(14.63%)、手足综合征(2.44%),上述不良反应均可通过减少药物剂量得到缓解。
有研究尝试探索阿帕替尼联合化疗治疗小细胞肺癌的临床有效性。一项关于阿帕替尼联合化疗用于治疗失败的广泛期小细胞肺癌的研究[15],使用阿帕替尼联合多西他赛用于四线治疗后进展的小细胞肺癌患者,治疗3 d 后患者气短症状及颜面浮肿好转,20 d 复查胸部CT 提示左肺不张明显减轻,疗效为PR。但在治疗35 d 时,由于心包受侵诱发心律失常,患者死亡,考虑与阿帕替尼无关。晚期小细胞肺癌的治疗能达到PR,说明该治疗有效,值得进一步扩大患者数量进行探索。此研究也为今后进一步探索化疗联合抗血管生成治疗晚期小细胞肺癌提供了理论依据。
综上所述,对于多线以上治疗失败的晚期小细胞肺癌患者,服用阿帕替尼250~500 mg/d 能够延长患者的生存时间,阿帕替尼的不良反应与既往临床试验报道的类似,多数患者可耐受。但目前关于阿帕替尼治疗肺癌的研究较少,如何寻找获益人群以及如何联合其他治疗手段,尚需大样本及对照试验进一步探讨。
