免疫检查点抑制剂治疗尿路上皮癌的临床经验
2019-04-18王喆吕程程付水毕缓付成曾宇
王喆 吕程程 付水 毕缓 付成 曾宇
尿路上皮癌是泌尿系统最常见的恶性肿瘤之一。肌层浸润性尿路上皮癌恶性程度高,易出现转移且预后差,传统的以铂类为基础的联合化疗方案只能使患者的中位总生存时间维持在15个月左右[1]。过去30多年,局部晚期或转移性尿路上皮癌的5年生存率一直不超过5%[2],近年来针对程序性死亡受体(programmed cell death protein-1,PD-1)及程序性死亡配体1(programmed cell death protein-ligand 1,PD-L1)为靶点的免疫检查点抑制剂(immune checkpoint inhibitors,ICIs)应用于临床,使局部晚期或转移性尿路上皮癌系统治疗有了突破性的进展。目前,美国食品药品监督管理局(FDA)批准了atezolizumab、pembrolizumab、nivolumab、avelumab、durvalumab 5种免疫检查点抑制剂(immune checkpoint inhibitors,ICIs)药物,用于治疗铂类化疗失败或不耐受化疗的局部晚期或转移性尿路上皮癌患者。以上5种药物在临床试验中的客观有效率(overall response rate,ORR)在20%左右,均优于传统二线化疗;而在肿瘤组织中PD-L1阳性表达的患者,其ORR更接近30%[3-7]。本研究旨在探讨ICIs在临床应用中治疗尿路上皮癌的临床有效性与安全性。
1 材料与方法
1.1 病例资料
回顾性分析2016年7月至2019年4月32例于辽宁省肿瘤医院使用ICIs治疗尿路上皮癌患者的临床资料,其中男性23例、女性9例,年龄范围为51~91岁,中位年龄为67岁。所有患者均经病理学证实为原发性肌层浸润性或转移性尿路上皮癌。32例患者中原发肿瘤为9例、转移性肿瘤为23例,主要转移部位包括淋巴结、肾上腺、肝脏等内脏、肺及骨骼等部位。
1.2 方法
1.2.1 ICIs药物使用情况 32例患者中20例为经至少1 种含铂类(顺铂、卡铂等)化疗失败者,12 例评估为不能耐受化疗。其中膀胱癌13 例、输尿管癌12例、肾盂癌7 例。32 例患者中自行选择pembrolizumab和nivolumab分别为19例、用药方案每3周/次和13例、用药方案每2周/次,均静脉滴注(3 mg/kg)。使用nivolumab 和pembrolizumab 治疗患者的中位用药周期分别为7个周期、约14周和5个周期、约15周。
1.2.2 PD-L1表达检测 32例患者中15例自愿行组织中PD-L1表达检测,并均使用VENTANA SP263试剂盒(瑞士罗氏公司),17 例未行检测。PD-L1 阳性定义:如肿瘤浸润免疫细胞(immune cell,IC)比例>1%,即肿瘤细胞(tumor cell,TC)或IC 比例均≥25%;如IC 比例≤1%,即TC 比例≥25%或IC 为100%。反之则定义为PD-L1阴性。15例患者中PD-L1阳性和阴性表达分别为12例和3例。
1.2.3 疗效评价 采用实体瘤疗效评价标准1.1(response evaluation criteria in solid tumors,RECIST 1.1),每2 个月行肿瘤影像学检查评价疗效。分为完全缓解(complete remission,CR),部分缓解(partial remission,PR),疾病稳定(stable disease,SD)和疾病进展(progression disease,PD)。疾病控制率(disease control rate,DCR)为确认的CR、PR、SD 患者占总患者的比例,客观有效率(overall response rate,ORR)为CR、PR 患者占总患者的比例,无疾病进展生存(progression free survival,PFS)期为患者行ICIs治疗至疾病进展或任何原因停止治疗的时间间隔,总生存(overall survival,OS)期为患者行ICIs治疗至任何原因死亡的时间间隔。
1.2.4 随访 所有患者随访通过电话、门诊及住院信息收集。随访内容包括患者生存状况,ECOG 评分,血、尿常规,血生化,甲状腺功能,心功能,针对病灶部位的CT、膀胱镜检查等,同时严密监测免疫相关不良事件(immune-related adverse events,irAEs),并根据常见不良反应术语评定标准(common terminology criteria for adverse events,CTCAE)5.0 版评定irAEs分级。随访截止时间为2019年4月,随访时间1~33个月,中位随访时间为6个月,无失访率。
1.3 统计学分析
应用SPSS 25.0软件进行统计学分析。年龄和生存时间采用中位数表示,分类变量采用计数及百分数表示,生存分析采用Kaplan-Meier法计算。
2 结果
2.1 疗效分析
32 例患者中4 例CR、7 例PR、5 例SD、9 例PD、7例尚未到达评估时间,总ORR 为44.0%(11/25)、总DCR为64.0%(16/25),至少经1种含铂类化疗失败患者的ORR为33.3%(5/15)、未经铂类化疗患者ORR为60.0%(6/10),见表1。部分PR及CR患者影像学表现见图1。
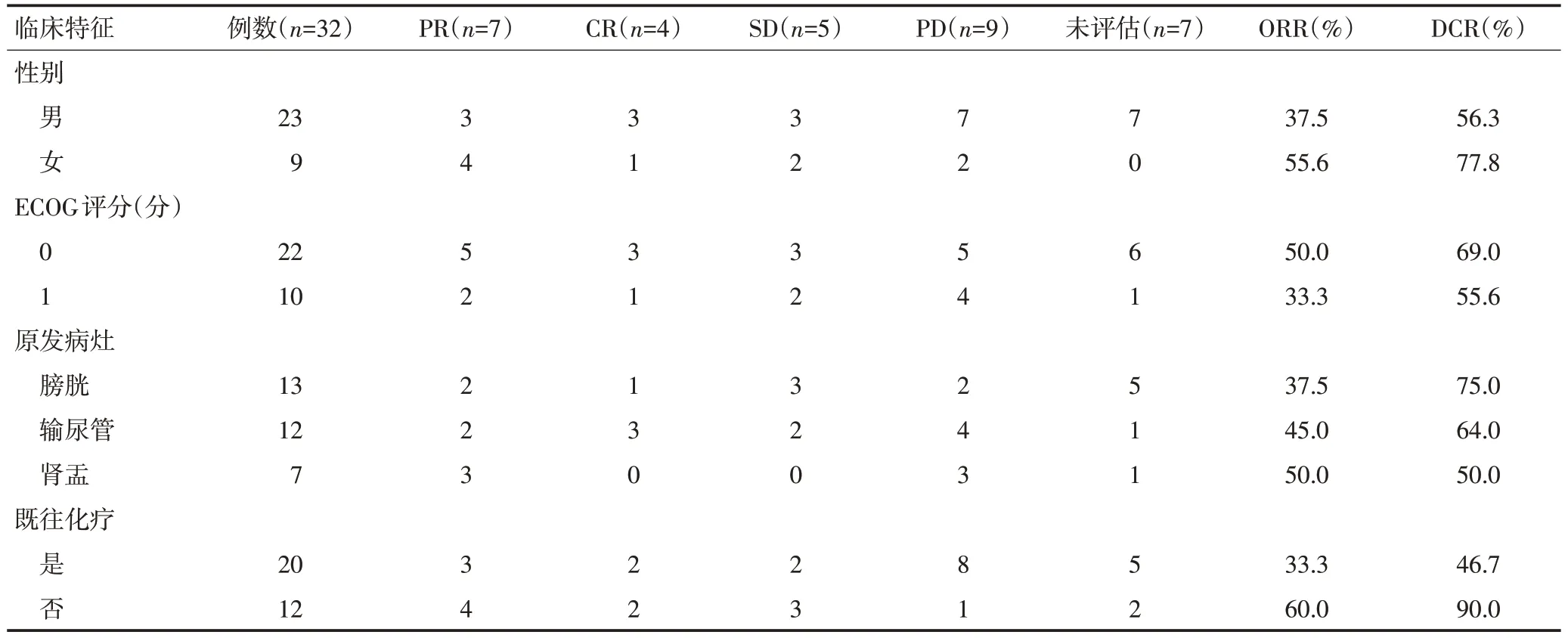
表1 32例患者的ICIs治疗疗效分析
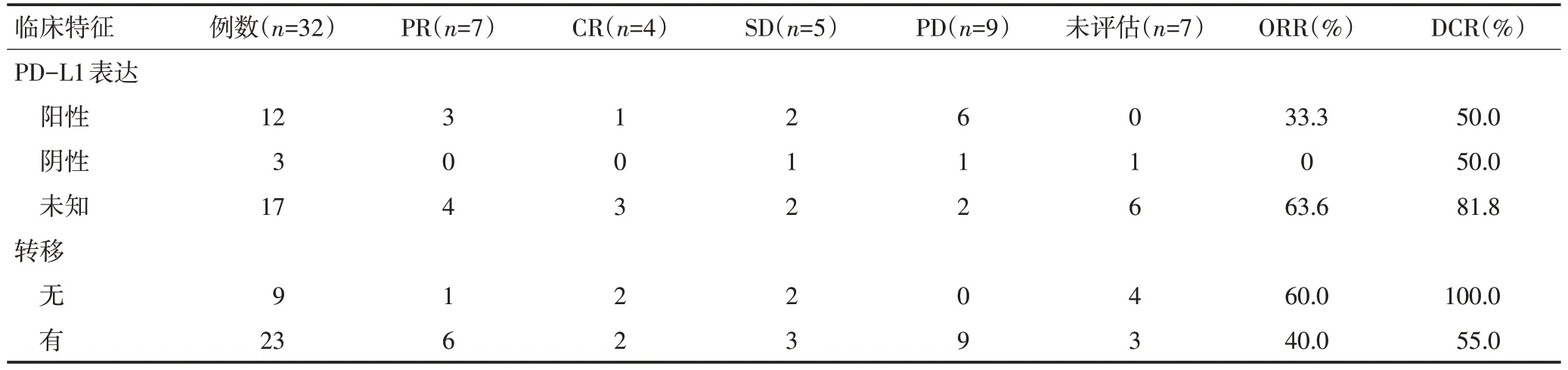
表1 32例患者的ICIs治疗疗效分析(续表1)

图1 部分PR及CR患者影像学表现
患者中位PFS 为8 个月,中位OS 为11 个月(图2)。32例患者中16例停用ICIs,9例出现PD,中断治疗的最常见原因是PD,其次是经济负担和irAEs。11例使用ICIs治疗后疾病得到缓解(PR+CR),其中5例在停药后随访期间内未发现肿瘤复发(图3)。
根据RICIST 1.1标准,32例患者共有43个可测量病灶,其中淋巴结转移为21个、肝脏等内脏转移8个、肺转移7个、骨转移4个、肾上腺转移3个(表2)。CR、PR、SD患者多为原位肿瘤或最多不超过2个转移病灶;PD患者多为存在2个及以上的转移病灶。32例患者中同时存在2个及以上转移病灶的共13例(40.6%),13例中包括9例PD患者。
2.2 不良反应
使用pembrolizumab 和nivolumab 治疗,患者耐受性良好,32例患者中29例出现irAEs,大多数irAEs为1~2 级,最常见的irAEs 为乏力、肝功能异常、皮疹、甲减等(表3)。32 例患者中2 例因出现严重和持续的irAEs导致治疗中断,5例出现irAEs后行静脉滴注皮质类固醇治疗,1 例发生与irAEs 可能相关的死亡(重度血小板减少)。

图2 32例患者使用ICIs治疗后生存分析

图3 11例CR和PR患者使用ICIs的治疗、起效及持续时间

表2 不同转移部位的ICIs疗效分析
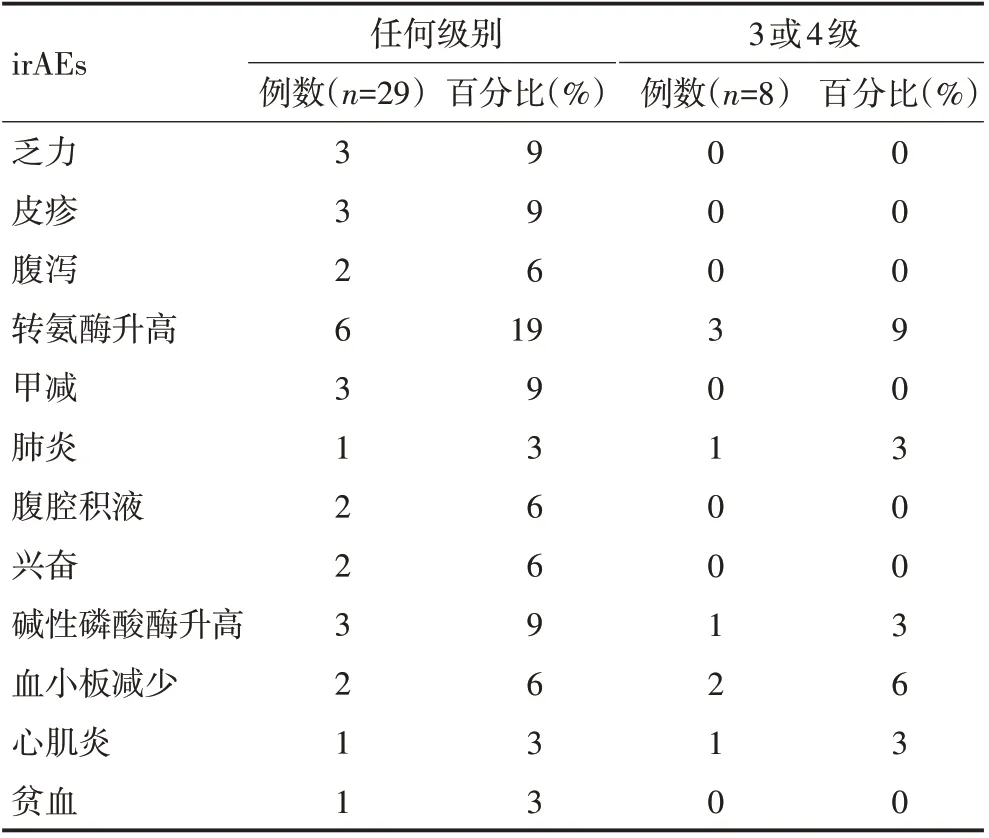
表3 32例患者irAEs分析
3 讨论
免疫检查点治疗是使用特异性抗体阻断PD-1与PD-L1结合,抑制该通路的激活,解除免疫检查点对T淋巴细胞的抑制状态,恢复T细胞对肿瘤细胞的杀伤性。在ICIs治疗尿路上皮癌的临床试验中,癌组织中PD-L1 表达水平被认为是ICIs 疗效的预测标记物之一[8],但也存在部分PD-L1表达阴性患者在ICIs治疗中获益。
本研究中12例PD-L1表达患者的ORR为33.3%(4/12),略高于报道中的30%[9],但与总ORR的44.0%(11/25)相比并未体现出人群优势,表明仅检测PDL1 表达对疗效预测的局限性。研究表明,肿瘤突变负荷(tumor mutation burden,TMB)高及存在DNA 错配修复缺陷(deficient mismatch repair,DMMR)患者使用ICIs 治疗有效率更高[10]。尿路上皮癌在所有实体肿瘤中TMB 较高,位于第4 位[11],这可能是其对ICIs治疗有效率较高的原因之一。目前研究提示,TMB及DMMR 可作为ICIs 治疗获益的补充标记物[8,12]。本研究中,总ORR 偏高的主要原因可能是研究样本量过小,存在选择偏倚。此外,患者整体的疾病负荷可能与临床试验入组患者不尽相同,如在临床试验中均为铂类一线化疗失败或不耐受化疗的晚期肿瘤患者,而本研究中9例患者因合并多种基础疾病等原因存在手术禁忌或被评估为不能耐受化疗,直接使用ICIs治疗。本研究的9例患者因未行铂类化疗,实为一线治疗使用ICIs,其中已行影像评估的5例患者ORR 高达60.0%(3/5),临床获益较为显著。目前,ICIs作为一线治疗转移性或局部晚期尿路上皮癌,或作为新辅助治疗原发肿瘤具有颇为乐观的前景[11,13]。
ICIs治疗在临床实践中由于费用较高,周期也是一个重要问题,多数临床试验设定最长ICIs治疗时间为2年,使绝大多数患者无法承受。本研究中,CR或PR 患者多数维持治疗时间在8 个月之内。截至目前,尚未有CR或PR患者因停药而发生PD。
irAEs是ICIs临床使用中需重点关注的问题。前期临床试验数据显示[3-7],大多数患者发生irAEs 为1~2 级的轻至中度不良事件,但严重或危及生命的3~4级irAEs也时有发生。本研究的irAEs死亡率约为3.1%(1/32),与文献报道约为2%[14]相近。irAEs是一种延迟性反应,持续时间较长。irAEs 的确切发病机制尚不清楚,irAEs 也可能因ICIs 药物的不同而不一致,而对治疗有持久反应的患者可能更易发生irAEs,但这种关联尚不完全清楚[15]。
综上所述,ICIs用于铂类化疗失败的局部晚期或转移性尿路上皮癌疗效明确,ICIs已被列入相关指南的首选推荐二线治疗方案。对于不能耐受或不愿接受化疗,或不适合手术的原发性尿路上皮癌患者,一线使用ICIs也是临床中可行的治疗方案。由于irAEs可能发生较晚,甚至在终止治疗之后仍可能出现长期慢性并发症,因此对irAEs 需早期识别和给予持续治疗。
