低品位锰矿石在NH4HSO4H2O2体系中的浸出行为
2019-04-17康禄华苏仕军丁桑岚孙维义
康禄华,朱 鹏,赵 珊,苏仕军,丁桑岚,孙维义
(四川大学建筑与环境学院,四川成都 610065)
Mn3O4广泛应用于软磁材料、催化材料和电极电容材料制备领域[1-4]。目前,Mn3O4一般是利用氨水将硫酸锰溶液pH调至大于8.5,使Mn2+转化为Mn(OH)2,然后加入H2O2或O2将其氧化而得到,同时也得到(NH4)2SO4溶液[5-9]。生产过程中,Mn2+难以完全转化,导致所得硫酸铵溶液中含有一定量MnSO4,所以Mn有部分损失,而且(NH4)2SO4品质不高。
(NH4)2SO4在213~308 ℃范围内可以分解为NH3和NH4HSO4[10-12]。利用NH4HSO4浸出锰矿石可得到MnSO4,而分解产生的NH3则可作为添加剂调节MnSO4溶液pH生产Mn3O4,形成闭路循环,避免含有MnSO4杂质的(NH4)2SO4产生。目前,对于(NH4)2SO4热解的研究较多,但对于NH4HSO4浸出锰矿石的研究相对较少。
试验研究以NH4HSO4为浸出剂、H2O2为还原剂,从低品位锰矿石中浸出锰,旨在提供一种低品位锰矿石资源回收闭路循环工艺。
1 试验部分
1.1 试验原料与试剂
试验所用低品位锰矿石取自四川汉源,粒度0.178 mm,XPF和XRD分析结果分别见表1、图1。矿石中,锰质量分数为14.09%,品位较低;锰主要以MnCO3、Mn2O3和MnO(OH)形式存在,铁主要以Fe2O3形式存在。

表1 低品位锰矿石的元素组成 %

图1 低品位锰矿石的XRD分析结果
硫酸氢铵,过氧化氢,抗坏血酸,冰乙酸,无水乙酸钠,邻菲罗啉,焦磷酸钾,高碘酸钾,硫酸(98%),硝酸,磷酸等,均为分析纯市售试剂。
1.2 试验仪器
BSA124S型电子分析天平,JJ-1型精密增力电动搅拌器,DK-98-ⅡA型电热恒温水浴锅,ZYUPK-Ⅱ-5T型卓越系列超纯水机,101-2AB型电热鼓风干燥箱,V-1200型可见分光光度计,XRF-1800型X射线荧光光谱仪,飞利浦X’PerXPD型X射线衍射仪。
1.3 试验原理与方法
低品位锰矿石中,锰主要以MnCO3、Mn2O3和MnO(OH)形式存在。用硫酸氢铵与双氧水共同浸出锰,反应如下:

(1)

(2)

(3)

(4)
取一定质量矿石于1 L圆底三口烧瓶中,固定在恒温水浴锅中。配制一定比例硫酸氢铵和双氧水混合溶液500 mL,倒入三口烧瓶中,设定温度后开启搅拌并计时。反应一定时间后,取浸出液测定锰、铁质量浓度,用式(5)计算锰、铁浸出率。
(5)
式中:m为矿石中锰、铁总质量,g;ρ为浸出液中锰、铁质量浓度,mg/L;V为浸出液体积,L。
1.4 分析方法
矿石物相用X射线衍射法分析,锰、铁含量分别用硫酸亚铁铵滴定法(GB1506—2002)和《铁矿石 全铁含量的测定 三氯化钛还原重铬酸钾滴定法》(GB/T 6730.65—2009)测定。浸出液中锰、铁质量浓度分别采用《水质锰的测定 高碘酸钾分光光度法》(GB 11906—1989)和《工业用化工产品 铁含量测定的通用方法 1,10-菲啰啉分光光度法》(GB/T 3049—2006)测定。
2 试验结果与讨论
2.1 液固体积质量比对锰、铁浸出率的影响
在硫酸氢氨浓度0.5 mol/L、双氧水浓度0.5 mol/L、浸出温度70 ℃、浸出时间180 min条件下,考察液固体积质量比对锰、铁浸出率的影响,试验结果如图2所示。

图2 液固体积质量比对锰、铁浸出率的影响
由图2看出:液固体积质量比从10/1增大到30/1,Mn浸出率从50.5%提高到99.07%,之后几乎保持不变;铁浸出率随液固体积质量比增大缓慢提高,最高只有13.7%。从节约成本角度考虑,确定液固体积质量比以30/1为最佳,此时铁浸出率仅为9.78%。
2.2 硫酸氢铵浓度对锰、铁浸出率的影响
在液固体积质量比30/1、双氧水浓度0.5 mol/L、浸出温度70 ℃、浸出时间180 min条件下,考察硫酸氢氨浓度对锰、铁浸出率的影响,试验结果如图3所示。
由图3看出,随硫酸氢氨浓度增大,锰浸出率先迅速提高,后趋于平稳,而铁浸出率缓慢提高。主要原因可能是,硫酸氢氨浓度过低时,不能与锰矿石充分反应,锰浸出不完全,浸出率较低;但硫酸氢氨浓度较大时,不仅易造成浪费,也可能引起矿石中其他杂质元素,如Fe、Ca、Mg、Al等被一同浸出:所以,硫酸氢氨浓度不宜太高,以0.5 mol/L为宜。
2.3 双氧水浓度对锰、铁浸出率的影响
在液固体积质量比30/1、硫酸氢氨浓度0.5 mol/L、浸出温度70 ℃、浸出时间为180 min条件下,考察双氧水浓度对锰、铁浸出率的影响,试验结果如图4所示。
由图4看出:未加入双氧水时,锰浸出率只有47.43%;随双氧水浓度增大,锰浸出率逐渐提高,双氧水浓度增至0.2 mol/L时,锰浸出率达最高,之后趋于稳定;而铁浸出率受双氧水浓度影响甚微。综合考虑,确定双氧水浓度以0.2 mol/L为最佳,此条件下Fe浸出率只有9.57%。
2.4 浸出温度对锰、铁浸出率的影响
在液固体积质量比30/1、硫酸氢氨浓度0.5 mol/L、双氧水浓度0.2 mol/L、浸出时间180 min条件下,考察浸出温度对锰、铁浸出率的影响,试验结果如图5所示。可以看出,随浸出温度升高,锰浸出率先升高,达到最大98.77%后又逐渐降低。其原因可能是,随温度升高,分子间运动加快,从而促进分子间碰撞,使反应更充分,有利于锰的浸出;但继续升温,还原剂双氧水变得不稳定,易发生分解[13-14],使溶液中双氧水浓度降低,导致锰浸出率降低。铁浸出率受温度影响较小,变化不大。综合考虑,确定浸出温度以50 ℃为宜。

图5 浸出温度对锰、铁浸出率的影响
2.5 浸出时间对锰、铁浸出率的影响
在液固体积质量比30/1、硫酸氢氨浓度0.5 mol/L、双氧水浓度0.2 mol/L、浸出温度50 ℃条件下,考察浸出时间对锰、铁浸出率的影响。试验结果如图6所示。

图6 浸出时间对锰、铁浸出率的影响
由图6看出:用硫酸氢氨+双氧水浸出低品位锰矿石,浸出速度很快,浸出5 min时,锰浸出率即达63.31%,随后迅速提高,在浸出60 min后达98.22%;铁浸出率随浸出进行缓慢提高。综合考虑,确定适宜的浸出时间为60 min,此时铁浸出率仅为8.52%。
2.6 浸出渣的物相组成
将矿石浸出渣于105 ℃下烘干5 h,用XRD测定其物相组成,结果如图7所示。

图7 低品位锰矿石浸出渣的XRD分析结果
由图7看出:浸出渣中,硅、铁含量较高;仅残存少量三价锰化合物,如MnO(OH)和Mn2O3,但量已非常低,锰的浸出相对较完全。浸出渣中元素组成见表2。可以看出:Mn残余量非常低;Fe含量相比于原矿有所下降,说明有部分Fe被浸出;而Ca以CaCO3形式存在于矿石中,容易与硫酸氢铵反应使矿渣中Ca含量有所降低;Al含量略有升高,其他如Mg、Ti、Zn、Cr、Co等杂质含量几乎没有变化。
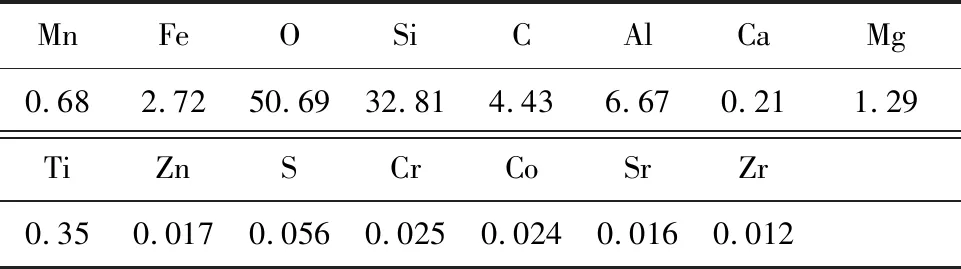
表2 低品位锰矿石浸出渣的元素组成 %
3 结论
以硫酸氢铵作浸出剂、双氧水作氧化剂,从低品位锰矿石中浸出锰是可行的。适宜条件下,锰浸出率达96%以上,而铁浸出率较低,可实现锰与铁及其他杂质元素的分离。该工艺操作简单,生产成本不高,用于处理低品位锰矿石可取得较好效果。
