V2O5/TiO2催化剂中Sb2O3掺杂对硫酸氢铵分解行为的影响
2019-05-07高磊祁贵生徐文青朱廷钰
高磊,祁贵生,徐文青,朱廷钰
(1.中北大学超重力化工过程山西省重点实验室,山西 太原 030051; 2.中国科学院过程工程研究所湿法冶金与清洁生产技术国家工程实验室,北京 100190)
氮氧化物是雾霾的重要前驱体之一,对生态环境和人体健康造成巨大危害[1-2]。低温SCR技术脱硝效率高,无二次污染。催化剂作为低温SCR的核心,容易发生硫酸氢铵使催化剂中毒问题[3-4]。硫酸氢铵会堵塞催化剂的孔道结构,覆盖活性位点,引起SCR脱硝活性下降[5-6]。目前硫酸氢铵沉积问题已成为低温SCR实现工业化应用的主要障碍。国内外学者对低温SCR中V2O5/AC[7-9]、V2O5/TiO2与V2O5-WO3/TiO2[10-11]表面硫酸氢铵的分解进行详细的研究。关于催化剂改性方面,化学元素锑由于具有较好的抗硫抗水性而被用作催化剂助剂[12-13]。本文研究Sb2O3-V2O5/TiO2中助剂Sb2O3的掺杂对催化剂表面硫酸氢铵分解行为的影响。
1 实验部分
1.1 试剂与仪器
偏钒酸铵、草酸、三氯化锑、硫酸氢铵、二氧化钛(锐钛,10~25 nm)均为分析纯。
101-1AB型电热鼓风干燥箱;SRJX-4-13马弗炉;Bruker-TensorⅡ型傅里叶变换红外光谱仪(FTIR);PANalytical B.V.-Empyrean型X射线衍射仪;Quantachrome-Autosorb-ZQ-XR-C型物理吸附仪;Thermo Scientific-Escalab 250XI型X射线光电子能谱仪;Seiko-TG-DTA6300型热重分析仪;Hidden-QGA型质谱仪。
1.2 催化剂制备
1.2.1 Sb2O3-V2O5/TiO2催化剂制备 采用一步浸渍法制备不同锑含量的Sb2O3-V2O5/TiO2催化剂。将偏钒酸铵、草酸和三氯化锑溶解于去离子水,搅拌30 min,使之形成活性组分的浸渍液。加入纳米级TiO2载体,在60 ℃水浴条件下恒温搅拌2 h。利用旋转蒸发仪60 ℃水浴将水分蒸干。放入烘箱中,110 ℃干燥过夜。放入马弗炉,在500 ℃焙烧4 h。经压片、粉碎、研磨、筛分,得到40~60目固体颗粒,进行活性评价,80目以上的粉末用于硫酸氢铵的负载以及相关表征测试。其中,V2O5含量全部为2%,Sb2O3含量1%,2%,3%,分别简写为V/Ti、1Sb2V/Ti、2Sb2V/Ti、3Sb2V/Ti催化剂。
1.2.2 硫酸氢铵预负载 将硫酸氢铵溶解于去离子水,得到硫酸氢铵溶液。加入催化剂粉末,60 ℃水浴下充分搅拌2 h,用旋转蒸发仪60 ℃水浴将水分蒸干。放入烘箱干燥过夜。经压片、粉碎、研磨、筛分,得到不同目数样品。其中硫酸氢铵的负载量全部为10%,分别简写为ABS-V/Ti、ABS-1Sb2V/Ti、ABS-2Sb2V/Ti、ABS-3Sb2V/Ti。
1.3 催化剂性能评价
1.3.1 催化剂活性评价 在固定床石英反应管中进行,反应温度150~300 ℃,通过程序升温加热炉进行控制,催化剂用量350 mg。反应气体主要为:400 mg/m3NO、400 mg/m3NH3,16%O2,N2作为反应平衡气。气体流量500 mL/min,空速60 000 h-1。采用FTIR在线检测NOx进出口浓度。计算NOx转化率。

(1)
NOx=NO+NO2
(2)
1.3.2 催化剂抗硫抗水实验 在固定床石英反应管中进行,反应温度220 ℃,通过程序升温加热炉进行控制,催化剂用量350 mg。反应气体主要为:400 mg/m3NO,400 mg/m3NH3,16%O2,400 mg/m3SO2,10%H2O,N2作为反应平衡气。气体流量500 mL/min,空速60 000 h-1。采用FTIR在线检测NOx进出口浓度。其中NOx转化率的计算按照公式(1)和(2)。
1.4 催化剂表征
1.4.1 XRD测试 在X射线衍射仪上进行。以Cu靶,Kα作为发射源,扫描范围5~90°,扫描步长为0.016 7°。
1.4.2 比表面积与孔径分布 在物理吸附仪上进行。测试之前首先在100 ℃脱气3 h,比表面积按照BET方法进行计算,孔容按照BJH理论计算。
1.4.3 透射FTIR 在傅里叶变换红外光谱仪上进行,波长范围400~4 000 cm-1,样品扫描次数32次。采用KBr压片法,样品与溴化钾比例为1∶100。
1.4.4 XPS测试 在X射线光电子能谱上进行,以Al Kα为激发光源,测试能量1 486.8 eV,分析室本底真空2×10-9mbar,以C1s 284.8 eV为准来进行峰位校正。
1.4.5 TGA测试 采用热重分析仪进行。称取5 mg 样品,在氮气气氛下以10 ℃/min的升温速率升到100 ℃,然后保持30 min,以去除样品表面的吸附水以及其他杂质。之后在氮气气氛下以10 ℃/min的升温速率由100 ℃升到600 ℃。
1.4.6 TPDC测试 采用催化剂活性评价系统进行。称取200 mg样品,在氦气气氛下以10 ℃/min的升温速率升到100 ℃,然后保持30 min,以去除样品表面的吸附水以及其他杂质。之后在氦气气氛下以10 ℃/min的升温速率由100 ℃升到600 ℃。分解产物随温度的分布特征通过质谱仪进行检测。
1.5 FTIR在线检测NOx浓度
具体步聚为(以NO)为例:(1)选取NO气体在红外光谱中的积分区间1 878~1 965 cm-1;(2)分别选取100,200,300,400,500 mg/m3的标准NO气体,通过对不同浓度的气体红外光谱进行面积积分(气体浓度与峰强度即积分面积成正比),以积分面积为横坐标,气体浓度为纵坐标,建立标准曲线;(3)利用OPUS(FTIR软件)的色谱测量功能,设置采样时间、采样间隔、采样次数,对不同时间点的气体的红外光谱中NO特征峰进行面积积分,或者利用重复采样功能,手动对得到的多条红外光谱进行面积积分;(4)利用标准曲线,根据不同时间点得到的积分面积去计算NO浓度。
2 结果与讨论
2.1 物理结构分析
采用XRD研究样品的晶体结构,结果见图1。

图1 样品的XRD谱图Fig.1 XRD patterns of series samples
由图1可知,新鲜催化剂与硫酸氢铵负载催化剂的XRD衍射峰全部呈现出典型的锐钛矿结构TiO2。同时从XRD谱图中并未观察到V2O5、Sb2O3以及NH4HSO4的晶体结构,说明这3种物质以无定形状态存在,并且高度分散在催化剂表面。2V/Ti与2Sb2V/Ti两种催化剂的XRD衍射峰并未发生任何改变,说明在催化剂中掺杂助剂Sb2O3对催化剂的晶体结构无影响。
样品的比表面积和孔径分布见表1。

表1 样品的结构特征Table 1 Textural and structural properties ofseries samples
由表1可知,对于新鲜催化剂,当助剂Sb2O3掺杂量发生改变时,样品的比表面积和总孔容也会发生变化。助剂Sb2O3掺杂量3%时,样品的比表面积和总孔容明显增大,达到72 m2/g。当负载硫酸氢铵后,样品的比表面积和总孔容出现一定程度下降,说明在催化剂表面负载的硫酸氢铵堵塞催化剂的孔道结构。
2.2 表面官能团分析
采用透射红外研究硫酸氢铵负载前后催化剂表面官能团的变化,结果见图2。

图2 纯硫酸氢铵、硫酸氢铵预负载催化剂与新鲜催化剂的红外光谱图Fig.2 FTIR spectra of pure NH4HSO4,NH4HSO4-depositedcatalysts and free catalysts

2.3 原子环境分析
采用XPS研究硫酸氢铵负载前后催化剂表面Ti、V、Sb、O、N以及S原子变化,结果见图3。





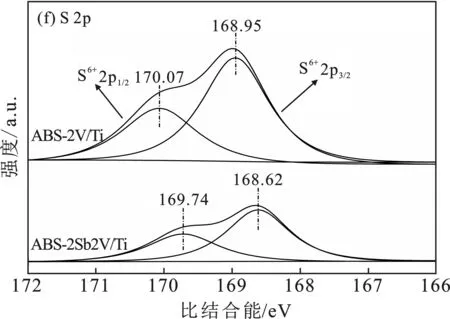
图3 样品的XPS谱图Fig.3 XPS spectra of series samples
由图3(a)可知,对于2V/Ti样品,电子比结合能458.83 eV和464.58 eV处的两个特征峰分别归属于Ti 2p3/2和Ti 2p1/2,并且Ti原子以+4价形式存在[18]。当负载硫酸氢铵后,Ti 2p特征峰向比结合能高的方向移动(+0.14 eV),说明Ti原子处于缺电子状态。对于2Sb2V/Ti样品,当负载硫酸氢铵后,Ti 2p特征峰的比结合能增加0.51 eV,说明当掺杂助剂Sb2O3后,Ti原子将处于一个更加严重的电子偏离状态。
由图3(b)可知,负载硫酸氢铵后,2V/Ti催化剂表面V 2p特征峰向比结合能高的方向移动(+0.31 eV),说明V原子的电子云密度减小。而且2Sb2V/Ti催化剂,负载硫酸氢铵后,V 2p特征峰的比结合能增加0.78 eV,说明催化剂表面的V原子的电子云密度更小。
由图3(c)可知,对于2Sb2V/Ti催化剂,电子结合能为539.88 eV处的特征峰归属于Sb 3d3/2,另一个电子结合能较低的特征峰主要是由于O 1s与Sb 3d5/2特征峰叠加而成[19]。负载硫酸氢铵后,Sb 3d的两个特征峰全部向比结合能高的方向移动,说明催化剂表面Sb原子的电子云密度降低,处于缺电子状态。
由图3(d)可知,O 1s的XPS谱图可以通过去卷积方式划分为两个特征峰,其中比结合能较低的特征峰可以归属为晶格氧Oβ,比结合能较高的特征峰可以归属为化学吸附氧Oα[20]。结合O 1s特征峰的比结合能移动方向,可以判断得出负载硫酸氢铵之后,O原子周围的电子云密度同样降低。

由图3(e)可知,在催化剂中掺杂助剂Sb2O3后,N 1s的特征峰的比结合能并未发生任何改变,说明N原子周围的电子云密度不变。
由图3(f)可知,根据S 2p特征峰结合能大小,可以将两个特征峰分别归属于S 2p1/2和S 2p3/2[21]。对比ABS-2V/Ti与ABS-2Sb2V/Ti样品中S 2p特征峰的比结合能可知,当掺杂助剂Sb2O3后,特征峰向比结合能低的方向移动,说明催化剂表面S原子周围的电子云密度增大。

2.4 助剂Sb2O3对硫酸氢铵分解行为的影响
所有硫酸氢铵负载样品的N、S元素分析,结果见表2。

表2 系列硫酸氢铵负载样品元素分析Table 2 Elemental analysis of series NH4HSO4-deposited samples
由表2可知,所有催化剂表面负载硫酸氢铵的含量基本一致。
V2O5/TiO2催化剂中助剂Sb2O3含量对硫酸氢铵分解行为的影响见图4。
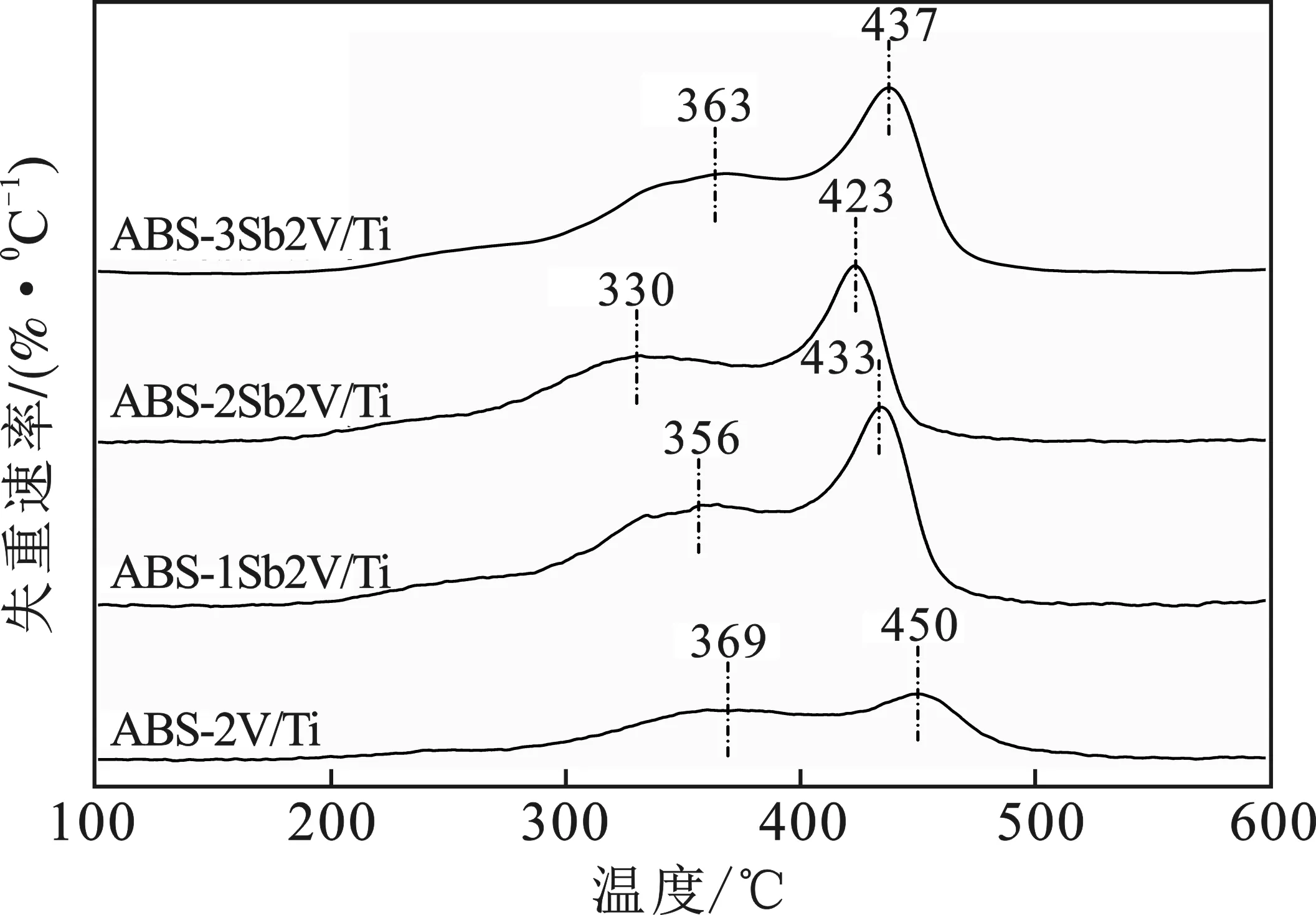
图4 ABS-SbV/Ti样品(0,1%,2%,3% Sb2O3)的失重速率曲线Fig.4 DTG profiles of the ABS-SbV/Ti samplescontaining 0,1%,2%,3% Sb2O3
由图4可知,每种样品在加热过程中都出现两个失重峰,分别位于300~400 ℃温度段和400~500 ℃温度段,说明硫酸氢铵在这两个温度段的分解速度较快,可以代表样品的分解行为。相比于300~400 ℃温度段的失重峰,400~500 ℃温度段的失重峰表现较为尖锐,而且失重速率值也较高。温度继续升高时,失重速率曲线逐渐趋于平缓,说明催化剂表面的硫酸氢铵已经全部分解完毕。催化剂中Sb2O3含量发生改变时,不同样品失重速率曲线的失重峰所对应的温度表现不一致,而且与第2个失重峰相比,第1个失重峰的差异更加明显。当Sb2O3含量为0时,硫酸氢铵分解失重峰所对应的温度分别为369 ℃和450 ℃,而Sb2O3含量增加至2%时,硫酸氢铵分解失重峰所对应的温度最低,分别为330 ℃和423 ℃。继续增加Sb2O3含量,则硫酸氢铵分解失重峰所对应的温度又会升高,不利于硫酸氢铵的分解。说明当催化剂中掺杂Sb2O3后,其表面硫酸氢铵的分解温度可以降低,在一定温度下有利于硫酸氢铵的分解,而且当Sb2O3含量为2%时,催化剂表面的硫酸氢铵更加容易发生分解。


图5 硫酸氢铵负载催化剂的分解产物SO2分布Fig.5 Decomposition product SO2 of the seriesNH4HSO4-deposited catalysts
由图5可知,所有样品释放SO2的质谱信号峰值所对应的温度全部集中在400~500 ℃温度段,同时该温度段与图4中第2个失重峰对应的温度段相同,说明硫酸氢铵在第2个失重峰阶段发生分解主要是由于SO2的释放所导致。对比于V2O5/TiO2催化剂,掺杂助剂Sb2O3后,催化剂表面硫酸氢铵分解产物SO2的释放温度降低,Sb2O3的含量为2%时,催化剂表面硫酸氢铵分解产物SO2的释放温度达到最低。结合热重实验数据可知,在V2O5/TiO2催化剂掺杂助剂Sb2O3后可以明显促进催化剂表面硫酸氢铵的分解行为,并且当助剂Sb2O3含量为2%时,促进效果最明显。
2.5 催化剂性能研究
在400 mg/m3NO+400 mg/m3NH3+16% O2,N2为平衡气,流量500 mL/min,空速60 000 h-1条件下,Sb2O3-V2O5/TiO2的催化活性随温度的变化规律见图6。
由图6可知,Sb2O3-V2O5/TiO2的催化活性随着温度的升高而随之升高。当反应温度达到250 ℃时,催化剂的催化活性可以达到94%,继续升高反应温度,催化剂的催化活性并没有明显升高,逐渐趋于稳定。当温度低于250 ℃时,相比于V2O5/TiO2催化剂,Sb2O3-V2O5/TiO2催化剂在同一温度下的催化活性更高,并且Sb2O3含量为2%时,其催化活性最高。

图6 催化剂脱硝活性Fig.6 Catalytic activity of the series catalysts
在400 mg/m3NO+400 mg/m3NH3+16% O2+400 mg/m3SO2+10% H2O,N2为平衡气,流量500 mL/min,空速60 000 h-1,反应温度220 ℃条件下,220 ℃下Sb2O3-V2O5/TiO2催化剂的抗硫抗水性见图7。

图7 催化剂抗硫抗水性Fig.7 Sulfur and water resistance of series catalysts
由图7可知,在反应的前2 h,反应体系中并未通入SO2和H2O,催化剂的催化活性达到稳定状态。当SO2和H2O通入反应体系时,随着反应的持续进行,催化剂的催化活性发生一定程度的下降。当反应进行到第22 h,催化剂的催化活性逐渐趋于平缓,2V/Ti,1Sb2V/Ti,2Sb2V/Ti和3Sb2V/Ti催化剂的NOx转化率分别达到52%,63%,80%,70%。与之前未通入SO2和H2O 的催化活性相比,其NOx转化率分别下降25%,20%,13%和17%。因此,在V2O5/TiO2催化剂中掺杂助剂Sb2O3,可以明显提高催化剂的抗硫抗水性,并且当助剂Sb2O3含量为2%时,对催化剂抗硫抗水性能的提高更加显著。
低温SCR过程中催化剂的抗硫抗水性主要取决于催化剂表面硫酸氢铵的累积量,而硫酸氢铵的累积量主要取决于反应过程中的生成量与消耗量。根据相关文献报道,锑的加入可以抑制硫酸氢铵在催化剂表面的生成[13]。在V2O5/TiO2催化剂中掺杂助剂Sb2O3后,可以明显促进催化剂表面硫酸氢铵的分解行为。因此,助剂Sb2O3的掺杂可以降低低温SCR反应过程中催化剂表面硫酸氢铵的累积量,进一步提高催化剂的抗硫抗水性。
3 结论
(1)Sb2O3-V2O5/TiO2催化剂负载硫酸氢铵后,催化剂的比表面积与孔体积发生一定程度下降,同时催化剂与硫酸氢铵之间会产生化学相互作用。

