人工腹水对膈面、脏面原发性肝癌微波消融治疗中的应用价值
2019-04-17颜朝晖张卫兵刘英棣
陈 建, 金 霞, 陈 晓, 颜朝晖,张卫兵, 李 萍, 刘英棣
(武警江苏省总队医院, 1. 超声科; 2. 肝胆外科, 江苏 扬州, 225003;3. 海军军医大学附属长征医院 超声科, 上海, 200003)
原发性肝癌(HCC)严重危害人类健康, 而大多数HCC患者发现时已属中晚期,仅10%~20%的患者适宜采用传统的根治性外科手术。以经皮微波消融术(PMA)以及射频消融术为代表的物理消融法正在改变HCC根治性治疗的现状,对于直径3 cm以内的病灶,上述热消融法的远期疗效与传统的外科切除术一致[1-3], 对中、大病灶的消融治疗也取得了显著的进展[4-8]。但特殊部位的HCC,如毗邻胃肠、胆囊、膈肌等肝外器官以及第一肝门、胆管、血管等肝内重要结构,在消融过程中仍存在热损伤的风险,可以引起较为严重的并发症,如肠穿孔、胆道狭窄、胆漏、膈肌穿孔、出血等,甚至危及生命[9-12]。作者采用人工腹水辅助超声引导下微波消融治疗肝膈面和脏面的肿瘤并进行对照观察,现报告如下。
1 资料与方法
1.1 一般资料
本研究通过本院伦理委员会审批,患者及家属术前均签署手术知情同意书。纳入标准: ① HCC诊断符合2011年《原发性肝癌规范化诊治专家共识》; ② 肝功能Child-Pugh评级A、B,肾功能正常; ③ HCC数2个以内,直径5 cm以内; ④ 所有病例只包含毗邻膈肌及脏面的HCC; ⑤ HCC与膈肌以及肝脏脏面包膜的距离在5 mm以内; ⑥ 无门静脉、肝静脉、肝内胆管及远处转移。排除标准: ① 严重凝血功能障碍,血小板<50×109/L, 凝血酶原时间>25 s, 凝血酶原活动度<40%, 其中任意一项异常未纠正到以上水平; ②癌性腹水或低蛋白血症性腹水; ③ 第一肝门区HCC明确与1、2级肝管紧密相邻者; ④ 多器官功能衰竭患者。
将2010年6月—2014年10月本院收治的膈面及脏面HCC患者139例(158个结节)指定为A组,均在经皮微波消融治疗前实施人工腹水,其中膈面HCC患者83例(88个结节),男66例,年龄33~78岁,女17例,`年龄26~79岁,平均肿瘤直径4.1 cm; 脏面HCC患者67例(70个结节),男54例,年龄32~81岁,女13例,年龄38~74岁,平均肿瘤直径3.9 cm。A组139例患者中, 120例患有1个HCC,其中位于膈面者67个结节,位于脏面者53个结节; 其余19例患有2个HCC, 11例患者脏面、膈面分别1个结节,其余8例中, 5例膈面2个结节, 3例脏面2个结节。由此计算,位于膈面者83例共88个HCC, 位于脏面者67例共70个HCC。
将2007年3月—2010年5月对临近膈肌及胃肠道进行经皮微波消融治疗的108例HCC患者(121个结节)指定为B组,治疗前未实施人工腹水,其中膈面HCC患者64例(67个结节),男44例,年龄31~76岁,女18例,年龄26~79岁,平均肿瘤直径3.5 cm; 脏面HCC患者52例(54个结节),男39例,年龄32~74岁,女13例,年龄36~77岁,平均肿瘤直径3.3 cm。B组108例患者中,95例患有1个结节,其中膈面者53例,脏面者42例; 13例患有2个结节,其中8例膈面、脏面分别1个结节,其余5例中,3例膈面2个结节,2例脏面2个结节。由此计算,位于膈面者64例共67个结节,位于脏面者52例共54个结节。
1.2 仪器与方法
1.2.1 仪器: 采用Philips-IU22或百胜mylab30彩色多普勒诊断仪,凸阵探头,频率2.5~5.0 MHz, 用于引导穿刺布针以及术中动态监测。采用维京九洲MTC-3C型微波消融治疗仪。全身麻醉机。
1.2.2 术前准备: ① 常规检查血常规、尿常规、凝血功能、肝肾功能、肝炎标志物、甲胎蛋白(AFP)、胸片、心电图; ② 超声、增强CT影像学检查,明确肿瘤的大小、部位、数目等情况,制定治疗方案; ③ 术前禁食、禁水8 h; ④ 肿瘤位于临近脏面的患者,术前1 d导泻,当日常规灌肠。
1.2.3 麻醉方式: ① 预计手术时间小于1 h,静脉全身麻醉(异丙酚+芬太尼); ② 预计手术时间大于1 h, 静吸复合全身麻醉。
1.3 人工腹水的方法
1.3.1 穿刺点选择: 右肝HCC的穿刺点选在右上腹部,穿刺路径指向肝肾隐窝。左叶HCC的穿刺点选在上腹部,穿刺路径指向肝胃间隙。穿刺路径回避肠管结构,彩色多普勒血流图(CDFI)检测无血流信号; 穿刺针突破壁层腹膜,置入导丝,沿导丝置入猪尾引流管(有侧孔),导入40 ℃生理盐水。
1.3.2 体位: ① 平卧位; ② 头低足高位: 必要时,与水平面夹角15~20°, 有利于液体在肝周围积聚。③ 左侧卧位: 20~30°, 穿刺点在腋中线以后,便于穿刺布针之操作。左外叶HCC, 如常规体位液体分布不满意,可以采取左侧卧位45~90°, 增加左叶周围的液体分布。④ 水量控制: 在HCC局部液体足够的前提下,尽量减少腹水量,在1 000~2 500 mL。
1.3.3 超声引导下PMA: ① 人工腹水成功后,确定穿刺路径,并将微波消融针植入肿瘤内部目标区。②微波消融治疗。肿瘤直径2.5 cm以内行单针单点消融。HCC直径2.5 cm以上,采取两点或多点消融累积,完成对瘤体的消融覆盖,消融区边缘超过HCC边缘0.5 cm左右(空间允许的前提下)。HCC直径2.5~4.0 cm采用双针双点。4.0~5.0 cm采用双针或三针同时多点融合消融。消融前先行布入2~3根消融针,可减少消融治疗产生的气体强回声干扰导致的再布针风险。毗邻的膈肌、胃肠道、胆囊以及肝门等重要结构,先从小功率开始,渐次增加功率。超声密切监视,若消融区气体强回声扩展快,与重要结构距离达到5.0 mm时,应停止消融后观察,等待片刻后降低功率,重新尝试消融。微波消融治疗仪输出功率50~80 W,时间10~12 min。超声全程监视消融范围,如有残留区,追加消融。消融结束后,边退针、边消融针道(功率70 W),使针道呈强回声带,预防针道出血。确定腹腔引流管通畅后,接引流袋。
1.4 疗效评价
术前以及术后1个月常规CT增强扫描及彩超。① CT有无异常增强区域,提示残留; ② 消融区域是否覆盖原HCC空间,若有错位则认为有残留; ③ 彩超: 瘤区内部存在血流信号则视为消融不完全。其后1年内每3个月复查1次增强CT与彩超。
1.5 统计学分析

2 结 果
A组与B组膈面、脏面HCC患者的性别、年龄、瘤体大小等比较,差异无统计学意义(P>0.05)。在微波消融治疗前,对145例HCC患者进行了超声引导下人工腹水术, 139例获得成功,成功率为95.8%。6例失败患者中, 4例发生在肝癌切除术后,肝脏周围间隙粘连; 2例发生在胆囊切除术后,肝脏脏面粘连。超声引导下人工腹水辅助治疗HCC个例情况见图1、2、3。
A组中, 83例膈面HCC(88个结节)患者的一次性完全消融率为93.2%(82/88), 67例脏面HCC(70个结节)患者的一次性完全消融率为94.3%(66/70); B组中, 64例膈面HCC(67个结节)患者的一次性完全消融率为76.1%(51/67), 52例脏面HCC(56个结节)患者的一次性完全消融率为72.2%(39/54)。2组组内膈面与脏面HCC患者的一次性完全消融率比较,差异无统计学意义(93.2% vs. 94.3%, 76.1% vs. 72.2%,P>0.05)。2组组间膈面、脏面HCC患者完全消融率比较,差异有统计学意义(93.2% vs. 76.1%, 94.3% vs. 72.2%,P<0.01)。
A组中膈面HCC患者发生反应性胸水0例, B组中膈面HCC患者发生反应性胸水26例, 2组差异有统计学意义(P<0.01)。A组中脏面HCC患者发生肠穿孔0例, B组中脏面HCC患者发生肠穿孔2例(小肠穿孔1例,结肠穿孔1例), 2组差异无统计学意义(P>0.05)。A组发生腹腔活动性出血3例, B组为1例, 2组差异无统计学意义(P>0.05)。积极处理后,未发生失血性休克。
位于膈下的肿瘤,消融针穿刺往往需要通过膈肌。人工腹水后,在压差的作用下,腹水通过膈肌穿刺孔进入右侧胸腔,造成“交通性胸水”。本研究中交通性胸水的发生率较高,达20.5%(17/83), 但均未引起术中呼吸困难、血氧饱和度下降。
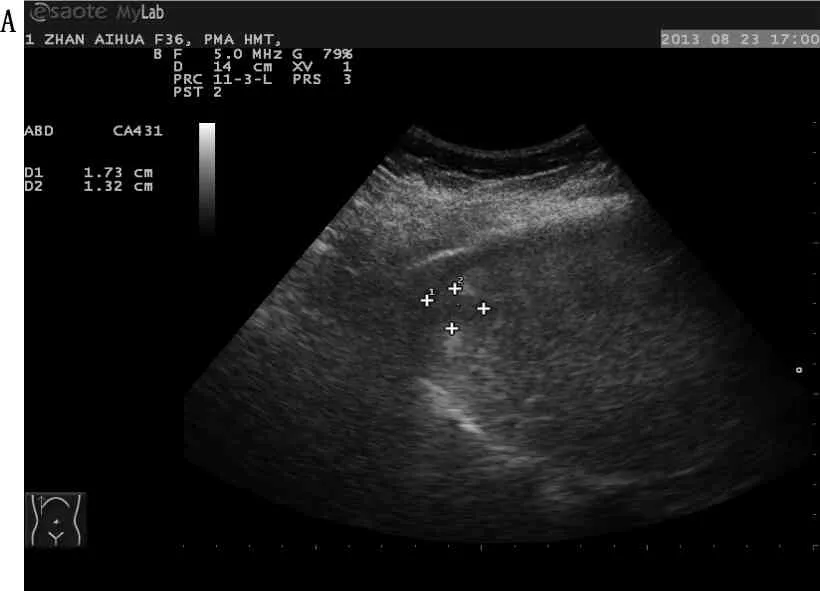


A: 膈下HCC小结节,受肺脏气体掩盖超声不显示,人工腹水分隔了膈肌与肝脏,同时使得该结节显示清晰;
3 讨 论
在《原发性肝癌诊疗规范(2017版)》中,PMA已经成为与外科切除术并列的一线治疗手段,同时二者具有明显的互补性。与外科切除术相比,PMA适应证更宽广,对非外科手术适应证以及手术后复发者,甚至巨块型肝癌患者,同样可以发挥根治或有效减瘤的作用,有效地缓解临床症状,改善预后[4-8]。超声引导下PMA是一种安全的微创治疗技术,但文献[9-14]报告也提及多种较为严重的并发症,值得重视。相关文献[15-20]对人工腹水及人工胸水在提升PMA治疗安全中的价值给予了肯定评价。与文献中普遍采用的单组观察不同,本研究采用分组对比观察,发现采用人工腹水干预膈面和脏面HCC微波消融治疗过程后,可明显降低PMA术后并发症,还能显著提高对瘤体的一次性完全消融率。


A: HCC位于右后叶脏面,肝下间隙人工腹水,使胃肠道远离肝脏脏面,避免胃肠道穿孔;B: 消融过程中,强回声区为微波消融区域
图3超声引导下人工腹水辅助治疗HCC个例情况
3.1 人工腹水的优势
HCC所在部位与肝脏重要结构及邻近脏器的解剖位置关系是影响治疗安全性的关键因素之一。人工腹水存在于HCC结节与膈肌、胃肠道、肾、心脏等毗邻器官之间,增加了安全距离,有效阻隔消融区热量直接波及相关器官而造成的烧伤[17-18]。
3.1.1 预防反应性胸水: B组由于未采用人工腹水,膈下HCC微波消融后,尽管未发生膈肌穿孔,但反应性胸水发生率较高,达40.6%(26/64), 说明膈肌热损伤较为常见。胸水较多时,辅以置管引流,消失时间较长(10~65 d)。A组行人工腹水则有效避免了反应性胸水的发生。
3.1.2 预防肠穿孔: B组未采用人工腹水, PMA脏面54个HCC结节(52例)后,出现肠穿孔2例,发生率占脏面肿瘤消融的3.8%(2/52), 其中横结肠穿孔1例,行外科手术后获得治愈; 十二指肠穿孔1例,并发腹膜炎,导致死亡。A组67个脏面HCC结节(64例),无1例发生肠穿孔,说明在不实施人工腹水干预下,超声引导下PMA已经是较为安全的方法,但由于肠穿孔的严重危害性,加之手术者的技术状况存在差异,采用人工腹水无疑是十分必要的一个环节。
3.1.3 预防额外肝损伤: 在无人工腹水干预的情况下,对于膈面浅表的HCC小结节(如1.5 cm左右),为了避免后向微波热能烫伤胸壁与膈肌,并确保微波消融区横径达到2.5 cm左右,微波针前段有必要穿刺进入肝脏3.5~4.0 cm, 超越上述HCC后缘2.0~2.5 cm, 势必对肝脏造成额外的损伤。相反,人工腹水干预后,微波针只需要穿刺进入肝脏1.5~2.0 cm, 后向的热能被水吸收,不会烧伤胸壁,避免了PMA对HCC周围肝组织的额外损伤。同时,热量更集中于瘤体内,有利于尽快消融。可见,人工腹水是预防膈肌、肠道热损伤和避免肝组织额外损伤的必要安全措施。
3.2 人工腹水可提高一次性完全消融率
① 充分消融: 由于人工腹水提高了手术安全性,术者不仅在穿刺、布点、消融过程中更有信心与把握,也更充分与合理[19]。而且,与毗邻器官安全距离增加后,采用相对较高的微波功率以及较长的消融时间成为可能,瘤体获得更加充分的消融,一次性完全消融率显著高于对照组(P<0.05), 这无疑有利于提高疗效、改善预后。② 改善瘤体显示质量: 部分右侧膈顶部HCC, 术前CT、MR显示,但受到肺脏气体阻挡,超声不能满意显示全貌或完全不显示,而在人工腹水形成后病灶得以显示。A组中术前超声未显示或部分显示的HCC 13例,人工腹水后,所有肿瘤清晰显示。可见,这对改善超声图像质量,进而指导精确合理布针,并动态监视消融过程均非常有利,有利于减少局部肿瘤残留。此外,人工腹水还有助于发现脏面肿瘤与肠道的粘连与侵犯。在这种情况下,极易造成肠道损伤,热消融区域必须远离脏面与肠道粘连处。作者视不同情况,或放弃消融,或在确保安全的情况下采取有限的消融。有术者对未充分消融部分结合无水乙醇注射局部,取得良好效果[12]。
3.3 人工腹水的不足
3.3.1 交通性胸水: 交通性胸水是人工腹水通过膈肌的微波消融针穿刺孔由腹腔进入胸腔所致形成。有别于消融后出现的反应性胸水,交通性胸水在治疗过程中即出现,超声监测易于发现,胸水较多可造成部分肺不张。A组交通性胸水发生率为20.5%(17/83)。虽然未出现术中呼吸困难、血氧饱和度下降的情况,但对伴有慢性肺功能不全的患者,有必要进行肺功能的术前评价,并积极预防交通性胸水导致急性肺功能不全的潜在风险。
预防交通性胸水的要点: ① 管控腹水量,选择穿刺点。术者密切注视肿瘤局部腹腔间隙的腹水情况,一旦形成满意的液体隔离带,即停止注入。过多腹水会显著增加腹压,加重交通性胸水。头低足高位也是交通性胸水的促进因素。此外,在膈肌穿刺点水平最好无腹水。② 如需消融2个或以上的HCC, 应优先消融无需人工腹水辅助的HCC, 最后消融膈下HCC, 以便缩短形成交通性胸水的时间。③ 术毕,尽快引流人工腹水,减少交通性胸水量。④ 如已形成大量继发性胸水,尤其是影响到呼吸功能,应及时置管,引流胸水。鉴于此,对于存在癌性腹水的患者,应避免经膈肌穿刺,以免造成癌性腹水逆流胸腔,导致种植性转移的不良后果。如确有必要进行穿刺膈肌的微波消融治疗,理应在引流腹水后进行。
3.3.2 加重术后出血的倾向: 在中国, 80%HCC存在不同程度的肝硬化,伴有出血倾向。本研究中,尽管同样进行充分地针道消融预防术后出血,人工腹水后针道活动性出血发生率较无人工腹水者为高,虽然2组间无显著差异,但提示人工腹水有增加出血的倾向,相关文献[21-22]中有类似描述。作者认为在人工腹水状态下,针道消融未完全止血时,创面浸泡在水中,影响局部凝血过程,是导致活动性失血的关键因素之一。预防、处理术后出血方面,应注意以下几点: ① 对有明显出血倾向患者,术前应常规输注血浆以及血小板,改善凝血功能。② 术中间断性抽吸腹水,观看颜色,判断是否有明显的活动性出血。③ 如果腹水颜色快速加深,应即刻引流腹水。如引流管不通畅,立即重置引流管于肝肾隐窝的液性区内,以便快速引流腹水。④ 消融结束,针道消融要充分。⑤ 术后采取半卧位,以减少肝周的积液,使腹水积聚于盆腔。⑥ 密切监护生命体征,进行抗凝治疗,积极预防、治疗失血性休克。
总之,人工腹水能有效减少PMA治疗HCC术后并发症的发生,提高一次性完全消融率,增强疗效。
