分散固相萃取结合液相色谱串联质谱法检测牛可食性组织中泰地罗新残留量
2019-04-09吴剑平张婧贡松松严凤潘娟黄士新
吴剑平,张婧,贡松松,严凤,潘娟,黄士新
(上海市兽药饲料检测所,上海 201103)
泰地罗新(tildipirosin),国际化学名为20-脱氧-23脱氧-5-氧-[3,6-二脱氧-3-(二甲氨基)- β-D-吡喃葡萄糖基]-20,23-二-1-哌啶基泰乐内脂,CAS No:328898-40-4,分子式为C41H71N3O8,分子量为734.02,其结构式如图1所示。泰地罗新是继替米考星和乙酰异戊酰泰乐菌素之后,又一种由泰乐菌素半合成制备的新型大环内酯类抗生素。荷兰英特威国际有限公司(Intervet International BV)最早研发了该药物,于2011 年经欧洲药物管理局(European medicinesagency, EMA)的审核,在欧盟国家批准上市销售[1-2]。泰地罗新主要通过作用于细菌核糖体50s亚基,阻断mRNA 位移,使得细菌的肽链合成和延长受阻,影响其蛋白质的合成,从而达到抑菌的目的。其主要用于治疗由副猪嗜血杆菌、胸膜肺炎放线杆菌等细菌引起的呼吸道疾病,其比泰乐菌素在抑制猪、牛呼吸道致病菌展现出更好的效果[3-5]。该药吸收迅速,半衰期长,生物利用度高,性质稳定,具有较好的开发价值。国内近期已有厂商引进研发了该药,因此,有必要尽快制定该药在猪、牛等动物可食性组织中的残留量检测方法。
目前,检测大环内脂类抗生素检测方法中的紫外分光光度法、荧光法等由于受基质干扰较严重不适用于残留检测,液相色谱法虽能较好的分离基质[6-8],但是后端的紫外检测器或二极管阵列检测器的灵敏度不足,难以适应残留检测的需要[9]。本实验室之前也建立了以静电场轨道阱高分辨液质解析泰地罗新注射液中的有关物质[10],但高分辨质谱在定量方面并不如其在定性方面的优势明显[11]。液相色谱-串联质谱法检测动物可食性组织中的药物残留量具有灵敏度高,特异性好的特点[12],有研究表明用该方法检测猪可食性组织中的泰地罗新检测限可达到10 μg/kg[13]。分散固相萃取相比传统的固相萃取柱,前处理具有成本低,速度快,便于操作的特点[14],本研究结合分散固相萃取技术与液相色谱-串联质谱法对牛可食性组织中的泰地罗新残留量检测方法进行了研究。
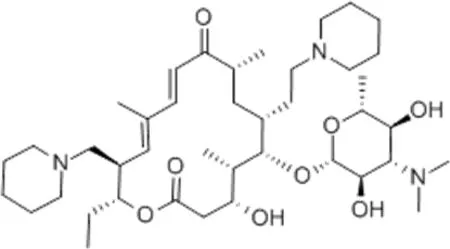
图1 泰地罗新化学结构式Fig 1 Structure of tildipirosin
1 材料和方法
1.1 仪器 Ultimate 3000双三元超高效液相色谱、Excalibur控制软件、串联四极杆质谱带HESI电离喷雾源(TSQ Quantiva)、Xcalibur数据处理系统等(Thermo, 美国)、高速冷冻离心机(Allegra X-22R,BECKMAN COULTER);电子天平(AL204,梅特勒-托利多仪器有限公司);减压旋转蒸发仪(B-490,BUCHI);水浴控温氮吹仪(N-EVAP,上海安谱公司)。
1.2 材料、药品与试剂 C18分析柱(Thermo Hypersil gold 50×2.1 mm,1.9 μm),泰地罗新对照品(上海同仁药业有限公司,批号:130503,99.1%),无水硫酸镁(分析纯),氯化钠(分析纯),正己烷(色谱纯),乙腈(色谱纯),酸性氧化铝(100~200目),乙腈、甲醇、甲酸(色谱纯);去离子水(电阻率≥18 MΩ·cm);高纯氮、高纯氩(纯度均为99.999%)。
1.3 色谱条件 色谱柱:Thermo Hypersil gold 50×2.1 mm,1.9 μm,柱温:30 ℃,流速:0.3 mL/min,进样量:10 μL,流动相:A为0.1%甲酸,B为乙腈,采用梯度洗脱程序(表1),所得特征离子质量色谱图如图2所示。
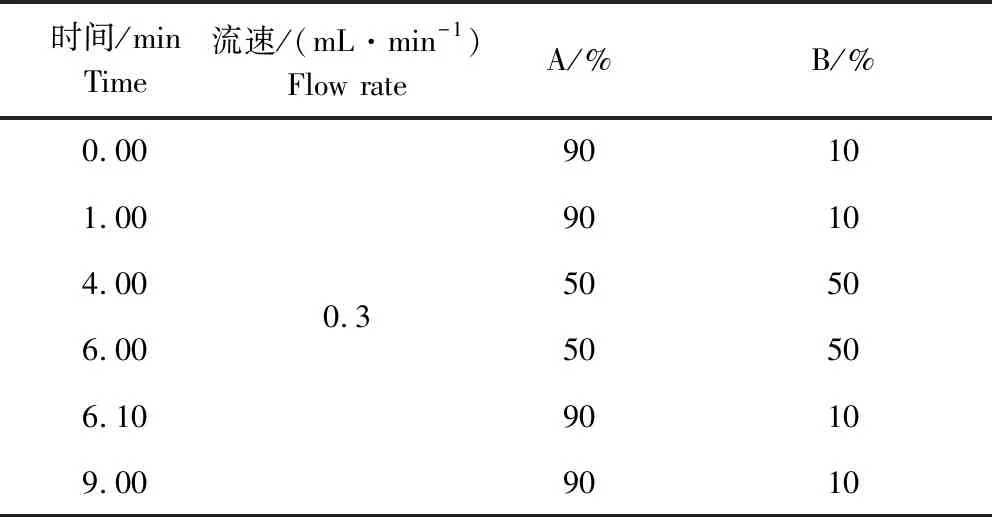
表1 梯度洗脱程序Tab 1 Procedure of gradient elution
1.4 质谱条件 使用Thermo Fisher公司的TSQ Quantiva串联四极杆质谱带HESI电离喷雾源质谱检测器,条件如下:ESI+模式,源电压3500 V,鞘气(Sheath gas)压力344 kPa,辅助气(Aux gas)流速5 L/min,吹扫气(Sweep gas)流速0.3 L/min,离子传输管(Ion transfer tube)温度 350 ℃,雾化器(Vapourizer)温度350 ℃,检测模式为选择反应监控(Selected reaction monitor,SRM),碰撞气压力0.2 Pa,Q1段分辨率设为半峰宽0.7,Q2段分辨率设为半峰宽0.7,目标化合物反应监测参数见表2。

表2 质谱选择反应监控(SRM)参数Tab 2 Qualitative and quantitative ion pair for tildipirosin
带*为定量离子对
1.5 前处理条件 取2.00 g样品置于50 mL试管中,加入50 %乙腈溶液10 mL,涡旋混匀后加入5.00 mL正己烷和无水硫酸镁与氯化钠各2 g,振荡提取10 min,8000 r/min离心5 min,用微量取液器准确吸取中间乙腈层清液0.50 mL至离心管中备用。备用液中加入1.50 mL的0.1%甲酸溶液和0.20 g酸性氧化铝粉末,涡旋均匀后12000 r/min离心3 min,取上清液过0.22 μm尼龙滤膜后装入棕色进样瓶上机测定。
2 结果与分析
2.1 方法灵敏度实验结果 分别称取(2.00±0.02)g牛空白组织各3份于具塞离心管中,其中一份作为空白基质,另外2份依次加入己知浓度的标准工作液,制成含泰地罗新药浓度为5 μg/kg 和10 μg/kg的组织样品。按照1.5项前处理方法处理后,按1.3项与1.4项仪器条件进样分析,所得特征离子质量色谱如图2所示,依据信噪比S/N>3作为检测限,信噪比S/N>10作为定量限,结果表明方法的检测限可达5 μg/kg,定量限可达10 μg/kg。据欧盟最新规定[15],泰地罗新在牛肉中的最大残留限量(MRL)为400 μg/kg,在牛脂肪中为200 μg/kg,在牛肝中为2000 μg/kg,在牛肾中为3000 μg/kg,实验结果表明该方法灵敏度符合要求。
2.2 基质效应实验结果 称取2.00±0.02 g牛空白组织各5份,按1.5项方法处理后获得相应组织空白基质溶液。另精密称定标准品10 ±0.5 mg,用甲醇溶解并定容至100 mL,得100 μg/mL的标准品贮备液。取标准品贮备液用0.1%甲酸稀释至100 ng/mL的标准品工作溶液。取适量标准品工作溶液用0.1%甲酸溶液稀释至1 ng/mL溶剂标准品溶液,另取适量标准品工作溶液用空白基质溶液稀释至1 ng/mL基质标准品溶液。将1 ng/mL的溶剂标准品溶液基质标准品溶液按1.3项与1.4项的仪器条件进样测试,所得面积均值和RSD%如表3所示。实验结果表明,牛肉、牛脂肪、牛肝和牛肾的基质标准品溶液与溶剂标准品相比都有不同程度的基质抑制作用,因此,后续实验均采用基质标准曲线进行定量校正。
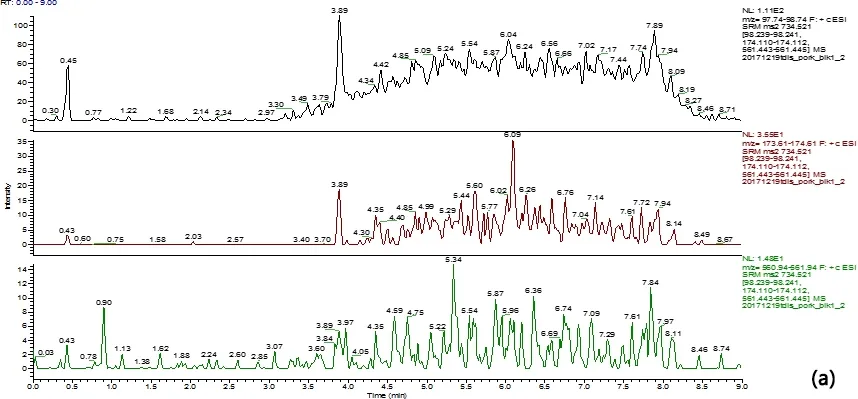

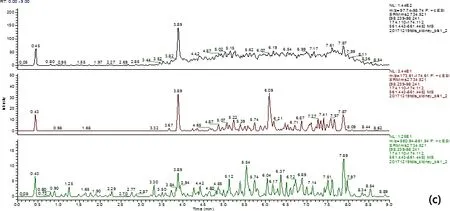
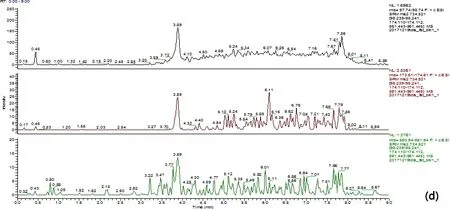
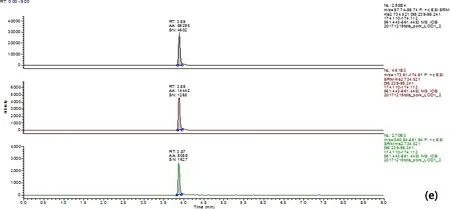

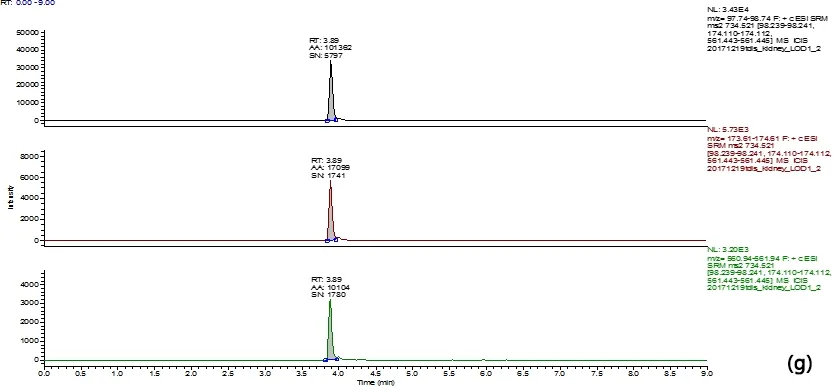
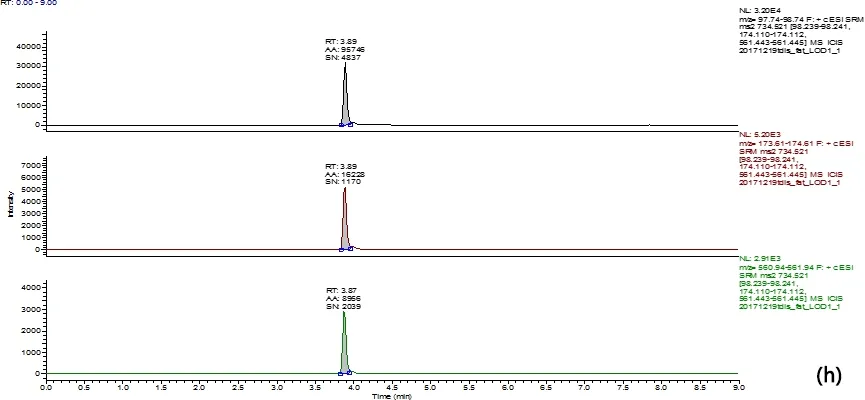
(a) 牛肉空白样品图;blank bovine muscle; (b) 牛脂肪空白样品图;blank bovine fat; (c) 牛肝空白样品图;blank bovine liver;(d)牛肾空白样品图;blank bovine kidney;(e) 牛肉空白样品添加10 μg/kg;10 μg/kg added in blank bovine muscle; (f) 牛脂肪空白样品添加10 μg/kg;10 μg/kg added in blank bovine fat;(g) 牛肝空白样品添加10 μg/kg;10 μg/kg added in blank bovine liver;(h) 牛肾空白样品添加10 μg/kg;10 μg/kg added in blank bovine kidney;图2 牛组织中添加泰地罗新实验特征离子质量色谱图Fig 2 Typical SRM chromatogram of tildipirosin added in bovine tissues
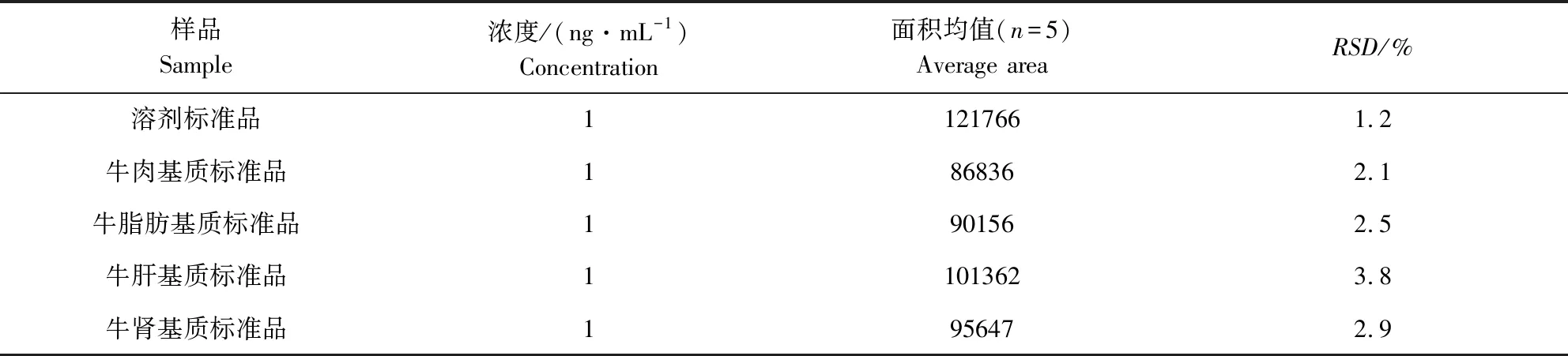
样品Sample浓度/(ng·mL-1)Concentration面积均值(n=5)Average areaRSD/%溶剂标准品11217661.2牛肉基质标准品1868362.1牛脂肪基质标准品1901562.5牛肝基质标准品11013623.8牛肾基质标准品1956472.9
2.3 线性定量范围 将100 μg/mL的泰地罗新标准品贮备液用0.1%甲酸溶液稀释至1 μg/mL的标准中间溶液,再以各种牛组织按1.5项前处理方法处理所得的空白基质溶液稀释标准中间溶液获得1、2、5、20、50、100 ng/mL系列基质标准工作曲线溶液,按1.3项与1.4项仪器条件进样检测。将所得定量通道色谱图积分后面积以Y表示,进样浓度以X表示,所得回归曲线结果如表4所示,其线性相关系数r都大于等于0.995。实验表明,该方法检测泰地罗新在4种牛组织基质中10~1000 μg/kg添加含量范围内线性良好。
2.4 方法准确度与精密度 分别取3批空白牛肉、牛脂肪、牛肝和牛肾中添加定量限(LOQ)、半最大残留限量(1/2MRL)、最大残留限量(MRL)和2倍最大残留限量(2MRL)4个不同含量水平的泰地罗新药物,进行添加回收率测定实验。其中牛肉添加量分别为10、200、400、800 μg/kg;牛脂肪添加量分别为10、100、200、400 μg/kg;牛肝中添加量分别为10、1000、2000、4000 μg/kg;牛肾中添加量分别为10、1500、3000、6000 μg/kg。其中由于牛肝和牛肾中的MRL数值较高,所添加的含量超出了方法的线性定量范围,因此,在按1.5项前处理方法处理后还需再用0.1%甲酸稀释10倍进样分析。所得实验结果如表5所示,实验结果表明,添加回收率在60%~110%范围内,RSD<10%,表明该方法具有较好的准确度与精密度。
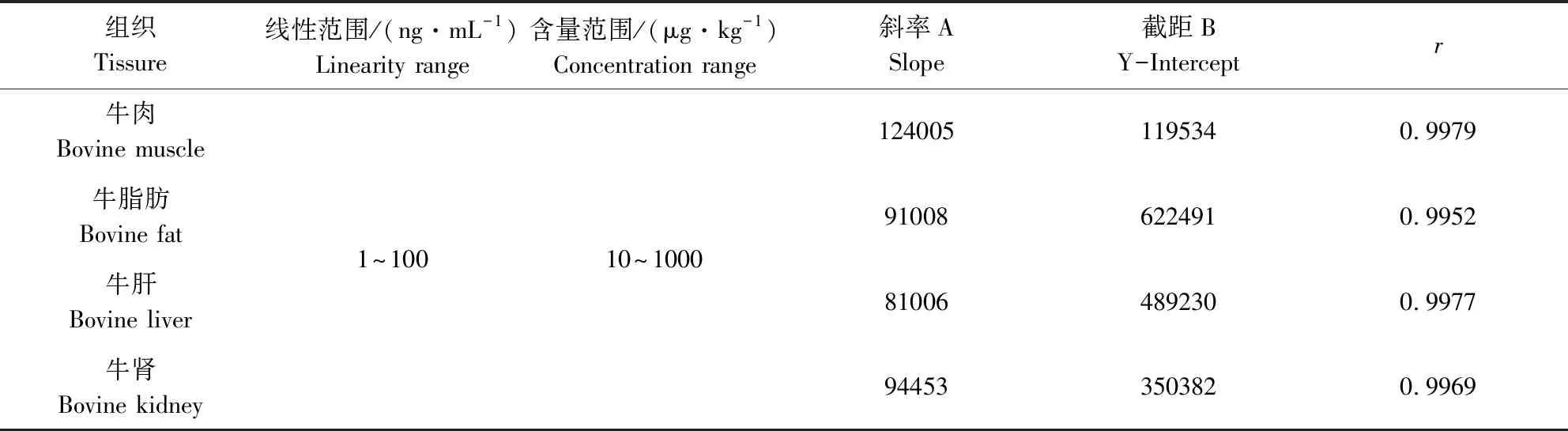
表4 牛组织中添加泰地罗新的标准曲线Tab 4 Standard curve of tildipirosin added in bovine tissure
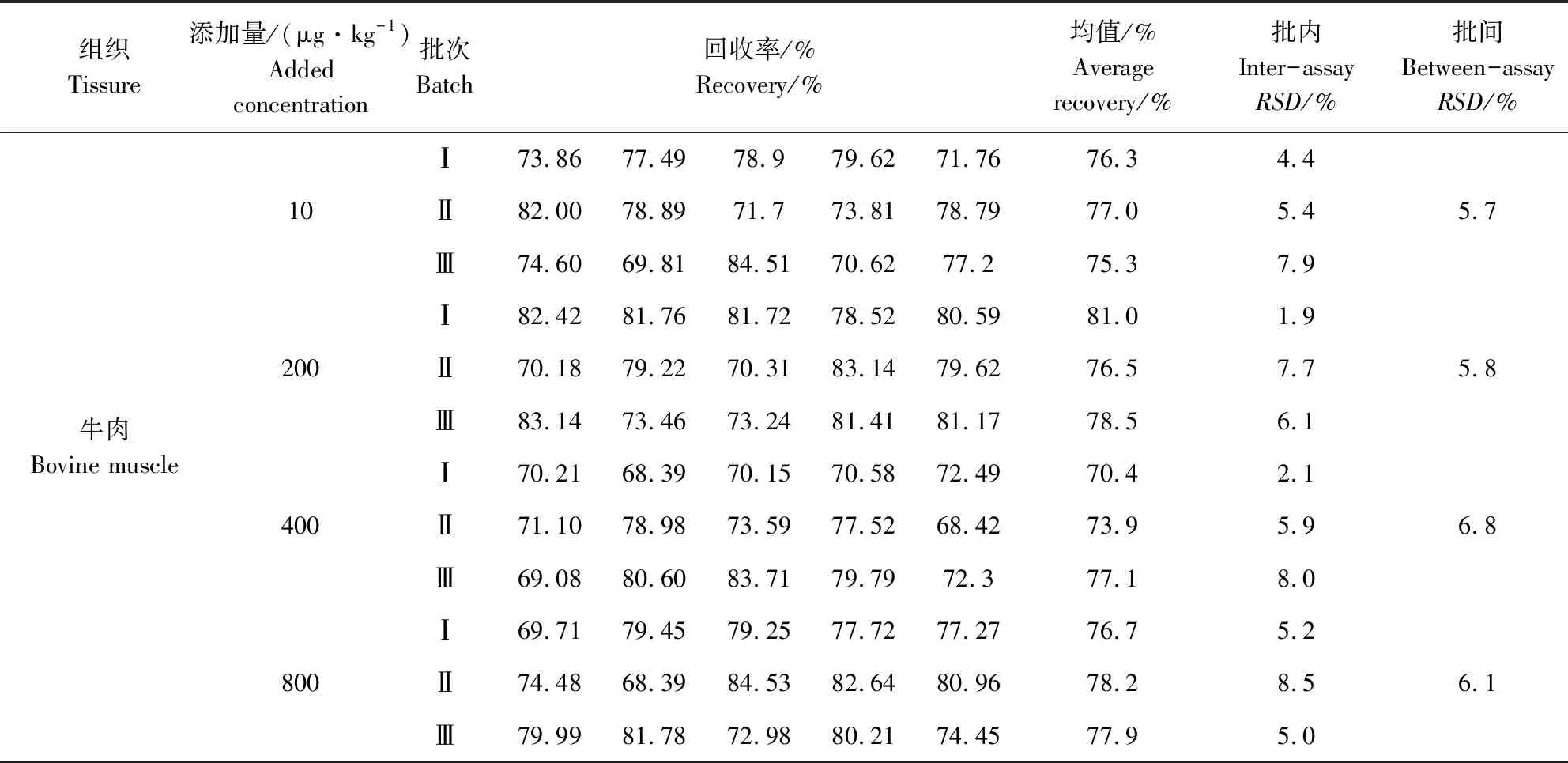
表5 方法准确度与精密度Tab 5 Accuracy and precision of the method

续表
2.5 方法选择性的验证 选择空白牛肉、牛脂肪、牛肝和牛肾各20个空白样品,按优化条件进行处理后上机测定,未发现有假阳性结果,表明该方法的选择性良好。
3 讨论与结论
3.1 提取液提取效率研究 在4种基质中尝试了多种提取液,包括纯乙腈、水、50%乙腈、正己烷、异辛烷提取。2 g空白试样中加入1 μg/mL的标准中间溶液 100 μL,分别加入上述提取液进行振荡提取,之后采用1.5项中前处理条件进行净化,测得结果如表6所示。测试结果表明,泰地罗新属于极性较大的化合物(LogP=4.05),在水和50%乙腈溶液中的提取效率接近90%,在纯乙腈溶液中的提取效率接近70%,而在正己烷或异辛烷这类极性小的溶剂中几乎不溶,因此,选择50%乙腈进行提取,正己烷可用来进行脱脂而不会造成目标药物过多的损失,而异辛烷由于极性太小虽然不会损失目标物但是除酯效果不如正己烷,因此,最终选择正己烷脱脂。
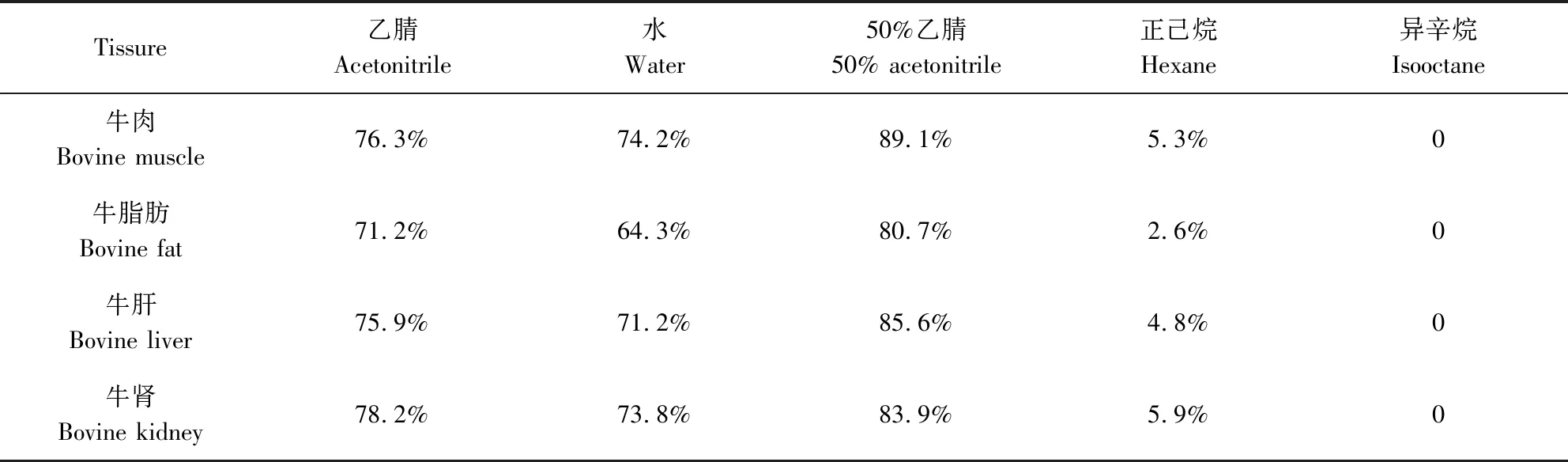
表6 牛组织中泰地罗新提取效率研究Tab 6 Research on extraction rate of tildipirosin added in bovine tissure
3.2 分散相基质的选择 牛组织中的干扰杂质主要以蛋白质和磷脂为主,主要通过无水硫酸镁和氯化钠进行盐析,其对基质中的血细胞之类的生物杂质也有一定的破坏和沉降能力。乙腈在提取的同时也具有破坏蛋白质结构造成沉淀的作用。皮脂和肝脏中不但有蛋白质,还有大量的脂肪会干扰后续的检测,原本尝试使用C18粉末吸附,结果发现在吸附脂肪的同时会造成提取效率的大幅下降,推测是C18粉对目标化合物也有较强的吸附能力,因为在3.1项实验中发现正己烷中泰地罗新溶解性很小,而脂肪在其中的溶解度较高,因此,采用正己烷脱脂。最后,通过高速离心可以将蛋白、磷脂、血细胞等沉降至下层,未溶解的脂肪粒会漂浮在正己烷层的表面,只要吸取中间的乙腈层即可获得富含目标物的提取液。
本研究建立了检测牛肉、牛脂肪、牛肝和牛肾中泰地罗新残留量的液相色谱串联质谱检测方法。前处理使用分散固相萃取法,液相部分使用反相色谱柱进行分离,三重四级杆质谱进行定性定量分析。实验结果表明,方法的最低检出限为5 μg/kg,最低定量限为10 μg/kg,在10~1000 μg/kg范围内线性关系良好(r>0.995),添加回收率在60%~110%,RSD<10%,表明该方法具有较好的灵敏度、准确度与精密度。
