基于十八烷基三甲基溴化铵修饰的磁性粒子在线磁性固相萃取-高效液相色谱法测定水样中磺酰脲类农药
2019-03-08张瑞琪王铁峰
李 迪, 张瑞琪, 王铁峰, 苏 萍, 杨 屹
(北京化工大学理学院, 北京 100029)
20世纪80年代,磺酰脲类除草剂(SUHs)问世,其具有较高选择活性的同时对哺乳动物毒性较低,而且施用剂量小,因此广泛用于主要农作物的除草[1,2]。然而随着磺酰脲类农药在环境中逐年积累,已经在天然水中检测出它们的痕量残留[3]。世界各国高度重视此类农药对环境的危害,我国从2013年起也陆续出台了对此类农药的限制公告[4]。考虑到其在水体中富集后可能通过食物链传导并危害人体健康,高效、灵敏地检测环境水样中的磺酰脲类农药具有实际意义。
磺酰脲类农药施用剂量小,在环境水中浓度较低,须将样品富集后分析。常用的前处理方法有固相萃取(SPE)法[5]和磁性固相萃取(MSPE)法[6]。其中磁性固相萃取是20世纪90年代末发展起来的新型样品前处理方法,其利用磁性粒子吸附样品中的目标化合物[7],实现与复杂基体的高效分离。但在实际的分析工作中,磁性固相萃取与洗脱过程中离线的手工操作(如超声、涡旋等)可能影响分析结果的精密度和准确度。近年来,在线磁性固相萃取技术的发展受到广泛关注[8-10]。在线磁性固相萃取整合了萃取和洗脱过程,实现前处理的自动化,且减少了手工操作误差,提高分析测试的精密度、准确度。
磁性萃取剂是磁性固相萃取的核心。Fe3O4磁性粒子由于表面易被氧化且易团聚,通常对其进行表面修饰以提高磁性粒子的稳定性。表面活性剂是一类两亲性物质,作为一种磁性粒子的表面修饰材料,已经广泛应用于有机化合物的分析中。利用表面活性剂的两亲性,将其与磁性粒子结合到一起,制备一种新型磁性固相萃取剂,以实现对疏水物质的分离富集,这种方法又被称为混合半胶束磁性固相萃取[11]。
本文以简单的两步常温反应合成了表面修饰十八烷基三甲基溴化铵(STAB)的磁性粒子,将其作为萃取剂,利用蠕动泵、聚四氟乙烯管和六通阀等零件设计了一种在线磁性固相萃取装置,与高效液相色谱相结合,应用于水样中两种磺酰脲类农药的检测。
1 实验部分
1.1 仪器、试剂、材料与标准溶液
BT100L流量型智能蠕动泵(保定雷弗流体科技有限公司),聚四氟乙烯硬管(内径1 mm,外径2 mm)(天津第九塑料厂),不锈钢接头(天津舜禹达克科技有限公司),六通阀(天津舜禹达克科技有限公司),软硬对接直通接头(南京市润泽流体控制设备有限公司),倒锥接头(南京市润泽流体控制设备有限公司), Saint-Gobain Norprene Chemical NSF-51 16#管(圣戈班(中国)投资有限公司), BS124S电子分析天平(北京赛多利斯仪器系统有限公司), KQ-100DB型数控超声波清洗器(江苏昆山市超声仪器有限公司), ZNCL-S智能恒温磁力搅拌器(上海予华仪器有限公司), DGX-073B-1电热鼓风干燥箱(上海福玛实验设备有限公司),真空干燥箱(上海一恒科学仪器有限公司),系列移液枪(上海大龙医疗设备有限公司), NDK200-2M自动快速浓缩仪(杭州米欧仪器有限公司),一次性注射器(常州悦康医疗器材有限公司), 0.45 μm滤膜(天津津腾实验设备有限公司), 0.22 μm滤膜(天津津腾实验设备有限公司), Shimadzu 20A Prominence超快速液相色谱仪(岛津公司,日本)配色谱柱Shimadzu InertSustain-C18(150 mm×4.6 mm, 5 μm)。
六水合三氯化铁购自天津市大茂化学试剂厂;甲醇(HPLC级)、乙腈(HPLC级),购自百灵威科技有限公司;原硅酸四乙酯(TEOS)(分析纯)购自北京百灵威科技有限公司;十八烷基三甲基溴化铵(分析纯)购自上海阿拉丁生化科技股份有限公司;无水乙酸钠、氢氧化钠、盐酸(含量37.5%)、乙酸乙酯、二氯甲烷、乙二醇、无水乙醇,购自北京化工厂;丙酮、正己烷,购自北京益利精细化学品有限公司;氨水(分析纯)购自北京化工厂;去离子水,高校自产;娃哈哈纯净水;苄嘧磺隆(BSM)(质量浓度100 μg/mL),购自上海阿拉丁生化科技股份有限公司;氯磺隆(CS)(质量浓度100 μg/mL),购自上海安谱实验科技股份有限公司。
3种环境水样分别采集自北京奥林匹克森林公园、北京西坝河和北京某高校灌溉用水。使用前使用真空抽滤除去不溶性杂质,之后用0.45 μm有机滤膜过滤,储存于玻璃瓶中并置于冰箱中。
1.2 磁性萃取剂的制备
首先以溶剂热法合成Fe3O4磁性微粒[6],再以溶胶-凝胶法[12]在Fe3O4表面修饰SiO2,制备Fe3O4@SiO2磁性微粒,之后以溶胶-凝胶法制备Fe3O4@SiO2@STAB-SiO2磁性粒子。称取0.40 g Fe3O4@SiO2磁性微粒倒入三口烧瓶,称取0.60 g STAB溶解于20 mL无水乙醇和40 mL去离子水的混合溶液,水浴加热至60 ℃充分溶解。将上述溶液及2.2 mL氨水逐滴加入三口烧瓶,机械搅拌30 min后,向三口烧瓶中加入1.0 mL TEOS,持续搅拌6 h,产物以300 mL去离子水和200 mL乙醇各洗涤3次,置于60 ℃真空烘箱中烘干备用。
1.3 在线磁性固相萃取过程
在线磁性固相萃取装置由供液系统和萃取/洗脱切换系统两部分组成。供液系统由两台蠕动泵组成,可以实现进样、洗脱以及管路清洗。萃取/洗脱切换系统由六通阀构成,能实现对萃取和洗脱的实时切换。在线磁性固相萃取柱由一段长3 m的聚四氟乙烯管路绕结于钕铁硼磁铁上,磁铁两侧管路各连接了一个内径3 mm的不锈钢管,内置筛板以防止磁性粒子的流失。系统管路连接情况见图1。
进样模式:提前将70 mg萃取剂超声分散于乙醇后装填入磁性固相萃取柱中。此时六通阀内流路为实线路径所示,量取10 mL实际样于50 mL离心管中,使用0.01 mol/L的盐酸调节pH=4,置于蠕动泵A进样口,触摸操控蠕动泵,设定流速0.6 mL/min开始进样。样品溶液通过磁性固相萃取柱,开始萃取过程,废液用离心管接收至进样完毕。
洗脱模式:切换六通阀至洗脱模式,此时六通阀内流路为虚线路径,量取3 mL甲醇于玻璃试管,置于蠕动泵B进样口,开始洗脱,洗脱液使用玻璃试管接收。产物经过有机滤膜过滤、N2富集后复溶于200 μL乙腈,使用高效液相色谱分析。

图 1 在线磁性固相萃取流程示意图Fig. 1 Schematic diagram of on-line magnetic solid phase extraction (MSPE)PDA: photodiode array detector.
1.4 色谱条件
Shimadzu InertSustain-C18色谱柱(150 mm×4.6 mm, 5 μm);柱温30 ℃;检测波长为233 nm;流动相A为含有0.01%(v/v)三氟乙酸的水溶液,B为乙腈。梯度洗脱程序:0~2.0 min, 30%B~45%B; 2.0~5.0 min, 45%B~50%B; 5.0~8.0 min, 50%B~60%B; 8.0~10.5 min, 60%B。进样体积20 μL;流速1.0 mL/min。
2 结果与讨论
2.1 Fe3O4@SiO2@STAB-SiO2磁性粒子的表征
图2为Fe3O4@SiO2和Fe3O4@SiO2@STAB-SiO2磁性粒子的扫描电镜图。从图2可以看出,STAB修饰前后磁性粒子均为球形,其中Fe3O4@SiO2表面比较光滑、粒径均一,而Fe3O4@SiO2@STAB-SiO2表面厚度有所增加,且较为粗糙。这是由于在合成步骤中,使用氨水将体系pH调控至碱性,此时Fe3O4@SiO2磁性粒子表面带负电荷[13],逐渐滴加STAB溶液的过程中,STAB阳离子通过库仑力吸附在硅层表面,疏水端延伸在溶液中,硅层表面形成单层胶束;随着滴加使STAB浓度增加时,会在单层胶束的基础之上,通过疏水作用力形成双层胶束[14];由于STAB用量大于磁性粒子,可以判断表面厚度增加为STAB形成的双胶束层。

图 2 (a)Fe3O4@SiO2磁性粒子和(b)Fe3O4@SiO2@STAB-SiO2磁性粒子的扫描电镜图Fig. 2 Scanning electron microscopy (SEM) images of (a) Fe3O4@SiO2 magnetic particles and (b) Fe3O4@SiO2@STAB-SiO2 magnetic particles STAB: stearyl trimethyl ammonium bromide.

图 3 STAB、Fe3O4@SiO2磁性粒子、Fe3O4@SiO2@STAB-SiO2磁性粒子的FT-IR谱图Fig. 3 FT-IR spectra of STAB, Fe3O4@SiO2 magnetic particles, and Fe3O4@SiO2@STAB-SiO2 magnetic particles
图3为Fe3O4@SiO2和Fe3O4@SiO2@STAB-SiO2磁性粒子的红外光谱图。由图3可知,1 056.8 cm-1的峰归属于Si-O键弯曲振动,可证明SiO2成功修饰于Fe3O4表面;2 919.7 cm-1和2 850.3 cm-1两个峰可归属为STAB长链中亚甲基的伸缩振动,可以证明STAB已成功包覆到磁性粒子表面。

图 4 Fe3O4磁性粒子、Fe3O4@SiO2磁性粒子、Fe3O4@SiO2@STAB-SiO2磁性粒子的热重分析Fig. 4 Thermogravimetric analysis of Fe3O4 magnetic particles, Fe3O4@SiO2 magnetic particles, and Fe3O4@SiO2@STAB-SiO2 magnetic particles
图4为磁性粒子修饰表面活性剂前后产物的热重分析。由图4可知,Fe3O4@SiO2与Fe3O4磁性粒子相比,在相同时间内质量损失更大,随着STAB在Fe3O4@SiO2表面进一步修饰,最终产物的质量损失速率最大。证明了STAB成功地包覆到磁性粒子表面。
2.2 萃取条件优化
本文优化了在线磁性固相萃取条件。对洗脱剂种类(甲醇、乙腈、二氯甲烷、乙酸乙酯)、洗脱剂用量(1、3、5、7、9 mL)、萃取剂用量(10、30、50、70、90 mg)、离子强度(盐含量0、1%、2%、3%、4%)、溶液pH值(3、4、5、6、7、8),以及进样流速(0.2、0.4、0.6、0.8、1.0 mL/min)6个因素进行了考察。结果表明,甲醇、乙腈都能对目标物质充分洗脱,考虑到毒性,选择甲醇作为洗脱剂。随着萃取剂、洗脱剂用量的增大,萃取效率也增大,但是洗脱剂超过3 mL,萃取剂用量大于70 mg时,萃取效率上升不再明显。离子强度的增大一方面增大了溶液黏度,降低STAB与目标物质的相互作用;另一方面,随着溶液中各种离子总浓度增大,增强了离子间的静电作用,在季铵阳离子周围有更多的阴离子(主要是Cl-),在硅羟基(表面带负电荷)附近存在更多阳离子(主要是Na+),形成了所谓的“离子氛”,使硅羟基与季铵阳离子都受到较强的牵制作用,硅层表面有效吸附的STAB减少,从而降低萃取效率。实验结果表明,盐含量为0时萃取效果最好。检测的两种磺酰脲类农药在水中均呈弱酸性,强酸或碱性条件下易水解,从而降低萃取效率,因此选择pH 4进行萃取。进样流速直接影响萃取剂与目标物质的接触时间是否充分,实验选取0.6 mL/min流速进样,较低的流速能保证萃取效率的同时避免进样过程中材料表面STAB胶层的流失。进样完毕后样品排入废液,不会对后续检测产生干扰。
2.3 方法学评价
首先精确配制质量浓度为200 μg/L磺酰脲混合标准溶液。逐级稀释混标溶液,依次配成质量浓度为1、5、10、20、40、80、160 μg/L的加标水样。在上述适宜条件下,对两种磺酰脲农药进行在线磁性固相萃取,用高效液相色谱-二极管阵列检测器检测,绘制工作曲线。如表1所示,CS在1~160 μg/L范围内呈良好的线性关系,BSM在5~160 μg/L范围内呈良好的线性关系。两种农药线性相关系数(r)良好,均≥0.999 7, CS检出限(LOD,S/N=3)为0.32 μg/L, BSM检出限为1.12 μg/L。选择80 μg/L的加标水样进行6次平行实验以考察方法的重现性,所得峰面积的RSD≤4.2%,证明本方法重现性良好。

表 1 两种磺酰脲类农药的线性范围、线性方程、 相关系数、检出限和相对标准偏差Table 1 Linear ranges, linear equations, correlationcoefficient (r), LODs and RSDs of two sulfonylurea herbicides (SUHs)
CS: chlorsulfuron; BSM: bensulfuron-methyl.y: peak area;x: mass concentration, μg/L.
2.4 与文献方法比较
如表2所示,将本文建立的方法与传统固相萃取、磁性固相萃取磺酰脲类农药进行对比[6,15,16]。结果表明,本方法的回收率、检出限和线性范围能满足定量分析的要求。
2.5 重复使用情况
磁性固相萃取剂的一个优势在于可以回收并重复利用。我们考察了Fe3O4@SiO2@STAB-SiO2磁性粒子的重复使用性。如图5所示,在进行3次萃取后,CS萃取效率仍保留有64.1%, BSM萃取效率
仍保留有88.7%,因此制备的Fe3O4@SiO2@STAB-SiO2磁性粒子较稳定,可重复利用。
2.6 实际样品检测
将本文建立的方法应用于环境水样分析(北京奥林匹克森林公园、北京西坝河和北京某高校灌溉用水),以评估其实际应用价值。如图6所示,富集后的3种环境水样均检测出CS,均未检出BSM。

图 5 萃取剂的可重复使用性Fig. 5 Reusability of the adsorbent
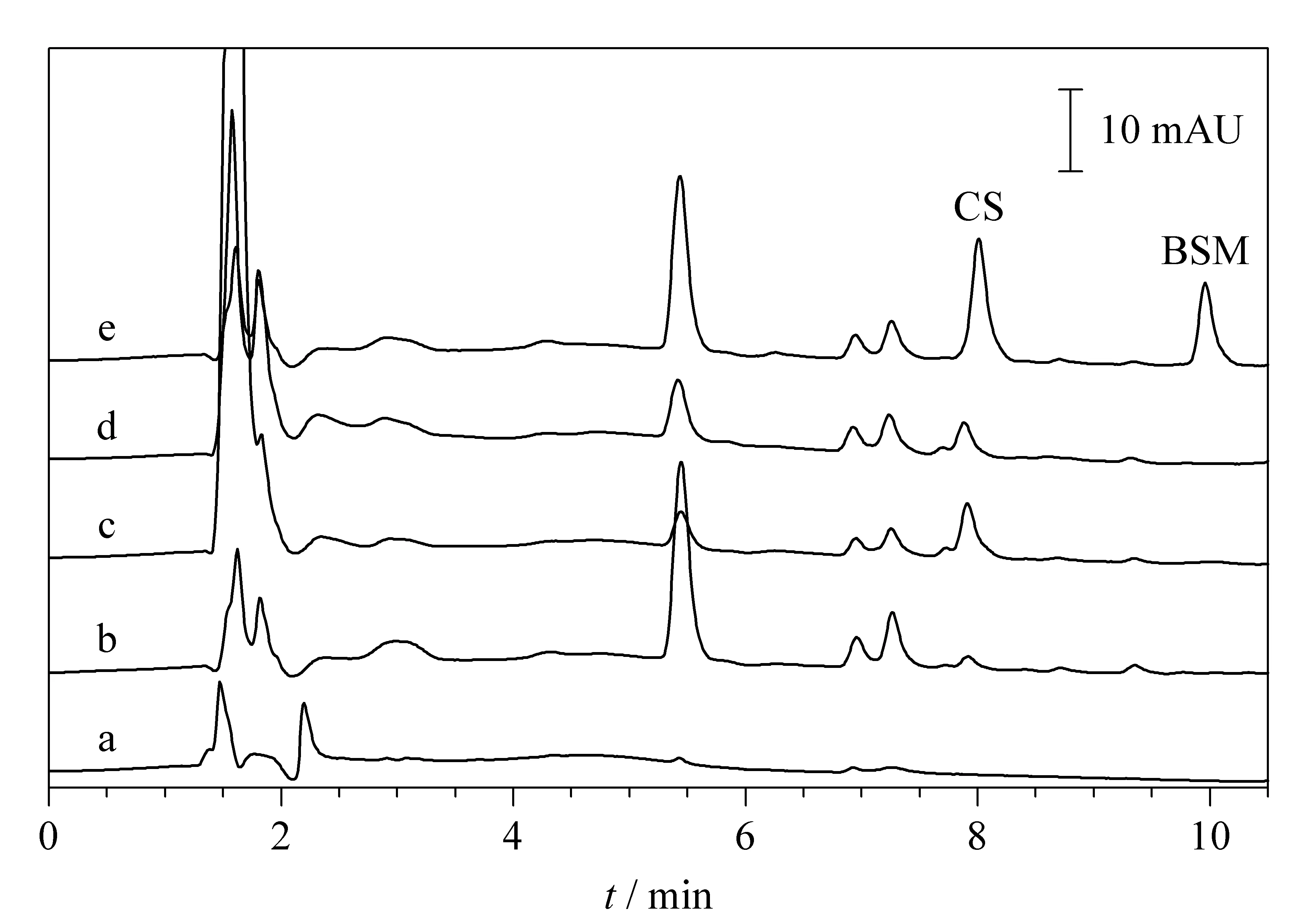
图 6 在线磁性固相萃取前后水样中两种磺酰脲类农药的色谱图Fig. 6 Chromatograms of two SUHs in water samples with or without on-line MSPE a. Olympic park water without on-line MSPE; b. Olympic park water with on-line MSPE; c. Xiba river water with on-line MSPE; d. Irrigation water with on-line MSPE; e. Olympic park water spiked at 50 μg/L with on-line MSPE.

AnalyteMethodSampleLOD/(μg/L)Linear range/(μg/L)Recovery/%RSD/%Ref.BSMMSPE-HPLC-DADwater0.692.5-20082.3-109.75.1-9.4[6]CSUASEME-HPLC-UVwater and soil0.51-10090.6-110.15.1-6.0[15]BSM0.51-10094.0-106.14.7-6.1CSCPE-HPLC-UVwater, soil and rice1.26-200085.4-93.60.4-7.8[16]BSM0.84-200081.9-94.51.9-4.2CSOnline-MSPE-HPLC-DADwater0.321-16070.0-113.40.3-5.0this workBSM1.125-16083.3-101.10.3-10.9
UASEME: ultrasound-assisted surfactant-enhanced emulsification microextraction; CPE: cloud point extraction; DAD: diode array detector.
分别量取10 mL 3种环境水样,两种磺酰脲农药标准品在10、50、100 μg/L 3个不同水平下加标(n=3),再按1.3节和1.4节进行前处理以及检测。计算加标回收率和RSDs,结果如表3,加标回收率在70.0%~113.4%之间,RSD≤10.9%,说明此方法可以应用于分析实际水样中的两种磺酰脲类农药。

表 3 3种水样中两种磺酰脲类农药的加标回收率和相对标准偏差(n=3)Table 3 Spiked recoveries and RSDs of two SUHs in three real water samples (n=3)
-: no data; N. D.: not detected.
3 结论
本实验合成了Fe3O4@SiO2@STAB-SiO2磁性粒子作为萃取剂,合成步骤较为简单,反应条件温和,对磺酰脲类农药有良好的吸附性能。设计并组装了一种在线磁性固相萃取装置,该装置洗脱过程中有机溶剂消耗较少。所建立的在线磁性固相萃取-高效液相色谱联用测定环境水样中两种磺酰脲类农药的方法检出限、回收率及重现性良好,满足定量分析的要求,且一定程度上减小了手工操作带来的误差。与在线固相萃取相比,亦有背压小、萃取剂可重复利用的优势[9,10]。因此,本方法在水样中磺酰脲类农药的检测中有一定的应用价值。
