基于氮化碳复合材料磁性固相萃取结合高效液相色谱法测定尿液中3种羟基多环芳烃
2019-03-08念琪循刘园满王曼曼
念琪循, 刘园满, 孙 冰, 王曼曼
(华北理工大学公共卫生学院, 河北 唐山 063210)
多环芳烃(polycyclic aromatic hydrocarbons, PAHs)是一类由木材、煤炭和烟草等有机物不完全燃烧产生的持久性有机污染物(persistent organic pollutants, POPs)。研究表明,长期暴露在PAHs下可增加人体罹患肺癌、膀胱癌和乳腺癌等癌症的发病率[1]。PAHs广泛分布在大气、土壤、水体和食品等介质中,仅靠外暴露剂量不能准确评价PAHs对健康的影响。羟基多环芳烃(hydroxylated PAHs, OH-PAHs)是PAHs经人体代谢后主要由尿液排出的一类生物标志物,常作为PAHs的内暴露指标用于全面评价PAHs的暴露水平[2]。
分析尿液中OH-PAHs时,由于尿液样品组分复杂,且OH-PAHs在尿液中含量较低,因此需要首先对尿液样品进行前处理以达到净化和富集的目的。目前,尿液中OH-PAHs的前处理通常采用液液萃取法(liquid-liquid extraction, LLE)和固相萃取法(solid-phase extraction, SPE)[2-5]。
磁性固相萃取(magnetic solid-phase extraction, MSPE)是一种以磁性或可磁化的材料作为吸附剂、仅依靠施加外部磁场将目标分析物与样品基质分离的前处理技术。相较常规的液液萃取法和固相萃取法,吸附剂比表面积大,扩散距离短,只需要使用少量的吸附剂和较短的平衡时间就能实现低浓度目标物的有效萃取,已成功应用于环境、食品和医药分析等领域[6-8]。MSPE吸附剂由磁源(通常为Fe3O4)和非磁功能性材料两部分组成,前者提供与外部磁场相互作用的磁性功能,后者为吸附目标分析物提供作用位点。目前,基于石墨烯、碳纳米管、金属有机骨架等功能性材料作为MSPE吸附剂的工作已有报道[9,10],新型MSPE吸附剂材料的开发仍是研究的热点。
氮化碳(carbon nitride, g-C3N4)材料是一种仅由C和N两种元素组成,具有二维蜂窝状晶格结构的新型纳米材料。该材料化学和热稳定性良好、比表面积大,另外,其结构中富N功能基团及电子离域特性使得它能够和一些离子或分子产生络合、疏水、π-π键、氢键、静电力等相互作用,因此有望成为一种理想的吸附分离材料[11]。目前,已有文献[12]报道将g-C3N4材料与Fe3O4通过物理研磨的方式制备得到磁性g-C3N4材料,但通常物理研磨获得的复合材料稳定性欠佳,实际应用有一定的局限性。本研究利用溶剂热法构筑了磁性g-C3N4材料,并结合高效液相色谱-荧光检测,建立了一种简单、快速、高效的人尿液中3种OH-PAHs的分析方法。
1 实验部分
1.1 仪器和试剂
Agilent 1200高效液相色谱仪-荧光检测器(HPLC-FLD,美国Agilent公司); FEI JEM-2800F聚焦离子束/场发射扫描电子显微镜(SEM,美国FEI公司); Brucker D8 VENTURE单晶X射线衍射仪(XRD,德国布鲁克公司); LDJ 9 600-1振动样品磁强计(VSM,美国LDJ公司); Micromeritics ASAP 2460全自动快速比表面积及孔隙分析仪(美国麦克公司)。
所用试剂除特别说明外均为分析纯。尿素和乙二醇(EG)购自上海阿拉丁生化科技股份有限公司;六水合三氯化铁(FeCl356H2O)、三水合乙酸钠(NaOAc53H2O)、乙酸和无水乙醇购自天津市光复精细化工研究所;β-葡萄糖醛酸酶(≥105unites/mL)购自上海市安谱实验科技有限公司;甲醇(MeOH)、乙腈(ACN)、乙酸乙酯和丙酮为色谱纯,均购自赛默飞世尔科技有限公司(美国)。超纯水购自杭州娃哈哈集团有限公司。
1-羟基菲(1-OHPhe,纯度98.0%)、3-羟基菲(3-OHPhe,纯度98.0%)和1-羟基芘(1-OHPyr,纯度98.0%)购自德国Dr. Ehrenstorfer公司,使用MeOH配制以上待测物的储备液,质量浓度为500 mg/L,于4 ℃下避光保存。将储备液用MeOH稀释成质量浓度为1 mg/L的标准工作液。
1.2 磁性g-C3N4的制备
参照Dong等[13]的方法制备g-C3N4材料,将10 g尿素置于箱式电阻炉中,以15 ℃/min的速率从25 ℃升温至550 ℃,维持4 h,待电阻炉冷却至室温后,得到g-C3N4材料。
将270 mg g-C3N4材料经超声均匀分散在一定体积的EG中,加入270 mg FeCl356H2O和700 mg NaOAc53H2O,剧烈搅拌30 min,将所得混合液转移至事先预热的反应釜中,于200 ℃下反应12 h,收集反应产物,使用超纯水和无水乙醇反复洗涤,真空干燥,得到磁性g-C3N4材料(见图1a)。
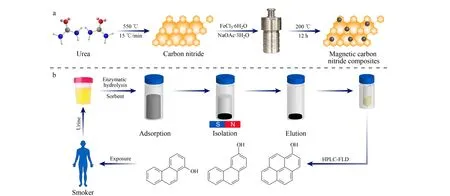
图 1 (a)磁性氮化碳(g-C3N4)材料的制备和(b)磁性固相萃取流程图Fig. 1 Flow chart for (a) the preparation of the magnetic carbon nitride (g-C3N4) composites and (b) the magnetic solid-phase extraction
1.3 尿液样品的制备
采集吸烟志愿者的晨尿,于-20 ℃下冷冻保存。使用时将尿液样品于室温下自然解冻并充分混匀,取5.0 mL于离心管中,加入10 μLβ-葡萄糖醛酸酶和5.0 mL 0.5 mol/L乙酸-乙酸钠缓冲溶液(pH 5),于37 ℃避光水解过夜。将水解后的尿样于1 500 r/min离心10 min,取上清液于4 ℃储存待用。
1.4 磁性固相萃取流程
准确称取4 mg磁性g-C3N4材料,加入2 mL酶解后的尿液样品中,萃取3 min后,利用磁铁将吸附剂与尿液样品分离,弃去上清液。采用0.5 mL丙酮对目标物进行洗脱,充分振荡3 min后,利用磁铁提取洗脱液,重复两次后合并洗脱液,氮吹至干,使用甲醇定容至0.1 mL,待测(见图1b)。
1.5 色谱分离条件
利用Agilent PAH柱(250 mm×4.6 mm, 5 μm,美国Agilent公司)对3种OH-PAHs进行分离,流动相为ACN和水的混合液。梯度洗脱程序为:0~8 min, 55%ACN; 8~10 min, 55% ACN~65%ACN; 10~16 min, 65%ACN。流速为1 mL/min,进样体积为20 μL。3种OH-PAHs的激发(Ex)/发射(Em)波长分别为:284/383 nm(1-OHPhe)、250/360 nm(3-OHPhe)、242/396 nm(1-OHPyr)。
2 结果与讨论
2.1 磁性g-C3N4的表征
通过SEM对复合材料的表观形貌进行表征,如图2a所示,Fe3O4均匀包覆在g-C3N4材料表面;利用XRD对材料的晶体结构进行表征,由图2b可知,复合材料同时具有Fe3O4的衍射峰和g-C3N4材料的特征衍射峰,由以上结果可知,Fe3O4与g-C3N4材料复合成功。经磁强度(见图2c)和比表面积分析后可知,磁性g-C3N4材料的磁化饱和度值为36.4 emu/g,比表面积达到113.7 m2/g,满足磁性固相萃取的需求。

图 2 磁性g-C3N4材料的(a)扫描电子显微镜图(放大倍数20000)、(b)X射线衍射图和(c)磁滞曲线图Fig. 2 (a) SEM image (magnification of 20000), (b) X-ray diffraction (XRD) patterns and (c) magnetization curve obtained for the magnetic g-C3N4 composites
2.2 磁性固相萃取条件的优化
吸附和洗脱条件是决定磁性固相萃取方法准确度的关键因素。本研究考察了吸附剂用量、吸附时间、洗脱溶剂的种类和体积(单次洗脱体积×洗脱次数)对目标物萃取效率的影响。使用2 mL 浓度均为40 μg/L的3种OH-PAHs水溶液进行优化试验,所有试验平行测定3次。
在固定吸附时间为3 min的条件下,考察吸附剂用量为0.5~5 mg时,对3种目标物吸附效率的影响。如图3a所示,当吸附剂用量为0.5~2 mg时,1-OHPyr的吸附效率达到最大,1-OHPhe和3-OHPhe的吸附效率逐渐增加;当继续增加吸附剂用量至4 mg时,1-OHPyr的吸附效率无显著变化,1-OHPhe和3-OHPhe的吸附效率均达到最大值。继续增加吸附剂用量至5 mg, 3种OH-PAHs的吸附效率均不再变化,故选用4 mg为最优吸附剂用量。

图 3 (a)吸附剂用量、(b)吸附时间、(c)洗脱溶剂和 (d)洗脱体积(单次洗脱体积×洗脱次数)对3种OH-PAHs萃取效率的影响(n=3) Fig. 3 Effects of the (a) amount of sorbent, (b) extraction time, (c) eluting solvent, and (d) eluting volume (single eluting volume×eluting times) on the extraction efficiencies of the three OH-PAHs (n=3)
固定吸附剂用量为4 mg,考察吸附时间为1~4 min对目标物吸附效率的影响。如图3b所示,当吸附时间为1 min时,1-OHPyr即达到吸附平衡,1-OHPhe和3-OHPhe的吸附效率仍在增加;继续增加吸附时间到3 min, 1-OHPyr吸附效率无明显变化,1-OHPhe和3-OHPhe均达到吸附平衡。继续增加吸附时间至4 min后,3种OH-PAHs的吸附效率均无显著变化,故选用3 min作为吸附时间,同时说明本方法可以快速吸附样品中的3种OH-PAHs。
在最优的上样条件下,考察MeOH、ACN、丙酮和乙酸乙酯作为洗脱溶剂对目标物回收率的影响。如图3c所示,洗脱溶剂为丙酮时3种目标物的回收率最佳。同时考察了洗脱溶剂的体积(单次洗脱体积×洗脱次数)对目标物回收率的影响,如图3d所示,洗脱体积从0.5 mL×1次增加至0.5 mL×2次时,3种目标物的回收率增加,当继续增加洗脱体积至0.5 mL×3次和0.5 mL×4次时,目标物的回收率下降,这是由于洗脱溶剂体积过大时,氮吹时间延长导致目标物损失,因此选用0.5 mL×2次的丙酮作为最佳洗脱条件。
2.3 方法验证
2.3.1线性范围、检出限和定量限
采用质量浓度为0.25~250 μg/L的OH-PAHs标准溶液进行分析,建立标准曲线。如表1所示,本方法在0.25~250 μg/L范围内对3种OH-PAHs均表现出良好的线性关系,相关系数(r)均为0.999。以信噪比为S/N=3和S/N=10计算方法的检出限(LODs)和定量限(LOQs),分别为0.08和0.25 μg/L。结果表明本方法具有良好的灵敏度。

表 1 本方法的线性范围、线性方程、相关系数、检出限和定量限Table 1 Linear ranges, linear equations, correlationcoefficients (r), LODs and LOQs of this method
y: peak area;x: mass concentration, μg/L.
2.3.2回收率和精密度
对同一尿液样品,将1-OHPhe、3-OHPhe和1-OHPyr标准品分别添加至0.5 、1.25 和2.5 μg/L 3个水平 ,经本方法前处理后,计算样品的加标回收率,以日内和日间分别重复3次测定得到的色谱峰面积的相对标准偏差(RSD)计算精密度,结果如表2所示,方法对3种OH-PAHs的回收率为90.1%~102%,日内精密度为1.5%~7.7%,日间精密度为2.2%~8.7%,表明本方法具有良好的准确度和重复性。

表 2 本方法的回收率和精密度(n=3)Table 2 Recoveries and precisions of this method (n=3)

图 4 加标3种OH-PAHs(均为2.5 μg/L)的尿液样品 酶解后(a)直接进样、(b)经本方法前处理后进样及(c)OH-PAHs标准溶液色谱图 Fig. 4 Chromatograms of the enzymatic hydrolyzed urine sample (spiked with 2.5 μg/L of each OH-PAH) (a) with direct analysis, (b) pretreated by this method before the analysis, and (c) the standard solution of OH-PAHs
2.3.3净化和富集效果
在最优条件下,结合HPLC-FLD分析,将加标3种OH-PAHs(质量浓度均为2.5 μg/L)的尿液样品酶解,经本方法富集净化前后分别进样分析。图4a为直接将尿液样品进行分析的结果,杂质峰明显,3种OH-PAHs均有检出,但样品峰响应较低;而经过本法固相萃取后,如图4b所示,杂质峰明显降低,在对应OH-PAHs出峰位置(见图4c)均检出样品峰且响应高于直接进样的结果,说明该方法能够有效去除尿液中的杂质,富集OH-PAHs,当酶解后的尿液上样体积为2 mL时,对OH-PAHs的富集倍数为10。
2.4 实际样品分析
利用本方法对4名吸烟志愿者的尿液样品进行分析。如表3所示,有2例样品中检出1-OHPhe,质量浓度分别为(1.65±0.04)和(1.75±0.02) μg/L;有3例样品检出3-OHPhe,质量浓度为(1.89±0.05)~(2.26±0.10) μg/L;全部样品均检出1-OHPyr,质量浓度为(4.24±0.02)~(4.46±0.01) μg/L。为了进一步说明本方法的可行性,对4例实际尿液进行加标回收试验,加标浓度为2.5 μg/L,对尿液中的OH-PAHs的回收率为90.7%~108%, RSD≤8.2%,方法准确度和精密度令人满意。

表 3 吸烟志愿者尿液中的OH-PAHs分析结果(n=3)Table 3 Analytical results of OH-PAHs in the urine samples of smoking volunteers (n=3)
2.5 与文献方法对比
将本方法同文献[3-5,14]方法进行对比(见表4),本方法灵敏度与文献方法相当,且方法准确可靠,吸附剂用量仅需要4 mg, 3 min即可完成吸附,说明本方法简单、快速、高效,可用于人尿液中OH-PAHs的常规分析。

表 4 本方法与文献方法对尿液中OH-PAHs分析结果的对比Table 4 Comparison of the analysis results of this method with methods in literatures for the determination of OH-PAHs in urine
DLLME: dispersive liquid-liquid microextraction; MSPE: magnetic solid-phase extraction.
3 结论
本研究首次以溶剂热法制备磁性g-C3N4材料,将其用于尿液中3种OH-PAHs的前处理中,并结合HPLC-FLD对吸烟志愿者的尿液样品进行分析。本方法能够简单、快速、高效的富集和净化尿液中的3种OH-PAHs,展现了良好的应用前景。
