SCN1A基因多态性与卡马西平治疗壮族癫痫患者疗效的关系
2019-03-08黄建敏钱哲陈海燕黄清黄灵刘国军唐雄林
黄建敏 钱哲 陈海燕 黄清 黄灵 刘国军 唐雄林
右江民族医学院附属医院神经内科(广西百色533000)
癫痫遗传学研究表明,基因突变是神经元异常放电的病理生理学基础,在癫痫发病机制中起关键性作用[1],同时又是耐药性癫痫形成的重要机制。电压门控性Na+通道(voltage-gated sodium channel,VGSC 或Nav)是神经元膜兴奋性改变的主要通道,其中SCN1A 通道是该通道的关键性亚型,研究发现,SCN1A 通道基因突变导致结构或功能改变可诱发神经元异常放电癫痫发作,甚至出现抗癫痫药物有效治疗量变化以及造成对某些抗癫痫药物抵抗[2-4]。基因突变的影响因素非常复杂,如地理环境、气候条件、种族因素等。本课题组既往对百色地区癫痫患者的流行病学研究发现,该地区癫痫发病率及患病率均高于全国平均水平,治疗依从性极差,2∕3 在农村地区[5],最近对该地区癫痫患者SCN1A 基因全系列测序分析,发现rs4667869 和rs10497275 突变率较高[6],推测rs4667869、rs10497275 多态性与卡马西平疗效可能存在一定关联性。本研究拟应用MassARRAY-IPLEX 和基质辅助激光解吸电离飞行时间质谱(Matrix-assisted laser desorption∕ionization time of flight mass spectrometry,MALDI-TOFMS)技术对186 例卡马西平规范治疗的壮族癫痫患者SCN1A 基因rs4667869 和rs10497275 位点基因型检测,探讨该基因多态性对百色地区壮族癫痫卡马西平疗效的影响,从基因水平为壮族癫痫患者影响卡马西平疗效的病因学提供理论依据。
1 资料与方法
1.1 一般资料 2014年1月至2017年8月右江民族医学院附属医院神经内科住院或门诊确诊的186 例癫痫患者。入选标准:(1)根据临床表现,结合脑电图和影像学(头颅MRI 或头颅CT)检查结果由临床医生确诊;(2)诊断参照1981年或1989年国际抗癫痫联盟制定标准,发作类型:部分性发作及全面性发作;(3)年龄18 ~60 岁,三代均为壮族;(4)卡马西平规范治疗1年以上,初始剂量每次100 ~200 mg,每天1 ~2 次,逐渐增加剂量,最大剂量每天1 200 mg;(5)自愿参加本研究。排除标准:(1)同时服用其他抗癫痫药或其他钠离子通道阻断药,如普罗帕酮;(2)严重器质性病变如恶性肿瘤、严重高血压、不稳定性心脏病、血液病、肝肾功能不全;(3)进行性器质性脑病或其他中枢神经系统疾病。疗效判断:(1)有效:固定剂量治疗1年内均没有任何类型癫痫发作或发作频率减少达50%以上;(2)无效:1年内经过最大剂量治疗仍无法控制发作或发作频率减少低于50%,需要改用其他抗癫痫药物治疗。根据疗效标准,有效组66例,无效组120 例,两组间发作类型、用药剂量、病程、年龄等差异均无统计学意义(P>0.05)。本研究已通过伦理委员会审查批准,所有患者均签署了知情同意书。
1.2 方法
1.2.1 卡马西平血药浓度测定 利用反相高效液相色谱法检测卡马西平血药浓度。卡马西平达到稳态血药浓度后于下次服药前空腹抽取静脉血3 mL,3 500 r∕min 离心5 min,抽取500 μL 血清加入内标艾司唑仑(0.229 8 mg∕mL)15 μL 及乙酸乙脂4 mL,3 000 r∕min 震荡离心3 min,吸取上清液,45 ℃水浴吹干,加入100 μL 甲醇溶解备用。Waters 高效液相色谱仪,色谱条件:Nova-Pak C18柱,3.9 mm ×150 mm,4 μm;流动相为甲醇:水(46:54),流速120 mL∕min,柱温35 ℃,检测波长210 nm,取20 μL 进样。
1.2.2 DNA 提取 抽取外周静脉血3 mL,3 500 r∕min 离心5 min,用下层血凝块提取DNA,试剂盒为康为世纪生物科技有限公司,保存于-80 ℃备用。采用紫外分光光度仪测定DNA 纯度,其A260∕A280范围在1.6 ~2.0 之间。
1.2.3 位点选择和引物设计 Pubmed 中检索SCN1A基因全序列,利用Haploview软件(version4.2)选取标签性rs4667869 和rs10497275 为研究靶点,通过Assay Designer(Sequenom 公司)软件设计引物,rs4667869 特异性扩增上游引物为5′-ACGTTGGATGCTCCATAGAGAAGTTGAGTG-3′,下游引物为5′- ACGTTGGATGTGAGGTTGGGGAGGTAGAC-3′,单碱基延伸引物为5′-CGTTTTACTTAAGGGTTGTT-3′。rs10497275 特异性扩增上游引物 为 5′ - ACGTTGGATGCCTGTGTAAAGCTTGCACTC-3′,下游引物为5′- ACGTTGGATGGCTCTCAGCAAGGTTGACAC-3′,单碱基延伸引物为5′-CTGCACGTTTGAGCAAACAAATAA-3′。
1.2.4 单核苷酸多态性检测及基因分型 应用MassARRAY-IPLEX 和MALDI-TOF-MS 技 术 对SCN1A rs4667869 和rs10497275 基因分型。(1)PCR扩增:样本纯化后将DNA 稀释至20 ng∕μL,建立PCR 反应体系:取DNA 样本1 μL、水1.850 μL、25 mmol∕L MgCl20.325 μL、PCR 缓冲液(含15 mmol∕L MgCl2)0.625 μL、25 mmol∕L dNTP 0.100 μL、PCR 引物1 μL、HotStar Taq(Qiagen)酶0.1 μL,反应条件:94 ℃5 min,90 ℃20 s,56 ℃30 s,进行43 个循环,最后72 ℃2 min。(2)虾碱性磷酸酶(shrimp alkaline phosphatase,SAP)反应:添加0.3 U 的SAP 去除反应剩余的dNTP,反应条件为:37 ℃40 min,85 ℃5 min。(3)单碱基延伸反应:向SAP 反应体系加0.940 μL 延伸引物、0.619 μL 水、0.2 iPLEX 缓冲液、0.2 μL 终止混合物,反应条件为94 ℃30 s、92 ℃10 s、56 ℃10 s、76 ℃5 s、52 ℃5 s,5 个步骤进行42 次循环,最后72 ℃2 min。(4)质谱检测:阳离子交换树脂将产物脱盐,384 孔SpectroCHIP bioarray 芯片(Sequenom)点样,MALDI-TOF-MS 技术检测多态性,MassARRAY Typer4.0 软件进行基因分型。
1.2.3 基因型判定 计算产物峰值与相应引物峰值之间的质荷比,确定所延伸类型,判定该位点基因型(表1)。

表1 各系列对应分子量Tab.1 The corresponding molecular weight of each succession
1.3 统计学方法 所有数据采用SPSS 22.0 进行统计学分析,对患者基因型分布频率进行Hardy-Weinberg 平衡检验,计数资料间比较采用χ2检验,计量资料间比较采用t检验,P<0.05 为差异有统计学意义。
2 结果
2.1 Hardy-Weinberg 遗传平衡检验 对所有癫痫患者rs4667869 和rs10497275 位点基因型分布频率测量值与预测值的差异性进行分析,结果发现各个位点均符合Hardy-Weinberg 遗传平衡(P>0.05),说明样本具有代表性。
2.2 基因型特征质谱图 rs4667869 杂合子GC 基因型在G 和C 等位基因处均出现强度信号峰,纯合子GG、CC 基因型只有在G、C 等位基因处才出现强度信号峰(图1);rs10497275 杂合子GA 基因型在G 和A 等位基因处均出现强度信号峰,纯合子GG、AA 基因型只有在G、A 等位基因处才出现强度信号峰(图2)。
2.3 rs4667869 和rs10497275 多态性与卡马西平疗效的关系 无效组与有效组相比,rs4667869 位点等位基因分布(χ2= 11.790,P= 0.001)和基因型分布(χ2= 10.655,P= 0.005)差异均有统计学意义(表2),而rs10497275 位点等位基因分布(χ2=3.335,P= 0.068)和基因型分布(χ2= 3.046,P=0.218)差异均无统计学意义(表3)。rs4667869CC基因型与GG + GC 基因型相比,CC 基因型对卡马西平抗癫痫疗效更低,OR值(95%可信之间)为2.800(1.495 ~5.244)(表4)。
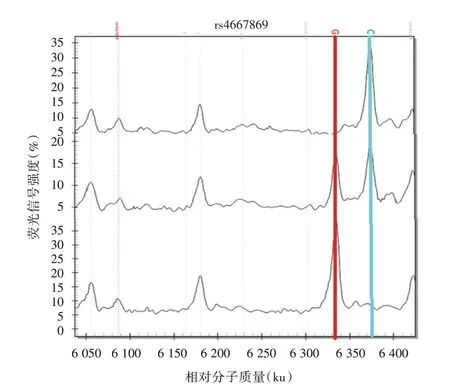
图1 rs4667869 基因型特征质谱图Fig.1 The feature spectrogram of rs4667869 genotype
2.4 有效组rs4667869 和rs10497275 多态性与卡马西平血药浓度的关系 在卡马西平治疗有效的66 例患者中,rs4667869 位点GG+GC 基因型和CC基因型患者的血药浓度比较(t= 1.273,P=0.083),差异无统计学意义(表5);rs10497275 位点GG + GA 基因型和AA 基因型患者血药浓度比较(t= 0.963,P= 0.064),差异也无统计学意义(表5)。

图2 rs10497275 基因型特征质谱图Fig.2 The feature spectrogram of rs10497275 genotype
3 讨论
卡马西平作用于神经元Nav 的药物作用靶点,阻断动作电位的发散和神经递质的释放发挥抗癫痫作用。SCNlA 基因编码了神经元Nav 1.1 的a1 亚单位,定位于染色体2q24.3 位置,在动作电位的产生和传播起到至关重要的作用,SCN1A 通道是神经元Nav 最为关键性亚型。基因水平研究显示,SCN1A 基因突变可改变钠离子通道的电生理功能,导致钠离子通道活性增高或降低均可引起癫痫发作,同时由于钠通道功能的改变,造成卡马西平作用靶点功能下降,从而影响疗效,导致癫痫耐药发生[7]。临床病例研究证实,该基因是一些癫痫发病的最重要基因,并发现某些位点突变可导致卡马西平疗效下降[8]。
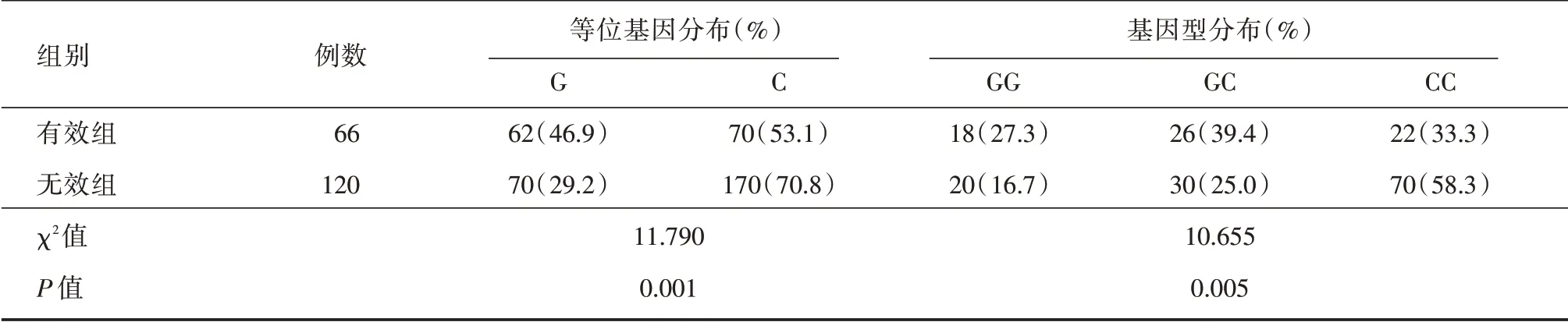
表2 有效组和无效组SCN1A 基因位点rs4667869 多态性分布Tab.2 The distribution of polymorphisms of SCN1A genes rs4667869 in effective group and ineffective group
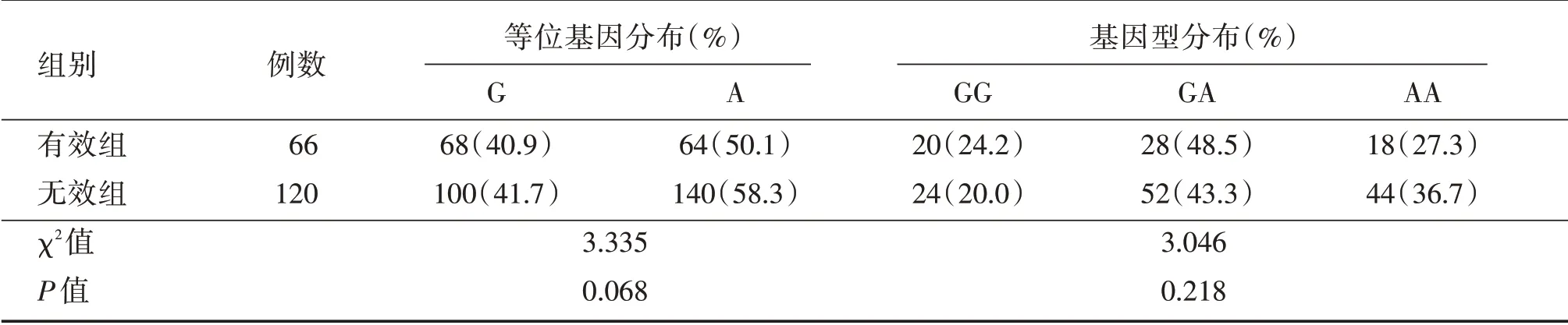
表3 有效组和无效组SCN1A 基因位点rs10497275 多态性分布Tab.3 The distribution of polymorphisms of SCN1A genes rs10497275 in effective group and ineffective group
在所有已知的癫痫相关基因中,SCN1A 基因是人类癫痫最常见的突变基因,被称为超级罪犯基因,目前数据库检索发现有1 504 种突变,但是有关SCN1A 基因多态性对抗癫痫药物疗效影响国内研究较少。国外学者已经在体外证实SCN1A 的外显子突变可以影响大部分抗癫痫药物的疗效[9]。基因突变受到遗传和环境因素影响,使其多态性在不同种族和不同地理环境的患者存在着明显的差异性,导致一些疾病在不同种族间发病率、疾病表型和对药物的疗效存在显著不同。百色地区是中国壮族聚集地,属亚热带气候,每年5、6月份持续38 ℃高温,铝土矿含量极大丰富,已经大规模开采露天暴露20 余年,基于这些特殊的民族分布、季候条件和地理环境对基因突变有较大的影响,百色地区癫痫患者SCNIA 基因多态性与卡马西平抗癫痫疗效相关性可能更加复杂化。
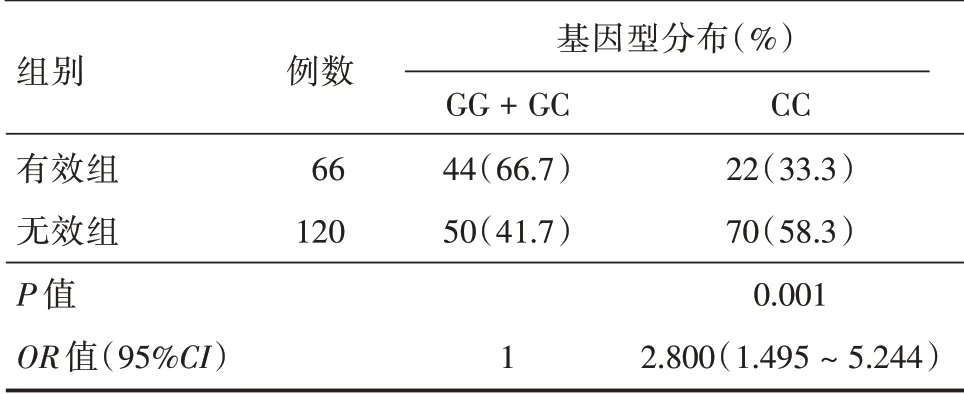
表4 rs4667869 基因型与卡马西平疗效的关联分析Tab.4 The association analysis between rs4667869 genotype and efficacy of carbamazepine
表5 rs4667869 基因型与卡马西平疗效的关联分析Tab.5 The association analysis between rs4667869 genotype and efficacy of carbamazepine ±s
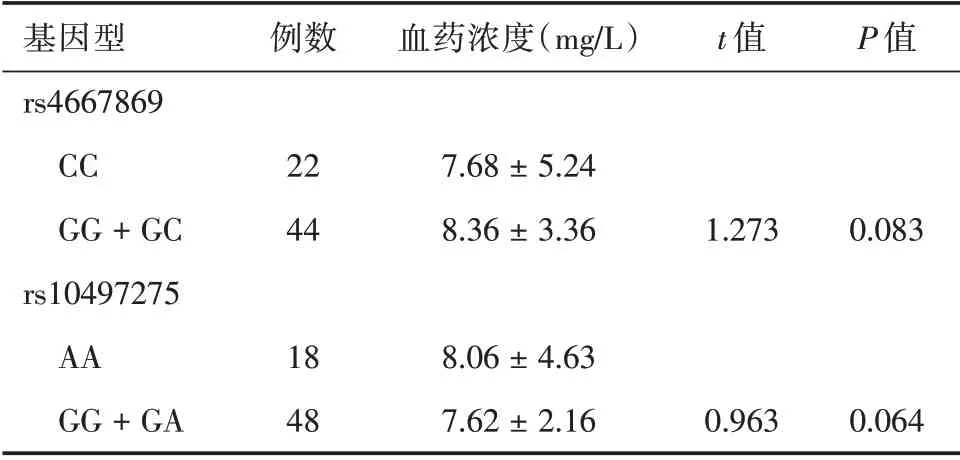
表5 rs4667869 基因型与卡马西平疗效的关联分析Tab.5 The association analysis between rs4667869 genotype and efficacy of carbamazepine ±s
基因型rs4667869 CC GG+GC rs10497275 AA GG+GA例数22 44 18 48血药浓度(mg∕L)7.68±5.24 8.36±3.36 8.06±4.63 7.62±2.16 t 值1.273 0.963 P 值0.083 0.064
笔者关注新发现的内含子rs4667869 和3′-非编码区rs10497275 多态性对卡马西平疗效的影响。本研究利用MassARRAY-IPLEX 和MALDITOF-MS 技术对186 例壮族癫痫患者SCNIA 基因rs4667869 和rs10497275 多态性检测,分析这两个位点多态性与卡马西平疗效的相关性,结果发现,无效组与有效组相比,rs4667869 基因型分布和等位基因分布的差异均具有统计学意义,无效组CC基因型比例明显高于有效组,而rs10497275 基因型分布和等位基因分布的差异均没有统计学意义,与GG+GC 基因型相比,rs4667869 的变异纯合子CC 基因型对卡马西平疗效更低,OR值(95%CI)为2.800。这研究结果表明SCNIArs4667869 多态性对卡马西平治疗壮族癫痫的敏感性有一定的影响,基因型为CC 的患者对卡马西平相对不敏感,达到治疗目标比GG 或GC 型的患者需要更大的药物剂量或更高的血药浓度,原因可能是该位点突变影响Na+通道mRNA表达、蛋白合成和转运,导致通道结构和功能改变,使得卡马西平作用位置和功能变化,从而导致卡马西平治疗无效或有效治疗剂量的改变。国内学者赵昕等[10]对卡马西平治疗儿童癫痫疗效的研究,发现基因SCN1Ars3812718 位点多态性与卡马西平耐药性癫痫有关,与本研究具有类似结果。
本研究同时对有效组66 例患者rs4667869 和rs10497275 多态性与卡马西平血药浓度的关系进行相关分析,结果发现这两个位点不同基因型患者血药浓度差异无统计学意义(P>0.05),表明SCNIA 只是卡马西平抗癫痫作用靶点而不是代谢途径,对卡马西平代谢没有影响,提示SCNIA 基因突变只有影响卡马西平抗癫痫效应,不会影响患者血药浓度。
本研究证实SCNIA 多态性影响百色地区壮族癫痫卡马西平抗癫痫效应,可能是壮族癫痫卡马西平耐药性形成机制之一,但只是局限在两个位点的独立研究。基于百色地区民族分布、季候条件和地理环境等特异性,如果要得到可靠的结论,必须扩大样本、细分民族,分析季候环境的影响,同时研究每个突变位点,以全面了解各个因素的作用方式和效应,才有可能进一步阐明百色地区壮族癫痫卡马西平耐药性癫痫形成机制,有效开展临床个体化治疗。
