响应面法优化羟丙基壳聚糖的合成工艺
2019-03-04郭睿,张瑶,韩双,王宁
郭 睿, 张 瑶, 韩 双, 王 宁
(陕西科技大学 教育部轻化工助剂化学与技术重点实验室, 陕西 西安 710021)
壳聚糖(CTS)是2-氨基-2-脱氧-β-D-葡萄糖通过β-(1,4)糖苷键连接而成的直链多糖,是一种天然存在的阳离子多糖[1],可由甲壳素经浓碱处理脱去N-乙酰基制得。因CTS结构中含有大量羟基及氨基,可用于吸附废水中杂质,CTS作为天然絮凝剂具有广泛的应用前景[2-3]。但因CTS水溶性差,只能溶解于酸性溶液中,应用范围受到很大限制[4-5]。目前改善壳聚糖水溶性的方法有羧甲基化、羟丙基化、烷基化以及通过化学反应引入亲水基团等[6-8]。由于羟丙基壳聚糖(HPCS)保留了CTS原有的碱性和正电性,同时又改善了CTS的水溶性,所以近些年成为了研究重点[9]。施亦东等[10]在异丙醇为溶剂的条件下,用环氧丙烷与碱化壳聚糖反应合成HPCS,研究表明:HPCS具有良好的水溶性,且保湿性和抗菌性较CTS都有显著的提高,但对HPCS的相对分子质量没有进行分析。温俊杰等[11]通过微波法由壳聚糖与环氧丙烷反应制备HPCS,虽然各项性能得到提高,但制备过程中需要特殊仪器。钟超等[12]在碱性环境下,以 CTS-Fe(Ⅱ)为反应物,环氧丙烷为改性剂,10%四甲基氢氧化铵为催化剂合成了壳聚糖亚铁离子配合物的羟丙基化产物[HPCTS-Fe(Ⅱ)],但CTS需要碱化过夜,耗时长,且相对分子质量大幅度降低。相对分子质量是絮凝剂的一个重要指标,相对分子质量高,在絮凝过程中可通过吸附架桥作用絮凝水中杂质。而特性黏数越大,则絮凝剂的相对分子质量越高。因此,可以通过分析HPCS的特性黏度来研究其相对分子质量。响应面法是一种较为科学和高效的工艺参数优化方法,可以在保证实验精度的基础上,尽量减少实验的次数[13]。本研究采用CTS、环氧丙烷为原料,异丙醇为溶剂,在NaOH碱化的条件下合成羟丙基壳聚糖(HPCS);并以特性黏数为指标,在单因素试验基础上,通过响应面设计实验优化了HPCS的最佳合成工艺参数,以期为羟丙基壳聚糖的工业化应用提供原料来源。
1 实 验
1.1原料、试剂与仪器
壳聚糖(BR,脱乙酰度88%,相对分子质量4.2×105),山东西亚化学工业有限公司;环氧丙烷、异丙醇、乙醇、氢氧化钠,均为市售分析纯;25%四甲基氢氧化铵水溶液、茚三酮、 98%浓硫酸,均为化学纯。
VECTOR-22型傅里叶变换红外光谱(FT-IR)仪、ADVANCⅢ400 MHz 型核磁共振氢谱(1H NMR)仪(以D2O为溶剂,TMS为内标),德国Burker公司;乌氏黏度计(Φ=0.5~0.6 mm),上海启航玻璃仪器厂;Q45+EDAX OctanePrime 型环境扫描电镜(ESEM),美国FEI公司;Ultima IV型X射线衍射(XRD)仪,上海仁特检测仪器有限公司;Cary 60型紫外光谱仪,美国安捷伦科技有限公司。
1.2羟丙基壳聚糖(HPCS)的合成方法
将1 g壳聚糖粉末浸泡在30 mL质量分数为20%~50%NaOH溶液中,溶胀10~60 min,除去上层碱液,取20 mL异丙醇,将碱化过的壳聚糖加入异丙醇中。搅拌30 min后,升温至40~80 ℃,再缓慢加入6~16 g的环氧丙烷和2 mL质量分数10%的四甲基氢氧化铵溶液。继续反应3~8 h,将得到的悬浮液静置一段时间,除去上层清液,加入20 mL去离子水溶解。用质量分数18.5%的盐酸调节溶液pH值至7,加入50 mL的丙酮/乙醇(体积比2∶1)混合溶液,静置后抽滤,然后依次用丙酮和乙醇洗涤、干燥后得到粗产物。以乙醇为溶剂索氏抽提8 h,在50 ℃下干燥后得到淡黄色的羟丙基壳聚糖。反应方程式如下:
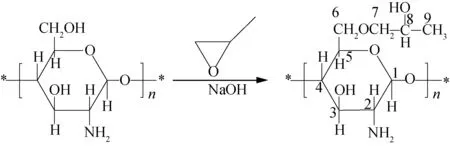
1.3分析与表征
1.3.1FT-IR分析 采用KBr压片法,使用傅里叶红外光谱仪对CTS和HPCS进行表征。
1.3.21H NMR分析 以D2O为核磁试剂,使用核磁共振仪对HPCS进行1H NMR表征。
1.3.3XRD分析 将CTS和HPCS用X射线衍射仪进行测试,扫描范围2θ为5~60°。
1.3.4ESEM分析 采用环境扫描电镜对CTS及HPCS进行测试,测试电压30 kV。
1.3.5特性黏数的测定 称取0.06 g充分干燥的羟丙基壳聚糖溶于50 mL CH3COOH/NaCl(物质的量比2∶1)混合溶液中,在25 ℃下使用乌氏黏度计测定空白溶剂及HPCS混合溶液在管中流下所用时间t0和t,采用一点法(式(1))计算得到HPCS的特性黏数([η]),平行测定3次取平均值[14-15]。根据式(2),计算HPCS的黏均相对分子质量(Mv)。
[η]=[ηsp+3lnηr]/4C
(1)
(2)
式中:ηr—相对黏度,ηr=t/t0;ηsp—增比黏度,ηsp=ηr-1;C—羟丙基壳聚糖溶液质量浓度, g/mL;Mv—HPCS的黏均相对分子质量。
1.3.6取代度的测定
1.3.6.1标准曲线的绘制 分别配制10、 20、 30、 40和50 mg/L的1,2-丙二醇标准溶液。量取不同质量浓度的丙二醇标准溶液各1 mL于25 mL具塞比色管中,在冷水浴条件下缓慢向管内加入8 mL浓硫酸,摇匀,于100 ℃加热3 min后,放入冰浴冷却,分别加入1 mL质量分数2%的茚三酮,30 ℃水浴静置20 min,加浓硫酸定容至25 mL,静置10 min,取出置于比色皿中,以1 mL蒸馏水作空白参比,测定592 nm处丙二醇吸光度(A),以质量浓度(C)为横坐标,吸光度为纵坐标,作标准曲线,回归方程为A=0.008 9C-0.027,R2=0.996 8,在C为10~50 mg/L时,线性关系良好。
1.3.6.2样品测定 称取0.05~0.1 g HPCS于100 mL容量瓶中,加入25 mL 0.5 mol/L H2SO4,加热至样品溶解,冷却,室温下加蒸馏水稀释至刻度,取1 mL溶液于25 mL具塞比色管中,按1.3.6.1节操作,测得样品溶液在592 nm处的A,按回归方程计算得到丙二醇质量浓度[16]。根据式(3)和式(4)计算样品的取代度(DS):
(3)
(4)
式中:w—羟丙基质量分数, %;C—丙二醇的质量浓度, mg/L; 0.776 3—丙二醇转换为羟丙基的转换值;m—羟丙基壳聚糖质量, g;DS—产物的取代度; 161—壳聚糖单元的相对分子质量; 58—羟丙基的相对分子质量。
2 结果与讨论
2.1合成工艺对HPCS特性黏数的影响
2.1.1反应温度 在NaOH质量分数40%,碱化时间30 min,反应时间6 h,环氧丙烷用量10 g条件下,考察反应温度对特性黏数的影响,结果见图1(a)。
由图1(a)可知,羟丙基壳聚糖的特性黏数随温度的上升表现出先增大后减小的趋势,在60 ℃时达到最大值。原因是由于环氧丙烷沸点较低[17],当温度较低时,原料分子间有效碰撞几率低,羟丙基化程度低;当温度逐渐升高,壳聚糖与环氧丙烷充分接触,分子之间有效碰撞几率增加,羟丙基化程度增加;但当温度过高时,环氧丙烷的挥发量随之增大,参与反应的环氧丙烷减少,与壳聚糖反应不完全;同时温度升高,壳聚糖的降解速率加快,特性黏数大幅度降低。因此,温度在60 ℃时为最佳值。
2.1.2反应时间 在NaOH质量分数40%,碱化时间30 min,反应温度60 ℃,环氧丙烷用量10 g条件下,考察反应时间对特性黏数的影响,结果见图1(b)。
由图1(b)可知,随着反应时间的延长,羟丙基壳聚糖的特性黏数出现先增大后减小的趋势,在6 h时特性黏数出现最大值。反应时间过短,羟丙基化反应不充分,接枝效率低,HPCS特性黏数较低;反应时间过长,则会增加分子链的断裂程度,壳聚糖大量降解,导致特性黏数下降。所以反应时间选择6 h比较合适。
2.1.3碱液质量分数 碱液质量分数是影响HPCS特性黏数的一个重要因素。在碱化时间30 min,反应温度60 ℃,反应时间6 h,环氧丙烷用量10 g条件下,探讨了碱液质量分数对特性黏数的影响,结果见图1(c)。
由图1(c)可知,HPCS特性黏数随着碱液质量分数的升高呈现先增加后减小的趋势。当质量分数较低时,壳聚糖C6位羟基不易被活化,且壳聚糖分子间的氢键和部分晶区不易破坏,接枝反应难以进行,特性黏数较低;但当碱液质量分数过高时,壳聚糖会在浓碱中大量降解,HPCS特性黏数大幅度减小;由图1(c)可知,碱液质量分数30%最为合适。
2.1.4碱化时间 在NaOH质量分数30%,反应时间6 h,反应温度60 ℃,环氧丙烷用量10 g条件下,考察碱化时间对特性黏数的影响,结果见图1(d)。
由图1(d)可知,HPCS特性黏数随着碱化时间的增加出现先增大后减小的趋势,在20 min出现最大值。碱化时间过短,壳聚糖不能溶胀,活性位点不能被活化,反应程度低;碱化时间过长,特性黏数随之减小,这是因为壳聚糖在碱液中会发生不同程度的降解,碱化时间越长,降解反应越严重,特性黏数越低,所以碱化时间20 min最为合适。
2.1.5环氧丙烷用量 在NaOH质量分数30%,反应时间6 h,反应温度60 ℃,碱化时间20 min条件下,考察环氧丙烷用量对特性黏数的影响,结果见图1(e)。
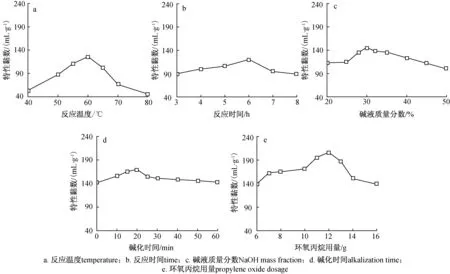
图1 不同反应条件对HPCS特性黏数的影响Fig. 1 Effect of different reaction conditions on intrinsic viscosity of HPCS
由图1(e)可知,特性黏数随着环氧丙烷用量的增加呈现出先增大后减小的趋势。随着环氧丙烷用量增加,壳聚糖与环氧丙烷接触更加充分,反应逐渐完全,反应程度逐渐增大;当环氧丙烷用量为12 g时,特性黏数达到最大值;继续增加环氧丙烷的用量,特性黏数开始下降,说明反应过程有副产物生成,影响反应的正向进行。所以环氧丙烷用量选择12 g较合适。
2.2响应面优化合成工艺
2.2.1回归模型的建立及数据分析 在单因素试验结果的基础上,选择碱液质量分数(X1)、碱化时间(X2) 和环氧丙烷用量(X3) 为自变量, 选用响应面分析法中的 Box-Behnken Design 建立数学模型[18],以特性黏数(Y)为指标进行实验设计,优化实验的工艺参数,试验设计及结果见表1。
采用Design expert 软件与SAS 8e统计软件包对表1的实验结果进行回归分析,建立特性黏数的二次回归方程如下:
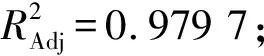
二次回归拟合后的回归方程方差分析见表2。
由表2中F值的大小可知,在回归方程的一次项中,各因素对特性黏数的影响程度为X3>X1>X2。通过方差分析可得回归模型的F=86.81,P<0.000 1,说明该模型具有良好的显著水平,失拟项的F=5.49,P=0.066 7>0.05,失拟不显著。特性黏数模型的R2为0.991 1,校正后为0.979 7,变异系数较低为0.77,再一次验证回归方程拟合程度好,证明试验的精确度较高,可靠性强。以上结果均表明回归模型与实测值能较好的拟合,该模型可以用来对实验结果进行预测和分析。
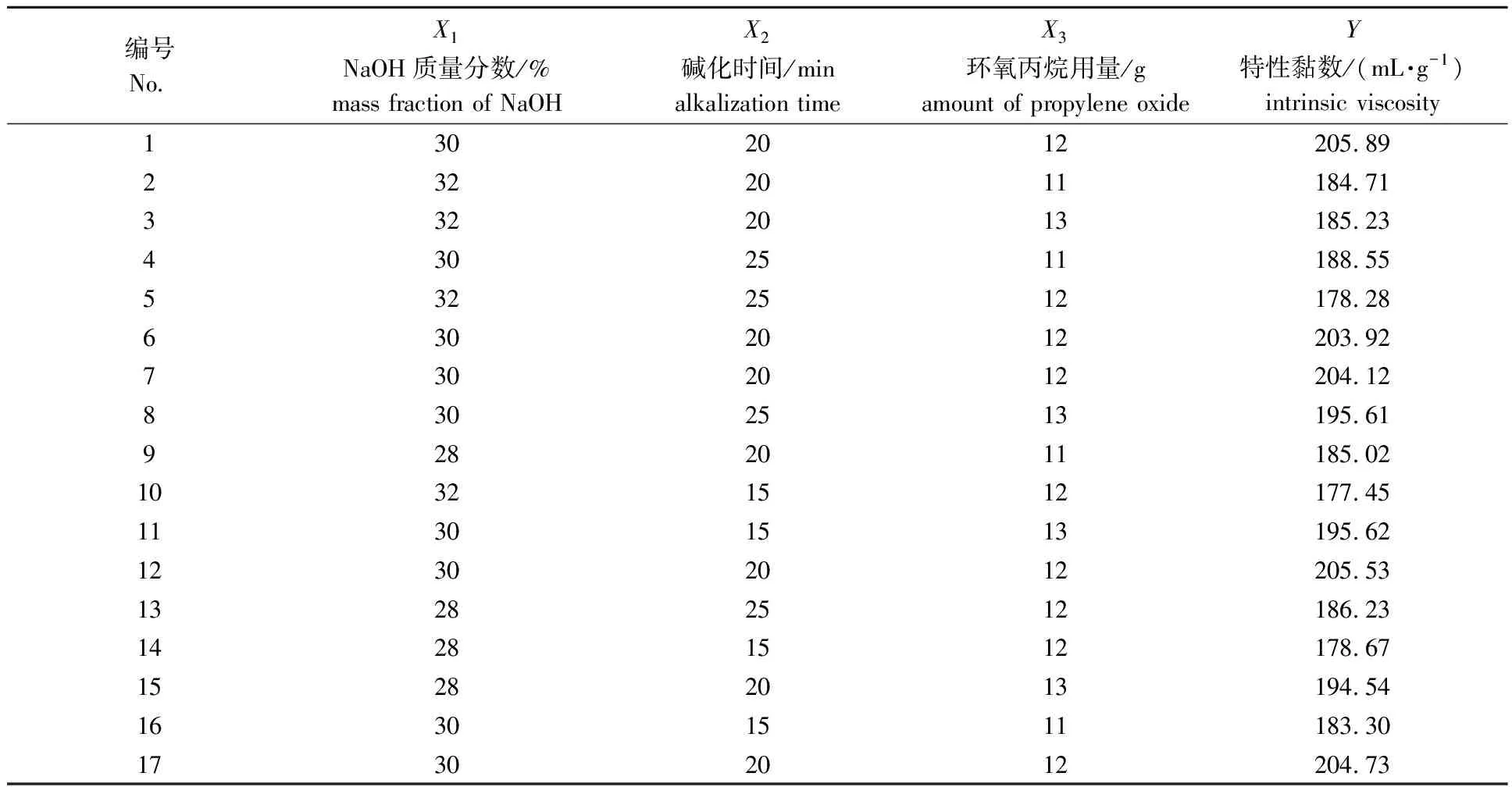
表1 Box-Behnken实验设计及结果
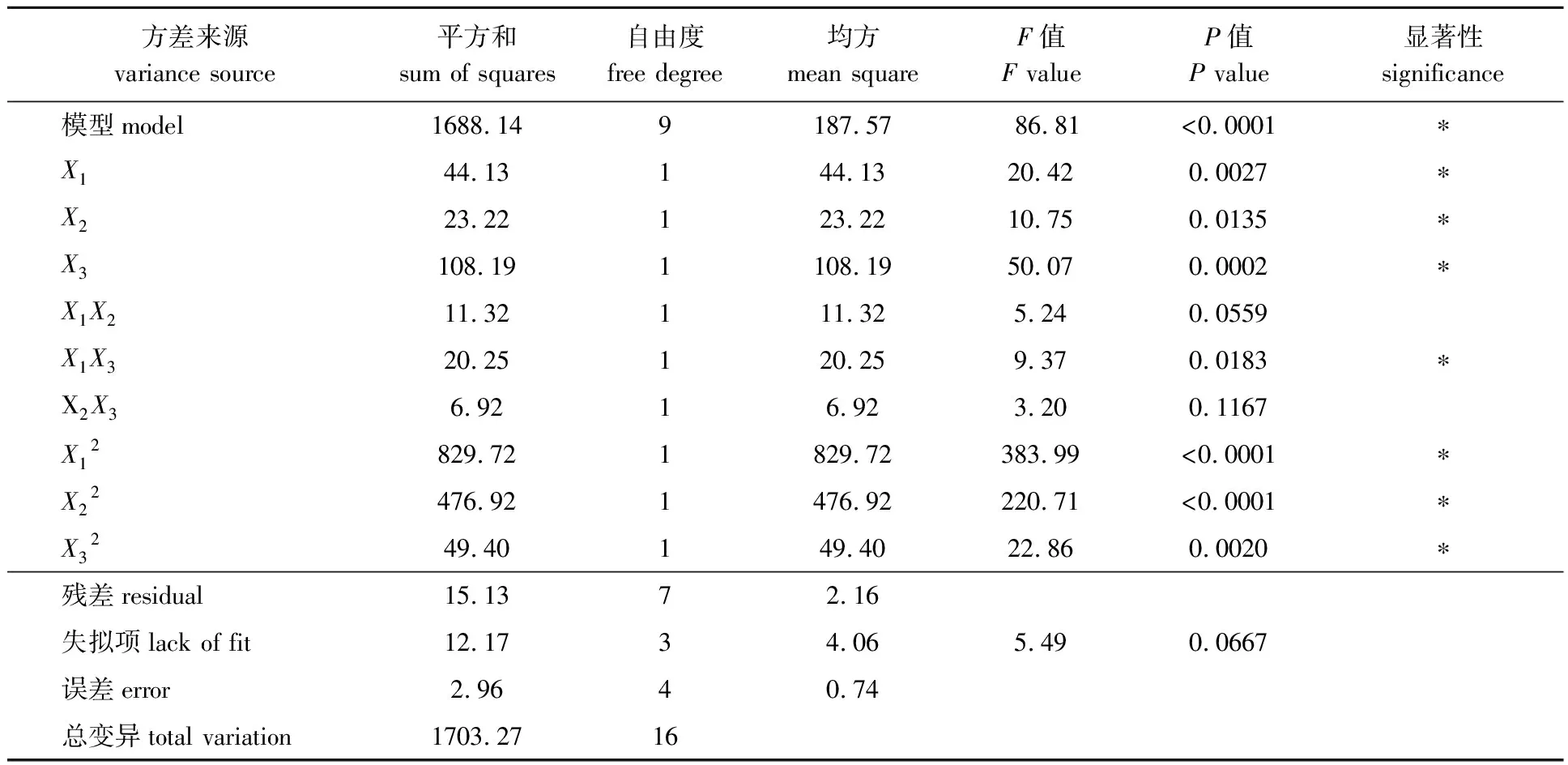
表2 特性黏数回归方程方差分析
2.2.2交互影响显著性分析 图2为各因素关于特性黏数的响应面和等高线图。
如图所示,壳聚糖分子在2θ为10°、 15°和20°存在衍射峰。这是由于壳聚糖分子规整排列以及氢键作用导致壳聚糖分子存在部分晶区,这也是壳聚糖不溶于水的原因。当在壳聚糖分子中引入羟丙基后,在2θ为10°的衍射峰接近消失,而在2θ为20°的衍射峰强度也明显减弱,这是因为在壳聚糖分子中的C6羟基位引入羟丙基后,削弱了分子内的氢键作用,其水溶性也因此提高。
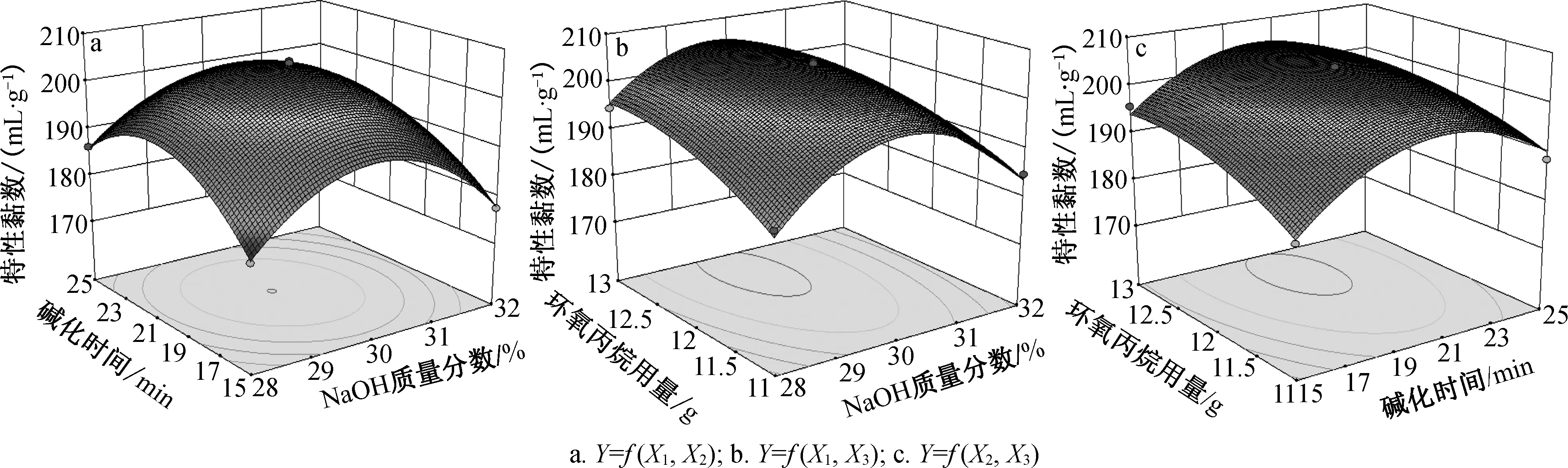
图2 HPCS特性黏数的响应曲面和等高线图Fig. 2 Response surface and contour line of intrinsic viscosity of HPCS
从响应曲面图可以看出,响应面开口朝下,特性黏数随各因素值先增大后减小,说明此模型存在最大值的稳定点。对稳定点进行分析,得出HPCS最优合成工艺为NaOH质量分数29.8%,碱化时间20.3 min,环氧丙烷用量12.57 g,在此条件下,特性黏数为206.089 mL/g。
2.2.3回归模型的验证 对HPCS合成工艺各影响因素的优化值进行验证。取NaOH质量分数为 30%,碱化时间为20 min,环氧丙烷用量为12.6 g,于60 ℃下反应6 h,HPCS特性黏数为206.32 mL/g,相对分子质量2.738×105。实测值与预测值接近,相对误差值为0.11%。说明该方程拟合度好,可以预测实际特性黏数。
2.3产物的分析与表征
2.3.1FT-IR分析 CTS与最佳工艺条件下合成的HPCS的红外谱图见图3。在HPCS的FT-IR中,2970 cm-1处出现—CH3的伸缩振动吸收峰,1380 cm-1处出现了—CH3弯曲振动吸收峰,且CTS 经过羟丙基反应后,在原壳聚糖分子链1030 cm-1处C6-OH 的吸收峰减弱,表明羟丙基被成功引入到CTS分子上,且羟丙基化反应主要发生在C6-OH上[19]。
2.3.21H NMR分析 将最佳工艺条件下得到的HPCS以D2O作溶剂,进行1H NMR分析,结果见图4。由图4可知,δ4.7处为H-1质子和溶剂的吸收峰,δ3.55~3.92为H-3、 H- 4、 H-5、 H- 6特征吸收峰,δ1.07处为H-9吸收峰即—CH3吸收峰;δ3.09为H-2和H-8吸收峰即—CH吸收峰;δ3.45为—CH2吸收峰。由此可证明,—CH2CH(OH)CH3被成功接枝到壳聚糖上[20-21]。
2.3.3XRD分析 CTS与最佳工艺条件下合成的HPCS的XRD谱图见图5。
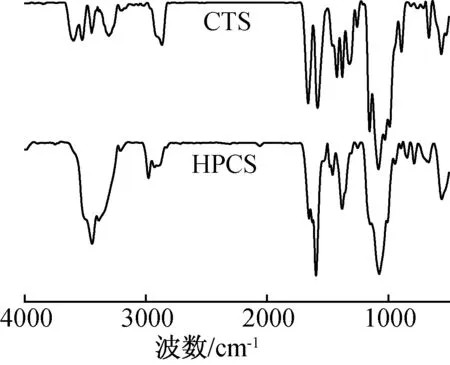
图3 CTS与HPCS的红外谱图Fig. 3 FT-IR spectra of CTS and HPCS
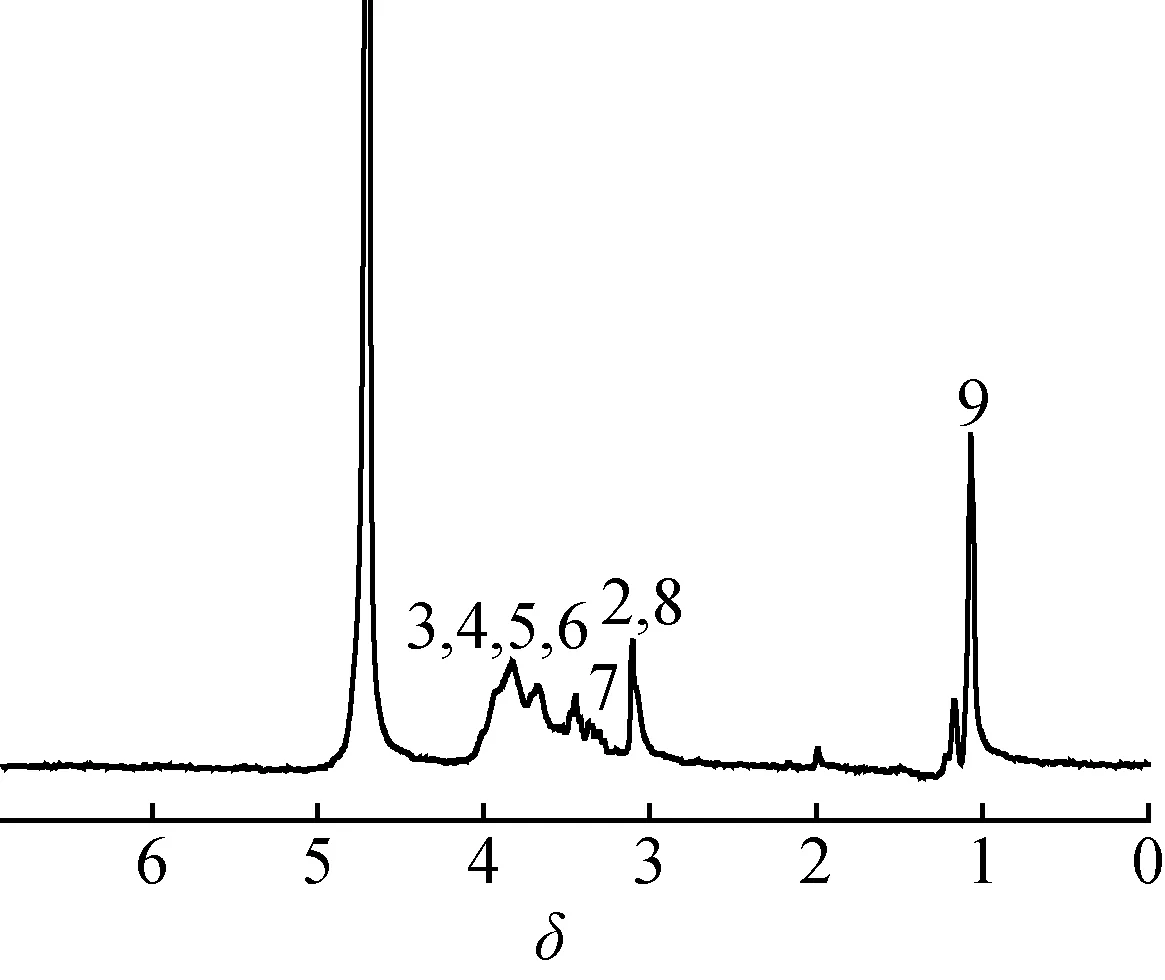
图4 HPCS的核磁共振氢谱Fig. 4 1H NMR spectrum of HPCS
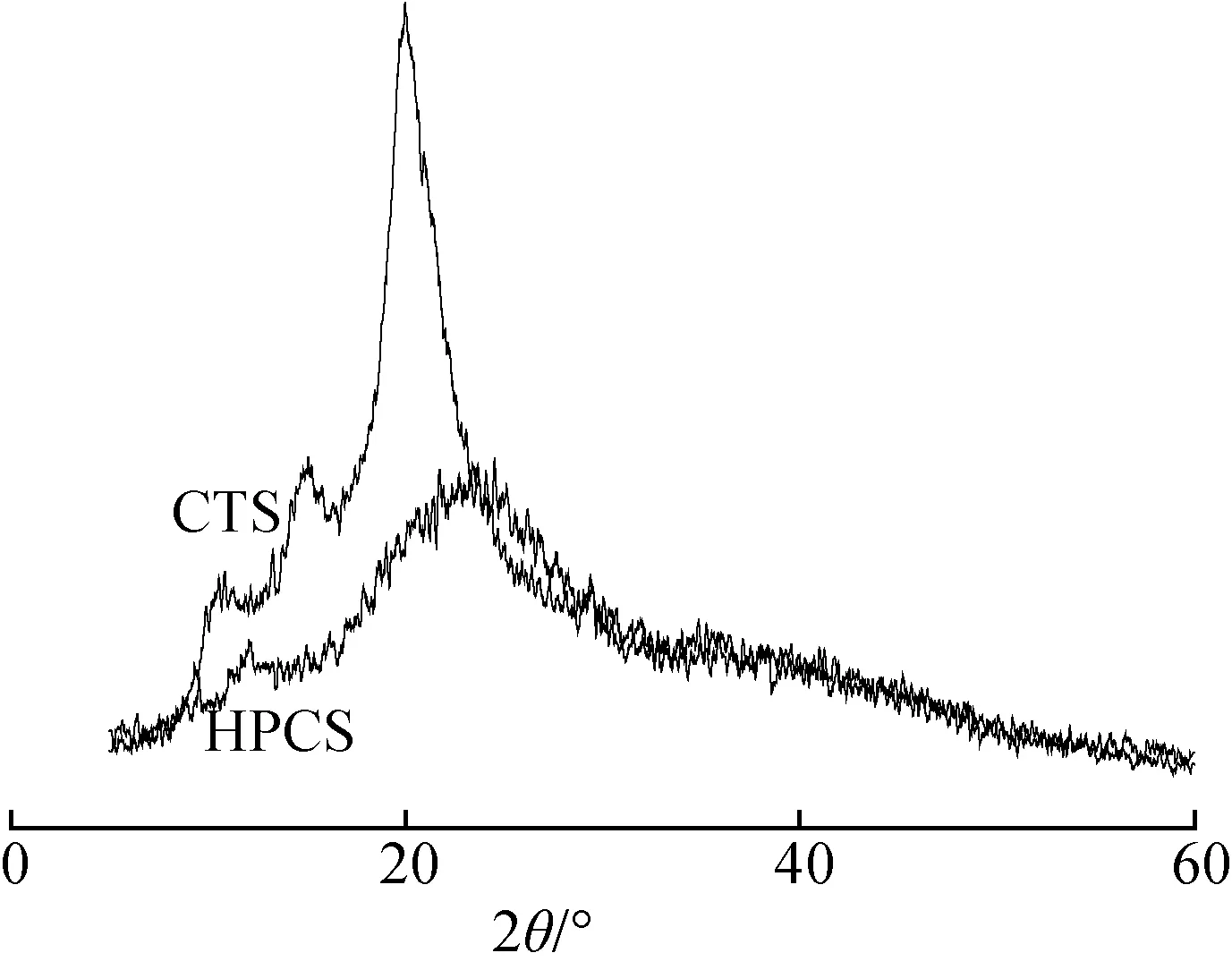
图5 CTS与HPCS的X射线衍射图Fig. 5 XRD patterns of CTS and HPCS
2.3.4ESEM分析 CTS与最佳工艺条件下合成的HPCS的ESEM谱图见图6。
由图6可以看出,CTS 与 HPCS相比,具有显著的形貌差异。CTS呈现出耳状的形貌,且表面相对平滑,而HPCS呈现不规则的块状外观形貌,且表面相对粗糙。原因在于引入羟丙基后,打破了壳聚糖分子的内部晶区,微观形貌也发生明显改变。

图6 CTS(a)与HPCS(b)的环境扫描电镜图片Fig. 6 ESEM images of CTS(a) and HPCS(b)
2.4取代度(DS)的测定
取最佳条件下合成的HPCS按1.3.6节操作方法处理,采用标准曲线方程、式(3)和式(4)计算取代度值DS,平行测定3次,取平均值,得到羟丙基壳聚糖取代度为0.426。
综上可知,在最佳工艺条件下测得HPCS取代度为0.426,特性黏数为206.34 mL/g,符合预期结果。
3 结 论
3.1采用环氧丙烷与壳聚糖(CTS)发生亲核取代反应合成羟丙基壳聚糖(HPCS),并用FT-IR、1H NMR、XRD和 ESEM 对其结构及形貌进行表征,结果表明:羟丙基被成功接枝到壳聚糖上,HPCS成功合成。
3.2通过单因素与响应面分析优化了HPCS的合成条件,探讨了反应温度、反应时间、碱液质量分数、碱化时间和环氧丙烷用量对HPCS特性黏数的影响。结果表明: HPCS合成的最佳工艺条件为NaOH质量分数30%、碱化时间20 min、环氧丙烷用量12.6 g,反应温度60 ℃,反应时间6 h。在该工艺条件下,HPCS特性黏数为206.32 mL/g,取代度为0.426,相对分子质量较高为2.738×105,与预期结果一致。
