磷钨酸掺杂高比表面积g-C3N4催化剂的制备及其光催化性能
2019-02-19蔡天凤李会鹏
张 杰,蔡天凤,李会鹏,赵 华
(辽宁石油化工大学化学化工与环境学部,抚顺 113001)
1 引 言
对于环境的治理和保护是目前乃至未来很长一段时间工作的重心。在众多的治理水体污染的手段中,应用光催化剂催化降解水中的有机污染物是一种绿色可持续的有效措施[1-2]。大多数光催化剂存在着两大瓶颈[3]:(1)禁带较宽,对太阳能的利用率较低,只能利用太阳能中不到5%的紫外光;(2)光生-电子空穴对易复合,量子效率较低。因此,开发一种具有高效光催化活性的半导体催化剂来降解水中的污染物至关重要。
类石墨相氮化碳(g-C3N4)是一种不含有金属的绿色半导体催化剂,其禁带宽度为2.7 eV,表明在可见光的照射下电子即可从价带迁移至导带[4]。此外,g-C3N4具有三嗪环结构单元以及极高的缩聚度,C原子和N原子之间以共价键相连,使得g-C3N4具有极强的热稳定性以及化学稳定性[5],并且原料廉价易得,制作工艺简便,这一切的优点使得g-C3N4成为了半导体中研究的重点。目前g-C3N4已经广泛的应用于水解制氢[6-7]、光催化污染物的降解[8-9]、有机合成[10]、光催化固氮[11]等领域。但是g-C3N4也具有其明显的缺点,例如比表面积低,光生电子-空穴易复合,光能利用率较低[12-15]等。
杂多酸是一种强氧化性的多电子氧化催化剂,具有可调变的酸性[16],在近紫外光的照射下具有较高的响应活性,发生电子-空穴对的分离,通过自氧化和羟基自由基的产生实现对有机物的降解作用[17]。但是杂多酸比表面积较小,易溶于水、丙酮等极性较强的小分子溶剂中且不宜分离。所以通过将杂多酸固载在载体上,可有效提高其比表面积,使其具有更高的催化活性以及选择性。Zhang等[18]将磷钨酸固载在ZrO2修饰的SiO2上,制得了H3PW12O40/ZrO2-SiO2催化剂进行氧化脱硫,在最佳条件下,二苯并噻吩的脱除率达到100%。
本文以SBA-15为硬模板剂制备高比表面积的g-C3N4,提高比表面积的同时降低电子-空穴的复合几率,增加对可见光的吸收。利用g-C3N4表面具有大量氨基的特点[19],将磷钨酸(HPW)引入到介孔g-C3N4中制备成HPW/g-C3N4催化剂。采用红外傅里叶变换(FTIR)光谱、X射线衍射(XRD)光谱、X射线衍射(XRD)光谱、氮气吸附脱附(BET)、荧光(PL)光谱、紫外可见(UV-Vis)漫反射光谱、扫描电镜(SEM)、透射电镜(TEM)进行表征,并且以罗丹明B为探针对催化剂的反应活性及稳定性进行了考察,并对反应机理以及光生电子的转移方式进行了探究。
2 实 验
2.1 催化剂的制备
(1)块状g-C3N4的制备:10 g三聚氰胺放在30 mL坩埚中,在550 ℃下煅烧2 h,升温速率为5 ℃/min。
(2)HPW掺杂g-C3N4的制备(命为CN-1):将HPW与g-C3N4按照1∶10的比例60 ℃水浴搅拌混合3 h,之后搅拌至干。得到的固体粉末在550 ℃下煅烧4 h,升温速率为5 ℃/min。
(3)HPW掺杂介孔有序g-C3N4的制备:
①SBA-15的制备:SBA-15的制备基于参考文献[20]。
②高比表面积g-C3N4的制备(命为CN-2):将三聚氰胺与SBA-15按照3∶1的比例在水溶液中90 ℃下混合搅拌6 h,离心、干燥。将得到的固体粉末在550 ℃下煅烧4 h,升温速率为5 ℃/min。
③HPW掺杂的高比表面g-C3N4的制备(命为CN-3):将HPW与CN-2按照质量比为1∶10的比例60 ℃水浴搅拌混合3 h,之后搅拌至干。得到的固体粉末在550 ℃下煅烧4 h,升温速率为5 ℃/min。
2.2 结构表征
X射线衍射光谱(XRD)采用德国布鲁克公司的D8 Advance进行测定,以Cu靶作为辐射电源;傅里叶变换红外(FT-IR)使用赛默非尼高力的红外光谱仪Nicolet iS10进行测定,采用ATR附件,扫描范围为600~4000 cm-1;X光电子能谱(XPS)采用赛默飞世科技有限公司的Thermo ESCALAB 250光电子能谱仪器进行测定;紫外可见(UV-ViS)漫反射光谱美国安捷伦公司的Agilent Cary 5000进行测定;荧光(PL)光谱采用的是安捷伦科技有限公司(美国)Cary Eclipse的荧光分光光度计进行测定;扫描电镜(SEM)采用日本日立公司的发射扫描电镜SU8010进行测定,观察粉体的表面形貌。
2.3 活性评价
活性评价:以500 W的氙灯为光源,以RhB为考察对象,对催化剂进行活性评价。称取0.02 g的催化剂加入到20 mL浓度为10 mg/L的RhB溶液中,在暗光下搅拌30 min达到催化剂对反应底物的吸附平衡。每30 min取样一次,在3000 r/min下进行离心30 min,用紫外可见分光光度计在550 nm的波长下测量其吸光度。
降解率的计算:η=(A0-A)/A0
(1)
其中η为降解率,A0为原样的吸光度,A为降解后的吸光度。
稳定性评价:称取0.02 g的催化剂加入到20 mL浓度为10 mg/L的RhB溶液中,在暗光下搅拌30 min达到催化剂对反应底物的吸附平衡。在氙灯下照射2 h后,将催化剂回收、洗涤进行稳定性试验。
2.4 催化剂带隙能的计算
利用公式(2)计算带隙能:
αhv=A(hv-Eg)n/2
(2)
其中α是可见光吸收常数,h是普朗克常数,v是光子频率,Eg是带隙能,A是比例常数。
2.5 动力学分析
从动力学角度对催化剂进行活性评价,光催化降解符合一级反应动力学。应用Langmuir-Hinshelwood模型,对水相下光催化降解进行动力学分析[21-22]
(3)
其中r0是最初的反应速率(mg/L·min),C是罗丹明B的浓度(mg/L),t是反应时间(min),k是Langmuir-Hinshelwood反应速率常数(mg/L·min),K是Langmuir吸附平衡常数(L/mg)。罗丹明B被稀释后把公式简化为:
(4)
(5)
kapp为表观速率常数(min-1),C0是罗丹明B的初始浓度。
3 结果与讨论
3.1 FT-IR测定
图1为g-C3N4,HPW和CN-X催化剂的FT-IR谱图。所有样品的特征衍射峰主要集中在500~4000 cm-1。其中,g-C3N4在808 cm-1附近的吸收峰对应的是三嗪环的伸缩振动,在3000~3500 cm-1附近的吸收特征峰对应的是-NH2和-NH基的伸缩振动,表明在加热过程中,三聚氰胺未完全缩聚[23]。相较于块状g-C3N4,CN-2和CN-3在808 cm-1处的特征峰强度明显增强,表明含有更多的三嗪结构[24],缩聚程度降低,提高了比表面积。HPW掺杂后,在CN-1和CN-3催化剂中,分别出现P-O键(980 cm-1)和W-Od(1080 cm-1)的伸缩振动[25],相对HPW出现位移;在3000~3500 cm-1处的特征峰强度减弱,-NH2减少。表明磷钨酸与-NH2反应,并以化学键的形式很好的与g-C3N4连接在一起。
3.2 XRD分析
采用XRD对催化剂的结构进行表征,其结果如图2所示。g-C3N4在27.5°附近具有很强的特征峰,对应的是芳香物的层间堆积特征峰,晶面指数为(002),对应的层间距d=0.33 nm,说明g-C3N4具有和石墨类似的层状结构[26]。13.1°附近的衍射峰对应的是melon类物质的特征峰,晶面指数为(100)。27.5°衍射峰出现了明显的宽化,表明层间距变大,比表面积增加。HPW掺杂后,CN-1、CN-3在13.1°附近的衍射峰强度明显减弱,这主要是由于HPW 与melon类物质中的氨基反应而使melon类物质含量降低。且在2θ<10°的范围内出现了Keggin结构的特征峰[27],表明HPW从晶态变为非定形态,并以化学键的方式很好的附着在载体上[28]。
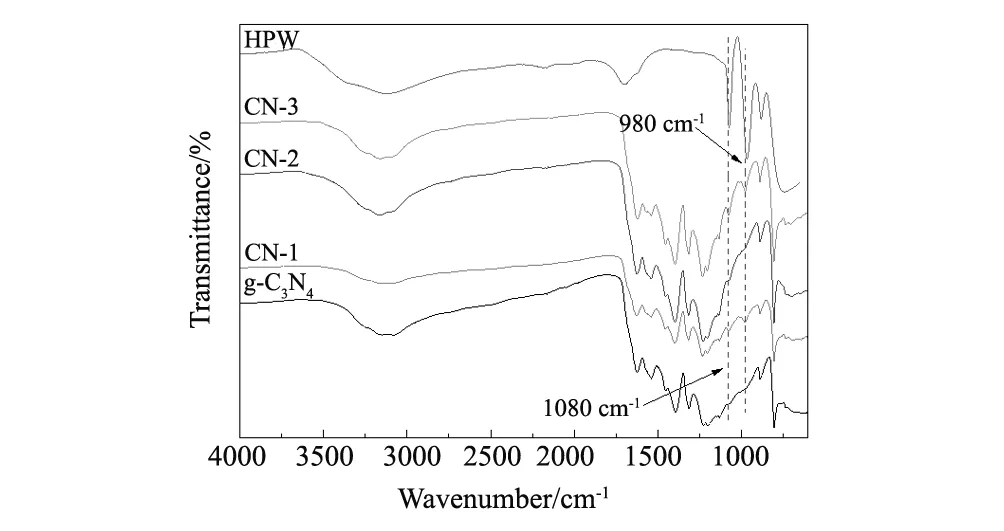
图1 g-C3N4,HPW和CN-X催化剂的FT-IR图谱 Fig.1 FT-IR spectra of g-C3N4, HPW and CN-X catalysts
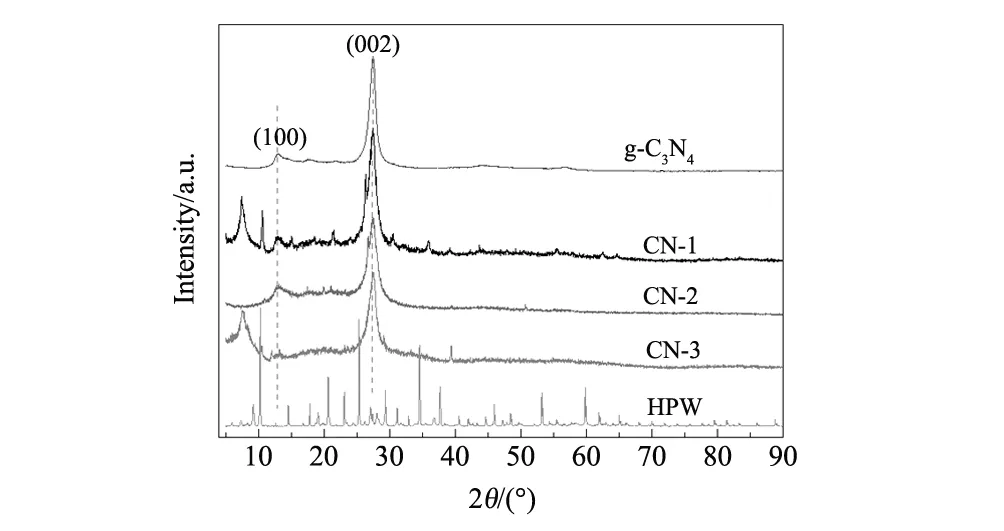
图2 g-C3N4,HPW和CN-X催化剂的XRD谱图 Fig.2 XRD patterns of g-C3N4, HPW and CN-X catalysts
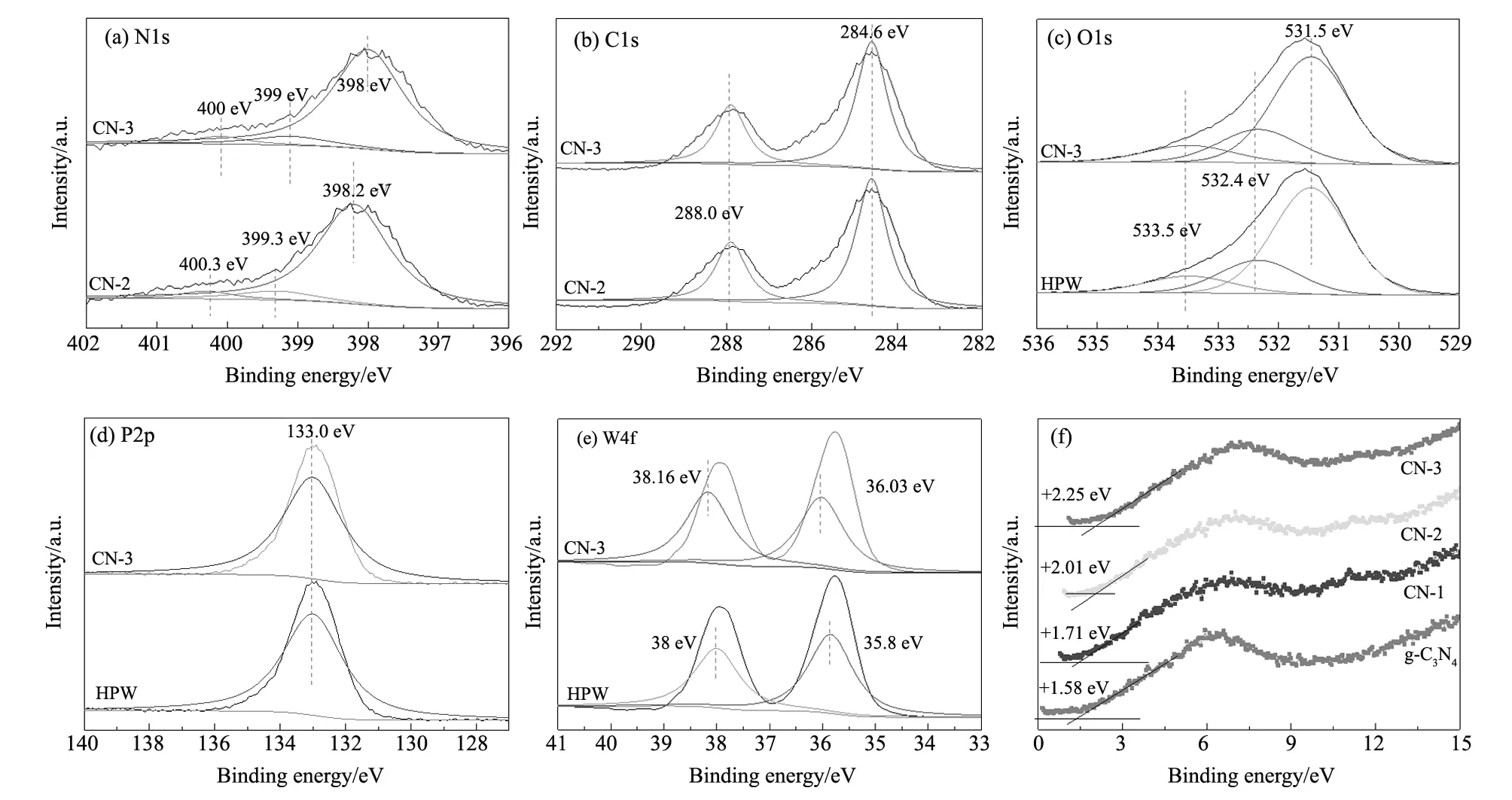
图3 制备催化剂的N 1s(a)、C 1s(b)、O 1s(c)、P 2p(d)、W 4f(e)能级的XPS谱图及价带XPS图谱(f) Fig.3 XPS patterns of as prepared catalysts in the region of N 1s(a),C 1s(b),O 1s(c),P 2p(d),W 4f(e) and VB XPS (f)
3.3 XPS分析
通过XPS对元素在催化剂表面的状态进行表征,结果如图所示。图3(a)中CN-2的N 1s能级可以分为398.2 eV、399.3 eV、400.3 eV,分别对应于CN-2中Sp2杂化的N原子(C-N=C)、连接环状构的N原子或氨基中的N原子、芳香环中连接三个C的N原子[26]。图3(b)中 C 1s能级可以分为两个峰,其中284.6 eV对应于催化剂的表面吸附C,288 eV对应的是分子结构中的N=C-N2。 与CN-2相比,CN-3催化剂样品中的N 1s能级向低结合能移动,而C 1s轨道峰的位置未发生变化。这主要是因为CN-3中的melon类物质与HPW发生强的相互作用,提高了N元素的电子密度,因此结合能降低. 图3(c)、(d)分别为O 1s和P 2p的谱图。相对于HPW,CN-3中的O、P结合能没有发生变化。HPW在结合能为35.8 eV、38 eV处有两个强峰,分别对应于W4f7/2和W4f5/2. 相对HPW,CN-3催化剂中W4f向高结合能方向移动。这主要是由于HPW掺杂后从低结合能的WX+(WOX/W)转变至高结合能处的W6+[29],这种转变也很好的解决了杂多酸易溶于水的缺点。图3(f)为g-C3N4、CN-1、CN-2、CN-3、CN-4的价带XPS谱图,其价带分别为+1.58 eV、+1.71 eV、+2.01 eV、+2.25 eV。结合UV-Vis可知其导带分别为-1.15 eV、-0.98 eV、-0.66 eV、-0.39 eV,由此可见HPW掺杂后显著影响了g-C3N4的能带结构,调节了其能带位置。
3.4 BET分析
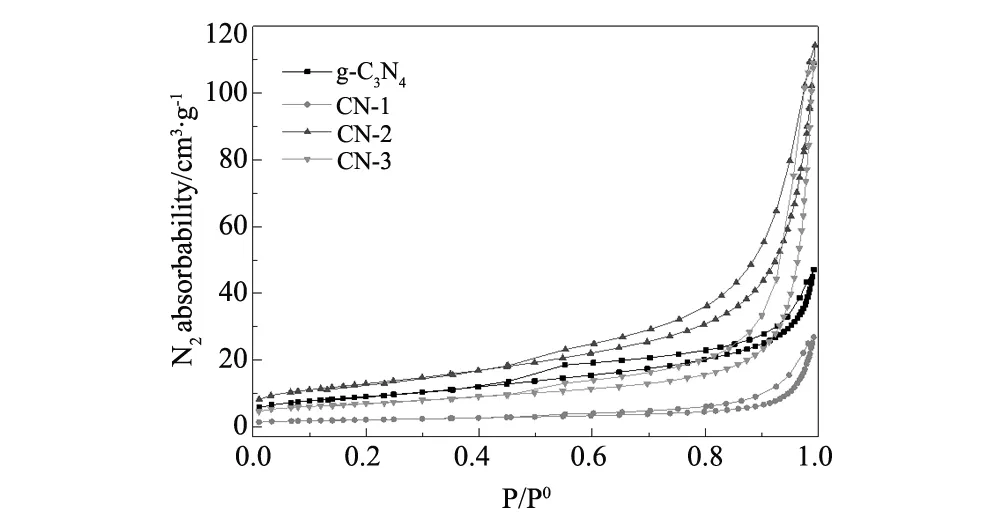
图4 g-C3N4和CN-X的N2吸附-脱附等温线 Fig.4 Nitrogen sorption isotherms of g-C3N4and CN-X catalysts
图4为g-C3N4和CN-X的N2吸附-脱附等温线,可以看出所有等温线均表现出IV型等温线,在高相对压力出现由于毛细冷凝现象引起的H1回滞环,表明g-C3N4是一种层状的堆积结构[30],所有的催化剂均有介孔结构。g-C3N4,CN-1,CN-2,CN-3样品的比表面积(SBET)分别为24.87 m2/g、7.567 m2/g、46.185 m2/g、32.559 m2/g。可以看出SBA-15为模板剂后SBET显著增加,表明SBA-15的引入限制了g-C3N4晶粒的增长,改变了结晶度,提高了催化剂的比表面积。但是HPW的掺杂使得比表面积降低,表明HPW不仅存在于g-C3N4的表面,还附着于g-C3N4的孔道中,但是并未改变g-C3N4的介孔结构。

图5 g-C3N4 (a); CN-1 (b); CN-2 (c); CN-3 (d);HPW的SEM(e); CN-3的TEM(f)及元素分布图 Fig.5 SEM images of g-C3N4 (a)CN-1 (b),CN-2 (c), CN-3 (d), HPW(e);TEM images of CN-3 and mapping
3.5 SEM,TEM分析
应用SEM谱图对催化剂的晶体形貌进行考察,图5a~d分别对应的是g-C3N4、CN-1、CN-2、CN-3半导体催化剂的SEM图,其中g-C3N4表现为块状堆积结构,与文献报导的相一致[31]。CN-2,CN-3比表面积增加后,表现出了明显的疏松状态,表明以SBA-15为模板剂限制了g-C3N4晶粒的生长,改变了三聚氰胺的缩聚模式,改变了结晶度,形成了介孔结构而扩大比表面积。图5e为HPW的SEM图,其表现为明显的团聚现象,但由CN-3的TEM(图5f)及元素分布可知,HPW已经均匀的分散在g-C3N4上。
3.6 UV-Vis分析
图6(a)为g-C3N4和CN-X催化剂的UV-Vis漫反射谱图。g-C3N4被光激发后产生的光电子从N 2p轨道形成的价带(VB)能级转移到C 2p轨道形成的导带(CB)能级,从而展现出典型的半导体吸收[3]。g-C3N4的吸收波长阈值为464 nm,与文献报道基本一致[32]。相较于g-C3N4,CN-X的光吸收强度明显增强,这主要是因为比表面积的增加以及磷钨酸的掺杂均可提高光吸收强度。此外,由于量子尺寸效应[33],使得CN-X催化剂表现出了明显的吸收边界蓝移现象。
利用公式(2)计算催化剂的带隙能,其结果如图6(b)所示,g-C3N4,CN-1,CN-2,CN-3的带隙能分别为2.73 eV、2.69 eV、2.67 eV、2.64 eV。其中HPW掺杂的介孔有序的g-C3N4的带隙能最小,表明比表面积的增加和HPW的掺杂均可改变催化剂的能带结构,降低带隙能,提高可见光的利用率。
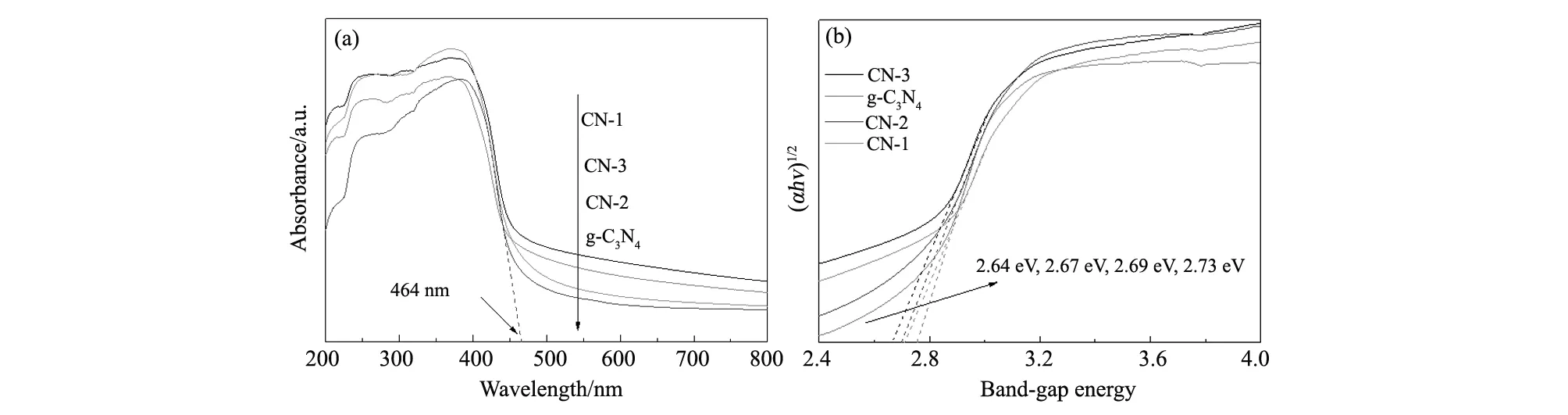
图6 (a)g-C3N4和CN-X催化剂的UV-Vis漫反射谱图及(b)能带图 Fig.6 UV-Vis diffuse reflection spectra (a) and band energy level (b) of g-C3N4 and CN-X
3.7 PL分析

图7 g-C3N4和CN-X的PL发射图谱 Fig.7 PL emission spectra of g-C3N4 and CN-X
光生电子-空穴的有效分离,对于提高光催化活性至关重要。图7为制备催化剂的PL图谱,激发光源波长为360 nm。g-C3N4在460 nm处具有很强的荧光发射峰,与UV-Vis谱图中g-C3N4的吸收阈值一致。CN-X催化剂的PL谱图表现出了明显的蓝移现象,这主要是由于VB与CB之间距离缩短,降低了带隙能,引起了量子限制效应[34]。HPW的掺杂以及比表面积的增加,均可引起电子-空穴的有效分离,使得PL谱图表现出明显的淬灭现象。其中比表面积因素对于降低PL信号的影响大于磷钨酸掺杂因素。
3.8 催化剂催化活性评价
在500 W的氙灯照射下通过降解RhB溶液对催化剂的催化性能进行评价,结果图8(a)所示。在空白实验中,RhB没有表现出明显的降解,这既表明RhB是一种结构稳定的分子,也表明催化剂在降解过程中的不可或缺。RhB在光照开始之前浓度降低,主要是因为在催化剂表面发生了吸附作用。RhB在g-C3N4,CN-1,CN-2,CN-3表面的吸附率分别为1.75%,50.92%,52.18%,66.11%。光照2 h后,对RhB的吸附-降解率分别为CN-3(96.12%)>CN-2(84.32%)>CN-1(74.17%)>g-C3N4(69.66%)。从结果可知,HPW掺杂的介孔有序的g-C3N4对RhB的吸附-降解率最高,这主要是因为由于比表面积的增加或者HPW的掺杂都能使更多的活性位暴露在催化剂的表面,并且HPW与g-C3N4之间的协同催化作用使得降解率进一步提高。
应用一级反应动力学对催化剂的反应活性进行进一步评价,结果如图8(b)所示。g-C3N4,CN-1,CN-2,CN-3催化剂的反应速率常数分别为0.00207 min-1,0.00722 min-1,0.01334 min-1,0.0269 min-1。CN-3表现出最高的反应活性,是块状g-C3N4的13倍。
3.9 催化剂稳定性评价
对CN-3催化剂进行4次循环使用来降解RhB溶液,考察CN-3催化剂的稳定性,催化剂使用后,通过离心分离的方式进行回收,再用去离子水清洗,结果如图9所示。CN-3催化剂具有极强的稳定性,在重复循环使用4次后,降解率基本相似。随着循环次数的增加,降解率略微下降,这可归因于在回收过程中有催化剂的流失。
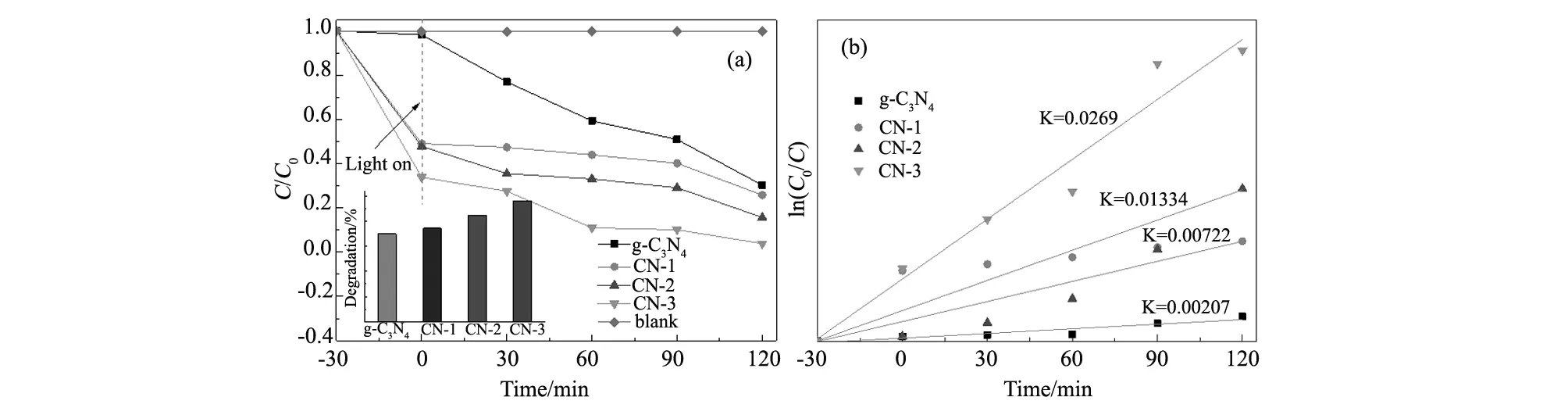
图8 (a)g-C3N4和CN-X在氙灯照射下的催化性能评价;(b)降解RhB的一级反应动力学曲线 Fig.8 (a)Photocatalytic performance of g-C3N4 and CN-X catalysts under xenon lamp irradiation; (b)first-order kinetics curves of RhB degradation
3.10 光催化反应机理的推测
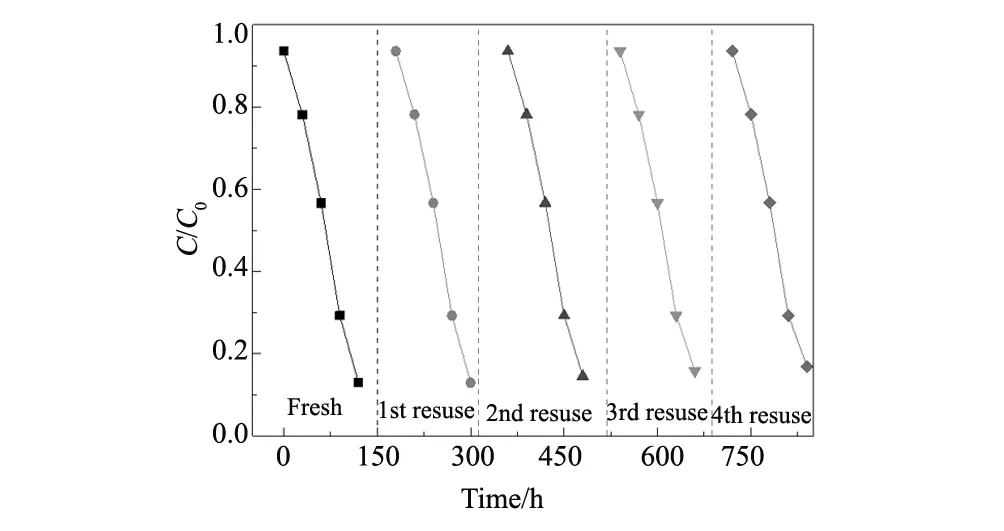
图9 CN-3催化剂降解RhB的循环实验 Fig.9 Cyclic experiment of RhB degradation of CN-3 catalyst
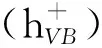




光生电子在复合催化剂上的迁移过程如图10(b)所示。由于HPW具有与金属氧化物半导体(TiO2)相似的能带结构,使其在自身的光催化作用之外,作为有效的电子捕获剂,它还能接受g-C3N4光激发所产生的电子,延长光生-电子空穴再结合的时间。g-C3N4的导带与价带分别为-1.13 eV,+1.58 eV而HPW的导带与价带分别为-0.37 eV,+2.63 eV[17]。由于g-C3N4的导带比HPW的导带更负,HPW的价带比PCN的价带更正,所以光生电子从g-C3N4的导带迁移到HPW的导带而空穴则停留在g-C3N4的价带,从而实现电子空穴的有效分离[40],降低复合几率。
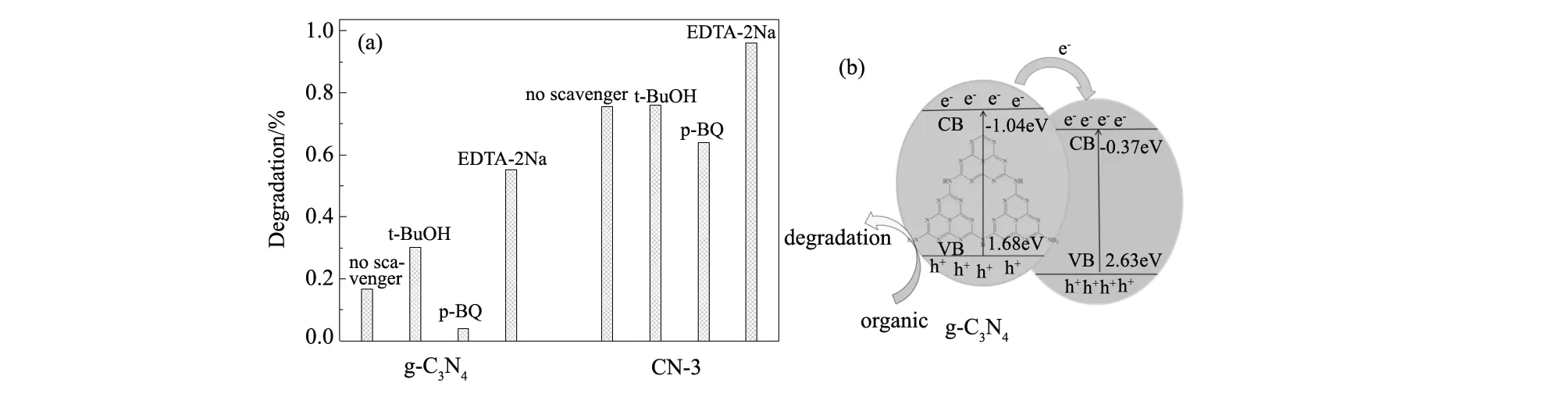
图10 不同捕获剂对g-C3N4和CN-3催化性能的影响(a)及光生电子在复合催化剂上的迁移过程(b) Fig.10 Influence of different scavengers on catalytic activity of g-C3N4 and CN-3(a) and migration of photogenerated electrons on composite catalysts(b)
4 结 论
以三聚氰胺、磷钨酸(HPW)为原料SBA-15为模板剂,成功制备了HPW掺杂的高比表面积g-C3N4。结果表明,HPW掺杂后以化学键的形式与g-C3N4相连,显著影响了g-C3N4的能带结构,且并未改变g-C3N4的孔道结构。比表面积的增加和HPW的掺杂均能显著降低光生-电子空穴的复合几率,降低带隙能,增加对可见光的吸收。HPW的掺杂和比表面积的增加均能显著提高光催化活性,其中HPW掺杂的高比表面积g-C3N4(CN-3)表现出最佳的活性,反应速率常数为0.0269 min-1,是块状g-C3N4的13倍,且循环使用4次后的光降解活性几乎不变。反应体系的主要活性物种为超氧自由基·O2-,HPW掺杂后主要的反应活性物种没有改变。
