正交试验优选白藜芦醇纳米囊泡处方
2018-10-15华芳
华芳
(安徽新华学院药学院,安徽农业大学,安徽 合肥 230000)
王国平,施伶俐
(安徽新华学院药学院,安徽 合肥 230000)
白藜芦醇(Resveratrol)作为一种蒽醌萜类化合物,广泛存在于天然植物中,如葡萄、虎杖等,具有抗炎、抗氧化、抗自由基等作用[1~5],而白藜芦醇在实际应用中存在的缺陷有:①水溶性低,口服吸收差,生物利用度低。②在光、热和氧化剂的作用下容易被氧化降解;在一定程度上限制了白藜芦醇在医药和食品等行业中的应用[6,7]。针对白藜芦醇的口服吸收差和易被氧化降解的缺陷,寻找温和、不良反应小的药物剂型来改善白藜芦醇的水溶性和降低氧化降解,提高其生物利用度具有非常重要的意义[8]。目前,提高难溶性药物的药剂学手段有纳米囊泡、纳米混悬剂、微乳技术、分子包合技术、脂质体技术、固体分散体等,其中纳米囊泡可作为水溶性差的药物载体,是一种具有组织相容性、细胞透过性的新型给药系统,可将亲水性或亲脂性药物包裹于其中,稳定性较高,不易被氧化或水解。因此,本实验以聚乙二醇化聚十六烷基氰基丙烯酸酯(PEG-PHDCA)作为载体材料,制备复合纳米囊泡,以期通过载体材料的性质提高白藜芦醇的稳定性,扩大其应用。
1 仪器与试药
1.1 仪器
红外光谱仪:Thermo公司
旋转蒸发仪:上海贝凯生物化工设备有限公司
Waters Acquity UPLC H-Class 超高效液相色谱系统:美国Waters 公司
1.2 试药
白藜芦醇:萨恩化学技术(上海)有限公司(质量分数:98%)。
白藜芦醇标准品:上海源叶生物科技有限公司(批号:R02J6S1)。
单甲氧基聚乙二醇(MePEG):萨恩化学技术(上海)有限公司(Mr=2000)。
二环己基碳二亚胺(DCC):国药集团化学试剂有限公司。
4-二甲氨基吡啶(DMAP):阿拉丁试剂责任有限公司。
色谱纯甲醇、乙腈:Merck公司。
其余均为分析纯。
2 实验方法与结果
2.1 纳米材料的合成
根据洪伟勇[9]等的合成方法进行改良合成。
1)聚乙二醇氰基乙酸酯(MePEGCA)的合成 将氰基乙酸、MePEG、DMAP适量加入三口瓶中,氮气保护下,抽真空,加入无水二氯甲烷,搅拌溶解后,将溶有DCC的无水二氯甲烷注入三口瓶中,室温搅拌24 h。抽滤,无水二氯甲烷洗涤滤渣,合并滤液,真空减压浓缩,旋干至半固体,缓慢倒入3倍量的乙醚搅拌至溶解,-20℃过夜重结晶析出沉淀,得浅黄色固体,即为MePEGCA,真空干燥箱中干燥。
2)十六烷基氰基乙酸酯(HDCA)的合成 将氰基乙酸,十六醇及DMAP适量加入到的三口瓶中,氮气保护下,抽真空,加入无水二氯甲烷,搅拌溶解后,将溶有DCC的无水二氯甲烷注入三口瓶中,室温搅拌24 h。正己烷抽滤,洗涤滤液,滤液真空减压浓缩,旋干至半固体,即为十六烷基氰基乙酸酯黄色粗品,经柱层析分离,得十六烷基氰基乙酸酯白色固体,真空干燥箱中干燥。
3)聚乙二醇化聚十六烷基氰基丙烯酸酯(PEG-PHDCA)的合成 将HDCA和MePEGCA加入三口瓶中,氮气保护下抽真空,加入20mL无水二氯甲烷和无水乙醇,搅拌至溶解后,将甲醛和吡咯烷缓慢注入三口瓶中,氮气保护下,室温搅拌24 h。真空减压旋干,加入10%盐酸溶液搅拌洗涤,无水二氯甲烷萃取三次,再用水洗涤,有机相用无水硫酸钠干燥,过滤,真空减压浓缩,旋干得淡黄色蜡状固体PEG-PHDCA粗品,经柱层析分离,得淡黄色蜡状固体PEG-PHDCA,真空干燥箱中干燥。

2.2 正交试验优选白藜芦醇纳米囊泡处方
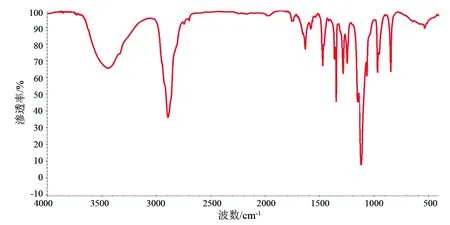
图1 PEG-PHDCA的红外谱
1)白藜芦醇纳米囊泡的制备 采用薄膜分散水化超声法制备:称取司盘60(span 60)50mg、白藜芦醇、胆固醇、PEG-PHDCA适量,置于圆底烧瓶中,加入氯仿/甲醇(V∶V=2∶1)混合溶液20mL,超声溶解后,放入几枚玻璃小珠,真空减压旋干至半固体,真空干燥过夜。搅拌条件下加入水相30mL并在65 ℃下水化1h,超声乳化8h(5min/次)后过滤,即得。
2)白藜芦醇含量测定 色谱柱为Waters Acquity UPLC BEH C18柱( 100mm×2.1mm,1.7 μm) ;流动相为0.05%磷酸水溶液-乙腈(70∶30);流速:0.2mL/min;检测波长:306nm;柱温:30℃;进样量:1μL。
由色谱图可得,白藜芦醇tR为2.841 min(如图2所示)。
精密称取白藜芦醇对照品适量,用甲醇溶解,分别配制成22.0、44.0、66.0、88.0、110.0、132.0、154.0、176.0μg/mL的对照品液,摇匀,0.45μm微孔滤膜滤过后进样。以色谱峰峰面积(A)为纵坐标,白藜芦醇质量浓度(C)为横坐标,绘制标准曲线,得回归方程为A=17523C-34411(r=0.9993)。结果表明,白藜芦醇在22.0~176.0μg/mL范围内与峰面积值呈良好的线性关系。
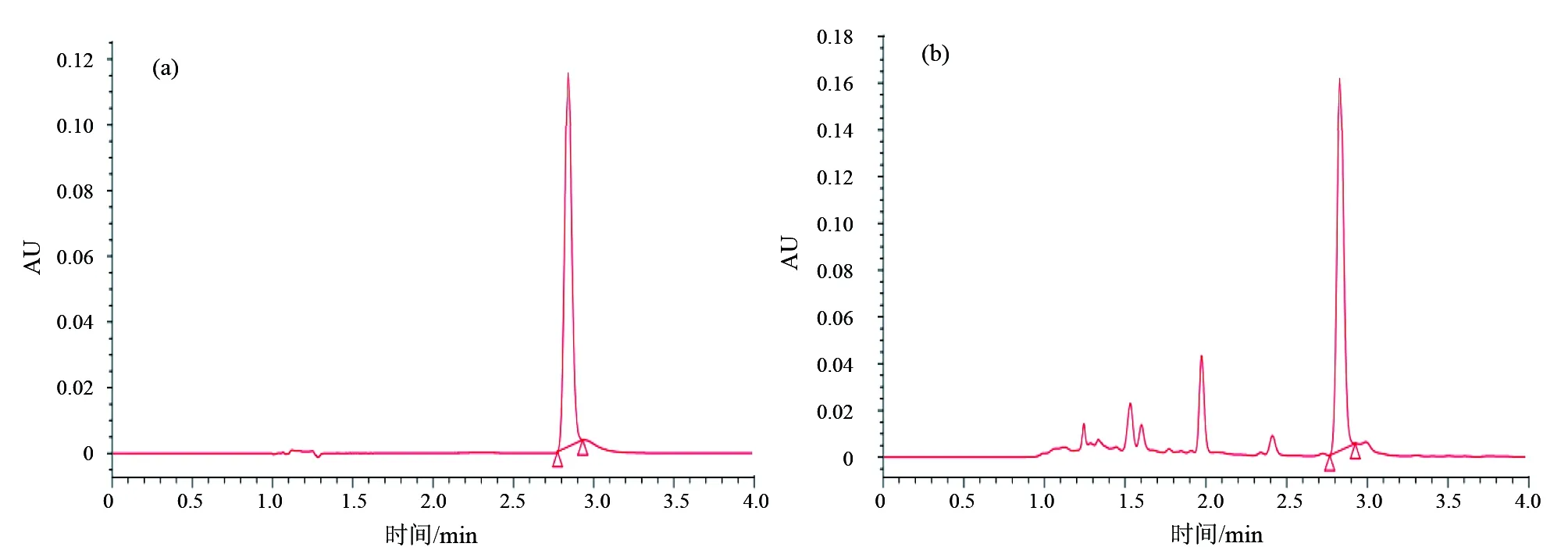
图2白藜芦醇纳米囊泡的UPLC色谱图(A白藜芦醇对照品, B白藜芦醇纳米囊泡)
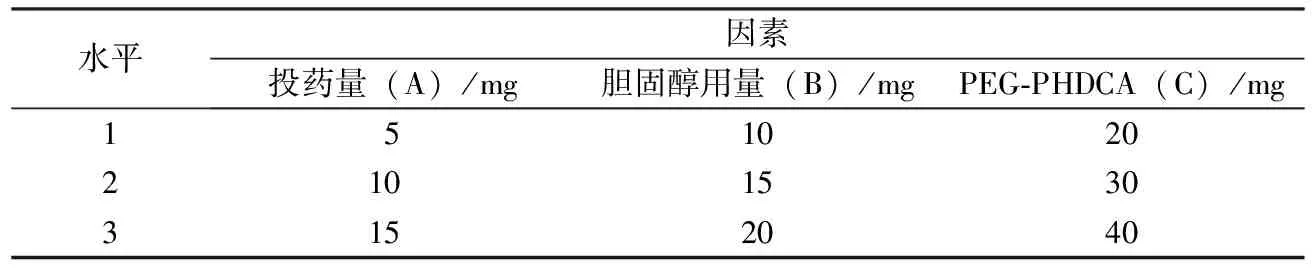
表1 L9(34)正交设计因素水平表
取线性范围内的3种浓度,分别进行精密度、稳定性、重复性试验,结果显示RSD(%) <5%,表明本实验方法稳定可靠。
3)白藜芦醇微囊包封率和载药量的测定 取纳米囊泡溶液适量,置截留分子量为10k的超滤管中,6000r/min离心10min,取超滤上清液注入测定游离药物量。另取纳米囊泡溶液适量加入乙腈溶解(V∶V=1∶3),离心取上清液注入测定药物总量。按下式计算包封率和载药量:
包封率%=[(白藜芦醇纳米囊泡中药物总量-未被包封的游离药物量)/白藜芦醇纳米囊泡中药物总量]×100%
载药量%=(投药量×包封率/白藜芦醇纳米囊泡总质量)×100%
4)正交试验优选处方 在前期预试验基础上,以投药量(A)、胆固醇用量(B)、PEG-PHDCA(C)为影响因素,选取载药量和包封率的综合评分(综合评分=0.5×载药量+0.5×包封率)为评价指标,确定正交试验方案,因素与水平见表1,正交试验结果见表2,方差分析结果见表3。

表 2 正交试验结果
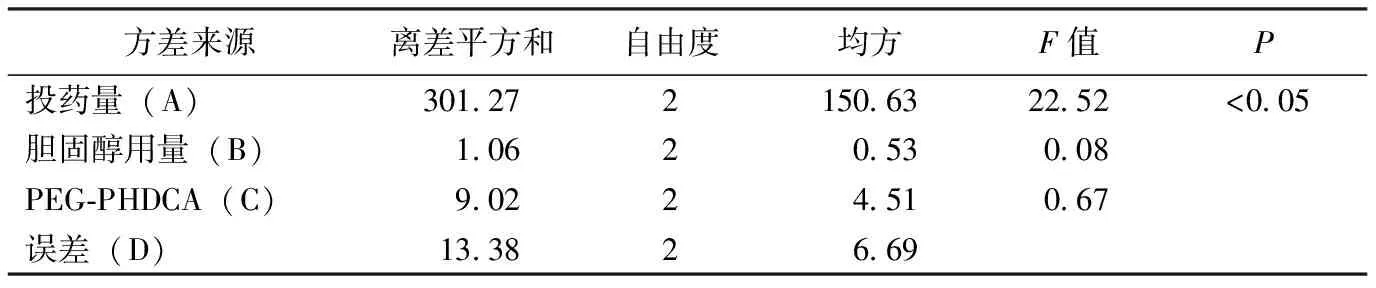
表3 方差分析表
F0.05(2,2) = 19.00; F0.01(2,2) = 99.00
由表2和表3中得出,白藜芦醇纳米囊泡处方影响因素的主次顺序:A>C>B,即投药量对白藜芦醇纳米囊泡制备的影响最大,PEG-PHDCA次之,胆固醇用量影响最小。白藜芦醇纳米囊泡制备的最佳工艺条件为 A3B1C1,即:投药量为15mg,胆固醇用量为10mg,PEG-PHDCA用量为20mg。
5)验证性试验 按上述最佳工艺条件,进行验证试验,白藜芦醇纳米囊泡的平均包封率(92.74 ± 0.27)%,载药量(14.64 ± 0.04)%。
3 讨论
本实验在囊材的合成中MePEGCA和HDCA是最常见的酯化反应,反应中需要脱去水分,所以开始实验前需要对试剂及仪器进行干燥处理,达到尽可能的无水。为了提高合成PEG-PHDCA产量和纯度,在前两步的MePEGCA和HDCA合成中需要进行一定的纯化处理。白藜芦醇纳米囊泡的制备中发现超声乳化时间对粒径有较大的影响,通过对比发现超声乳化8 h的粒径会远远小于超声乳化6h。本实验中未对改造后的白藜芦醇纳米囊泡的释药及药理活性等进行考察,后期需要进一步研究探讨。
