新型恶唑烷酮化合物对耐药性结核分枝杆菌抗菌作用的探讨
2018-10-11化莉赵亚静朱贵荣
化莉,赵亚静,朱贵荣
(1.北京大学国际医院 呼吸与危重症医学科,北京 102206;2.解放军第309医院呼吸科,北京 100091)
近年来,临床结核分枝杆菌的耐药率不断增加[1-2]。恶唑烷酮类化合物是新型抗菌剂,利奈唑胺(linezolid)是唯一被批准应用于临床的恶唑烷酮类药物[3]。然而,linezolid用药会引起神经、视力及血液等毒副作用,因此医药学界一直致力于发现活性更高、毒性更弱的新型恶唑烷酮化合物[4]。本文针对临床分离的多重耐药及广泛耐药结核分枝杆菌,通过体外和动物模型两种不同层面评价新型恶唑烷酮及linezolid的抗菌活性。
1 材料与方法
1.1 菌株和试剂
选取2012年1月-2016年1月309医院收治肺结核患者。17株多重耐药结核分枝杆菌(multi-drug resistance tuberculosis, MDR-TB)和10株广泛耐药结核分枝杆菌(extensive drug resistance tuberculosis,XDR-TB)。以标准菌株H37RV作为质控菌株(购自中国药品生物制品研究所)。Linezolid及新型恶唑烷酮化合物(sy-40、sy-41、sy-142、sy-144)均由中国药科大学制药学院合成。
1.2 结核分枝杆菌培养和药物活性检测
1.2.1 结核分枝杆菌分离培养 采用米氏琼脂培养基,其制备见相关报道。痰标本用2% NaOH液化,作用20 min后,以无菌吸管取0.2 ml分别接种于斜面上,置37℃温箱内培养,每周观察。
1.2.2 药物活性检测 Linezolid及新型恶唑烷酮化合物以倍比稀释配置0.125~32.000 μg/ml。将上述配好的药物溶液按相应比例加入到含有OADC营养添加剂(油酸、牛血清蛋白、右旋糖苷及过氧化氢酶)的Middlebrook 7H10琼脂培养基中。刮取约10 mg生长物,研磨均匀后,用蒸馏水稀释至1 μg/ml,各取0.1 ml接种于含药斜面和对照斜面,置于36℃温箱培养21 d,测定其最小抑菌浓度(minimum inhibitory concentration, MIC)。利用测定最低抑菌浓度(MIC)以上各试验管培养物,分别吸取0.1 ml,移种在不含药物的培养基上,经孵育培养21 d,菌落数<5个的药物浓度为最小杀菌浓度(minimum bactericidal concentration, MBC)。
1.2.3 动物模型活体抗结核活性测试 将0.2 ml含有5×106个活菌的H37Rv及临床分离株(MDR和XDRTB)菌悬液通过尾静脉注射的方式感染BALB/c小鼠。将测试化合物溶于磷酸盐缓冲液中,配成50 mg/ml的溶液。以胃灌方式每天给药1次,恶唑烷酮的灌胃药物浓度为100 mg/kg,利福平(rifampicin, RFP)的灌胃浓度是10 mg/kg。每组8只小鼠,不给药的小鼠作阴性对照。持续给药1个月后,解剖小鼠,取肺组织进行HE染色,并测定全肺的结核分枝杆菌活菌计数。实验动物室注册批文:SYXK(军)2012-0016。
1.3 统计学方法
数据分析采用SPSS 19.0统计软件,计量资料以均数±标准差(±s)表示,计量资料多组比较使用方差齐性检验,进一步两两比较用LSD-t检验,P<0.05为差异有统计学意义。
2 结果
2.1 Linezolid及新型化合物对结核分枝杆菌抗菌活性分析
Linezolid及新型化合物体外抗结核MIC值见表1。对17例MDR-TB及10例XDR-TB,化合物sy142、sy144及linezolid都体现出较低的MIC值。对于sy142,只有1例MDR-TB的MIC值为≥4 mg/L,而XDR-TB的MIC值均在2 mg/L及以下。从MIC分布上分析,sy142对MDR-TB及XDR-TB的体外抗菌效果要略优于linezolid,而sy144的活性与linezolid处在同一水平。Linezolid及新型化合物体外抗结核MBC值见表2。对于临床菌株,MBC的分布状况与MIC分布类似,sy142的效果同样略优于linezolid。
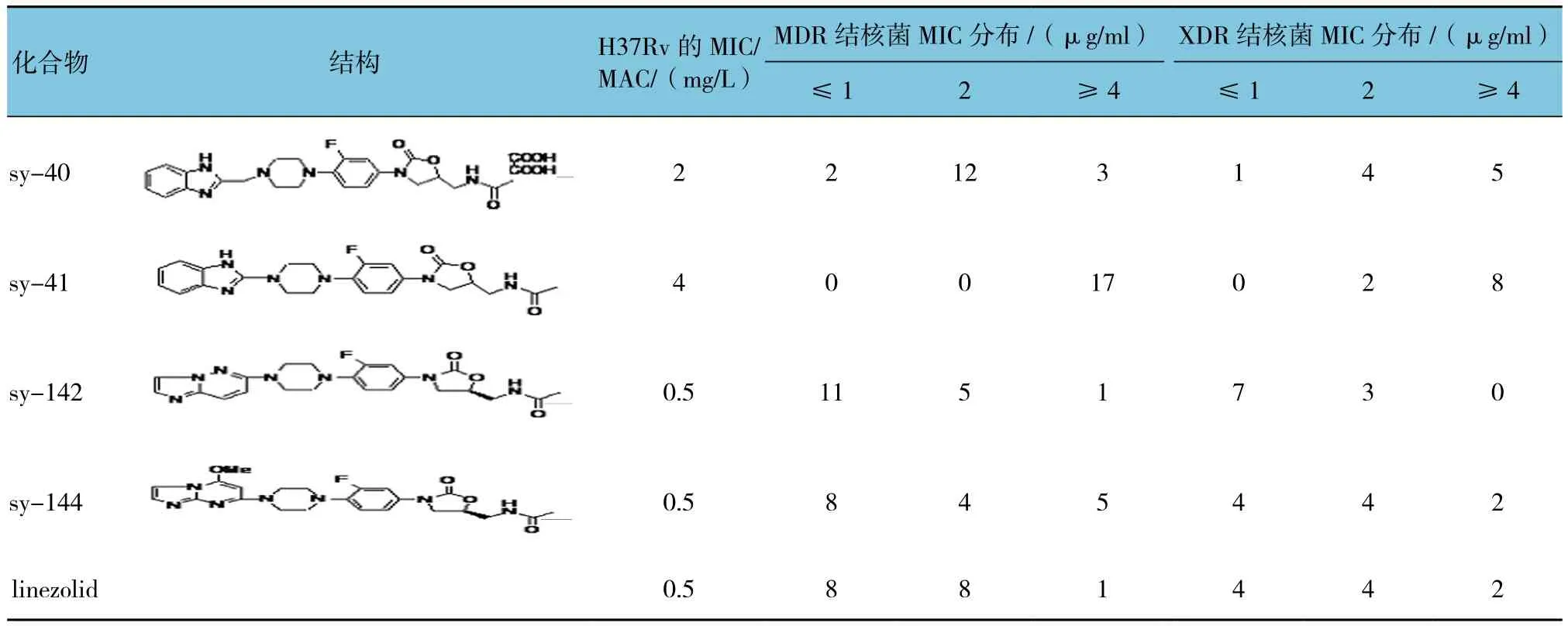
表1 Linezolid及新型化合物体外MIC检测
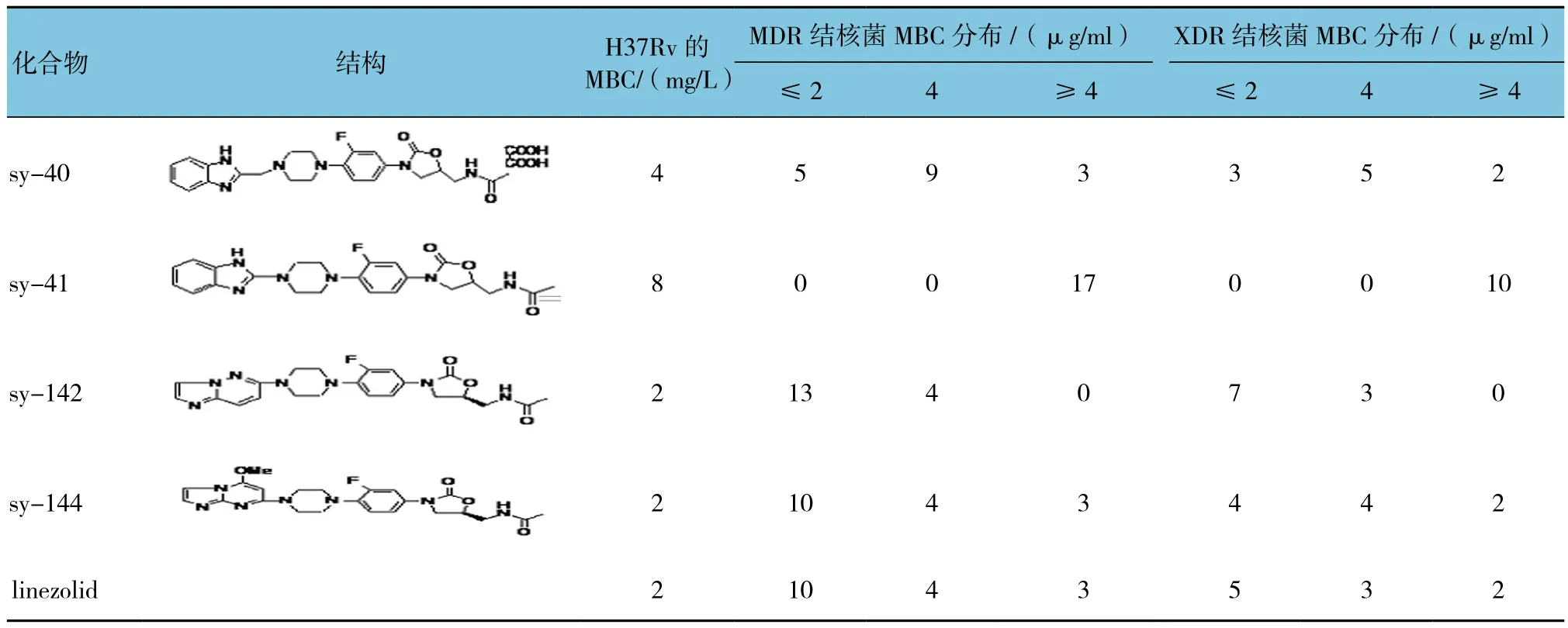
表2 Linezolid及新型化合物体外MBC检测
2.2 linezolid及新型恶唑烷酮化合物对小鼠体内结核分枝杆菌抗菌活性分析
选取sy142、sy144及linezolid进行小鼠体内抗结核治疗并分析比较其优劣差异。将BALB/c小鼠进行结核分枝杆菌攻毒感染1周后,对其进行linezolid、sy142、sy144化合物灌胃治疗。1个月后,将小鼠进行解剖取肺,行HE染色抗酸染色及全肺菌落计数。HE染色后,蓝色细胞聚集区域为炎症区域,这部分区域面积越大表示炎症反应越高。结果显示,未治疗对照组肺部出现大量的炎症细胞(见附图A),说明感染成功。Linezolid、sy142及sy144治疗组中的炎性细胞区域少于对照组,而sy142治疗组的炎症区域面积较Linezolid治疗组的炎症区域面积小,结果差异有统计学意义(见附图B~D,F)。而未感染的阴性对照组,并未出现明显的炎症细胞区域(见附图E)。同时,肺部菌落计数结果显示,linezolid、sy142、sy144及 RFP 治疗对 H37Rv(F=11.34,P=0.000)、MDR(F=14.58,P=0.000)、XDR(F=8.82,P=0.000)菌株治疗差异有统计学意义。进一步两两比较显示,sy142治疗组菌落计数低于linezolid治疗组及sy144治疗组,结果差异有统计学意义。利福平(RFP)对标准菌株H37Rv具有明显的活性,但对MDR及XDR-TB均不具有明显活性(见表3)。

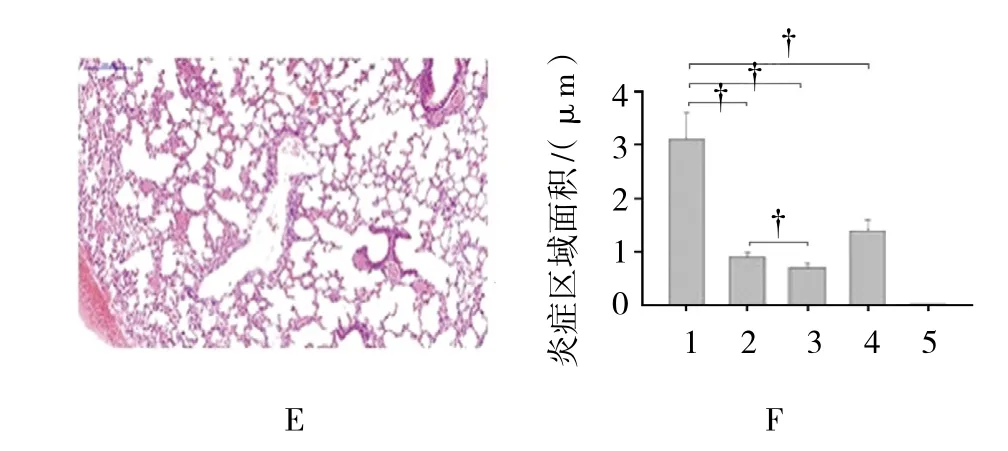
附图 不同化合物治疗结核感染小鼠染色分析(HE×10倍)

表3 linezolid、sy142、sy144及RFP动物体内抗结核活性差异比较
3 讨论
恶唑烷酮类化合物是新型的抗生素,对革兰阳性球菌、结核分枝杆菌等都具有良好的活性。在应用初期针对MDSA及XDR-TB取得较好的治疗效果。Linezolid长期使用会产生很强的副作用,如神经毒性休克及血小板减少症等。由于抗结核治疗周期往往需要半年以上,因此linezolid的毒副作用制约其在抗结核领域的应用。因此,很多药物化学家致力于开发研制毒副作用更低、抗菌谱更广、活性更强的新型二代恶唑烷酮类新药[5]。
目前在研的二代恶唑烷酮类化合物包括AZD-2563[6]、RANBEZOLID[7]、DA7867 等[8]。不同的新型制剂都具有某些自己独到的优势和不足。AZD-2563由Astrazeneca公司研发并已经进入一期临床研究。其活性较linezolid有所提高,并且能够产生长期持久的效果。但由于未知原因,临床研究被中断,而临床研究数据并未被公布。Ranbezolid活性是linezolid的2倍,在体内也具有良好的药代动力学和安全性,但曾有文章报道,含有硝基呋喃基团的化合物可被体内酶类催化,将硝基转化为亚硝基自由基中间体,从而产生细胞毒性,因此Ranbezolid也于一期临床研究后被中断。
在小鼠感染模型中,linezolid,sy142和sy144可以杀灭肺部感染结核分枝杆菌。sy142无论在控制炎性区域面积和直接抑菌作用均强于linezolid,这初步预证了sy142在活体条件下的抗结核活性前景。但具体是否能成为新一类上市药物,还需要药代动力学、安全性、稳定性等大量数据支持。与linezolid的结构比较发现,4哌嗪基被N-杂环取代会提高抗结核活性。所以后续的基于该点的结构改造也至关重要。笔者的发现很有可能成为研发抗广泛耐药结核新药的先导化合物。
