自制和原研地氯雷他定片溶出曲线的比较和评价
2018-09-20严一铭
严一铭


摘 要 目的:比较自制和原研地氯雷他定片剂的溶出行为。方法:根据普通口服固体制剂溶出曲线测定与比较指导原则,采用浆法,高效液相色谱法检测自制和原研片剂分别在pH 1.0、pH 4.5、pH 6.8的缓冲液和水中的溶出度,f2相似因子法比较溶出曲线的相似程度,初步评价其体外释放行为的一致性。结果:主成分的溶液稳定性良好,自制片剂和原研片剂在不同介质中的溶出曲线均相似,四组f2因子都大于50,符合评价要求。结论:自制片剂和原研片剂的体外释放度一致。
关键词 地氯雷他定片 溶出曲线 相似因子 一致性评价
中图分类号:R927.11 文献标志码:A 文章编号:1006-1533(2018)17-0068-04
Comparative study and evaluation on the dissolution profiles of home-made desloratadine tablets and its reference listed drug
YAN Yiming*
(Shanghai SPH New Asia Pharmaceutical Co., Ltd., Shanghai 201203, China)
ABSTRACT Objective: To compare and evaluate the dissolution behaviors between home-made desloratadine tablet and its reference listed drug. Methods: The dissolution of desloratadine tablets was analyzed by an HPLC method according to guiding principles of determination and comparison on dissolution profile of general oral solid preparation. The dissolution of both drugs was determined in buffer solutions at pH 1.0, pH 4.5, pH 6.8 and water, respectively. The degree of similarity of the dissolution curve was compared by similarity factor f2 and then the consistency of the in vitro release behavior was initially evaluated. Results: The solutions containing main components were stable, and the dissolution profiles of both drugs were similar in various types of media (f2 factors>50). The f2 factors were all met the quoted requirements. Conclusion: The in vitro release behavior of both drugs is consistent.
KEy WORDS desloratadine tablets; dissolution profiles; consistency; f2 factor
地氯雷他定是一種强效、非镇静性的长效组胺拮抗剂,具有选择性地拮抗外周H1受体的作用及抗过敏、抗组胺及抗炎作用,可用于缓解与慢性特发性荨麻疹及过敏性鼻炎相关的症状[1]。
随着国家有关部门对仿制药质量与疗效一致性评价工作的深入,药品的体外溶出度对比试验受到越来越广泛的重视。药物在体外的释放行为,可以用来判断其生产工艺的优劣,进而在一定程度上提示该药在体内的消化、吸收和利用的情形,是临床前鉴别药品质量高低、更是与原研药品进行质量比较的重要手段[2]。
本研究通过对自制地氯雷他定片和市售的原研片剂溶出度的测定,比较在不同溶出介质下溶出曲线的相似性,分析自制片剂的体外释放行为,从而进一步提升制剂品质,促进仿制药一致性评价工作在本企业的开展[2]。
1 材料和方法
1.1 试药
地氯雷他定对照品(中国药品生物制品鉴定所,批号100919-200902,含量99.7%);原研片剂恩理思(英国Merck Sharp & Dohme Limited,批号N010881,规格5 mg);自制地氯雷他定片(上海上药新亚(闵行)药业有限公司,批号 170901,规格 5 mg);原料药:自制地氯雷他定,含量:99.1%,批号161201;冰醋酸(85.0%)和三氟醋酸(99.6%)购自Tedia公司;乙腈(色谱纯)购自Merck公司;其他试剂均为市售分析纯;水为纯化水。
1.2 仪器
Agilent 1100高效液相色谱仪、Agilent Technologies 708-DS自动溶出仪(Agilent科技公司); BP121S分析天平(Sartorius AG);HYG-II迴转式调速恒温摇瓶柜(上海新星自动化控制设备成套厂制造);Kromasil 100-5mC18色谱柱(4.6 mm×250 mm,5 mm,AkzoNobel公司)。
1.3 方法
1.3.1 色谱条件
按文献[3]以乙腈-十二烷基磺酸钠溶液(取十二烷基磺酸钠0.87 g,加水至1 000 ml,加三氟醋酸0.5 ml)(43∶67)为流动相,检测波长为280 nm,柱温30 ℃,流速1.0 ml/min,进样量10 ml。理论塔板数按地氯雷他定峰计算不低于2 000,拖尾因子不大于1.5。
1.3.2 线性关系测定
称取地氯雷他定标准品适量,用0.1 mol/L盐酸溶液溶解,配制成20.0 mg/ml浓溶液,然后系列稀释成1.0、4.0、7.0、10.0和12.0 mg/ml的溶液,按色谱条件进样,计算浓度和峰面积的线性回归[4]。
1.3.3 精密度试验
取上述1.0和12.0 mg/ml地氯雷他定的溶液(相当于溶出量的10%和120%),按色谱条件分别进样6次,记录峰面积,计算得到RSD值[4]。
1.3.4 加样回收率试验
称取地氯雷他定原料药50 mg,先用少量乙腈溶解,配成0.25 mg/ml的浓溶液,量取一定体积的浓溶液,按处方比例加入一定量空白辅料,再用水依次稀释成0.001、0.005、0.01和0.012 mg/ml的溶液,取续滤液,作为回收率10%、50%、100%和120%的供试溶液,平行操作3份。再称取地氯雷他定对照品适量,制得浓度为0.01 mg/ml的对照溶液,按色谱条件进样,记录峰面积,计算回收率[4]。
1.3.5 溶解度测定
根据美国药典附录中关于缓冲液配制一章的方法[5],配成pH 1.0、pH 2.0、pH 3.0、pH 4.0、pH 4.5、pH 5.1、 pH 6.0、pH 6.8、pH 7.0和pH 8.0的介质适量,备用。
取过量的地氯雷他定原料药,研细,置11支具塞试管中,其中10支分别加入适量的上述10种溶出介质,1支加入适量水,都放入摇瓶柜内,置37 ℃水浴振荡过夜,使它们形成饱和溶液,滤过,取续滤液待用[6]。
精密称取地氯雷他定对照品适量,以0.1 mol/L盐酸溶解,配制成0.01 mg/ml的对照溶液。取一定体积的上述11种过饱和溶液的续滤液,用0.1 mol/L盐酸稀释至一定浓度,制成供试溶液。按色谱条件进样,记录色谱峰面积,计算地氯雷他定在每种溶剂下的溶解度[6]。
1.3.6 地氯雷他定在溶出介质中的稳定性
称取地氯雷他定原料药适量,分别用pH 1.0,pH 4.5,pH 6.8的溶液适量和水(在水里主药难溶,先加入少量乙腈)充分溶解,用相关介质稀释成0.01 mg/ml的供试溶液。于0、1、2、4、6、8 h各时间点,按色谱条件进样,测定峰面积,计算RSD[6]。
1.3.7 溶出度测定法
取原研和自制样品各12片,按照中国药典溶出度测定第二法(桨法)操作[7]。杯内温度37.0 ℃,水浴温度37.2 ℃,溶剂500 ml,转速为50 r/min,轴延迟转动时间3 s。取样体积3 ml,取样前润洗管路体积5 ml,取样后排空管路体积5 ml,取样针前端弃去体积1 ml,溶媒回补体积4 ml。在5、10、15、20、30、45、90、120 min取样,以后每隔1 h采样,pH 1.0的介质测定时间不超过2 h,其他介质也在6 h内。连续两点溶出量均达85%以上,且差值在5%以内,实验即截止[8]。
精密称取地氯雷他定对照品适量,先以适量0.1 mol/L盐酸溶解,再分别用4种介质稀释至0.01 mg/ml作为对照溶液。取各个时间点采集的溶液,滤过,取续滤液作为供试溶液。按色谱条件进样,计算出各个时间点的溶出量,绘制溶出曲线[9]。
2 结果
2.1 方法学验证
计算得到线性方程:Y=18 082X-0.215 7,R2=0.999 7,表明地氯雷他定在溶出量的10%~120%的范围内线性关系良好。RSD值为0.57%和0.31%,精密度良好。加样回收率良好,可用于溶出曲线的测定(表1)。
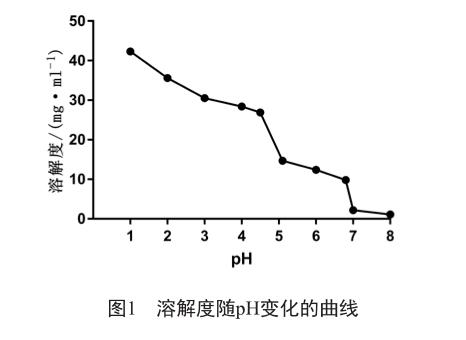
2.2 溶解度的变化
pH-溶解度曲线见图1。选取的溶出介质都符合漏槽条件,根據曲线图所示和有关文献[10],以pH 1.0,pH 4.5,pH 6.8和水作为介质是适宜的。
2.3 稳定性
8 h内,地氯雷他定在上述介质中的稳定性良好,适用于溶出曲线的测定(表2)。
2.4 溶出曲线相似性比较
自制和原研片剂在4种溶出介质中的累积溶出曲线见图2。
经计算,所有溶出曲线各个时间点的RSD值都符合规定。原研片和自制片在pH 1.0的介质里,15 min内的溶出度均大于85%,无需计算f2值。在pH 4.5的介质下,30 min后进入平台期,f2值为69。在pH 6.8的介质下,90 min后进入平台期,f2值为58,在水为介质下180 min后进入平台期,f2值为77。
3 讨论
根据溶出曲线相似性的比较的有关规定,采用非模型依赖法中的相似因子(f2)法进行比较[11]。
本试验通过方法学验证,四组溶液的稳定性都很好,各自的溶出速度也与pH-溶解度曲线相符。原研片和自制片在pH 1.0的介质里,属于快速溶出,即判为溶出行为相似,自制样品在5到10 min时溶出较原研片快一些。在pH 4.5和pH 6.8的介质下溶出较慢,两者的f2值都大于50,认为他们的溶出曲线相似。在水为介质下溶出最慢,但仍能在6 h内结束,f2值也符合规定,曲线相似[11]。
我们认为地氯雷他定自制片与原研片的体外释放行为一致,本批自制片的质量初步达到要求。为了深入比对,我们将对连续三批量产规模的样品进行测定,并继续考察它们在加速和长期条件下,体外释放行为的一致性,进一步完成国家对一致性研究所规定的其他评价项目,为不断提高国产药品的质量而努力。
参考文献
[1] 地氯雷他定片(恩理思)说明书[EB/OL]. [2018-04-05]. https://www.jianke.com/product/24199.html.
[2] 李勇, 陈勇, 杜斌, 等. 替莫唑胺胶囊的溶出曲线和稳定性比较[J]. 上海医药, 2015, 36(19): 76-79.
[3] 国家食品药品监督管理总局. 地氯雷他定片[EB/OL].(2005-05-09)[2018-04-05]. http://www.drugfuture.com/ standard/CN/新药转正标准第60册/地氯雷他定片.pdf.
[4] 高永坚, 袁春平, 黄厚楷, 等. 自研硝苯地平缓释片与对照制剂体外释放度一致性评价[J]. 药物分析杂志, 2017, 37(2): 362-368.
[5] 美国药典委员会. Second Supplement to USP35-NF30, Buffer solutions/Solutions[EB/OL]. [2018-04-05]: https:// wenku.baidu.com/view/f0f7f10991c69ec3d5bbfd0a79563 c1ec5dad707.html.
[6] 谢沐风. 如何测得原研品多条特征溶出曲线指导原则[EB/OL]. [2018-04-30]. https://wenku.baidu.com/view/ 233b40495727a5e9856a61e8. html.
[7] 国家药典委员会. 中华人民共和国药典2015年版四部[M].北京:中国医药科技出版社, 2015: 121-124.
[8] 国家食品药品监督管理总局. 總局关于发布普通口服固体制剂参比制剂选择和确定等3个技术指导原则的通告(2016年第61号)[EB/OL]. (2016-03-18) [2018-04-05]. http://samr. cfda.gov.cn/WS01/CL0087/147583.html.
[9] 商鼎. 阿奇霉素片的溶出度研究[J]. 上海医药, 2017, 38(13): 63-66.
[10] 日本PMDA药品数据库. 医药品IF文件(地氯雷他定片5 mg)[EB/OL]. [2018-04-05]. https://db.yaozh.com/pmda?na me=&date;=&name;=&classificationcode;=&jan;=&company;=&cname;=地氯雷他定.
[11] 孙蓉, 李丁, 康巍, 等. 酒石酸美托洛尔片溶出曲线的测定和评价[J]. 上海医药, 2017, 38(1): 72-75.
