左亚叶酸钠注射液局部安全性实验研究
2018-09-20王丽娜章颖慧焉媛媛王秀英信婷婷吴英良
林 鹏,王丽娜,章颖慧,焉媛媛,王秀英,信婷婷,吴英良
(1.沈阳药科大学生命科学与生物制药学院,沈阳 110016;2.辽宁省药品检验检测院药理室,沈阳 110036;3.沈阳抗生素厂质控处,沈阳 110122)
左亚叶酸是亚叶酸的5-甲酰衍生物的非对映异构体混合物的左旋体,具有生物活性[1]。左亚叶酸钠是左亚叶酸的二钠盐,在临床上用作叶酸拮抗剂如甲氨蝶呤的解毒剂[2],也可与5-氟尿嘧啶合用增强5-氟尿嘧啶在肿瘤治疗中的疗效,用于治疗胃癌和结直肠癌[2]。临床上左亚叶酸钙的应用要比左亚叶酸钠广泛,但其联合用药时不良反应的报道履见[3-4]。左亚叶酸的钠盐和钙盐药动学特征基本一致[5],但左亚叶酸的钠盐相较于其钙盐具有良好的水溶性和生物相容性,能避免合并5-氟尿嘧啶引起的输液管堵塞现象和输注速度不宜过快的缺点,在临床上用钠盐替代钙盐的可行性也有一定的研究[6-8]。本文主要对左亚叶酸钠注射液的安全性进行研究,为临床用药安全提供参考。
1 仪器与材料
1.1仪器 ES1OK-1电子天平(沈阳龙腾电子有限公司);ALC1100.2电子天平(赛多利斯科学仪器(北京)有限公司);BD115恒温培养箱(BINDER公司);80-1电动离心沉淀机(上海手术器械厂);OLYMPUS-BX41相差显微镜[奥林巴斯(中国)有限公司];TP1020全自动脱水机,ST5020全自动染色机,RM2135切片机(德国徕卡仪器公司)。
1.2试药 左亚叶酸钠注射液(1 mL∶50 mg,以左亚叶酸计,沈阳沃森药物研究所,批号20130501);氯化钠注射液(4.5 g∶500 mL,批号130709A02,双鹤药业沈阳有限责任公司);甲醛溶液(500 mL·瓶-1,批号20080922,国药集团化学试剂有限公司);20 mL·L-1鸡蛋清溶液(全身主动变态实验阳性对照液,临用现配)。
1.3动物 日本大耳白家兔,雌雄兼用,普通级,体质量2.1~2.5 kg;豚鼠,荷兰种,雌雄兼用,普通级,体质量306~368 g,均由沈阳药科大学提供。
2 方法与结果
2.1血管刺激性实验 取检疫合格的家兔4只,左侧耳静脉注射左亚叶酸钠注射液50 mg·kg-1,右侧耳静脉注射同体积氯化钠注射液,连续给药5 d。每天给药前及末次给药后48,72和96 h肉眼观察并记录动物及注射部位的反应。观察期结束后处死动物,在兔耳静脉远离注射部位1 cm处剪下长2.5~3.0 cm的组织,进行组织病理学检查。结果表明,肉眼观察左亚叶酸钠注射液组血管及周围组织无刺激性;组织病理学检查显示,兔耳缘静脉组织结构均正常,血管内皮及管壁完整,内皮无受损,血管内无血栓,血管无破裂,血管周围组织无水肿、出血和炎性细胞浸润等病变,对兔耳缘静脉无刺激性。肉眼观察刺激实验评分标准和光镜观察刺激实验评分标准见表1[9-10],刺激性实验结果见表2。
表1血管刺激性实验评分标准
Tab.1 Scoring standard of vascular irritation test

观察指标肉眼观察描述评分光镜观察描述评分血管充血正常0内皮及管壁完整0充血1内皮受损1血管纹路不清2血管内血栓2血管呈紫红色3血管破裂3周围组织水肿无水肿0正常0轻微水肿1水肿1明显水肿2出血2严重水肿3炎性细胞浸润3坏死4结果判断无刺激性≤0.5无刺激性≤0.5轻度刺激性≤2.5轻度刺激性≤2.5中度刺激性≤4.5中度刺激性≤4.5重度刺激性≤6.0重度刺激性≤7.0
表2左亚叶酸钠注射液血管刺激性实验结果
Tab.2 Results of Sodium Levofolinate Injections on vascular irritation test

组别剂量/mg·kg-1肉眼观察评分48 h72 h96 h光镜观察评分氯化钠注射液-0000左亚叶酸钠注射液500000
注:-表示只给体积,无剂量。
2.2肌肉刺激性实验 取检疫合格的家兔4只,左侧股四头肌注射左亚叶酸钠注射液1 mL,右侧注射氯化钠注射液1 mL。给药后48 h用动物麻醉机安乐死处死动物,纵向切开注射部位,肉眼观察肌肉注射部位有无充血、水肿、变性和坏死等刺激现象。取注射部位肌肉常规固定、制片,做组织病理学检查。结果表明,肉眼观察兔肌肉给药部位无明显变化。组织病理学检查显示,左亚叶酸钠注射液组肌肉横纹清晰细胞核位于肌纤维周边,肌间无出血、水肿、炎性细胞浸润和坏死等病变,对兔股四头肌未见明显刺激性。肉眼观察肌肉刺激评分标准和光镜观察肌肉刺激反应评分标准见表3,4块股四头肌反应评分的总和,若各股四头肌反应评分的最高与最低之差小于2时,认为受试物对肌肉无明显刺激性。若各股四头肌反应评分的最高与最低之差大于2时,应另取2只动物重新实验,如重新实验超过2分则认为受试物对肌肉存在明显刺激性,不可供肌肉注射用[11]。结果见表4。
表3肌肉刺激性实验评分标准
Tab.3 Scoring standard of muscle irritation test
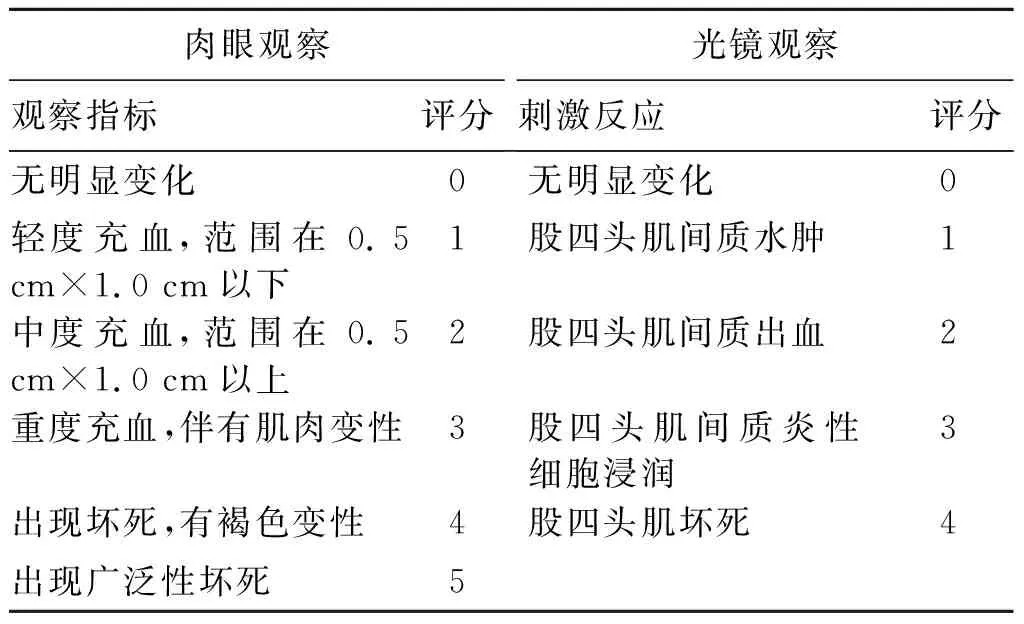
肉眼观察观察指标评分光镜观察刺激反应评分无明显变化0无明显变化0轻度充血,范围在0.5 cm×1.0 cm以下1股四头肌间质水肿1中度充血,范围在0.5 cm×1.0 cm以上2股四头肌间质出血2重度充血,伴有肌肉变性3股四头肌间质炎性细胞浸润3出现坏死,有褐色变性4股四头肌坏死4出现广泛性坏死5
表4左亚叶酸钠注射液肌肉刺激性实验结果
Tab.4 Results of Sodium Levofolinate Injections on muscle irritation test

组别剂量/mg·kg-1肉眼观察评分光镜观察评分氯化钠注射液-00左亚叶酸钠注射液5000
注:-表示只给体积,无剂量。
2.3全身主动变态实验 取检疫合格的豚鼠24只,按照体质量随机均分为4组,分别为左亚叶酸钠注射液高剂量组(50 mg·kg-1)、低剂量组(13 mg·kg-1,临床等效剂量)、阳性对照组(20 mL·L-1鸡蛋清溶液)及阴性对照组(氯化钠注射液)。分别腹腔注射左亚叶酸钠注射液0.5 mL,隔日致敏,连续5次。末次致敏后第14天,各组分别静脉注射上述药液的激发液1.0 mL,观察记录给药后30 min(低剂量组由于30 min时仍有症状出现,故观察时间延长至1 h)内动物有无竖毛、抽搐、呼吸困难、休克和死亡等变态反应症状、症状的出现时间及消失时间。判断变态反应的发生程度,计算变态反应发生率。结果表明,静脉注射激发后观察,阴性对照组全部均未见变态反应症状(发生率为0%),评价为变态反应阴性;阳性对照组全部立即出现呼吸困难、步态不稳、跳跃和死亡等变态反应症状,4 min内6只动物全部死亡(发生率为100%),属变态反应极强阳性;左亚叶酸钠高剂量组3只动物5~24 min内出现搔鼻、喷嚏和咳嗽等症状(发生率为50%),属变态反应阳性。左亚叶酸钠低剂量组3只动物12~41 min内出现颤抖、搔鼻、喷嚏、咳嗽、排便和流泪等症状(发生率为50%),属变态反应阳性。全身主动变态反应评价标准见表5[12],结果见表6。
表5全身主动变态反应评价标准
Tab.5 Standard of valuation of active systemic anaphylaxis test

症状反应分级症状反应分级症状反应分级正常-呼吸急促++步态不稳+++躁动+排尿++跳跃+++竖毛+排粪++喘息+++颤抖+流泪++痉挛+++搔鼻+呼吸困难+++旋转+++喷嚏++哮鸣音+++潮式呼吸+++咳嗽++紫癜+++死亡++++
表6左亚叶酸钠注射液全身主动变态实验结果
Tab.6 Results of Sodium Levofolinate Injections on active systemic anaphylaxis

组别每只动物反应程度123456变态率/%阴性对照组------0左亚叶酸钠高剂量组++--++++-50左亚叶酸钠低剂量组--++++++-50阳性对照组++++++++++++++++++++++++100
2.4溶血与凝聚实验 取检疫合格的健康家兔1只,心脏采血10 mL,玻璃珠振摇除纤维蛋白原,使成脱纤血。用氯化钠注射液洗涤,离心(1 500 r·min-1,15 min),反复3次至上清液不显红色,沉淀的红细胞按照体积比用氯化钠注射液配制成体积分数为2%的红细胞混悬液。取洁净试管9支,1~6号管为左亚叶酸钠实验管,7号管为阴性对照管,8号管为阳性对照管,9号管为左亚叶酸钠对照管。见表7。按照表7[13-14]所示,依次加入不同体积的左亚叶酸钠注射液、氯化钠注射液、纯化水及体积分数为2%的红细胞悬液,混匀,置于培养箱中37±0.5 ℃温育。观察各管在0.25,0.5,0.75,1,2和3 h是否有溶血与凝聚现象。结果表明,3 h内阴性对照管上层溶液呈无色透明,红细胞全部下沉,未见溶血现象,阳性对照组各管溶液呈澄明红色,管底无细胞残留,完全溶血。左亚叶酸钠注射液各管在3 h内红细胞全部下沉,未见红棕色絮状沉淀,上层溶液澄清无色,无溶血及凝聚现象。对红细胞是否产生溶血及凝聚作用判断标准见表8[15],结果见表9。
表7溶血与凝聚实验加样体积
Tab.7 Test volume in hemolysis and coagulation test

名称各管加液体积/mL1234567892%红细胞混悬液2.52.52.52.52.52.52.52.5氯化钠注射液2.42.32.22.12.02.52.5纯化水2.5左亚叶酸钠注射液0.10.20.30.40.52.52.5
表8溶血与凝聚实验结果判断标准
Tab.8 The standard of hemolysis and coagulation test

现象评价溶液呈澄明红色,管底无细胞残留全溶血溶液呈澄明红色或棕色,管底有少量红细胞残留部分溶血红细胞全部下沉,上层液体无色澄明无溶血溶液中有棕红色或红棕色絮状沉淀,振摇后不分散凝聚
表9左亚叶酸钠注射液溶血与凝聚结果
Tab.9 Results of Sodium Levofolinate Injections on hemolysis and coagulation test

时间/h管号1234567890.25-------±/0.50-------+/0.75-------+/1-------+/2-------+/3-------+/凝聚-------//
注:+表示全溶血,-表示无溶血或无凝聚现象,±表示部分溶血,/表示无需观察溶血或凝聚现象。
3 讨论
在本实验条件下,左亚叶酸钠注射液对兔耳缘静脉、股四头肌均无刺激作用,对兔血红细胞无体外溶血与凝聚作用。全身主动变态实验是通过观察抗原与IgE抗体结合后导致肥大细胞、嗜碱性脱颗粒、释放活性介质而导致的全身性变态反应,该实验目的是为了观察受试物经全身给药后对动物引起的变态反应,而非为了检验供试品对动物产生的毒性积累作用[16-17],因此本实验设置左亚叶酸钠高和低2个剂量组以观察受试物在不同质量浓度时引起的变态反应是否相同。左亚叶酸钠注射液对豚鼠全身主动变态反应呈阳性,但低剂量组(临床等效剂量)的阳性反应均为喷嚏、咳嗽等并不严重的现象,反应出现的时间较晚,且尚未见到临床应用的不良反应报道,因此可判断其全身主动变态反应并不严重。亚叶酸钙临床偶见皮疹、荨麻疹或哮喘等变态反应[18],左亚叶酸钠出现与亚叶酸钙类似的变态反应也有可能。左亚叶酸钠注射液的主要杂质为7-羟基-8-氢叶酸和10-甲酰叶酸,其中10-甲酰叶酸结构收录于欧洲药典中[19]。由此可见,左亚叶酸钠注射液在本实验条件下,基本符合注射剂的安全要求,但临床应用时应密切关注其变态反应的发生。
