肺透明细胞瘤临床病理分析
2018-08-30付万垒刘博王亚丽
付万垒 刘博 王亚丽
肺透明细胞瘤(clear cell tumor of the lung, CCTL)亦名糖瘤(sugar tumor),是一种较为罕见的良性肿瘤,1963年Liebow 和Castleman[1]首次作了报道,到目前为止全球仅仅报道50多例。近年文献将肺透明细胞瘤归入血管周围上皮样细胞分化的肿瘤(neoplasms with perivascular epithelioid cell differentiation, PEComa)谱系中[2-5]。虽该肿瘤为良性肿瘤,但是可以多发,又位于肺脏内,特殊的病理特征易与肺原发的透明细胞癌和转移的恶性透明细胞癌等相混淆[6-9]。本研究报告3例CCTL,结合临床与病理资料及复习相关文献进而探讨该肿瘤的临床病理特征、诊断、鉴别诊断及预后,旨在提高对该肿瘤的认识以减少误诊。
资料与方法
一、临床资料
例1男性,49岁;健康体检发现右肺中叶包块半个月,患者无明显症状;术后包块大小2.0 cm×1.2 cm×0.6 cm;术后随访65个月,无复发。例2女性,25岁,护士;单位体检发现肺部阴影1个月,无其他不适;原单位胸部CT示:右下肺可见一类圆形阴影,边界清楚,大小约2.8 cm×2.3 cm,未见明显钙化及卫星灶;我院复查肺部CT示:右下肺叶两个结节影,性质待定,结核?其他?临床诊断:考虑结核球可能性大,不排除炎性假瘤、原发性支气管癌,肺良性肿瘤可能;后行CT引导下经皮肺穿刺活检术,病理明确诊断后未行包块切除;带瘤随访46个月,无症状,包块无明显增大。例3女性,67岁;患者因胸部隐痛半年余为主诉入院。外院CT示:左肺中叶纵膈旁见类圆形肿块影,截面大小约3.8 cm×4.3 cm,边缘光滑清晰,与心包分界不清,诊断意见:左肺中叶纵膈旁占位,考虑来源纵膈良性瘤性病变,神经源性肿瘤可能性大;本院CT示:左肺中叶心影旁可见团块影,大小约4.3 cm×3.2 cm,形态规则,边界清,增强扫描静脉期较动脉期明显强化,诊断结论:左肺中叶团块影,考虑良性病变,硬化性血管瘤不除外;临床诊断:右肺包块?纵隔肿瘤?术后随访14个月,无复发。
二、研究方法
3例标本均经10%中性福尔马林固定,石蜡包埋,3 μm切片、常规HE及免疫组化染色(EliVision两步法染色),Olympus BX40显微镜下观察;所用抗体HMB-45、Melan-A、CD34、CK、EMA、S-100、Syn、CgA及Ki-67均为即用型抗体,均购自福州迈新生物技术开发有限公司。CK采用胃酶消化修复,其余试剂均采用高温高压法修复,用已明确的阳性病例做阳性对照,用PBS缓冲液做阴性对照,所有实验操作流程严格按试剂说明书进行。
结 果
一、巨检
例1扁圆形包块一枚,大小2.0 cm×1.2 cm×0.6 cm,表面光滑,似有包膜,切面灰白色,实性质软。例2灰白色线样条组织3条,长0.2~1.2 cm,直径约0.1 cm。例3肺组织一块,大小6.5 cm×5.0 cm×3.0 cm,被膜下见一圆形肿物一枚,大小:3.5 cm×3.0 cm×3.0 cm表面光滑,似有包膜,切面灰白色,实性质地偏软。
二、镜检
肿瘤主要由器官样或片状弥漫排列的胞浆透亮的细胞组成,瘤细胞间见纤细的薄壁血管分隔,血管大小不一,部分区域可呈血管外皮瘤样结构,见图1。瘤细胞多呈圆形或多边形,大小较一致,胞界清楚,大部分胞浆透亮,部分胞浆呈嗜酸性细颗粒状;胞核体积较小、居中,大小较一致,呈圆形或卵圆形,染色质均匀、浓密,未见核分裂;肿瘤组织内均未见坏死。
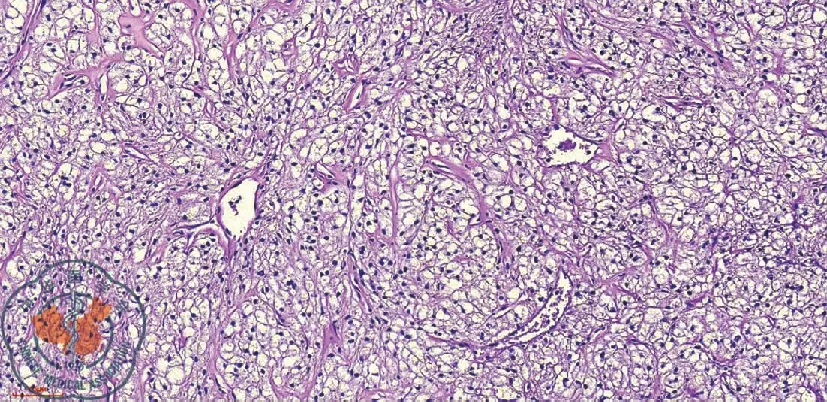
图1 肿瘤细胞胞浆透亮呈弥漫一致分布,瘤细胞间见纤细的薄壁血管分隔,血管大小不一,部分区域可呈血管外皮瘤样结构(HE×40)
三、 免疫组化
3例肿瘤细胞HMB-45、CD34、Melan-A均呈(+)(图2~4),Ki-67均低表达(<1%+),1例SMA(+);而CK、TTF1、EMA、S-100、CD117、desmin、Syn、CgA均呈(-)。组织化学 PAS(+)。
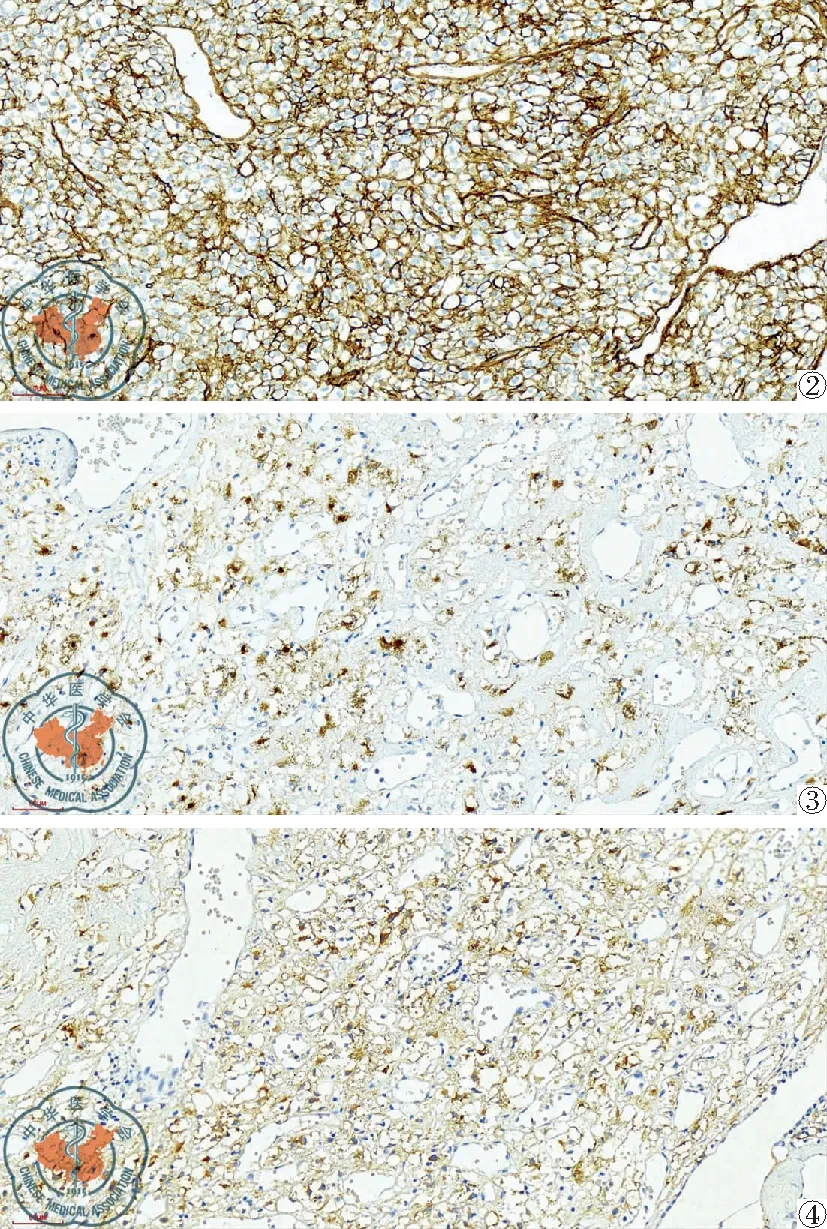
图2 肿瘤细胞CD34(+),EliVision法,200×;图3 肿瘤细胞HMB-45(+),EliVision法,200×;图4 肿瘤细胞Melan-A(+),EliVision法,200×
讨 论
一、临床特点
肺透明细胞瘤发病年龄范围较广为8~78岁,主要好发于40~60岁的中年人,女性略多于男性[10-12]。患者通常无任何症状,常因体检或其他因素行胸片检查时偶然发现,该肿瘤通常位于肺的周边部[13-15],多为孤立性结节,少数也可为多发灶,生物学行为一般为良性,手术完整切除可治愈。肺透明细胞瘤也可发生转移,甚至致死的情况[16]。本组3例患者,年龄25~67岁,平均年龄47岁,均发生在肺的周边部,2例为单发孤立结节,1例为多发的结节(2个);2例无症状体检发现,1例患者因胸部隐痛半年余,CT发现肺部包块,无特异性症状;与文献报道基本相符[17]。本组3例患者临床及影像学无一例可明确诊断,甚至肿瘤的良恶性都无法提示。
二、诊断要点
肺透明细胞瘤是WHO(2013)软组织分类中具有血管外周上皮样细胞分化肿瘤的一种良性间叶性肿瘤。该肿瘤多位于肺的周边部,个别位于气管内,绝大多数为孤立的边界清楚的圆形或卵圆形结节,少数病例可呈多发灶;直径一般小于3 cm,少数病例可达到10 cm,表面可见包膜,易与肺实质剥离,切面灰白至灰红色,实性质中偏软。光镜下肿瘤细胞丰富,呈腺泡状、巢状或片状弥漫排列;瘤细胞巢间见丰富的、纤细的薄壁血管分隔,可有血管外皮瘤样结构;瘤细胞大小较一致,呈圆形或多边形,细胞胞界清楚,胞浆透亮或淡嗜酸性细颗粒状;胞核呈圆形或卵圆形,居中,体积较小、且大小较一致,染色质均匀无明显异型性,通常缺乏核分裂像及坏死。极少数病例,瘤细胞异型性明显(核大深染、多形、核分裂易见),可见凝固性坏死,呈浸润性生长,称为恶性透明细胞糖瘤[18]。本组3例患者,肿瘤为圆形或卵圆形,直径2~3.5 cm,边界清晰,完整切除的2例可见包膜;3例肿瘤细胞形态均分化较为良好,胞浆透明,无异型性及坏死,随访14~46个月,切除标本无复发,带瘤生长的多发性的患者包块无明显增大及不适,符合良性生物学行为。肺透明细胞瘤的瘤细胞免疫表型主要表达呈HMB-45、Melan-A、部分病例SMA,少数病例可表达NSE、Syn(局灶或弱阳性)[19];而CK、TTF1、EMA、S-100、CD117、desmin、CgA均呈阴性反应;近来认为CD34阳性有助于诊断[13,20]。本组3例中HMB-45、CD34、Melan-A 均呈阳性,1例SMA弱阳性,Ki-67均低表达(<1%+),余指标阴性。结合形态学及免疫表型本组3例诊断明确,为良性肺透明细胞瘤,进一步验证了CD34为肺透明细胞瘤的另一个可靠免疫指标。
三、组织起源
目前对肺透明细胞留的起源尚不十分明确,鉴于免疫表型发现瘤细胞特征性表达黑色素生成标记及肌源性(HMB-45和SMA),与肾血管平滑肌脂肪瘤等有相似点,WHO(2013)软组织分类中将肺透明细胞瘤暂归入PEComa家族,目前认为肺透明细胞瘤可能来源于血管外周上皮样细胞[21]。近来发现肺透明细胞瘤广泛表达CD34,而PEComa家族中其他肿瘤,如血管平滑肌脂肪瘤、淋巴管平滑肌瘤等一般不表达,且PEComa家族的肿瘤相对较少见,以至于对该组肿瘤的起源仍然存在一定的争议。
四、鉴别诊断
1. 肺原发透明细胞癌: 是一种极为罕见的向无明确的腺癌、鳞癌或神经内分泌分化的大细胞癌[22];与肺透明细胞瘤主要区别在于细胞核形状不规则,异型性明显,核分裂易见,无血窦样血管,免疫组化表达上皮性标记,不表达黑色素和肌源性标记。组织化学证实瘤细胞内常含糖原,也可不含糖原,无黏液。电镜下无特征性超微结构。
2. 肺透明细胞类癌: 镜下肿瘤细胞大小较一致,胞质透亮,异型性小,富于薄壁血管等特征与肺透明细胞瘤易混淆。但前者免疫组化Syn、CgA、NSE等弥漫阳性,细胞角蛋白阳性,而 HMB-45及Melan-A均为阴性;后者HMB-45及Melan-A,CD34阳性,一般Syn、CgA、NSE等神经内分泌指标呈阴性,但也有个例报道NSE和Syn可以表达,仅为局灶或弱表达,不会弥漫阳性,而且细胞角蛋白阴性[23]。
3. 转移性透明细胞癌: ①肾脏来源:有肾癌史(多为肾透明细胞癌),镜下肿瘤细胞呈腺泡状或腺样排列,免疫组化表达CK、EMA、CD10、Vim,不表达HMB45 和Melan-A,PAS 染色阴性[24];②肝脏来源:肝透明细胞癌,肿瘤细胞呈片状弥漫或器官样结构,胞浆透明,但细胞核稍大,广泛取材几乎总能找到典型的肝细胞性肝癌区域,免疫组化表达CK8、CK18、EMA、Hepatocye,不表达HMB45 、CD34、Melan-A;③卵巢来源:多见于老年女性,肿瘤细胞多由透明及鞋钉样细胞组成,呈实性和管状结构排列,透明细胞PAS 染色也可以呈阳性,免疫组化表达上皮标记EMA、CK 和CA125,不表达HMB45。
4. 副神经节瘤: 镜下肿瘤细胞多为上皮细胞样形态,呈巢状、片状或器官样排列,细胞呈多角形,体积较大,细胞质丰富、透明或嗜酸性细颗粒,间质血管丰富、扩张成窦,免疫组化表达神经内分泌标记,如Syn、NSE、CgA;形态学与肺透明细胞瘤需要鉴别,尤其后者少量病例也表达神经内分泌指标Syn、NSE,使两者鉴别更为困难;但是后者细胞体积稍小,瘤细胞免疫组化:HMB-45、Melan-A及CD34呈阳性,组织化学PAS(+)可以鉴别。
5. 透明细胞肉瘤或透明变性恶性黑色素瘤: HMB-45、Melan-A和S-100常呈阳性,且ki-67指数较高,常有病史及明显恶性的生物学行为;而肺透明细胞瘤虽HMB-45、Melan-A呈阳性,但一般不表达S-100,而CD34、SMA常呈阳性,ki-67指数呈低表达,生物学行为呈良性进程[25]。本组一例穿刺活检患者自发现至今已4年,且为多发性,每年胸片随访仍无明显变化,患者未出现其他不适。
6. 肺颗粒细胞瘤: 肿瘤细胞呈弥漫分布,常为卵圆形或多角形,富含嗜酸性颗粒状或空泡状的胞浆,胞核较小呈圆形或卵圆形,无明显异型性,需要与肺透明细胞瘤鉴别;但是前者更为罕见,肿瘤一般呈息肉样生长,突入气管或支气管腔内,细胞体积较大、胞浆更为丰富;免疫组化: S-100(+),HMB45(-),CD34(-)可以协助鉴别[26]。
五、治疗与预后
肺透明细胞瘤通常为良性肿瘤,根据WHO的治疗原则首选手术完整切除,无需其他辅助性治疗,多数患者可治愈[20,27]。本组共3例,其中2例手术包块完整切除,一例穿刺活检;随访14~46个月,2例切除患者无复发,1例带瘤生长患者随访46个月包块无明显增大及其他不适,进一步印证了其良性生物学行为。但仍少量恶性生物学行为的病例报道[28-29]。Gaffey 等[30]曾报道明确诊断为肺透明细胞瘤患者,术后随访10年发生肝和腹腔转移而致死的病例。因此,对于肺透明细胞瘤统称为良性肿瘤尚存一定争议,该肿瘤的生物学行为有待大量临床病理研究进一步求证;对于诊断肺透明细胞瘤的患者应长期随访。
