人类BRAF 基因突变检测试剂盒性能评价
2018-08-15游延军胡泽斌蒲小聪杨达梅龙腾镶高飞
游延军,胡泽斌,蒲小聪,杨达梅,龙腾镶,高飞
作者单位:611731 成都,四川省食品药品检验检测院(游延军、蒲小聪);611731 成都,迈克股份有限公司(杨达梅、龙腾镶);100050 北京,中国食品药品检定研究院体外诊断试剂所非传染病诊断试剂室(胡泽斌、高飞)
BRAF 基因位于 7q34,长约 190 kb,编码丝/苏氨酸特异性激酶。该激酶是 RAS/RAF/MEK/ERK/MAPK 信号通路最为关键的激活因子,参与调控细胞的生长、分化、增殖及凋亡等[1]。BRAF 基因主要有两种突变类型:11% 的突变发生在编码甘氨酸环的 11 号外显子上,如 G463、G465、G468 等点突变;89% 的突变发生在编码激活区的15 号外显子上,其中 80% ~ 90% 的突变位于第 1799号碱基上,T 突变为 A(T1799A),导致其编码的缬氨酸被谷氨酸取代(V600E)[2]。在多种人类恶性肿瘤中,如恶性黑色素瘤[3]、结直肠癌[4]、非小细胞肺癌[5]、甲状腺癌[6]等均存在不同比例的 BRAF 突变。研究表明,BRAF 基因发生V600E 突变时,病患无法从抗 EGFR 的相关靶向药物的治疗中获益,而且还可导致部分 KRAS 基因野生型患者对EGFR 靶向药物治疗不敏感[7]。在肿瘤个性化治疗高速发展的现在,检测 BRAF 基因 V600E 的突变状态,能够为临床医生对肿瘤患者制定个性化治疗方案提供很好的依据,提高患者的生存率,减少盲目用药,减少病患家庭的经济压力。
1 材料与方法
1.1 材料
1.1.1 样本 本研究的样本是采用石蜡包埋组织提取的核酸样本经标化制备的企业参考品,保存条件为 –10 ~ –30 ℃。
1.1.2 仪器和试剂 评价试剂为 A 公司的人类 BRAF基因突变检测试剂盒(荧光 PCR 法),扩增分析仪器采用美国 ABI 公司的 7500 荧光定量 PCR 仪;对比试剂为经过国家食品药品监督管理部门审批的已上市的 B 公司的人类 BRAF 基因 V600E 突变检测试剂盒(荧光 PCR法)。
1.2 方法
1.2.1 准确性 检测人类 BRAF 基因突变经标化的阳性企业参考品 P1 ~ P3,检测结果应为突变阳性。
1.2.2 特异性 检测人类 BRAF 基因突变经标化的阴性企业参考品(野生型人类基因组)N1 ~ N4,检测结果应为野生型;检测试剂盒检测范围外的人类 BRAF 基因突变经标化的企业参考品 N5 ~ N9,检测结果应为未检出突变;检测非人类基因组样本 N10,检测结果应为未检出突变。
1.2.3 最低检测限 10 ng 野生型人类基因组背景下,对突变比例为 1.0% 的 BRAF 基因 V600E 突变参考品 L1进行检测,检测结果应为突变阳性。
1.2.4 重复性 阴性参考品(野生型)R1,检测结果应均为野生型;阳性参考品 R2 ~ R3,检测应为突变阳性且 Ct值批内变异系数(CV%)应不大于 5.0%。
1.2.5 抗干扰能力 将弱阳性企业参考品 L1(10 ng 野生型人类基因组背景下,突变比率低至 1%),平均分成 3 组,向样本中分别加入等体积不同浓度的蛋白酶 K、甲醛和乙醇,同时采用纯化水加入样本作为对照,判断是否存在干扰,Ct 均值差异 ≤ 1.0 为无干扰,Ct 均值差异 > 1.0 为有干扰。
1.2.6 临床比对 分别用 A 公司人类 BRAF 基因突变检测试剂盒(荧光 PCR法)和 B 公司比对试剂盒检测相同的临床样本 156 例,进行两个试剂盒的一致性评价。
2 结果
2.1 准确性
阳性企业参考品 P1、P2、P3,每个参考品重复一次,检测结果见表 1,根据判定规则(下同):ΔCt = Ct体系II–Ct体系I,若 ΔCt ≤ 9,表明样本为 BRAF 基因 V600E 突变阳性;若 ΔCt > 9,表明样本为 BRAF 基因 V600E 突变阴性。检测结果均为突变阳性。
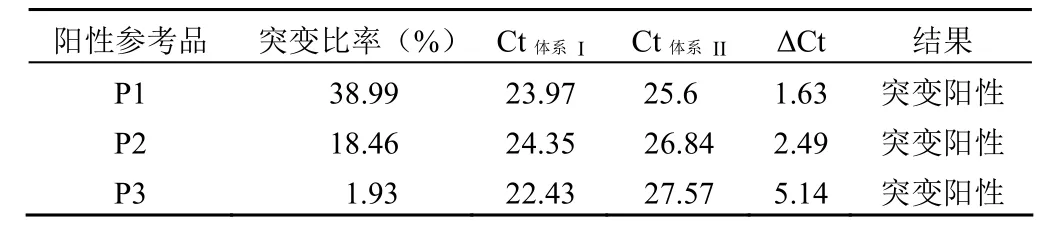
表 1 阳性企业参考品检测结果
2.2 特异性
阴性企业参考品(N1 ~ N10),每个参考品重复 1 次,检测结果见表 2,检测结果均为野生型或未检出突变。
2.3 最低检测限
10 ng 野生型人类基因组背景下,对突变比例为 1.0%的 BRAF 基因 V600E 突变参考品(L1)进行检测,重复3 次,检测结果见表 3,检测结果均为突变阳性。
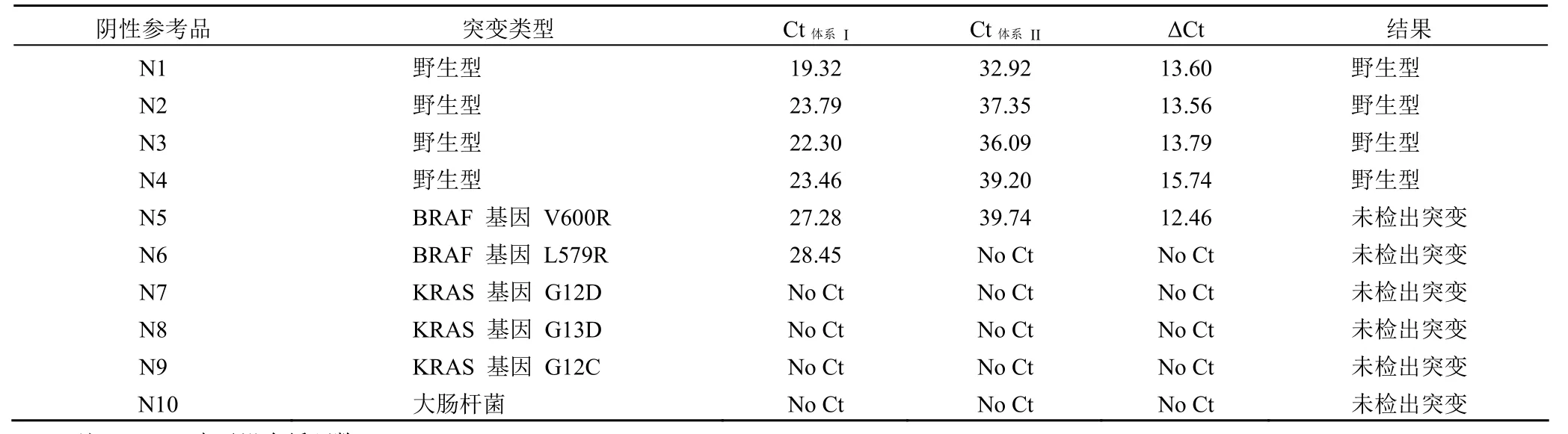
表 2 阴性企业参考品检测结果
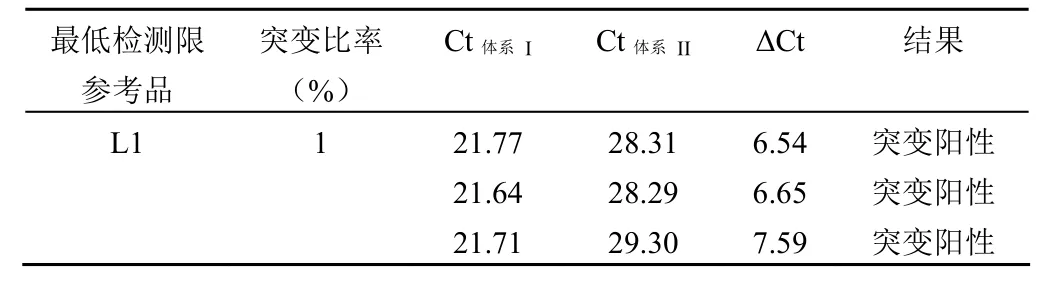
表 3 最低检测限企业参考品检测结果
2.4 重复性
2.4.1 重复性企业参考品 R1 连续检测重复 10 次,检测结果如表 4,检测结果均为野生型。
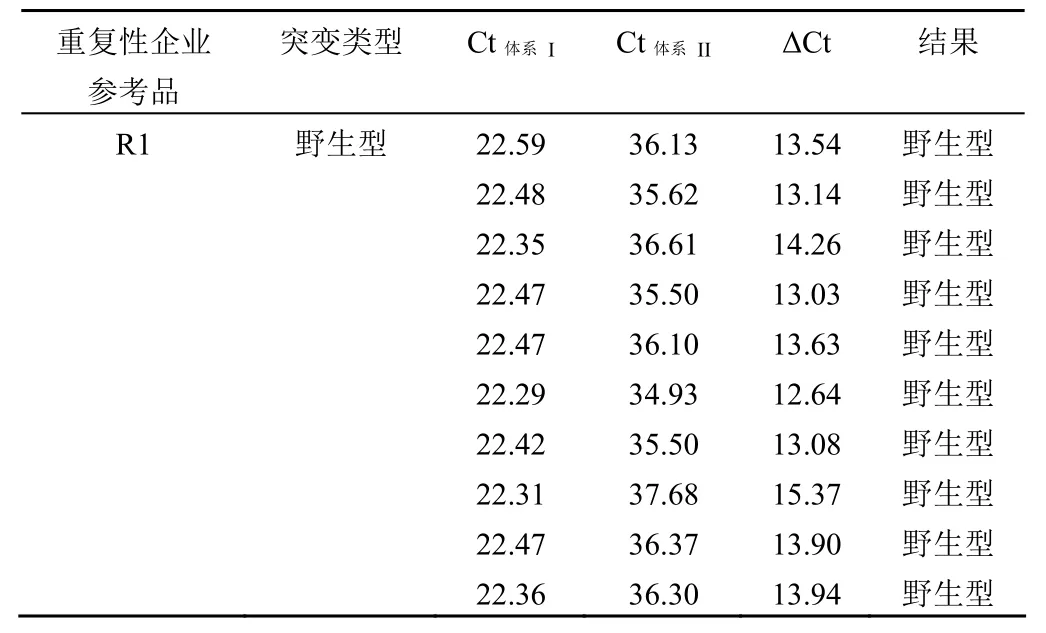
表 4 重复性企业参考品 R1
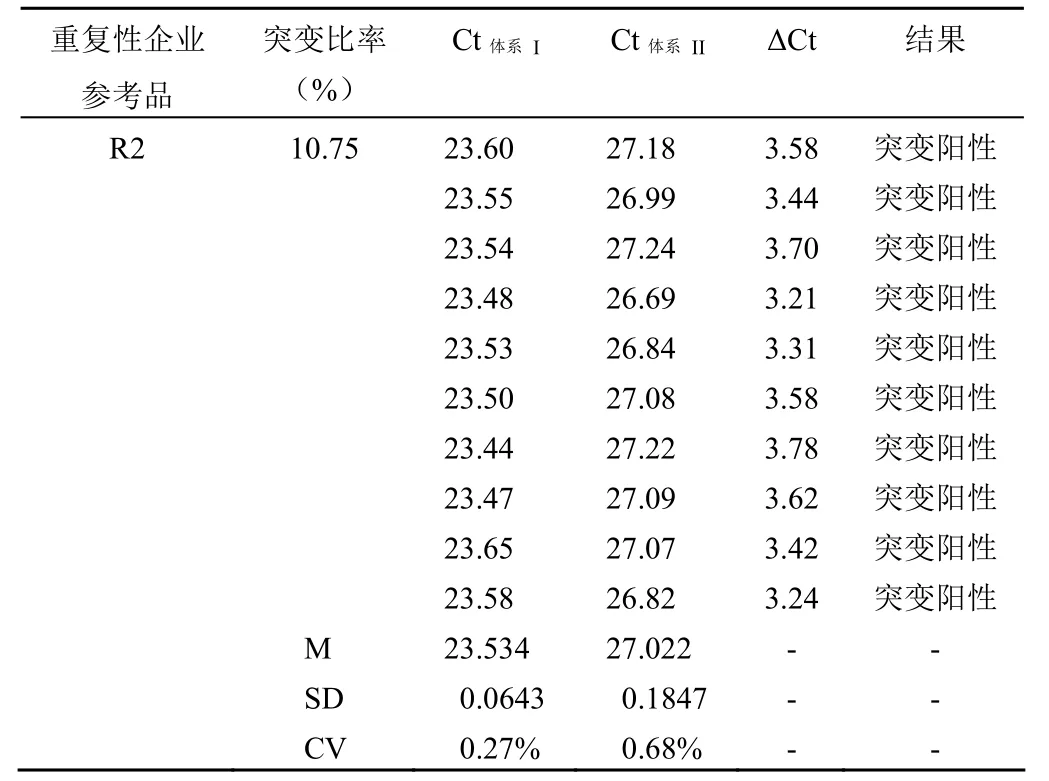
表 5 重复性企业参考品 R2
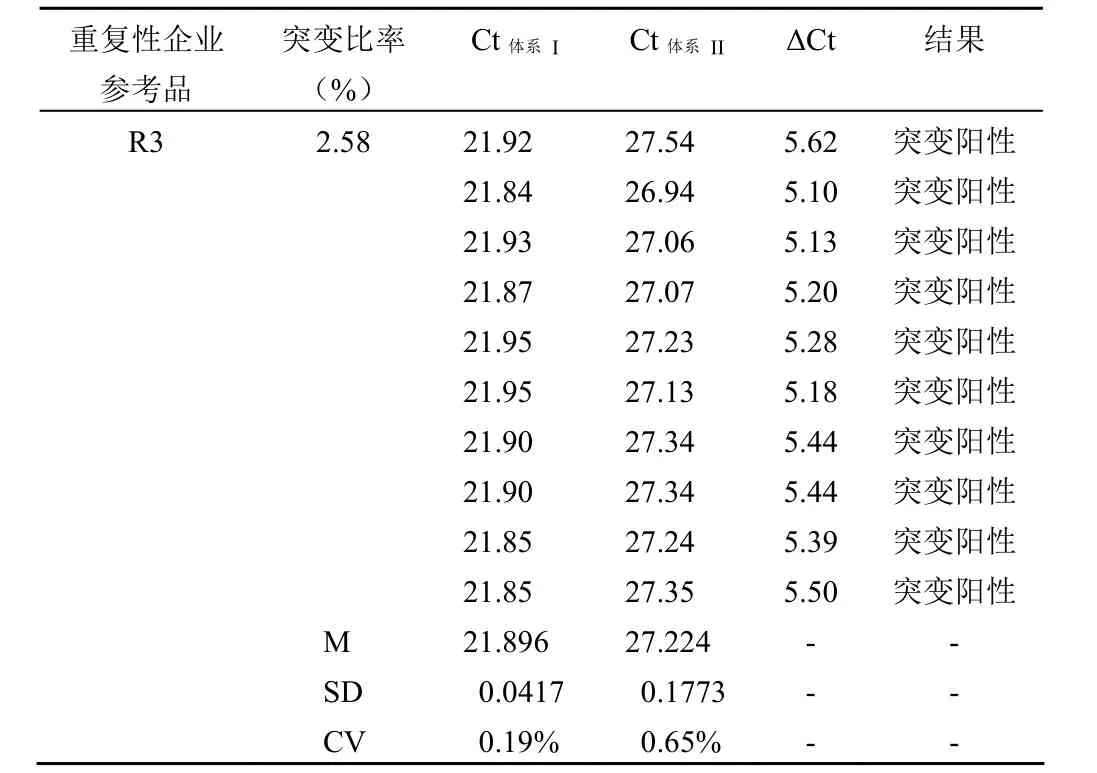
表 6 重复性企业参考品 R3
2.4.2 重复性企业参考品 R2 连续检测重复 10 次,检测结果见表 5,检测结果为突变阳性且对应体系 Ct 值批内变异系数(CV%)分别为 0.27%、0.68%;重复性企业参考品 R3,连续检测重复 10 次,检测结果见表 6,检测结果为突变阳性且对应体系 Ct 值批内变异系数(CV%)分别为 0.19%、0.65%。
2.5 抗干扰能力
2.5.1 蛋白酶 K 的残留含量对试剂扩增的影响 在扩增样本中加入等体积的不同浓度的蛋白酶 K,使反应体系中终浓度为 0%、0.0075%、0.075%、0.75%、7.5%,检测结果如表 7,终浓度高于 0.0075% 蛋白酶 K 残留会影响试剂扩增。
2.5.2 甲醛的残留含量对试剂扩增的影响 在扩增样本中加入等体积的不同浓度的甲醛,使反应体系中终浓度为0%、0.0075%、0.075%、0.75%、7.5%,检测结果如表 8,终浓度高于 0.075% 的甲醛残留会影响试剂扩增。
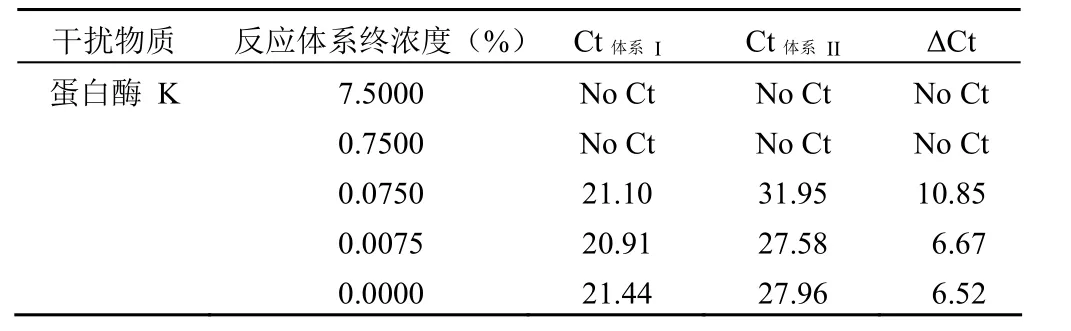
表 7 蛋白酶 K 的残留量对扩增的影响
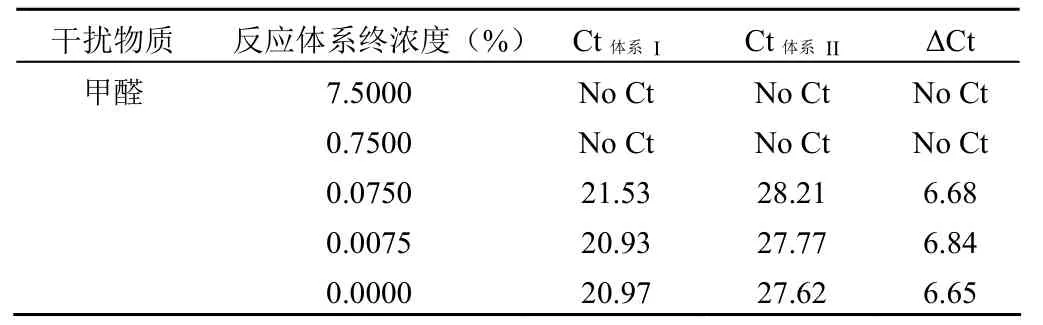
表 8 甲醛的残留量对扩增的影响
2.5.3 乙醇的残留含量对试剂扩增的影响 在扩增样本中加入等体积的不同浓度的乙醇,使反应体系中终浓度为0%、0.0075%、0.075%、0.75%、7.5%,检测结果如表 9,终浓度高于 0.75% 的乙醇残留会影响试剂扩增。
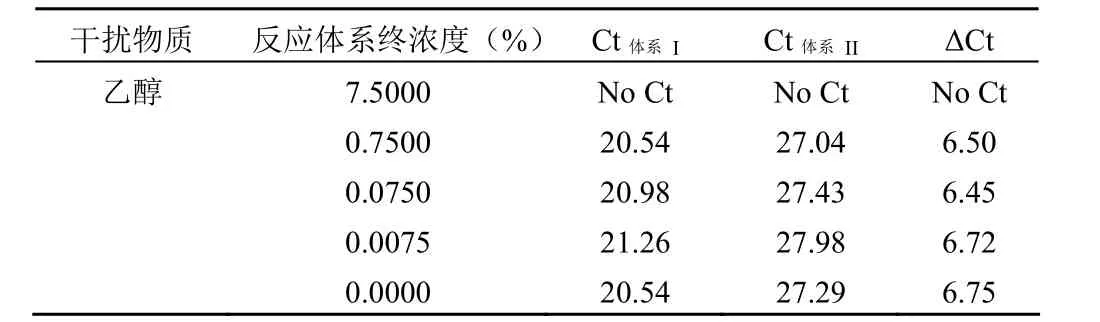
表 9 乙醇的残留量对扩增的影响
2.6 临床比对
使用 156 例临床石蜡包埋组织样本比较 A 公司人类BRAF 基因突变检测试剂盒(荧光 PCR 法)和比对试剂盒进行符合性分析,计算阳性符合率、阴性符合率、总符合率及 Kappa 系数,检测结果如表 10。
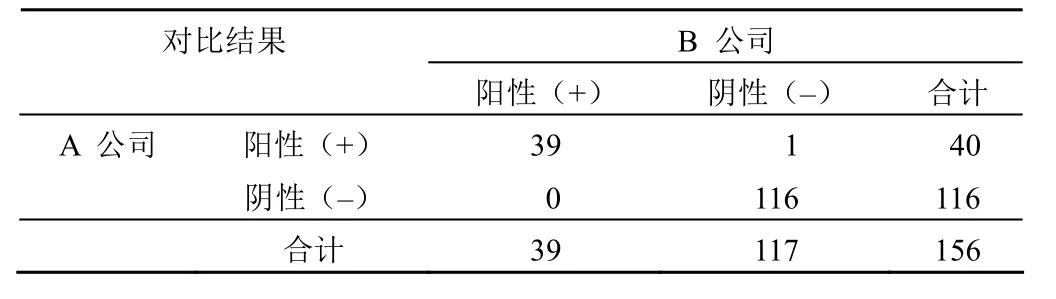
表 10 同类产品比较结果
对两种方法的检测结果进行符合性分析,阳性符合率为100.00%,阴性符合率为 99.15%,总符合率为 99.37%,Kappa 系数为 0.98。表明两种方法具有高度一致性。
3 讨论
本产品以实时荧光定量 PCR 技术和引物特异性 PCR(ARMS)技术为平台,特异性检测 DNA 样本中的 BRAF基因 V600E 突变。其中,试剂 1 中的特异性引物能够在Taq 酶作用下靶向扩增 BRAF 基因野生型和突变型模板;试剂 2 中的特异性引物在 Taq 酶作用下只扩增突变型模板。通过两者 Ct 差值实现 BRAF 基因 V600E 突变的定性检测。
ARMS-PCR 是目前实验室常用的基因突变检测方法,主要优点为检测灵敏度高,可检测肿瘤细胞中突变比例为1% 甚至更低的突变基因[8]。
通过对 A 公司人类 BRAF 基因突变检测试剂盒(荧光 PCR 法)的性能进行评价可知,该产品具有重复性好,灵敏度高和特异性强等特点,满足行业标准和市场需求。
