一测多评法测定山楂叶提取物中4种成分的含量*
2018-07-24徐宝欣杜义龙潘海峰赵胜男
徐宝欣,杜义龙,潘海峰,赵胜男
(承德医学院中药研究所/河北省中药研究与开发重点实验室, 河北承德 067000)
山楂叶提取物是蔷薇科植物山里红Crataegus pinnatifida Bge.var.major N.E.Br.或山楂 Crataegus pinnatifida Bge.的干燥叶经加工制成的提取物,其成方制剂为益心酮片。本课题组多年来采用高效液相色谱法等不同的分析手段,通过测定不同采收期、不同产地的山楂叶及制剂中多种成分和总黄酮成分含量,在建立指纹图谱的基础上评价了山楂叶及其制剂的质量[1-6]。本课题组在研究过程中一直利用外标曲线法(ESM)测定其中目标成分的含量,但外标法所用的对照品价格昂贵,甚至有些对照品性质不稳定,因此增加了含量测定的成本和难度,限制了多成分质量控制模式在企业生产、科研和监督中的应用。一测多评法(QAMS)可在缺少对照品或对照品不稳定的情况下对中药及其制剂进行快速、低廉的质量控制。为此,本研究采用一测多评法测定山楂叶提取物中4种成分的含量,以期建立适用性更强的含量测定方法,完善山楂叶提取物的质量标准。
1 仪器与试药
1200 Series高效液相色谱仪(美国Agilentg公司),配套Chemstation色谱工作站;AG-245型十万分之一电子分析天平(瑞士梅特勒)。
10批山楂叶提取物(山东临沂爱康药业有限公司,批号:AKH15-1~AKH15-10);牡荆素鼠李糖苷(批号:16060103)、牡荆素葡萄糖苷(批号:16072806)、金丝桃苷(批号:16081504)、牡荆素(批号:16070601),均购买于成都普飞德生物技术有限公司。四氢呋喃、甲醇、乙腈为色谱纯(购买于美国Fisher公司);纯净水(购买于娃哈哈集团有限公司);其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件 色谱柱:ZORBAX SB-C18(250×4.6 mm,5μm);流动相为0.6%乙酸水-乙腈-四氢呋喃系统,梯度洗脱:0~10min,7~15%乙腈,10~25min,15%乙腈,四氢呋喃25min内所占比例一直为2%;检测波长350nm;体积流量1ml/min;柱温30℃;进样量0.01μl。
2.2 混合对照品溶液的制备 分别精密称量牡荆素鼠李糖苷、牡荆素葡萄糖苷、金丝桃苷、牡荆素对照品适量,用流动相溶解,制成每1ml含牡荆素鼠李糖苷1.046mg、牡荆素葡萄糖苷0.756mg、金丝桃苷0.219mg、牡荆素0.211mg的混合溶液,作为储备液。
2.3 供试品溶液的制备 精密称取样品0.025g,置具磨口塞10ml量瓶中,加60%无水乙醇溶解并稀释到刻度,进样前以微孔滤膜(0.45μm有机膜)滤过,取续滤液即得。
2.4 线性关系考察 量取2.2中混合对照品储备液适量,按倍数稀释法制成一系列对照品溶液。按2.1的色谱条件进行测定,记录4种成分的峰面积。以待测成分进样量质量(μg)为横坐标、峰面积(Y)为纵坐标进行线性回归,分别得到4种成分的回归方程和线性范围。见表1:

表1 4种成分的回归方程与线性范围
2.5 精密度试验 取倍数稀释后的混合对照品溶液(2.2),按同一色谱条件(2.1)连续进样测定6次,分别记录4个成分的峰面积。结果牡荆素鼠李糖苷、牡荆素葡萄糖苷、金丝桃苷、牡荆素峰面积的RSD值分别为1.33%、0.94%、0.80%、0.72%(n=6),表明仪器精密度良好。
2.6 稳定性试验 取2.3中的供试品溶液,测定样品室温下放置0、2、4、8、12、24h的峰面积,4种成分24h内峰面积的RSD值分别为1.02%、1.52%、1.31%、0.84%(n=6),表明供试品溶液在24h内基本稳定。
2.7 重复性试验 取同一批样品适量,按2.3的方法制备6份溶液,按2.1的色谱条件进行测定,4个成分峰面积的RSD值分别为0.62%、0.84%、1.58%、1.08%,结果表明本方法重复性良好。
2.8 加样回收率试验 取同一批样品适量,分别加入一定量的4种成分对照品,按2.3的方法制备6份溶液,以2.1的色谱条件进行测定,计算加样回收率及RSD值。结果4种成分的回收率依次为100.82%、99.62%、102.88%、99.40%,RSD值分别为0.54%、1.22%、1.47%、2.16%,结果符合2015版《中国药典》的要求[7]。
2.9 相对校正因子(RCF)的计算 本研究以牡荆素葡萄糖苷为内标物,按一测多评法公式[8]计算,结合系列混合对照品溶液所测得的峰面积,计算牡荆素葡萄糖苷对另外3种成分的RCF值。结果,牡荆素鼠李糖苷、金丝桃苷、牡荆素的RCF值分别为0.963、1.116、1.034。
2.10 RCF耐用性的考察 本研究考察了不同仪器(Agilent1200、Agilent1220、Agilent1260)和不同色谱柱[色谱柱型号均为(5μm,250×4.6mm)]对RCF的影响,结果见表2:RCF在本研究考察的仪器与色谱柱中耐用性较好(RSD<3%)。
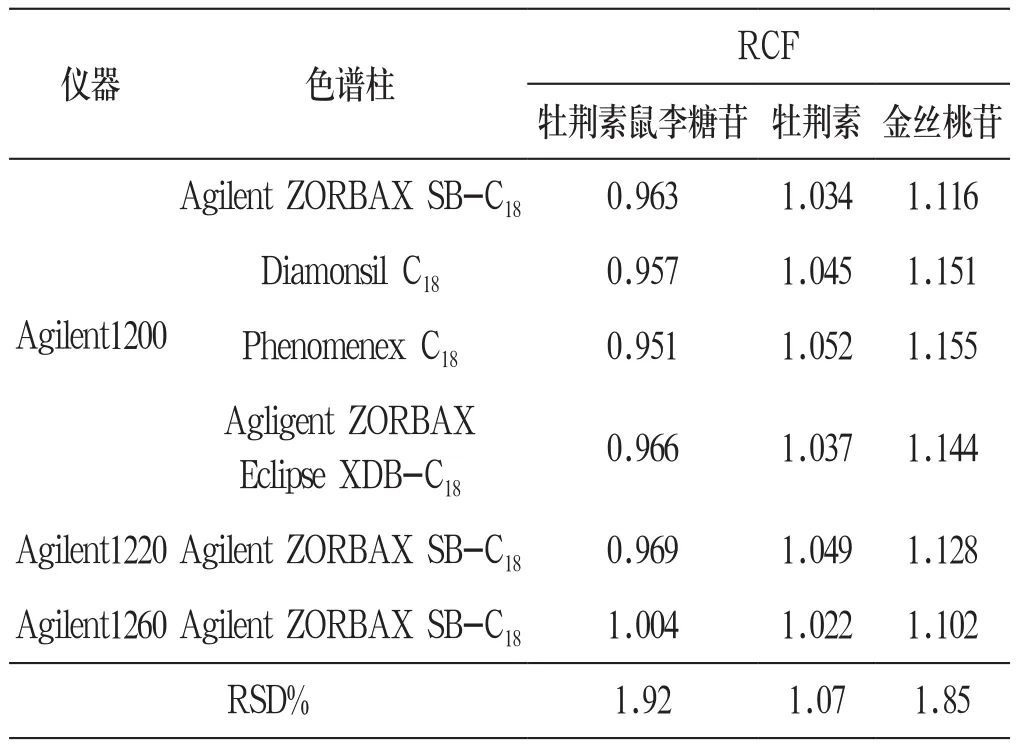
表2 不同仪器和色谱柱测得的RCF
2.11 样品含量的测定 分别取10批山楂叶提取物适量,按照2.3的方法制备供试品溶液,按照2.1的色谱条件进样测定,对比了经典外标曲线法与一测多评法测得的4种成分的含量,见表3:一测多评法(QAMS)与外标曲线法(ESM)测定结果比较,牡荆素鼠李糖苷、金丝桃苷、牡荆素的含量无明显差异。

表3 样品中4种成分的含量测定结果(mg/g)
3 讨论
山楂叶提取物目前收载于2015版药典,仅以金丝桃苷单一成分作为质量标准,存在一定的局限性。本研究对山楂叶提取物中4种成分建立了一测多评法,在方法建立的过程中发现,影响此方法的因素有很多,包括仪器、色谱柱、实验环境等。本研究为保证方法的适用性和重现性,对不同型号、不同产家仪器和不同品牌的色谱柱进行了考察,结果显示山楂叶提取物中选用牡荆素葡萄糖苷为内标物时,牡荆素鼠李糖苷、金丝桃苷和牡荆素的相对校正因子具有很好的重现性。另外,内参物的选择、待测成分浓度、色谱条件等也是一测多评法是否成功建立的主要内部因素。
本研究以牡荆素葡萄糖苷为内标物,外标曲线法与一测多评法测定牡荆素鼠李糖苷、金丝桃苷、牡荆素3种成分的含量无明显差异,且易得、稳定、检测成本低,综合考虑故选择牡荆素葡萄糖苷为内标物。
因此,本研究建立的一测多评法稳定性、重复性、精密度好,可用于山楂叶提取物中牡荆素鼠李糖苷、牡荆素葡萄糖苷、金丝桃苷和牡荆素含量的同时测定。
