共培养杜英叶片内生菌次级代谢产物研究
2018-05-22吕朦朦谭明慧路莉文包尚松郭志勇邓张双
吕朦朦 谭明慧 路莉文 包尚松 郭志勇 邓张双 邹 坤
(1. 三峡大学 天然产物研究与利用湖北省重点实验室,湖北 宜昌 443002; 2. 三峡大学 生物与制药学院,湖北 宜昌 443002)
植物内生菌是指其生活史或者部分生活史寄生于植物体内不引起植物病害症状的一大类微生物的总称[1].有证据表明从植物在地球上出现时,微生物就已经寄生于其中[2],经过约25亿年的进化,植物与微生物之间早已形成稳定的互惠共生关系,有的甚至进化出特有专一性寄生[3].近年来,植物内生真菌活性次级代谢产物的研究成为天然药物化学的研究热点,大量具有各种生物活性同时拥有新颖结构的活性次级代谢产物被报道[4].在植物内生真菌活性次级代谢产物研究中,经典方法是在实验室条件下单一菌株的纯培养,即把植物组织中的能分离纯化的内生真菌一一分离纯化,然后筛选合适的培养基进行纯培养来寻找新的活性次级代谢产物.在这些研究中存在如下问题,首先,只有少数内生真菌能在普通培养基中生长,而大部分内生菌无法纯化得到单一菌株;其次,纯培养不能反映植物内生真菌原始的共存状态,内生菌群在植物受到病害入侵或者环境巨变时,内生菌群会产生特殊的次级代谢产物来应对这些变化,纯培养次级代谢产物不是植物内生菌发挥生态作用的“原始代谢产物”;最后,植物组织和成分还能给其内生菌提供特定营养因子或者固体支撑,在纯培养中没有体现植物的作用.为解决上述存在的问题同时探究内生菌次级代谢产物在植物组织内的生态作用及模拟植物内生菌的生存环境,本文采用植物组织共培养的方法来研究植物内生菌.
杜英(ElaeocarpusdecipiensHemsl.),杜英科,杜英属,俗称杜栗,常绿乔木.原产我国长江流域和南亚热带地区,日本也有分布,多生于海拔400~1 200 m的丘陵山地[5],常用于绿化植物,在其生长周期中病害,虫害非常少.因而推测其内生菌可能在其抵御病虫害的过程中扮演着重要作用,因此采用共培养的方法从杜英叶片内生真菌次级代谢产物中分离得到7个次级代谢产物,运用核磁共振(NMR),质谱(MS)等光谱学方法鉴定,分别为daldinone A(1), alternariol(2), 4-methylalternariol(3), alternuene(4),(E)-3-benzylidene-2-Methylhexahydropyrrolo [1,2-a]pyrazine-1,4-dione(5),(Z)-3-benzylidene-2-methylhexa-hydropyrrolo[1,2-a] pyrazine-1,4-dione(6)及甘油三醋酸酯(7).
2 实验部分
2.1 主要仪器与试剂
Bruker 400 核磁共振波谱仪(瑞士); Dionex U3000二极管阵列检测器DAD分析型高效液相色谱仪(美国)和Waters 1525型双通道紫外检测器半制备型高效液相色谱仪(美国); Thermofisher EI质谱仪(美国);Chirascan qCD圆二色谱仪(英国);X-4数字显示显微熔点仪(温度未校正)(北京泰克仪器有限公司);AL204电子天平(METTLWRTOLEDO);色谱柱Kromasil分析型(250 mm×4.6 mm,5 μm),半制备型Kromasil(250 mm×4.6 mm,10 μm),N21001型旋转蒸发仪(上海爱郎仪器有限公司)等;柱层析和薄层色谱用硅胶均为青岛海洋化工厂产品,其它溶剂均为分析纯,经过常压蒸馏纯化后使用.
2.2 植物内生菌的共培养
植物样品杜英叶片采自三峡大学校园内,杜英叶片在超净台上依次以5%~10% NaClO消毒5 min,75%的乙醇消毒2 min,最后以无菌水洗涤3次,以无菌滤纸吸附叶片表面的无菌水,以无菌的剪刀剪成0.5 cm×0.5 cm大小的组织块,直接置于消毒后的固体培养基上.固体培养基中含140 g大米,70 g的麦麸皮,加入250 mL自来水,置于3 L的三角瓶中,经121℃(0.1 MPa)高温灭菌30 min后使用.在超净工作台上接入表面消毒后的杜英植物组织,共接种10瓶,于室温中静置培养40 d.
2.3 提取与分离
待真菌菌丝长满培养基后,在培养瓶中捣碎固体培养基,以乙酸乙酯浸提,置于超声波下重复提取3次,每次2 h,合并萃取液,经旋转蒸发仪浓缩得浸膏25 g,样品溶于甲醇中,以正己烷脱脂,得脱脂后样品20 g,取其中18 g样品,经200~300目硅胶拌样,正相硅胶柱层析,依次以石油醚-乙酸乙酯[95/5、90/10、85/15、80/20、75/25、70/30、65/35、60/40、55/45、50/50(v/v)]梯度洗脱得到10个组分Fr.1-Fr.10,各组分经薄层层析(TLC)和高效液相色谱(HPLC)分析后,选取其中4个组分(Fr.3-Fr.6)分离纯化.Fr.3经正相硅胶柱层析[石油醚/丙酮=80/20(v/v),洗脱],液相半制备柱[水/乙腈=35/65(v/v),2 ml/min]分离得到化合物1(tR=22.7 min, 46 mg),Fr.4经正相硅胶柱层析[石油醚/丙酮=90/10(v/v),洗脱],Sephadex LH-20层析[二氯甲烷/甲醇=50/50(v/v),洗脱],得到化合物2(87 mg)和化合物3(45 mg); Fr.5经正相硅胶柱层析[石油醚/乙酸乙酯=85/15(v/v),洗脱],液相半制备柱[水/乙腈=25/75(v/v),2 ml/min]得到化合物4(tR=17.4 min,10 mg),化合物5(tR=22.5 min, 8 mg),化合物6(tR=24.1 min, 11 mg);Fr.6经过正相硅胶柱层析[石油醚/乙酸乙酯=75/25(v/v),洗脱],Sephadex LH-20层析[二氯甲烷/甲醇=50/50(v/v),洗脱],得到化合物7(10 mg).化合物1-7的结构如图1所示.
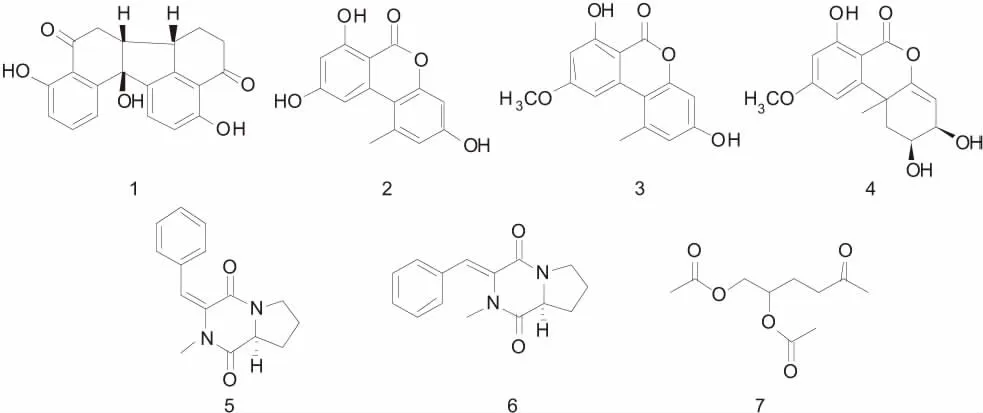
图1 化合物1-7的结构
3 结果与讨论
化合物1,无色油状物,EI-MS得分子离子峰(m/z)366,其一维氢谱在δ 6.8-7.77之间显示5个芳香质子,分别位于δ 6.80(d, 9.1, 1H), 6.83(d, 9.1, 1H), 7.10(d, 7.4, 1H), 7.43(t, 8.2, 1H), 7.77(d, 8.5, 1H), 根据耦合常数推断化合物1中存在1个1, 2, 3-三取代的苯环和1个1, 2, 3, 4-四取代苯环;在低场有2组尖锐的质子信号分别位于δ 10.87和12.28,显然是α,β不饱和酮羰基与其γ-位的酚羟基形成分子内氢键的活泼氢信号;剩余的氢信号分布于δ 1.74-3.23之间.一维碳谱显示20个碳信号包括2个酮羰基信号,分别位于δ 203.1 和202.8处,位于δ 113.9-161.4的12个碳信号显然是2个苯环上芳香碳信号,1个连氧季碳位于δ 79.7处,剩余的碳信号分别位于δ 55.6, 41.4, 37.8, 35.6, 28.1处,通过DEPT判断δ 55.6, 41.4,为次甲基,而δ37.8, 35.6, 28.1为3个亚甲基.通过查阅文献发现化合物1与daldinone A的波谱数据一致[6],因而化合物1的结构确定为daldinone A(如图1所示).
化合物1的波谱数据:13NMR(100 MHz, CDCl3): δ 203.1(C), 202.8(C), 161.4(C), 160.6(C), 148.7(C), 143.3(C), 137.4(CH), 136.9(C), 131.1(CH), 119.7(CH), 117.3(CH), 116.6(CH), 115.2(C), 113.9(C), 79.7(C), 55.6(CH), 41.4(CH), 37.8(CH2), 35.6(CH2), 28.1(CH2);1H NMR(400 MHz, CDCl3): δ 12.28(s, 1H), 10.87(s, 1H), 7.77(d, 8.5, 1H), 7.43(t, 8.12, 1H), 7.10(d, 7.4, 1H), 6.83(d, 9.1, 1H), 6.80(d, 9.1, 1H), 3.23(dd, 5.85, 17.6, H), 2.86(dd, 1.8, 17.6, 2H), 2.74(td, 4.6, 11.2, 1H), 2.63(m, 1H), 2 .57(m, 1H), 2.51(dd, 4.6, 13.2, 1H), 2.37(m, 1H), 1.74(dddd, 3.96, 13.2, 1H).
化合物2,淡黄色无定型固体,mp. 345~347 ℃,EI-MS得分子离子峰(m/z) 258.其一维氢谱很简单,仅有四组苯环上处于间位的芳香氢信号δ 7.21(d, 1.2, 1H), 6.70(d, 2.4, 1H), 6.62(d, 2.4, 1H), 6.34(d, 1.2, 1H),而剩余的氢信号位于δ 11.8(br s, 1H) 和2.68(s, 3H) 处, 通过查阅文献发现化合物2与alternariol的波谱数据一致[7],因而确定化合物2为alternariol.化合物2的NMR数据:13C NMR(100 MHz, DMSO-d6): δ 166.0(C), 164.8(C), 164.0(C), 158.4(C), 152.6(C), 138.3(CH), 138.0(C), 117.5(CH), 109.0(C), 104.5(CH), 101.6(CH), 100.9(C), 97.1(C), 25.2(CH3);1H NMR(400 MHz, DMSO-d6): δ 11.8(br s, 1H), 7.21(d, 1.2, 1H), 6.70(d, 2.4, 1H), 6.62(d, 2.4, 1H), 6.34(d, 1.2, 1H), 2.68(s, 3H).
化合物3,淡黄色无定型固体,mp. 297~299℃,EI-MS得分子离子峰(m/z) 272.化合物3与化合物2的波谱数据非常类似,在一维氢谱上仅仅是多1个甲氧基信号δ 3.89(s, 3H), 通过与文献对比发现化合物3与4-methylalternariol的波谱数据一致[8],因而确定化合物3为4-methylalternariol.化合物3的波谱数据:13C NMR(100 MHz, DMSO-d6): δ 166.2(C), 164.7(C), 164.2(C), 158.6(C), 152.7(C), 138.5(CH), 137.8(C), 117.6(CH), 108.8(C), 103.4(C), 101.7(CH), 99.2(C), 98.5(C),55.9(CH3), 25.1(CH3);1H NMR(400 MHz, DMSO-d6): δ 11.8(br s, 1H), 7.18(d, 1.6, 1H), 6.70(d, 2.4, 1H), 6.62(d, 2.4, 1H), 6.34(d, 1.6, 1H), 3.89(s, 3H), 2.71(s, 3H).
化合物 4,无色油状物,EI-MS得分子离子峰(m/z) 292,其一维氢谱显示3组烯氢信号,位于δ 6.51(d, 1.6, 1H), 6.43(d, 1.6, 1H), 6.12(s, 1H), 还有2组连氧碳上的氢信号δ 4.17(d, 6.4, 1H), 3.85(s, 1H), 其余的氢信号处于δ 2.57(dd, 3.6, 14.8, 1H), 1.86(dd, 3.6, 14.8, 1H), 1.32(s, 1H), 1.28(m, 1H) 处.通过查阅文献发现化合物4与alternuene 一致[9]. 化合物4的波谱数据:13NMR(100 MHz, CDCl3): δ 168.9(C), 166.2(C), 164.1(C), 138.9(C), 133.8(CH), 130.0(CH), 103.0(CH), 100.7(CH), 100.6(C), 81.1(C), 72.9(CH), 70.2(CH), 55.7(CH3), 40.7(CH2), 28.0(CH3);1H NMR(400 MHz, CDCl3): δ 11.2(br s, 1H), 6.51(d, 1.6, 1H), 6.43(d, 1.6, 1H), 6.12(s, 1H), 4.17(d, 6.4, 1H), 3.85(s, 1H), 2.57(dd, 3.6, 14.8, 1H), 1.86(dd, 3.6, 14.8, 1H), 1.32(s, 1H), 1.28(m, 1H).
化合物5,为无色油状物,EI-MS得分子离子峰(m/z) 256,其一维氢谱和碳谱较为简单,在其一维氢谱中,显示3组芳香氢信号分别位于δ 7.36(m, 2H),7.31(m, 3H),7.15(s, 1H),其中位于δ 7.36(m, 2H),7.31(m, 3H)的氢信号显然是单取代苯环的特征,表明化合物5中可能存在1个单取代苯环;其余的氢信号均处于高场区,其中位于δ 2.88(s, 3H)的单峰甲基信号,可能为氮原子上的甲基信号;其一维碳谱显示化合物5中仅有13个碳信号,其中δ 167.9,161.4的碳信号可能为羰基碳信号,综合分析化合物5的一维谱推断该化合物可能为环肽类化合物,通过查阅文献发现化合物5与(E)-3-benzylidene-2-methylhexahydropyrrolo [1,2-a]pyrazine-1,4-dione 的波谱数据一致[10],因而化合物5确定为(E)-3-benzylidene-2-methylhexahydropyrrolo[1,2-a] pyrazine-1,4-dione.
化合物5的波谱数据:13NMR(100 MHz, CD3COCD3-d6): δ 168.7(C), 161.3(C), 135.7(C), 135.3(C), 130.5(CH), 129.3(CH) , 129.1(CH), 119.7(CH), 59.3(CH), 45.8(CH2), 34.8(CH3), 28.8(CH2), 23.4(CH2);1H NMR(400 MHz, CD3COCD3-d6): δ 7.36(m, 2H), 7.31(m, 3H), 7.15(s, 1H), 4.25(dd, 2.4, 15.6, 1H), 3.66(m, 2H), 2.88(s, 3H), 2.41(m, 1H), 2.21(m, 1H), 2.08(m, 1H), 1.96(m, 1H).
化合物6,为无色油状物,EI-MS得分子离子峰(m/z) 256,其一维氢谱和碳谱与化合物5的氢谱和碳谱几乎完全一样,但是在HPLC上显示是明显的2个峰,仔细分析化合物5的NMR图谱和结构,化合物5能够变化的位置只有双键构型顺反的变化,因而推测化合物6的双键为顺式构型即与化合物5的双键构型相反.为了证实这种推断,进一步分析化合物5和6的NOESY谱,发现化合物6的单峰芳香氢与甲基的相关信号峰消失了,NOESY实验都是在相同的条件下进行,因而我们推测化合物6为化合物5的顺式异构体.化合物6为首次从自然界中分离得到.
化合物6的波谱数据:13NMR(100 MHz, CD3COCD3-d6): δ 167.9(C), 161.4(C), 135.1(C), 134.7(C), 129.9(CH), 128.8(CH), 128.5(CH), 119.2(CH), 58.8(CH), 45.2(CH2), 34.2(CH3), 28.0(CH2), 22.8(CH2);1H NMR(400 MHz, CD3COCD3-d6): δ 7.36(m, 2H), 7.31(m, 3H), 7.15(s, 1H), 4.25(dd, 2.4, 15.6, 1H), 3.66(m, 2H), 2.88(s, 3H), 2.41(m, 1H), 2.21(m, 1H), 2.08(m, 1H), 1.96(m, 1H).
化合物7,为无色油状物,其一维氢谱和碳谱非常简单.在其一维氢谱中,仅仅只有5组峰,分别位于δ 5.25, 4.29, 4.15, 2.09, 2.08处,其碳谱更简单,分别位于δ 170.5, 170.1, 69.1, 62.3, 20.9和20.8处,在一维碳谱中δ 170.5的碳信号比 170.1的碳信号,δ 62.3的碳信号比69.1的碳信号, δ 20.7的碳信号比20.9的碳信号明显高很多,因而推断δ 170.5,62.3,20.7的碳信号代表的是2个碳信号.结合上述的一维碳谱和氢谱的分析结合查阅文献发现,化合物7是三乙酰化的甘油[11].化合物7的波谱数据:13NMR(100 MHz,CD3OD-d4): δ 170.5(C), 170.1(C),69.1(CH), 62.3(CH2), 20.9(CH3), 20.7(CH3);1H NMR(400 MHz, CD3OD-d4): δ 5.25(m, 1H), 4.29(dd, 4.4, 12.0, 2H), 4.15(dd, 4.2, 12.0, 2H), 2.09(s, 3H), 2.08(s, 6H).
4 结 论
采用共培养的方法培养杜英叶片内生菌,并通过柱层析,凝胶色谱,半制备液相色谱等技术对其共培养次级代谢产物分离纯化,共获得7个化合物,通过核磁共振,质谱等方法确定其结构,分别为daldinone A (1),alternariol(2), 4-methylalternariol(3), alternuene(4),(E)-3-benzylidene-2-methylhexahydropyrrolo [1,2-a]pyrazine-1,4-dione(5),(Z)-3-benzylidene-2-methylhexahydropyrrolo[1,2-a] pyrazine-1, 4-dione(6), 甘油三醋酸酯(7).化合物1-7是首次从杜英的内生菌中获得,化合物6首次从自然界中分离得到.化合物1是一个以少见的稠合方式形成的一个二聚体类的聚酮化合物,是在自然界中第二次从植物内生菌中分离得到,据文献报道化合物1对真菌有一定的抑制作用[12],而化合物2 -4为链格孢酚类的真菌毒素,该类化合物广泛存在于Fusaium sp.类真菌中,化合物1-4为共培养杜英叶片内生菌的主要代谢产物,量相对其它类化合物较多,可能是植物杜英抵抗其病虫害的“生态武器”,在后期的后续研究中还需要进一步确认上述4种次级代谢产物对杜英的生态保护作用.同时还需要通过与经典方法纯培养比较,并分析两者之间的代谢产物的差别,从而明确杜英与其内生真菌之间的生态依存关系.
目前,对内生菌活性次级代谢产物的研究主要集中在单一菌株纯培养及2-3种菌株之间的共培养,而多菌株的共培养发酵技术更多应用于传统食品的制作,如醋,黄酒酿造等[13],但是多菌株之间相互作用关系及对相关产品质量的影响正成为新的研究热点.本文采用共培养植物组织内生菌的技术诱导内生菌产生结构新颖活性次级代谢产物,对挖掘提高内生菌产生次级代谢产物的潜力具有探索意义.
参考文献:
[1] Petrini O. Fungal Endophytes of Tree Leaves[M]. Microbial Ecology of Leaves. Springer New York, 1991:179-197.
[2] Redecker D, Kodner R, Graham L E. Glomalean Fungi from the Ordovician[J].Science,2000, 289: 1920-1921.
[3] Zuccaro A, Lahrmann U, Guldener U, et al. Endophytic Life Strategies Decoded by Genome and Transcriptome Analyses of the Mutualistic Root Symbiont Piriformospora Indica [J].PLoS Pathog, 2011, 7(10): e1002290.
[4] Zhao H. Advances in Endophytic Fungi From Medicinal Plant[J].Northern Horticulture, 2017, 13: 170-175.
[5] 鲍 锋.杜英生物学特性及园林环保应用价值的研究[J].湖南林业科技, 2010, 37(2):74-75.
[6] Koch K, Podlech J, Pfeiffer E, et al. Total Synthesis of Alternariol[J].J. Org. Chem., 2005, 70(8):3275-3276.
[7] Quang D N, Hashimoto T, Tanaka M, et al. Chemical Constituents of the Ascomy-cete Daldinia Concentrica[J].Journal of Natural Products, 2002, 65(12):1869-1874.
[8] Tan N, Tao Y, Pan J, et al. Isolation, Structure Elucidation and Mutagenicity of Four Alternariol Derivatives Produced by the Mangrove Endophytic Fungus No. 2240[J].Chem. Nat. Compd., 2008, 44(3):296-300.
[9] Altemöller M, Podlech J, Fenske D. Total Synthesis of Altenuene and Isoaltenuene[J].European Journal of Organic Chemistry, 2006, 7(4):1678-1684.
[10] Jin S, Liebscher J. Optically Active Precursors for Quaternary Amino Acids by Addition of N-Heteroaromatics to 3-Alkylidene-2,5-diketopiperazines[J].Synlett., 1999(4): 459-461.
[11] Tagawa Y, Hiramatsu N, Kato H, et al. Induction of CCAAT/enhancer-binding Protein-homologous Protein by Cigarette Smoke Through the Superoxide Anion-triggered PERK-eIF2α Pathway[J].Toxicology, 2011, 287(1-3): 105-112.
[12] Wang G, Fan J, Zhang W, et al. Polyketides from Mantis-Associated Fungus Daldinia Eschscholzii IFB-TL01[J].Chemistry & Biodiversity, 2015, 12(9): 1349.
[13] 任 聪,杜 海,徐 岩.中国传统发酵食品微生物组研究进展[J].微生物学报, 2017, 57(6): 885-898.
