单胺类囊泡转运体2抑制剂治疗迟发性运动障碍研究进展☆
2018-05-16翁加俊于文娟李华芳
翁加俊 于文娟 李华芳
迟发性运动障碍(tardive dyskesia,TD)是一种长期服用抗精神病药物所引起的严重药物副反应,其主要临床症状以口-舌-咽三联征以及躯干肌张力增高和躯体的舞蹈样动作为主。虽然很多研究显示第二代抗精神病药物的使用可以显著降低TD的发病风险,但是美国的CATIE研究的结局不支持此结论[1]。TD临床发病率依然较高,显著影响精神分裂症患者的预后与转归。2017年美国FDA批准了首个适应证为TD的新药戊苯那嗪(valbenazine)。该药是一种单胺类囊泡转运体2(vesicular monoamine transporter 2,VMAT2)抑制剂,此类药物在以TD为代表的锥体外系反应和以亨廷顿病(Huntington's disease,HD)兴奋性运动障碍的治疗中有着良好的前景[2]。本文针对VMAT2抑制剂治疗TD的作用机制与临床研究进展综述如下。
1 TD的发病机制与治疗现状
TD的发病机制复杂,至今确切病因依然未明。其中较为成熟的学说有D2受体超敏、5-羟色胺(5-HT)遗传多态性、γ-氨基丁酸(GABA)能缺乏、氧化自由基超载、神经可塑性受损等[3]。其中以D2受体的超敏学说最为经典。D2受体超敏学说认为TD的发病与抗精神病药物长期阻滞突触后膜D2受体而引起的D2受体数目和敏感性增加有关。D2受体可抑制中枢神经系统运动调控通路的间接通路从而抑制过度的运动,而D2受体的超敏可导致TD的发生[4]。
在VMAT2抑制剂被FDA批准之前,TD一直面临着无药物治疗的窘境。当患者出现TD症状时,被推荐的疗法包括缓慢换用EPS发病率低的非典型抗精神病药物(氯氮平、喹硫平)、合用维他命 B6(vitamin B6)、合用 GABA 能抑制剂(氯硝西泮)、合用银杏叶提取物(ginkgo biloba)等[5]。但是这些疗法均无充足临床研究证据的支持,疗效与安全性不明确。
2 VMAT2抑制剂治疗TD的机制
单胺类囊泡转运体2(VMAT2)是一种广泛分布于突触前膜的囊泡神经递质转运蛋白。其通过ATP耗能和离子通道建立起来的氢离子浓度差将突触前膜的胞浆内的单胺类物质如多巴胺(DA)、去甲肾上腺素(NE)、5-HT、组胺等转运入囊泡内,囊泡中的神经递质可进一步分泌至突触间隙发挥作用[6]。这表明VMAT2对于突触前神经元单胺类神经递质的释放有显著调控作用。见图1。
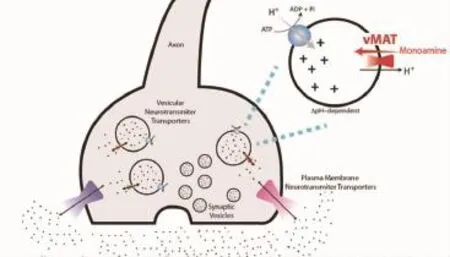
图1 VMAT2抑制剂对于TD的作用机制。V型ATP受体使用ATP供能增加突触囊泡内H+浓度再通过VMAT受体协助将胞浆内的单胺类物质转运入囊泡内[7]
VMAT2抑制剂可能通过抑制突触前神经元DA的释放,避免DA对超敏D2受体刺激的同时也不阻滞突触后膜的D2受体,从而减轻TD的症状[7]。因其对突触前膜DA分泌的抑制作用VMAT2抑制剂也被称为DA能耗竭剂。
有关VMAT2抑制剂治疗TD的相关动物研究依然缺乏,这可能与TD的可靠动物模型缺失有关。TD的主要动物模型为长期注射氟哌啶醇后所引起的无意义咀嚼运动模型(vacuous chewing movements,VCM)。但是小鼠的无意义咀嚼运动症状也可以出现于注射抗精神病药物的早期,而且这种症状可以在停止注射抗精神病药物后2周内自行缓解,这与人类TD的临床特点不符[8]。哺乳类的动物模型(卷尾猴、猕猴等)与人类TD的疾病特征相似,但是其价钱昂贵、造模时间较长与造模成功率低的特点限制了哺乳类动物模型的应用价值[8]。VMAT2抑制剂治疗TD机制的探索依然需要可靠动物模型研究的支持。
3 VMAT2抑制剂治疗TD的临床研究
3.1 戊苯那嗪戊苯那嗪是首个被FDA批准用于治疗TD的药物,对于TD治疗具有划时代的意义。戊苯那嗪的代谢慢,药物血浆峰浓度低,血药浓度峰谷比值低,而与VMAT2的亲和力较高[7,9]。这些药代动力学特点可以显著降低患者体内血药浓度的波动。戊苯那嗪与中枢神经系统内的单胺类受体如DA受体(D1,D2受体)、5-HT受体(5-HT1A,5-HT2A,5-HT2B受体)、NE受体、HT受体无亲和力[10]。上述药理学特点可减少戊苯那嗪药物副反应发生的可能性。戊苯那嗪的药物浓度达峰时间短(4~10 h)而药物半衰期长(15~22 h),所以戊苯那嗪只需每天服用一次就可以保持有效的血药浓度[11]。
戊苯那嗪治疗TD的三期临床试验 (随机双盲对照试验)共纳入225例TD患者,共205例(87.6%)完成了6周的临床试验观察[12]。TD患者以1:1:1的比例平均被分入80 mg组、40 mg组、安慰剂组,测试不同药物剂量下戊苯那嗪对于TD的疗效与耐受性。研究的主要临床结局指标为基线至终点AIMS量表运动功能评分(量表前七项总分)变化。结果显示戊苯那嗪80 mg组降分显著高于对照组,40 mg组降分也高于对照组。在第8周时,TD症状的应答率 (AIMS量表运动功能评分降分率≥50%)80 mg组与40 mg组显著高于对照组,两组差异均有统计学意义。副反应事件而导致的停药、减药、试验终止事件各治疗组无差异,试验过程中发生的严重不良事件包括1例自杀和1例因心血管问题死亡事件也与药物作用无关。一项对于戊苯那嗪治疗TD的系列临床研究KINCET试验的结果的汇总分析认为长期服用戊苯那嗪 (≥48周)总体耐受性较好,发生的副反应大多仅为轻至中度如嗜睡、头痛、尿路感染、背痛等,且长期服用戊苯那嗪也不会影响患者的精神症状[13]。但是另一项针对KINCET系列临床研究的荟萃分析发现患者服用戊苯那嗪后嗜睡的发生率明显高于对照组(10.9%vs.4.2%),高剂量的戊苯那嗪还有潜在增加QTc间期的趋势,而这些副反应均未在FDA的药物说明书中被黑框警告[14]。综上所述,戊苯那嗪对TD的疗效有高质量临床研究支持,意义重大,但是其安全性与耐受性仍需要更大样本量真实世界研究的验证。
3.2 丁苯那嗪丁苯那嗪(tetrabenazine,TBZ)是最早被使用于临床的VMAT2抑制剂,其在临床上被FDA批准运用于治疗多巴胺功能亢进引起的兴奋性运动功能障碍如亨廷顿病、Tourette综合征等。虽然未被FDA批准用于治疗TD,但是丁苯那嗪也被相关指南推荐用于TD的超说明书治疗用药并在一些国家如德国、加拿大得到了批准[5]。丁苯那嗪可高度选择性作用于中枢神经系统VMAT2而不作用于另一种单胺类囊泡转运体VMAT1,其在消耗中枢神经系统内的单胺类神经递质的同时可不引起外周自主神经副反应如体位性低血压和胃肠功能紊乱等[15]。由于丁苯那嗪活性代谢产物DH-TBZ的半衰期短而代谢较快,为了保持其治疗效应的血药浓度,需要每天三次服药,而这容易加重血药浓度的波动性而造成药物副作用[16]。由于活性代谢产物半衰期短和人群中CYP2D6多态性的可能性,当丁苯那嗪用量超过50 mg/d时,患者需进行CYP2D6药物代谢基因组学的检测以防体内药物浓度过高引起的副反应[17]。
在一项单盲、录像随机化评分的临床研究中,丁苯那嗪组AIMS量表的运动功能评分较基线期缓解了54.2%,而AIMS症状总体症状评分(8-10项总分)下降了60.2%,差异均有统计学意义。仅有少量轻至中度的不良事件如嗜睡、帕金森综合征被发现[18]。但是这项研究样本量(20例)小,未做到双盲,无对照组,这大大降低了丁苯那嗪对于TD疗效的说服力。丁苯那嗪引起的副反应如嗜睡、抑郁、静坐不能、帕金森综合征也均有被报道[19-20]。丁苯那嗪可引起EPS症状的机制可能与其对于突触后D2受体的阻滞作用有关[10]。综上所述,丁苯那嗪的代谢快、血药浓度波动大、耐受性不佳的问题大大限制了其在TD治疗上的临床应用。
3.3 氘化丁苯那嗪氘化丁苯那嗪(Deut-TBZ)的化学结构和药效动力学与丁苯那嗪(TBZ)类似,但是丁苯那嗪结构中的一个氢原子被更加稳定的同位素氘原子替代。氘原子的替代显著增加了其稳定性,解决了丁苯那嗪代谢快且需要一天内多次服药的问题。氘化丁苯那嗪的有效药物浓度暴露量增高,血浆药物峰浓度较丁苯那嗪明显降低,药物副反应也随之减少[21]。
一项样本量为117的随机,双盲,多中心的临床试验中,TD患者被随机分为氘化丁苯那嗪组和对照组,氘化丁苯那嗪组在基线期服用剂量12 mg/d(一天服用两次),之后每周增加6 mg/d的药物剂量,直至达到治疗效果或出现副反应或达到药物设定的最大剂量(48 mg/d)为止[22]。在终点12周时,治疗组的AIMS的运动功能评分减分值与安慰剂组有显著性差异,与安慰剂组相比氘化丁苯那嗪对于TD疗效更为显著。48.3%的氘化丁苯那嗪组和35.6%的安慰机组出现了与治疗相关的不良反应,但是研究中发生的严重不良反应如抑郁、自杀情绪、EPS症状、QTc间期延长严重程度均与安慰剂类似甚至低于安慰剂组。这证明了氘化丁苯那嗪药物耐受性好的特点。现在氘化丁苯那嗪对于TD的临床试验以及进入到了Ⅲ期临床试验阶段[23]。Ⅲ期临床试验阶段在前面所述的临床试验[22]基础上,进一步探究不同剂量的氘化丁苯那嗪 (12 mg/d、24 mg/d、36 mg/d)对于TD的疗效。在12周观测终点时,36 mg组与24 mg组的运动功能评分减分值效应与对照组相比均有统计学差异。停药率、减药率、退出研究事件发生率各剂量组与对照组无统计学差异,实验室检查指标与EPS症状无恶化。此试验证明高剂量(36 mg/d)和中剂量(24 mg/d)的氘化丁苯那嗪对于TD的疗效、耐受性均较好,临床医生可以根据TD的严重程度、耐受性(年龄、躯体状况)、精神症状而增加氘化丁苯那嗪的剂量或合并抗精神病药物治疗[24]。综上所述,氘化丁苯那嗪疗效和耐受性上的优势使其很有可能成为继戊苯那嗪之后最有希望被FDA批准用于治疗TD的第二种药物。

表1 VMAT2抑制剂
4 总结
TD的发病机制复杂,病因机制至今未明。D2受体超敏仍是TD发病最经典最为可信的学说。VMAT2抑制剂是国际上对于TD治疗的首选一线用药。其治疗TD的机制可能是通过对于突触前神经元囊泡上VMAT2的抑制从而减少突触前神经元DA的分泌,调节由于长期D2受体阻滞所引起的D2受体超敏现象,缓解TD的症状。VMAT2抑制剂治疗TD的机制仍需要可靠的动物模型与基础研究结果的支持。
丁苯那嗪是国际上第一个被用于治疗TD的VMAT2受体阻滞剂,但由于其代谢快、需一天多次服用、药物副反应大等特点影响了其临床运用。氘化丁苯那嗪解决了丁苯那嗪多次服药导致的药物耐受性问题,血药浓度更稳定,药物副反应少,对TD的疗效佳,是继戊苯那嗪后最有希望被批准用于治疗TD的VMAT2抑制剂。戊苯那嗪对VMAT2受体亲和力高,半衰期长,药物代谢稳定,已有大量高质量的临床研究的证据证明其对于TD的疗效和安全性,对于TD的治疗有着划时代的意义。但是其安全性与耐受性仍需要更大样本量的真实世界研究的支持。三种VMAT2抑制剂的药理学和临床应用特点总结见表1。鉴于TD症状的长期性、复发性和对于精神分裂症预后的危害,有关VMAT2抑制剂对于TD的长期疗效以及耐受性的临床试验依然迫切被需要。
[1] MILLER DD,CAROFF SN,DAVIS SM,et al.Extrapyramidal side-effects of antipsychotics in a randomised trial[J].Br J Psychiatry,2008,193(4):279-288.
[2] JANKOVIC J.Dopamine depleters in the treatment of hyperkinetic movement disorders[J].Expert Opin Pharmacother,2016,17(18):2461-2470.
[3] CASEY DE.Pathophysiology of antipsychotic drug-induced movement disorders[J].J Clin Psychiatry,2004,65(9):25-28.
[4] VIJAYAKUMAR D,JANKOVIC J.Drug-Induced Dyskinesia,Part 2:Treatment of Tardive Dyskinesia[J].Drugs,2016,76(7):779-787.
[5] ZAI CC,TIWARI AK FAU,MAZZOCO M,et al.Association study of the vesicular monoamine transporter gene SLC18A2 with tardive dyskinesia[J].J Psychiatr Res,2013,47(11):1760-1765.
[6] WALN O,JANKOVIC J.An update on tardive dyskinesia:from phenomenology to treatment[J].Tremor Other Hyperkinet Mov(N Y),2013,3:1-11.
[7]MEYER JM.Forgotten but not gone:new developments in the understanding and treatment of tardive dyskinesia[J].CNS spectrums,2016,21(S1):13-24.
[8] BLANCHET PJ,PARENT MT,ROMPRE PH.Relevance of animal models to human tardive dyskinesia[J].Behav Brain Funct,2012,(8):12.
[9] MULLER T.Valbenazine granted breakthrough drug status for treating tardive dyskinesia[J].Expert Opin Investig Drugs,2015,24(6):737-742.
[10] GRIGORIADIS DE,SMITH E,HOARE SRJ,et al.Pharmacologic Characterization of Valbenazine (NBI-98854)and Its Metabolites[J].J Pharmacol Exp Ther,2017,361(3):454-461.
[11] O'BRIEN CF,JIMENEZ R,HAUSER RA,et al.NBI-98854,a selective monoamine transport inhibitor for the treatment of tardive dyskinesia:A randomized,double-blind,placebo-controlled study[J].Mov Disord,2015,30(12):1681-1687.
[12] HAUSER RA,FACTOR SA,MARDER SR,et al.KINECT 3:A Phase 3 Randomized,Double-Blind,Placebo-Controlled Trial of Valbenazine for Tardive Dyskinesia[J].Am J Psychiatry,2017,174(5):476-484.
[13] JOSIASSEN RC,KANE JM,LIANG GS,et al.Long-Term Safety and Tolerability of Valbenazine(NBI-98854)in Subjects with Tardive Dyskinesia and a Diagnosis of Schizophrenia or Mood Disorder[J].Psychopharmacol Bull,2017,47(3):61-68.
[14] CITROME L.Valbenazine for tardive dyskinesia:A systematic review of the efficacy and safety profile for this newly approved novel medication-What is the number needed to treat,number needed to harm and likelihood to be helped or harmed? [J].Int J Clin Pract,2017,71(7):1-14.
[15] KENNEY C,JANKOVIC J.Tetrabenazine in the treatment of hyperkinetic movement disorders[J].Expert Rev Neurother,2006,6(1):7-17.
[16] Huntington Study Group.Tetrabenazine as antichorea therapy in Huntington disease:a randomized controlled trial[J].Neurology,2006,16(3):366-372.
[17] JANKOVIC J,CLARENCE-SMITH K.Tetrabenazine for the treatment of chorea and other hyperkinetic movement disorders[J].Expert Rev Neurother,2011,11(11):1509-1523.
[18] ONDO WG,HANNA PA FAU-JANKOVIC J,JANKOVIC J.Tetrabenazine treatment for tardive dyskinesia:assessment by randomized videotape protocol[J].Am J Psychiatry,1999,156(8):1279-1281.
[19] CHEN JJ,ONDO WG FAU-DASHTIPOUR K,DASHTIPOUR K,et al.Tetrabenazine for the treatment of hyperkinetic movement disorders:a review of the literature[J].Clin Ther,2012,34(7):1487-1504.
[20] LEWITT PA.Tardive dyskinesia caused by tetrabenazine[J].Clin Neuropharmacol,2013,36(3):92-93
[21] FRANK S,TESTA CM,STAMLER D,et al.Effect of Deutetrabenazine on Chorea Among Patients With Huntington Disease:A Randomized Clinical Trial[J].JAMA,2016,316(1):40-50.
[22] FERNANDEZ HH,FACTOR SA,HAUSER RA,et al.Randomized controlled trial of deutetrabenazine for tardive dyskinesia:The ARM-TD study[J].Neurology,2017,88(21):2003-2010.
[23] ANDERSON KE,STAMLER D,DAVIS MD,et al.Deutetrabenazine for treatment of involuntary movements in patients with tardive dyskinesia (AIM-TD):a double-blind,randomised,placebo-controlled,phase 3 trial[J].Lancet Psychiatry,2017,4(8):595-604.
