认知行为疗法联合右佐匹克隆片治疗ICU转出患者睡眠障碍的疗效观察
2018-05-11张颖苏俊王锦权唐光政胡炜毛洪京任婉文刘义余正和
张颖 苏俊 王锦权 唐光政 胡炜 毛洪京 任婉文 刘义 余正和
近年来随着重症医学的快速发展,重症患者转出ICU的患者逐渐增多,由于疾病本身、ICU环境、有创通气、活动限制等因素影响,患者在转出ICU后常发生一系列心身障碍,如ICU获得性衰弱、认知障碍、创伤后应激障碍等,又称为ICU后综合征,其中以睡眠障碍最为常见[1],这些障碍严重影响ICU转出患者的身体康复和生存质量,导致一系列家庭与社会问题。失眠认知行为疗法(cognitive behavioral therapy for insomnia,CBT-I)通过改变患者对睡眠的错误认知和不良生活行为习惯,以改善其睡眠状况,多项研究结果均证明了CBT-I治疗失眠症的有效性和持久性,被国内外治疗指南作为一线推荐[2]。非苯二氮卓类药物右佐匹克隆是一种可以兴奋GABA能神经元的镇静催眠药,半衰期短,次日残余效应低,一般不产生日间困倦,产生药物依赖的风险较传统苯二氮卓类药物低,治疗失眠安全有效,长期使用无显著不良反应[3]。目前虽然ICU后综合征已经引起学者的普遍关注,但是针对ICU转出患者的睡眠障碍研究较少,笔者通过对ICU转出患者进行问卷调查及临床对照研究,探讨ICU转出患者睡眠障碍发生的易患因素与干预措施,并观察CBT-I联合右佐匹克隆片对ICU转出患者睡眠障碍的临床疗效与安全性。
1 对象和方法
1.1 对象 选择2015年1月至2016年12月杭州市第七人民医院睡眠障碍门诊或住院患者共58例,年龄18~55岁,均右利手;均为曾收住综合医院ICU的危重病患者,ICU住院时间>72h,病情稳定后转入普通病房,出现睡眠障碍并持续超过1个月,均符合精神障碍诊断与统计手册(第5版)(DSM-5)[4]失眠症诊断标准。排除标准:各类精神疾病引起的继发性失眠或共病失眠,正在有规律服用安眠药或抗精神病药,躯体性疾病导致的失眠患者如癫痫病史、脑外伤、脑肿瘤、脑炎、脑血管疾病、脑代谢等疾病史。采用随机数字表法将58例患者分为认知行为疗法联合右佐匹克隆片治疗组(研究组)29例和单纯右佐匹克隆片治疗组(对照组)29例。研究组男 14例,女 15例;年龄(44.6±9.1)岁;BMI(21.3±2.4)kg/m2;对照组男 15 例,女 14 例;年龄(46.1±7.8)岁;BMI(21.4±4.1)kg/m2;两组患者性别、年龄、BMI等方面比较差异均无统计学意义(均P>0.05)。本研究方案经杭州市第七人民医院医学伦理学委员会审核批准,并经所有患者签署书面知情同意书。
1.2 方法
1.2.1 药品与仪器 右佐匹克隆片,规格为每片3mg,成都康弘药业集团股份有限公司生产。Embla N/S7000睡眠监测系统为冰岛Medcare Flaga公司产品。
1.2.2 认知行为疗法 包括睡眠卫生教育、行为治疗(刺激控制、睡眠限制、肌肉放松法、生物反馈等)、认知治疗(认知重建、矛盾意向法等)[5]。
1.2.3 治疗方法 治疗开始右佐匹克隆片均予以3mg/d,2周后减至 2mg/d,4周后减至1mg/d,睡前1h服用,连续服用28d。认知行为治疗共4周,2次/周;采用面对面治疗+电话指导治疗模式,第1次为面对面访谈治疗40~60min;第1、2、3周末患者来医院进行面对面认知行为治疗30min;第1、2、3、4周内各进行1次电话指导治疗,每次15~20min。治疗内容包括睡眠限制、刺激控制疗法、松弛为基础的干预、认知疗法、睡眠卫生保健教育等方面。在第1次面对面访谈治疗时向患者介绍整个CBT-I操作流程与方法,并将CBT-I的具体内容书写打印成文字资料与睡眠日记一起装印成册,交给患者保管并要求其在每周内日常生活中自助实施及记录,每周复诊时带来医院,在第1、2、3、4周内由睡眠障碍科医生与患者电话联系,沟通患者睡眠情况及CBT-I实施中的问题,给予相应指导及支持鼓励。
1.3 观察指标 两组患者入组时根据ICU出院记录与费用清单,记录患者在ICU住院时间以及是否使用镇静、镇痛药物及种类;采用问卷调查方式调查患者在ICU住院期间是否存在疼痛、焦虑、失眠、不安全感、交流困难等不适,是否希望家属陪护,以及对机械通气、各种治疗干预和侵入性操作(如深静脉置管、留置胃管、静脉注射)的记忆程度和痛苦程度。
分别于入组时和治疗4周后对两组患者采用多导睡眠监测(polysomnography,PSG)和匹兹堡睡眠质量指数(pittsburgh sleep quality index,PSQI)量表评估睡眠改善的情况。应用焦虑症状自评量表(self-rating anxiety scale,SAS)、抑郁症状自评量表(self-rating depression scale,SDS)评估情绪水平;不良反应量表(treatment emergent symptom scale,TESS)评估不良反应发生情况。
睡眠监测室需保持安静且室温保持在18~25℃。为避免首夜效应的影响,对患者进行连续2个晚上的睡眠监测,第一晚让患者适应睡眠监测室的环境,第二晚的睡眠监测数据用于研究。如果测试结果显示患者不符合入组标准,或者具有原发性失眠以外的睡眠障碍,则将其排除入组。本研究中,PSG 监测,PSQI、SAS、SDS 评分,TESS评定均由精神科主治以上临床医师评定,且不参与临床治疗过程(对分组单盲)。
1.4 疗效评价
1.4.1 PSG 测量指标包括:(1)睡眠总时间:从入睡开始计时至最后觉醒的时间减去整个睡眠期间出现觉醒的时间;(2)入睡时间:从熄灯开始至Ⅰ期睡眠(S1)出现的时间;(3)觉醒时间:从睡眠开始计时至最后觉醒前的睡眠期间内所有觉醒时间的累计;(4)睡眠效率:睡眠总时间与总记录时间的比值。(5)睡眠结构:包括非快速眼动Ⅰ、Ⅱ、Ⅲ期睡眠和快速眼动睡眠。
1.4.2 PSQI 评定两组患者干预前、后的睡眠质量。PSQI是由19项自评条目和5项他评条目构成,其中的第19项自评条目和5项他评条目不参与计分。参与计分的18项自评条目各成分得分累积起来为PSQI总分,总分范围为0~21分,得分越高表示睡眠质量越差;被试者完成该问卷需要5~10min。
1.4.3 SAS及SDS 采用SAS及SDS评定两组患者干预前、后的焦虑及抑郁状态,SAS标准分的分界值为50分,50~59分为轻度焦虑,60~69分为中度焦虑,69分以上为重度焦虑;SDS标准分的分界值为53分,53~62分为轻度抑郁,63~72分为中度抑郁,>72分为重度抑郁。
1.4.4 TESS 采用TESS对两组患者治疗过程中出现的每项症状作三方面的评定:严重程度、临床症状和药物相关性以及采取的措施,症状按系统分为:行为毒性,化验异常,神经系症状,自主神经症状,心血管系症状和其它症状等6类,分别予以统计。
1.5 统计学处理 采用SPSS 19.0统计软件。计量资料以表示,组间比较采用两独立样本t检验,组内比较采用配对t检验。计数资料组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 患者不适体验存在比例 发生睡眠障碍的ICU转出患者其有中56.9%ICU住院时间超过7 d,62.1%的患者使用过咪达唑仑,20.7%的患者使用过右美托咪定;60.3%的患者经历过焦虑,72.4%的患者缺乏睡眠,84.5%的患者记得机械通气;39.6%的患者经历过疼痛,48.3%的患者希望陪护,25.9%的患者记得有创操作。
2.2 两组患者治疗前后PSQI、PSG和睡眠结构比较治疗后两组患者PSQI得分均显著下降,而且研究组PSQI分低于对照组;治疗后两组患者无论在入睡时间和觉醒时间,还是在总睡眠时间和睡眠效率等方面均有明显改善,而且研究组较对照组改善地更为明显;在睡眠结构方面研究组改善明显优于对照组(均P<0.05),见表1。
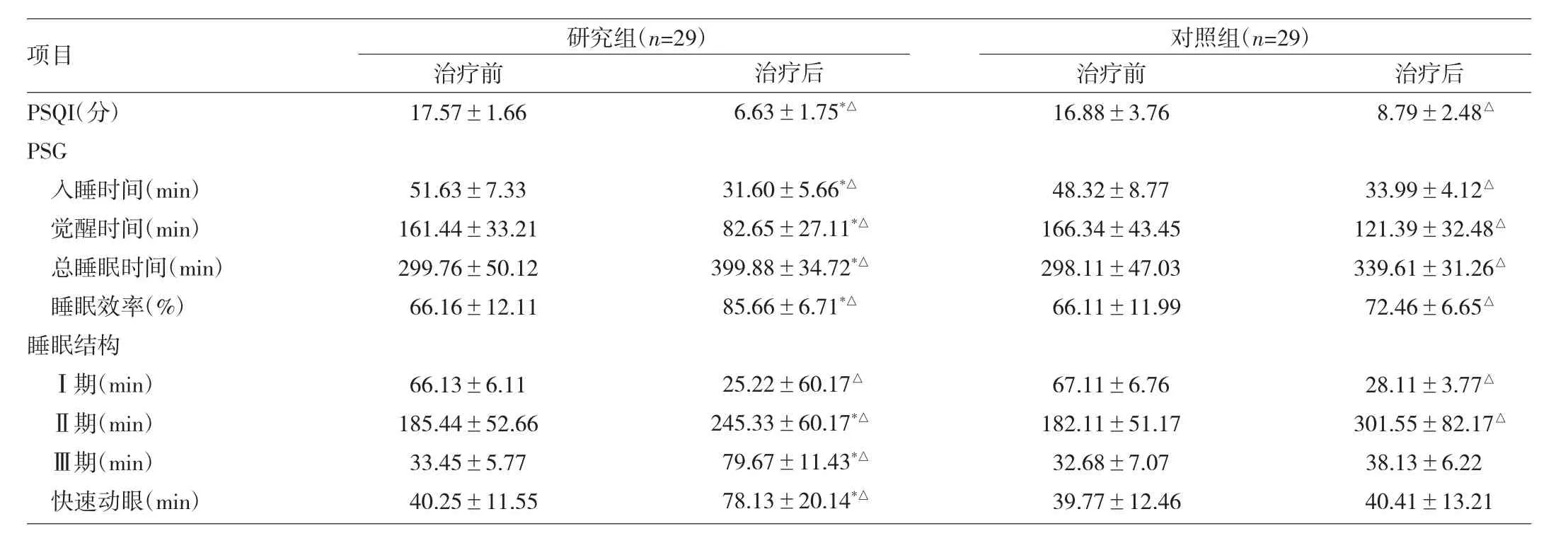
表1 两组患者治疗前后PSQI、PSG和睡眠结构的比较
2.3 两组患者治疗前后SAS、SDS评分比较 两组患者治疗前SAS、SDS评分差异均无统计学意义(均P>0.05),治疗后研究组SAS、SDS评分均显著低于对照组(均P<0.05);与治疗前相比,研究组及对照组SAS、SDS评分均显著降低(均P<O.01),见表2。
2.5 两组患者不良反应发生情况 两组患者治疗过程中出现的不良反应有头痛、恶心、消化不良、味觉异常、嗜睡、口干、眩晕等症状均较轻,持续1~3d后均自动缓解,无特殊处理,均未因不良反应而退出研究。因此对两组患者出现的不良反应发生率按计数资料进行统计,研究组与对照组的不良反应总体发生率分别为52.50% 和 55.00%,差异无统计学意义(χ2=0.633,P >0.05),见表 3。

表2 两组患者组间及组内治疗前后SAS、SDS的比较(分)
3 讨论
重症患者病情严重程度高、诊断治疗过程长,入住ICU后虽然采取了一些非药物治疗(包括改善环境、心理治疗、物理疗法)和药物手段常规进行镇痛、镇静,但是仍然有高达50%的患者离开ICU后遗有疼痛、焦虑、睡眠障碍和希望陪护、记得气管插管、有创操作等不适体验的痛苦记忆[6]。本研究发现ICU住院超过7d,使用过苯二氮卓类药物、经历过焦虑失眠、机械通气的患者,往往转出ICU后发生睡眠障碍的概率增加。这可能与患者长时间处于ICU特殊的环境下,心理和生理均遭受不同程度的恶劣影响有关。入住ICU后患者的时间观念混乱、日夜规律颠倒、噪音灯光吸痰刺激、气管插管有创通气、长期卧床肢体制动、远离亲人无法交流、潜在的心理压力以及苯二氮卓类药物应用等,众多的刺激与压力向患者袭来,使其产生一系列急性心理应激反应,如情绪低落、易激惹、躁动、谵妄等伴有强烈情感体验的精神运动性兴奋或精神运动性抑制,这些都是ICU后综合征发生的高危因素或者说是早期心理障碍的表现[7]。同时,这些因素都会影响患者的睡眠,他们的睡眠通常处于清醒期、慢波睡眠的1期与2期这3个时期,很少有患者能够进入3期和快速眼动睡眠期,因而大脑皮层细胞得不到充分的休息,导致一系列生理心理功能障碍又会随之而来[8]。

表3 两组患者不良反应发生情况的比较[例(%)]
目前苯二氮卓类药物仍然是国内处方量最大、应用最广的镇静催眠药物,在急性短期失眠时使用可以快速缓解症状,但是长期使用容易引发药物依赖、认知损害、共济失调甚至增加交通事故等不良后果[9]。
右佐匹克隆是非苯二氮卓类镇静催眠药,为佐匹克隆的右旋单一异构体,选择性地作用于w1、2受体[10],口服吸收迅速,达峰时间为1~2h,血浆半衰期为5~6h,目前右佐匹克隆已经成为睡眠障碍门诊和住院治疗失眠的常用药物。有研究显示右佐匹克隆通过延长慢波睡眠时间百分比,对失眠患者睡眠结构的改善优于绝大多数传统的苯二氮卓类药物[11]。但是药物治疗并不能改变患者对睡眠的错误观念和态度,而这不可避免地影响药物的疗效,尤其是ICU转出患者的心理障碍症状普遍存在,55%的ICU转出患者会出现创伤后应激障碍(posttraumatic stress disorder,PTSD)、焦虑抑郁、睡眠障碍等症状[12]。PTSD是指由于受到突发性、威胁性或灾难性的生活事件,导致个体延迟出现和长期持续存在的心理障碍,最常见的临床表现是再度体验,回避反应和高度警觉,以至出现难以入睡、易惊醒等睡眠障碍[13]。
目前CBT-I因其有效性和安全性已被世界卫生组织(WHO)推荐为治疗失眠的首选方法[14],CBT-I通过改变患者对睡眠的错误认知和不良生活行为习惯,以改善其睡眠状况,得到了2016年美国医师协会的推荐。
本研究采用CBT-I联合右佐匹克隆对ICU转出患者睡眠障碍进行疗效观察,研究组CBT-I联合右佐匹克隆与对照组单用右佐匹克隆相比在睡眠时间、睡眠效率方面改善更明显。在睡眠结构方面,研究组认知行为治疗明显增加Ⅲ期睡眠及快速眼动期睡眠,Ⅲ期睡眠即深度睡眠,人体各种生命活动降低到最低程度,大脑皮层细胞处于休息状态,促进生长发育的激素分泌和释放达到高峰,显著增强机体免疫能力;快速眼动期睡眠期脑内蛋白质合成增加,对脑功能的发育,延缓脑细胞的衰老至关重要[15]。有研究显示,苯二氮卓类药物主要延长Ⅱ期睡眠,对Ⅲ期及快速眼动睡眠无明显改善;右佐匹克隆的药理作用与经典的苯二氮卓类药物非常相似,能有效缩短睡眠潜伏期、减少夜间觉醒次数和增加睡眠时间,但是对Ⅲ期及快速眼动睡眠也无明显改善[16],从而导致患者主观感觉睡眠改善不明显,体力及精力没有恢复,甚至出现记忆力下降等不适表现,与本研究结果一致。
本研究中,CBT-I联合右佐匹克隆组患者焦虑抑郁情绪改善好于单纯药物右佐匹克隆组,考虑失眠症不仅是一个睡眠生理紊乱,同时还是一个心理紊乱过程,失眠症患者常伴有不同程度的焦虑、抑郁情绪,也是抑郁症的高危人群。CBT-I的实施要素主要包括认知治疗、行为治疗和睡眠卫生健康教育等[17],治疗周期一般在4周左右;CBT-I联合右佐匹克隆既可以促使患者入睡时间缩短、睡眠效率提高、进而改善睡眠状况,同时认知治疗又可以改善患者睡眠相关不良信念与态度,使患者对睡眠满意度增加,减轻患者的焦虑和抑郁症状。
本研究不足之处在于样本量较小,临床观察时间较短,对中长期疗效预后未做比较,同时由于传统面对面CBT-I常常受到时间、地域、治疗师缺乏、治疗费用昂贵等因素影响而难以有效、广泛地开展[18]。近年来,随着互联网和智能手机不断普及,使得CBT-I通过网络方式传播成为可能[19],我院目前进行的个体与互联网认知行为治疗失眠症患者的疗效观察已经取得一定的经验,正在积极研究中[20]。
综上所述,CBT-I联合右佐匹克隆治疗ICU转出患者睡眠障碍总体疗效好于单纯药物右佐匹克隆,且对改善失眠症患者的入睡时间、睡眠效率及焦虑抑郁情绪效果较好,安全性好,值得临床应用及进一步观察远期疗效。
[1]Parsons EC,Kross EK,CaldwellES,et al.Post-discharge insomnia symptoms are associated with quality of life impairment amongst survivors ofacute lung injury[J].Sleep Med,2012,13(8):1106-1109.
[2]Kyle SD,Miller CB,Rogers Z,et al.Sleep restriction therapy for insomnia is associated with reduced objective total sleep time,increased daytime somnolence,and objectively impaired vigilance:implications for the clinical management of insomnia disorder[J].Sleep,2014,37(2):229-237.
[3]Pinto LR Jr,Bittencourt LR,Treptow EC,et al.Eszopiclone versus zopiclone in the treatment of insomnia[J].Clinics(Sao Paulo),2016,71(1):5-9.
[4]Kalmbach DA,PillaiV,Arnedt JT,et al.DSM-5 Insomnia and Short Sleep:Comorbidity Landscape and Racial Disparities[J].Sleep,2016,39(12):2101.
[5]Burman Deepa.Sleep Disorders:Insomnia[J].FP Essent,2017,60:22-28.
[6]McKinley S,Fien M,Elliott R,et al.Sleep and psychological health during eady recovery from critical illness:an observational study[J].J Psychosom Res,2013,75(6):539-545.
[7]Wade DM,Howell DC,Weinman JA,et al.Investigating risk factors for psychological morbidity three months after intensive care:a prospective cohort study[J].Crit Care,2012,16(5):R192.
[8]Jackson JC,Ely EW.Cognitive impairment after critical illness:etiologies,risk factors,and future directions[J].Semin Respir Crit Care Med,2013,34(2):216-222.
[9]Anthierens S,Pasteels I,Habraken H,et al.Barriers to nonpharmacologic treatments for stress,anxiety,and insomnia:family physicians'attitudes toward benzodiazepine prescribing[J].Can Fam Physician,2010,56:398-406.
[10]Kumar S,Alam MN,Rai S,et al.Central nervous system sites of the sleep promoting effects of eszopiclone in rats[J].Neuroscience,2011,181:67-78.
[11]Ye M,Garcia-Rill E.Potentiating effect of eszopiclone on GABA(A)receptor-mediated responses in pedunculopontine neurons[J].Sleep,2009,32:879-887.
[12]Wade DM,Brewin CR,Howell DC J,et al.Intrusive memories of hallucinations and delusions in traumgtized intensive care patients:An interview study[J].Br J Health Psychol,2015,20(3):613-631.
[13]Chlan L,Savik K.Patterns of anxiety in critically ill patients receiving mechanical ventilatory support[J].Nurs Res,2011,60(3 Suppl):S50-S57.
[14]Geiger-Brown JM,Rogers VE,Liu W,et al.Cognitive behavioral therapy in persons with comorbid insomnia:a meta-analysis[J].Sleep Med Rev,2015,23:54-67.
[15]Younes M,Raneri J,Hanly P.Staging Sleep in Polysomnograms:Analysis of Inter-Scorer Variability[J].J Clin Sleep Med,2016,12(6):885-894.
[16]Bettica P,Squassante L,Groeger JA,et al.Differentialeffects of a dual orexin receptor antagonist(SB-649868)and zolpidem on sleep initiation and consolidation,SWS,REM sleep,and EEG power spectra in a model of situational insomnia[J].Neuropsychopharmacology,2012,37(5):1224-1233.
[17]Siebem AT,Suh S,Nowakowski S.Non-Pharmacological Treatment ofInsomnia[J].Neurotherapeutics,2012,9(4):717-727.
[18]Cheng SK,Dizon J.Computerised cognitive behavioural therapy for insomnia:a systematic review and meta-analysis[J].Psychother Psychosom,2012,81(4):206-216.
[19]Ritterband LM,Thorndike FP,Gonder-Frederick LA,et al.Efficacy of an internet-based behavioral intervention for adultswith insomnia[J].Arch Gen Psychiatry,2009,66(7):692-698.
[20]毛洪京,徐莲莲,余正和,等.个体与互联网认知行为治疗失眠症患者的疗效观察[J].中华精神科杂志,2017,50(1):41-46.
